11-12高一上·广东广州·期中
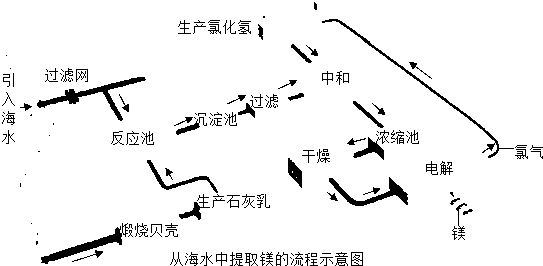
1 . 镁合金的强度高、机械性能好.这些特性使金属镁成为制造汽车、飞机、火箭的重要材料,从而获得“国防金属”的美誉.海水提镁是国际上的主要趋势,工业流程图如下;
其步骤为:
Ⅰ.将海边大量存在的贝壳(主要成分为CaCO3)煅烧成生石灰,并将生石灰制成石灰乳
Ⅱ.将石灰乳加入到海水反应池中,经过沉降、过滤得到Mg(OH)2沉淀
Ⅲ.在Mg(OH)沉淀中加入盐酸中和得到MgCl2溶液,再经蒸发结晶得到MgCl2∙6H2O
Ⅳ.将MgCl2∙6H2O在一定条件下加热得到无水MgCl2
V.电解熔融的无水MgCl2可得到Mg
(1)请根据上述步骤回答问题:
(1)写出步骤Ⅰ、Ⅱ、Ⅲ、Ⅳ的有关化学方程式,并注明基本反应类型:
Ⅰ、______________________________ 、反应类型:
Ⅱ、___________________________________ 反应类型:
Ⅲ、_______________________________________ 反应类型:
Ⅳ、__________________________________________ 反应类型:
(2)步骤Ⅳ在实验室中进行蒸发结晶得到MgCl2需要的主要仪器有______ 、__________ 酒精灯、带铁圈的铁架台、坩埚钳等。

其步骤为:
Ⅰ.将海边大量存在的贝壳(主要成分为CaCO3)煅烧成生石灰,并将生石灰制成石灰乳
Ⅱ.将石灰乳加入到海水反应池中,经过沉降、过滤得到Mg(OH)2沉淀
Ⅲ.在Mg(OH)沉淀中加入盐酸中和得到MgCl2溶液,再经蒸发结晶得到MgCl2∙6H2O
Ⅳ.将MgCl2∙6H2O在一定条件下加热得到无水MgCl2
V.电解熔融的无水MgCl2可得到Mg
(1)请根据上述步骤回答问题:
(1)写出步骤Ⅰ、Ⅱ、Ⅲ、Ⅳ的有关化学方程式,并注明基本反应类型:
Ⅰ、
Ⅱ、
Ⅲ、
Ⅳ、
(2)步骤Ⅳ在实验室中进行蒸发结晶得到MgCl2需要的主要仪器有
您最近一年使用:0次
11-12高一上·广东佛山·阶段练习
2 . 下列分离、提纯物质的方法正确的是
| A.用过滤的方法除去NaCl溶液中含有的少量淀粉胶体 |
| B.分离汽油和水的混合物最好用蒸馏的方法 |
| C.用分液的方法分离四氯化碳和水的混合物 |
| D.用溶解、过滤的方法提纯含有少量BaCl2的NaCl |
您最近一年使用:0次
11-12高一上·广东深圳·期中
3 . 利用过滤的方法可以初步除去粗盐中的泥沙等不溶性的杂质,但仍含有CaCl2,CaCl2是一种易溶于水的物质,无法用过滤的方式将其和NaCl分离,经过分析讨论,某小组同学在此基础上继续设计了如下实验:

回答下列问题:
(1)该小组同学的实验目的是________________________ ;
(2)上图括号内的操作步骤为①________ ②________ ;
(3)按此实验方案得到的NaCl固体中肯定含有________ (填化学式)杂质,为了解决这个问题可以向过滤得到的滤液中加入适量的__________ (填名称)。
(4)写出上述实验中加入过量Na2CO3后发生反应的化学方程式______________ 。

回答下列问题:
(1)该小组同学的实验目的是
(2)上图括号内的操作步骤为①
(3)按此实验方案得到的NaCl固体中肯定含有
(4)写出上述实验中加入过量Na2CO3后发生反应的化学方程式
您最近一年使用:0次
11-12高一上·广东梅州·期中
名校
4 . 在除杂质的实验操作中,为了将溶液中的杂质完全去除,通常需加入过量的除杂质试剂。某校化学课外活动小组为了除去粗盐中含有少量Na2SO4、MgCl2,设计了下列实验步骤:

试简要说明:
(1)加入过量BaCl2的溶液的原因___________________ 。
(2)判断BaCl2已过量的方法是_________________________________________
(3)加入过量Na2CO3的溶液的原因_________________________ 。
(4)滴加稀盐酸直至pH=7的目的是_____________________ ;写出这时反应的化学方程式_____________________________ 。

试简要说明:
(1)加入过量BaCl2的溶液的原因
(2)判断BaCl2已过量的方法是
(3)加入过量Na2CO3的溶液的原因
(4)滴加稀盐酸直至pH=7的目的是
您最近一年使用:0次
11-12高一上·广东汕头·期中
5 . 海带中含有丰富的碘,为了从海带中提取碘,某研究性学习小组设计并进行了以下实验:
请填写下列空白:
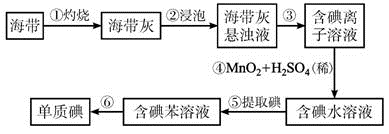
(1)步骤③的实验操作名称是_______ ;步骤⑤所用实验仪器的名称是_______ ;步骤⑥的目的是从含碘苯溶液中分离出单质碘和回收苯,该步骤的实验操作名称是____ 。
(2)步骤④反应的离子方程式是2I-+MnO2+4H+ = Mn2++I2+2H2O,该反应的氧化剂是______ ,每生成0.5 mol I2转移的电子的物质的量为______________ 。
(3)步骤⑤中,某学生选择用苯来提取碘的理由是_______________ 。
(4)请设计一种检验提取碘后的水溶液中是否还含有单质碘的简单方法:_____ 。
请填写下列空白:

(1)步骤③的实验操作名称是
(2)步骤④反应的离子方程式是2I-+MnO2+4H+ = Mn2++I2+2H2O,该反应的氧化剂是
(3)步骤⑤中,某学生选择用苯来提取碘的理由是
(4)请设计一种检验提取碘后的水溶液中是否还含有单质碘的简单方法:
您最近一年使用:0次
11-12高一上·广东·单元测试
6 . 根据下列实验装置图回答(装置用代号表示):

(1)实验室制氧气时,应选用的发生装置是____ ;制氢气时应选用的发生装置是_____ ,制二氧化碳时应选用的发生装置是_____ ,检验二氧化碳气体可选用D装置,其装置中盛放的试剂一般是___________ 。
(2)用锌粒和浓盐酸反应制氢气,将制成的气体通入硝酸银,有白色沉淀,说明氢气中含有(写化学式)______ ,反应方程式为___________________ ,若要制出纯净的氢气,除发生装置外还应选用的一种装置是_____ ;该装置中药品的作用是_________ 。

(1)实验室制氧气时,应选用的发生装置是
(2)用锌粒和浓盐酸反应制氢气,将制成的气体通入硝酸银,有白色沉淀,说明氢气中含有(写化学式)
您最近一年使用:0次
11-12高一上·广东·单元测试
名校
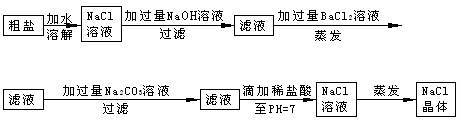
7 . 在除杂质的实验操作中,为了将溶液中的杂质完全去除,通常需加入过量的除杂质试剂。某校化学课外活动小组为了除去粗盐中含有少量Na2SO4、MgCl2,设计了下列实验步骤:
试简要说明:
(1)加入过量BaCl2的溶液的原因___________________ 。
(2)加入过量Na2CO3的溶液的原因_________________________ 。
(3)滴加稀盐酸直至pH=7的目的是_____________________ 。

试简要说明:
(1)加入过量BaCl2的溶液的原因
(2)加入过量Na2CO3的溶液的原因
(3)滴加稀盐酸直至pH=7的目的是
您最近一年使用:0次
2016-12-09更新
|
772次组卷
|
5卷引用:2011-2012学年广东省金山实验中学高一上学期化学单元测试试卷
(已下线)2011-2012学年广东省金山实验中学高一上学期化学单元测试试卷2016-2017学年甘肃省武威二中高一上10月月考化学试卷四川省武胜烈面中学2019-2020学年高一10月月考化学试题四川省广安市武胜烈面中学2019-2020学年高一上学期11月月考化学试题(已下线)第4讲 以食盐为原料的化工产品-2020-2021学年秋季班高一上学期化学教材知识点精讲练(沪科版)
9-10高一·广东·假期作业
解题方法
8 . 海水中含有丰富的化学元素,如图是某化工厂利用海水的生产镁的流程简图,请回答:

(1)实验室中蒸发浓缩液体需要的仪器有玻璃 棒、酒精灯、三角架和 。
(2)反应③需加入的试剂为 。
(3)反应④中电能转化为 。
(4)反应②完成后,需进行的操作是 。
(5)B物质中含有化学键为 。

(1)实验室中蒸发浓缩液体需要的仪器有玻璃 棒、酒精灯、三角架和 。
(2)反应③需加入的试剂为 。
(3)反应④中电能转化为 。
(4)反应②完成后,需进行的操作是 。
(5)B物质中含有化学键为 。
您最近一年使用:0次
9-10高一下·广东广州·期末
解题方法
9 . 硅酸钠被国家列为“我国优先发展的精细化学品”和“今后我国无机化工产品发展重点”之一.如图是用海边的石英砂(含氯化钠、氧化铁等杂质)制备硅酸钠的工艺流程示意简图:
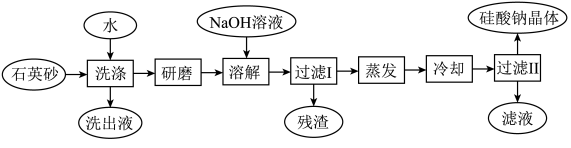
(1)要将上流程图中洗出液中的溶质析出,采用的方法是_____________;
(2)蒸发时用到的硅酸盐仪器有_____________ ;
(3)在以上流程中,要将洗净的石英砂研磨成粉末,目的是_____________;
(4)上流程中加入NaOH溶液,反应的离子方程式是_____________ ;
(5)硅酸钠溶液呈碱性,其原因是(用一离子方程式表示)_____________ ,硅酸钠的用途很广,其中的一种用途是_____________ ;
(6)用上流程中的残渣来焊接铁轨,反应的化学方程式是_____________ 。

(1)要将上流程图中洗出液中的溶质析出,采用的方法是_____________;
| A.蒸发结晶 | B.冷却结晶 | C.先蒸发,再冷却结晶 | D.先冷却,再蒸发结晶 |
(3)在以上流程中,要将洗净的石英砂研磨成粉末,目的是_____________;
| A.增加反应物的浓度,增大化学反应速率,提高生产效率 |
| B.作为催化剂载体,增加反应物与催化剂接触面积,增加反应速率,提高生产效率 |
| C.增加反应物之间的接触面积,增大反应速率,提高生产效率 |
| D.增加正反应速率,减小逆反应速率,使平衡向正反应方向移动,降低生产成本 |
(5)硅酸钠溶液呈碱性,其原因是(用一离子方程式表示)
(6)用上流程中的残渣来焊接铁轨,反应的化学方程式是
您最近一年使用:0次
名校
解题方法
10 . 实验室用KClO3分解(MnO2做催化剂)制取氧气,实验后回收剩余固体中的MnO2,正确的操作步骤是
| A.溶解、过滤、蒸发 | B.溶解、过滤、洗涤、干燥 |
| C.溶解、过滤、结晶 | D.溶解、结晶、干燥 |
您最近一年使用:0次
2016-11-21更新
|
175次组卷
|
4卷引用:广东省揭阳华侨高级中学2019-2020学年高一上学期12月月考化学试题



