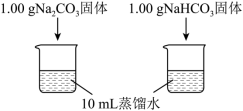
1 . 某小组同学利用以下实验装置研究SO2的性质(经检验,装置的气密性良好)。实验过程中遇到以下问题:___________ 。
(2)ii中观察品红溶液现象___________ 。结论是:SO2有___________ 性。
(3)iii中石蕊溶液变___________ ,说明SO2与H2O反应生成了酸性物质。
(4)iv中观察到的现象是___________ ,离子方程式是:___________ ,结论是:SO2有___________ 性。
(5)v中产生现象___________ ,结论是:SO2有___________ 性。
(6)NaOH溶液的作用是___________ 。反应的离子方程式___________ 。
(7)若将铜丝换成足量铁丝与一定量浓H2SO4反应,随着硫酸溶液变稀得到的两种气体产物依次为___________ 、___________ 。

(2)ii中观察品红溶液现象
(3)iii中石蕊溶液变
(4)iv中观察到的现象是
(5)v中产生现象
(6)NaOH溶液的作用是
(7)若将铜丝换成足量铁丝与一定量浓H2SO4反应,随着硫酸溶液变稀得到的两种气体产物依次为
您最近一年使用:0次
2 . 硫脲 是一种杀菌剂。某小组设计实验制备硫脲并探究其性质。
是一种杀菌剂。某小组设计实验制备硫脲并探究其性质。
实验(一):制备硫脲。装置如图1所示(加热装置已省略)。
已知:① ;
;
②25℃时硫脲溶解度为14.2 g/100 g水;
③实验室常用FeS与稀H2SO4在常温下制H2S。______ ,B的加热方式宜选择______ (填标号)。
a.直接用酒精灯加热
b.油浴加热(100~250℃)
c.热水浴加热
(2)当C装置中出现______ (填实验现象)时表明B中生成了 。
。
(3)实验发现,硫脲产率与投料比{ }的关系如图2所示。
}的关系如图2所示。______ 。
实验(二):探究硫脲的性质。
资料显示:①150℃时 转化成NH4SCN。
转化成NH4SCN。
②酸性KMnO4溶液和硫脲反应,还原产物为 ,氧化产物为N2和
,氧化产物为N2和 。
。
(4)取少量 溶于水,加热至150℃,一段时间后再冷却至室温时,滴加
溶于水,加热至150℃,一段时间后再冷却至室温时,滴加______ ,可检验是否有 生成。
生成。
(5)取少量 溶于NaOH溶液,加入CuSO4溶液,过滤、洗涤,得到黑色固体,由此推知,
溶于NaOH溶液,加入CuSO4溶液,过滤、洗涤,得到黑色固体,由此推知, 在碱性条件下会生成
在碱性条件下会生成______ (填离子符号)。
(6)甲同学取少量 溶于水,滴加几滴酸性KMnO4溶液,振荡,溶液褪色;再滴加BaCl2和盐酸溶液,产生白色沉淀。
溶于水,滴加几滴酸性KMnO4溶液,振荡,溶液褪色;再滴加BaCl2和盐酸溶液,产生白色沉淀。
①乙同学认为甲同学的实验不能证明生成了 ,理由是
,理由是______________ 。
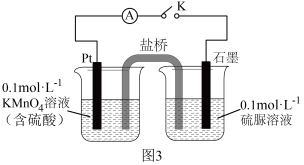
②乙同学设计如图3装置验证氧化产物中含有 。
。_____________ ,经检验石墨电极附近还有N2和CO2生成,每生成1 mol N2,电路中转移的电子数为______  。
。
 是一种杀菌剂。某小组设计实验制备硫脲并探究其性质。
是一种杀菌剂。某小组设计实验制备硫脲并探究其性质。实验(一):制备硫脲。装置如图1所示(加热装置已省略)。
已知:①
 ;
;②25℃时硫脲溶解度为14.2 g/100 g水;
③实验室常用FeS与稀H2SO4在常温下制H2S。

a.直接用酒精灯加热
b.油浴加热(100~250℃)
c.热水浴加热
(2)当C装置中出现
 。
。(3)实验发现,硫脲产率与投料比{
 }的关系如图2所示。
}的关系如图2所示。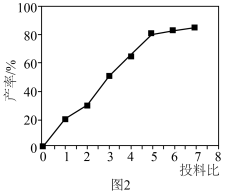
实验(二):探究硫脲的性质。
资料显示:①150℃时
 转化成NH4SCN。
转化成NH4SCN。②酸性KMnO4溶液和硫脲反应,还原产物为
 ,氧化产物为N2和
,氧化产物为N2和 。
。(4)取少量
 溶于水,加热至150℃,一段时间后再冷却至室温时,滴加
溶于水,加热至150℃,一段时间后再冷却至室温时,滴加 生成。
生成。(5)取少量
 溶于NaOH溶液,加入CuSO4溶液,过滤、洗涤,得到黑色固体,由此推知,
溶于NaOH溶液,加入CuSO4溶液,过滤、洗涤,得到黑色固体,由此推知, 在碱性条件下会生成
在碱性条件下会生成(6)甲同学取少量
 溶于水,滴加几滴酸性KMnO4溶液,振荡,溶液褪色;再滴加BaCl2和盐酸溶液,产生白色沉淀。
溶于水,滴加几滴酸性KMnO4溶液,振荡,溶液褪色;再滴加BaCl2和盐酸溶液,产生白色沉淀。①乙同学认为甲同学的实验不能证明生成了
 ,理由是
,理由是②乙同学设计如图3装置验证氧化产物中含有
 。
。
 。
。
您最近一年使用:0次
3 . 某学习小组设计如图所示实验装置(装置中空气已排尽)探究氮的氧化物的性质。下列说法正确的是
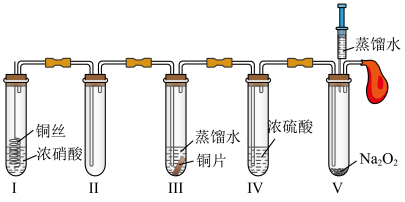
| A.装置I中产生红棕色气体,体现浓硝酸具有强酸性 |
| B.装置II为防倒吸装置 |
C.装置III中的溶液变蓝,说明 氧化了金属铜 氧化了金属铜 |
| D.向装置V中加入蒸馏水,能使无色气体变为红棕色 |
您最近一年使用:0次
名校
4 . 铜与浓硝酸反应,装置如图。
(1)铜与浓 反应的化学方程式为
反应的化学方程式为___________ 。
(2)分别取3mL浓 与不同质量的纯铜片(铜片均完成溶解)充分反应,反应剧烈,纯铜片逐渐溶解,试管内呈现
与不同质量的纯铜片(铜片均完成溶解)充分反应,反应剧烈,纯铜片逐渐溶解,试管内呈现___________ 色气体,溶液颜色发生变化如下:
取2份等体积①中溶液以相同流速分别通入 和空气,观察现象如下:
和空气,观察现象如下:
溶液呈绿色的可能原因为___________ (填标号),通入气体后,溶液由绿色变为蓝色的原因为___________ (填标号)。
A.硝酸铜溶液就是绿色
B.硝酸铜溶液浓度大
C. 溶解在硝酸铜溶液中
溶解在硝酸铜溶液中
D.溶液通入 时,
时, 被缓慢氧化为
被缓慢氧化为
E.溶液含有某种与绿色有关的还原性微粒,通入空气时较快被氧化
F.空气中的 溶于水显酸性,促进了溶液变蓝色
溶于水显酸性,促进了溶液变蓝色
(3)查阅文献知, 在溶液中存在如下反应:
在溶液中存在如下反应:
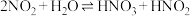 ,
,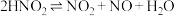
取3份等体积的①中绿色溶液,分别加入不同物质,现象如下:
加入 后溶液迅速变蓝,原因是
后溶液迅速变蓝,原因是 可能参与了下列反应(用化学方程式表示):
可能参与了下列反应(用化学方程式表示):
 ,
,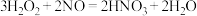 ,
,___________ 。
(4)综上分析,本实验中尾气处理反应的离子方程式为___________ ,硝酸铜溶液中存在___________ (填化学式)参与了形成绿色溶液的过程。

(1)铜与浓
 反应的化学方程式为
反应的化学方程式为(2)分别取3mL浓
 与不同质量的纯铜片(铜片均完成溶解)充分反应,反应剧烈,纯铜片逐渐溶解,试管内呈现
与不同质量的纯铜片(铜片均完成溶解)充分反应,反应剧烈,纯铜片逐渐溶解,试管内呈现| 编号 | ① | ② | ③ | ④ | ⑤ |
| 铜粉质量/g | 0.1 | 0.2 | 0.3 | 0.4 | 0.5 |
| 溶液颜色 | 绿色 | 草绿色 | 蓝绿色偏绿 | 蓝绿色偏蓝 | 蓝色 |
 和空气,观察现象如下:
和空气,观察现象如下:| 通入气体 |  | 空气 |
| 现象 | 液面上方出现明显的红棕色气体,25min后溶液变为蓝色 | 液面上方出现明显的红棕色气体,5min后溶液变为蓝色 |
A.硝酸铜溶液就是绿色
B.硝酸铜溶液浓度大
C.
 溶解在硝酸铜溶液中
溶解在硝酸铜溶液中 D.溶液通入
 时,
时, 被缓慢氧化为
被缓慢氧化为
E.溶液含有某种与绿色有关的还原性微粒,通入空气时较快被氧化
F.空气中的
 溶于水显酸性,促进了溶液变蓝色
溶于水显酸性,促进了溶液变蓝色(3)查阅文献知,
 在溶液中存在如下反应:
在溶液中存在如下反应: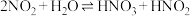 ,
,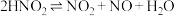
取3份等体积的①中绿色溶液,分别加入不同物质,现象如下:
| 加入物质 |  | 3滴30% 溶液 溶液 | 3滴水 |
| 现象 | 溶液绿色变深 | 溶液迅速变为蓝色 | 溶液颜色几乎不变 |
 后溶液迅速变蓝,原因是
后溶液迅速变蓝,原因是 可能参与了下列反应(用化学方程式表示):
可能参与了下列反应(用化学方程式表示): ,
,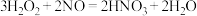 ,
,(4)综上分析,本实验中尾气处理反应的离子方程式为
您最近一年使用:0次
名校
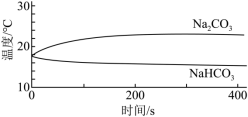
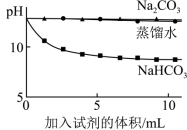
5 . Ⅰ.实验小组利用传感器探究Na2CO3和NaHCO3的性质。
【查阅资料】
溶液pH越小,OH- 的浓度越小,溶液碱性越弱。
【实验过程】
【分析与解释】
(1)实验Ⅰ中,溶解时吸收热量的物质是___________ (填化学式)。
(2)实验Ⅱ中,Na2CO3溶液和澄清石灰水反应的离子方程式为___________ ,OH- 未参与该反应的实验证据是___________ 。
(3)实验Ⅱ中,滴加NaHCO3溶液的烧杯中溶液pH的变化与滴加Na2CO3溶液的有明显差异,原因是滴加NaHCO3溶液的烧杯中,___________ (填离子符号)参与了反应。
Ⅱ.向Na2CO3和NaHCO3的混合溶液中逐滴滴加盐酸,所得气体的体积与所加盐酸的体积关系如图所示:___________ 、___________ 。
(5)B点时,反应所得溶液中溶质是___________ 。
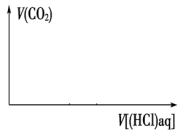
(6)将题中的NaHCO3改为NaOH时,请在下图中画出V(CO2)-V(HCl)的大致图像___________ 。
【查阅资料】
溶液pH越小,OH- 的浓度越小,溶液碱性越弱。
【实验过程】
| 编号 | 实验操作 | 实验数据 |
| 实验Ⅰ | 测量下面实验过程中温度的变化
|
|
| 实验Ⅱ | 测量下面实验过程中溶液pH的变化
|
|
(1)实验Ⅰ中,溶解时吸收热量的物质是
(2)实验Ⅱ中,Na2CO3溶液和澄清石灰水反应的离子方程式为
(3)实验Ⅱ中,滴加NaHCO3溶液的烧杯中溶液pH的变化与滴加Na2CO3溶液的有明显差异,原因是滴加NaHCO3溶液的烧杯中,
Ⅱ.向Na2CO3和NaHCO3的混合溶液中逐滴滴加盐酸,所得气体的体积与所加盐酸的体积关系如图所示:
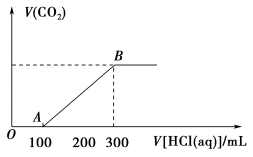
(5)B点时,反应所得溶液中溶质是
(6)将题中的NaHCO3改为NaOH时,请在下图中画出V(CO2)-V(HCl)的大致图像
您最近一年使用:0次
6 . 人类的农业生产离不开氮肥,几乎所有的氮肥都以氨为原料,某化学兴趣小组利用图1装置制备氨气,图2装置探究其相关性质。
(1)图1装置中生成 的化学方程式为
的化学方程式为________________ ,
(2)检验圆底烧瓶中已收集满氨气的方法是________________ 。
Ⅱ、探究氨气与氧化铜的反应,验证氨气的性质及部分反应产物
(3)无水硫酸铜的作用是________ ,有同学认为需要在无水硫酸铜的后面再接一个装有无水 固体的球形干燥管,这样做的目的是
固体的球形干燥管,这样做的目的是________________ 。
(4)实验中观察到a中 粉末变红,b中无水硫酸铜变蓝,并收集到一种单质气体。则该反应的化学方程式为
粉末变红,b中无水硫酸铜变蓝,并收集到一种单质气体。则该反应的化学方程式为________________ 。
(5)若向a中通入标准状况下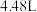 的氨气,最终得到铜的质量为
的氨气,最终得到铜的质量为________ g。
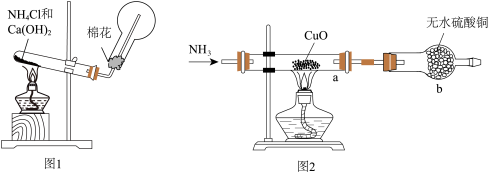
(1)图1装置中生成
 的化学方程式为
的化学方程式为(2)检验圆底烧瓶中已收集满氨气的方法是
Ⅱ、探究氨气与氧化铜的反应,验证氨气的性质及部分反应产物
(3)无水硫酸铜的作用是
 固体的球形干燥管,这样做的目的是
固体的球形干燥管,这样做的目的是(4)实验中观察到a中
 粉末变红,b中无水硫酸铜变蓝,并收集到一种单质气体。则该反应的化学方程式为
粉末变红,b中无水硫酸铜变蓝,并收集到一种单质气体。则该反应的化学方程式为(5)若向a中通入标准状况下
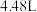 的氨气,最终得到铜的质量为
的氨气,最终得到铜的质量为
您最近一年使用:0次
2024-05-04更新
|
131次组卷
|
2卷引用:天津市第二十一中学2023-2024学年高一下学期第一次月考化学试卷
7 . 用如图实验装置探究二氧化硫的氧化性。按图充入气体,连接装置,关闭旋塞1和2。___________ 。
2.若A瓶和B瓶的体积相等,恢复到常温,关闭旋塞1,打开旋塞2,可观察到的现象是___________ 。
3.将 气体通入下列装置中,一定不可能产生沉淀的是
气体通入下列装置中,一定不可能产生沉淀的是___________ 。

2.若A瓶和B瓶的体积相等,恢复到常温,关闭旋塞1,打开旋塞2,可观察到的现象是
3.将
 气体通入下列装置中,一定不可能产生沉淀的是
气体通入下列装置中,一定不可能产生沉淀的是
您最近一年使用:0次
8 . 利用 的漂白性检测干白葡萄酒(液体为无色)中的
的漂白性检测干白葡萄酒(液体为无色)中的 或
或 设计如图的实验:
设计如图的实验: 水溶液显酸性,用离子方程式说明
水溶液显酸性,用离子方程式说明___________
2.甲同学得出的实验结论是干白葡萄酒中不含 或
或 这个结论
这个结论___________ (填“成立”或“不成立”),理由是___________ 。
 的漂白性检测干白葡萄酒(液体为无色)中的
的漂白性检测干白葡萄酒(液体为无色)中的 或
或 设计如图的实验:
设计如图的实验: 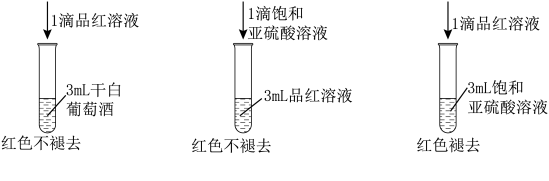
 水溶液显酸性,用离子方程式说明
水溶液显酸性,用离子方程式说明2.甲同学得出的实验结论是干白葡萄酒中不含
 或
或 这个结论
这个结论
您最近一年使用:0次
名校
解题方法
9 . 硫酸的性质:某化学学习小组为了探究铁质材料(碳素钢)和浓硫酸反应的产物,利用下列装置进行了如图实验探究活动:___________ 性。实验过程中观察到装置 中固体由黑变红,装置
中固体由黑变红,装置 中无水硫酸铜由白色粉末变蓝,说明碳素钢与浓硫酸的反应产物中有
中无水硫酸铜由白色粉末变蓝,说明碳素钢与浓硫酸的反应产物中有___________ 气体产生。
2.若要验证碳素钢与浓硫酸反应产生的气体有 ,应在上述装置中观察到
,应在上述装置中观察到___________ 。
3.将浓硫酸滴入蔗糖中,下列说法中错误的是___________。
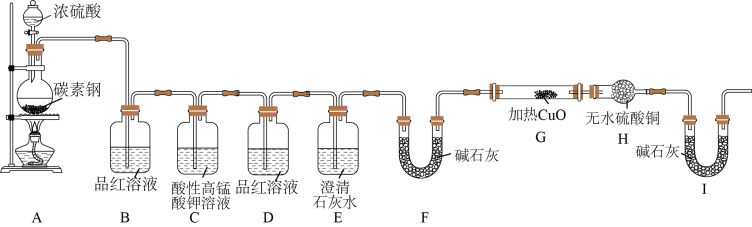
 中固体由黑变红,装置
中固体由黑变红,装置 中无水硫酸铜由白色粉末变蓝,说明碳素钢与浓硫酸的反应产物中有
中无水硫酸铜由白色粉末变蓝,说明碳素钢与浓硫酸的反应产物中有2.若要验证碳素钢与浓硫酸反应产生的气体有
 ,应在上述装置中观察到
,应在上述装置中观察到3.将浓硫酸滴入蔗糖中,下列说法中错误的是___________。
| A.蔗糖变黑体现了浓硫酸的脱水性 |
| B.蔗糖体积膨胀变成疏松多孔的海绵状物质 |
| C.实验中产生大量气体体现了浓硫酸的强酸性 |
| D.将实验中产生的气体通入品红溶液,溶液会褪色 |
您最近一年使用:0次
名校
10 . 某化学小组以下列4种物质的溶液作为研究对象,比较不同物质的羟基中氢原子的活泼性。
A.乙酸 B.苯酚 C.碳酸 D.乙醇
(1)甲同学设计并实施了如下实验方案。
(2)乙同学对甲同学的实验提出如下改进方案,能一次比较 、碳酸和苯酚的羟基中氢原子的活泼性,实验仪器如图所示。
、碳酸和苯酚的羟基中氢原子的活泼性,实验仪器如图所示。_____ (填接口字母)。
②丙同学查资料发现乙酸有挥发性,于是在试管F之前增加了一个盛有_____ 的洗气装置,使乙同学的实验设计更加完善。
A.乙酸 B.苯酚 C.碳酸 D.乙醇
(1)甲同学设计并实施了如下实验方案。
| 编号 | 实验操作 | 实验现象 | 结论及解释 |
| 1 | 分别取4种溶液,滴加紫色石蕊溶液 | ①溶液变红的是溶液 | 略 |
| 2 | 将 通入 通入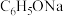 溶液中 溶液中 | ②现象: | ③方程式: |
| 3 | 配制等物质的量浓度的 、 、 溶液,并比较其pH 溶液,并比较其pH |  溶液的pH大于 溶液的pH大于 溶液 溶液 | 略 |
| 4 | 向含酚酞的 溶液中,各滴加等量的BD两种溶液 溶液中,各滴加等量的BD两种溶液 | D中无明显现象; B中红色明显变浅 | ④滴加B时方程式: |
| ⑤结论:4种物质的羟基中的氢原子的活泼性由强到弱的顺序是 | |||
 、碳酸和苯酚的羟基中氢原子的活泼性,实验仪器如图所示。
、碳酸和苯酚的羟基中氢原子的活泼性,实验仪器如图所示。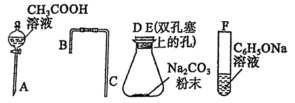
②丙同学查资料发现乙酸有挥发性,于是在试管F之前增加了一个盛有
您最近一年使用:0次