名校
解题方法
1 . 已知硫酸亚铁铵晶体[(NH4)2SO4·FeSO4·6H2O,M=392g/mol](俗称莫尔盐)可溶于水,在100℃~110℃时分解。为探究其化学性质,甲、乙两同学设计了如下实验。
Ⅰ.探究莫尔盐晶体加热时的分解产物。
(1)甲同学设计如图所示的装置进行实验,装置C中可观察到的现象是_______ ,由此可知分解产物中有_______ 。_______ →G。
(3)证明含有SO3的实验现象是_______ ,安全瓶H的作用是_______ 。
Ⅱ.为测定硫酸亚铁铵晶体纯度,称取m g莫尔盐样品,配成500 mL溶液。甲、乙两位同学设计了如下两个实验方案。
(甲)方案一:取20.00 mL硫酸亚铁铵溶液用0.1000mol/L的酸性KMnO4溶液进行三次滴定。
(4)方案一中发生反应的离子方程式为:_______ 。
(5)方案二中判断所加BaCl2溶液已足量的操作及现象为_______ 。
(6)若甲乙两同学实验操作都正确,但方案一的测定结果总是小于方案二,推测可能原因:_______ 。
(7)乙方案测定出硫酸亚铁铵纯度为_______ (列出计算式即可)。
Ⅰ.探究莫尔盐晶体加热时的分解产物。
(1)甲同学设计如图所示的装置进行实验,装置C中可观察到的现象是

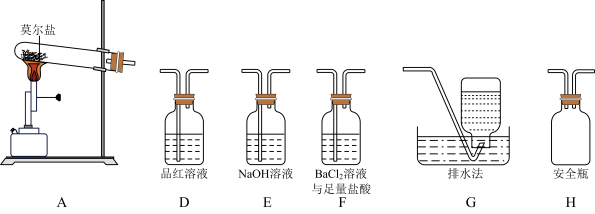
(3)证明含有SO3的实验现象是
Ⅱ.为测定硫酸亚铁铵晶体纯度,称取m g莫尔盐样品,配成500 mL溶液。甲、乙两位同学设计了如下两个实验方案。
(甲)方案一:取20.00 mL硫酸亚铁铵溶液用0.1000mol/L的酸性KMnO4溶液进行三次滴定。
(乙)方案二:
(4)方案一中发生反应的离子方程式为:
(5)方案二中判断所加BaCl2溶液已足量的操作及现象为
(6)若甲乙两同学实验操作都正确,但方案一的测定结果总是小于方案二,推测可能原因:
(7)乙方案测定出硫酸亚铁铵纯度为
您最近一年使用:0次
名校
2 . 某实验室利用 和
和 反应合成硫酰氯(
反应合成硫酰氯( ),并对
),并对 和HClO的酸性强弱进行探究。已知
和HClO的酸性强弱进行探究。已知 的沸点为69.1℃,在空气中遇水蒸气发生剧烈反应,并产生大量HCl,100℃以上容易分解。实验室合成
的沸点为69.1℃,在空气中遇水蒸气发生剧烈反应,并产生大量HCl,100℃以上容易分解。实验室合成 的原理:
的原理: ,反应会放热。实验装置如图所示,请回答下列问题:
,反应会放热。实验装置如图所示,请回答下列问题:_____
(2)装置戊上方分液漏斗中最好选用_____ (填字母)。
a.蒸馏水 b.饱和食盐水 c.浓氢氧化钠溶液 d. 盐酸
盐酸
(3)装置乙和丁盛放的试剂均是_____ (写名称)。
(4)装置丙放置在冰水浴中的原因是_____ 。
(5) 和水反应的化学方程式为
和水反应的化学方程式为_____
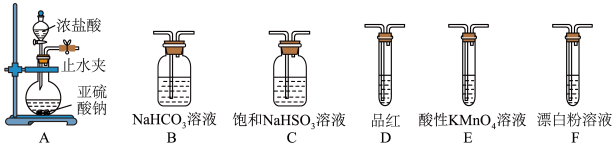
(6)选用下面的装置探究酸性: ,其连接顺序为A→C→B→E→D→Fa'装置E中反应的离子方程式为
,其连接顺序为A→C→B→E→D→Fa'装置E中反应的离子方程式为_____ ,能证明 的酸性强于HClO的实验现象为
的酸性强于HClO的实验现象为_____ (已知: 酸性大于
酸性大于 )
)
 和
和 反应合成硫酰氯(
反应合成硫酰氯( ),并对
),并对 和HClO的酸性强弱进行探究。已知
和HClO的酸性强弱进行探究。已知 的沸点为69.1℃,在空气中遇水蒸气发生剧烈反应,并产生大量HCl,100℃以上容易分解。实验室合成
的沸点为69.1℃,在空气中遇水蒸气发生剧烈反应,并产生大量HCl,100℃以上容易分解。实验室合成 的原理:
的原理: ,反应会放热。实验装置如图所示,请回答下列问题:
,反应会放热。实验装置如图所示,请回答下列问题: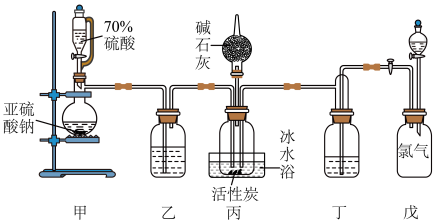
(2)装置戊上方分液漏斗中最好选用
a.蒸馏水 b.饱和食盐水 c.浓氢氧化钠溶液 d.
 盐酸
盐酸(3)装置乙和丁盛放的试剂均是
(4)装置丙放置在冰水浴中的原因是
(5)
 和水反应的化学方程式为
和水反应的化学方程式为(6)选用下面的装置探究酸性:
 ,其连接顺序为A→C→B→E→D→Fa'装置E中反应的离子方程式为
,其连接顺序为A→C→B→E→D→Fa'装置E中反应的离子方程式为 的酸性强于HClO的实验现象为
的酸性强于HClO的实验现象为 酸性大于
酸性大于 )
)
您最近一年使用:0次
名校
解题方法
3 . 人类的农业生产离不开氮肥,几乎所有的氮肥都以氨为原料,某化学兴趣小组利用图1装置制备氨气,图2装置探究其相关性质。
(1)图1装置中生成 的化学方程式为
的化学方程式为_____ 。
(2)检验圆底烧瓶中已收集满氨气的方法是_____ 。
Ⅱ.探究氨气与氧化铜的反应(如图2)验证氨气的性质及部分反应产物:
(3)无水硫酸铜的作用是_____ ;有同学认为需要在无水硫酸铜的后面再接一个装有 固体的球形干燥管,这样做的目的是
固体的球形干燥管,这样做的目的是_____ 。
(4)该实验缺少尾气吸收装置。如图中能用来吸收尾气的装置是_____ (填字母)。 粉末变红,b中无水硫酸铜变蓝,并收集到一种单质气体。则该反应的化学方程式为
粉末变红,b中无水硫酸铜变蓝,并收集到一种单质气体。则该反应的化学方程式为_____ ,证明氨气具有_____ (填“氧化”或“还原”)性。
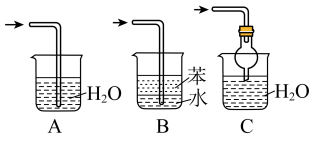
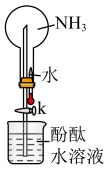
(6)①如图是进行氨气喷泉实验的装置,氨气使烧杯中溶液由无色变为红色,其原因是(用方程式表示)_____ 。
②在上图的烧瓶中充满干燥气体,胶头滴管及烧杯中分别盛有液体。下列组合中不可能形成喷泉的是_____ 。 和
和 B.
B. 和氢氧化钠溶液 C.
和氢氧化钠溶液 C. 和饱和食盐水 D.
和饱和食盐水 D. 和烧碱溶液
和烧碱溶液
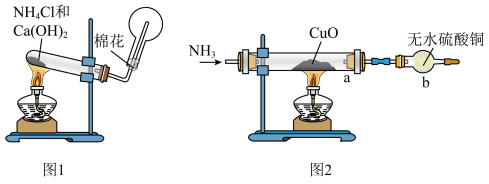
(1)图1装置中生成
 的化学方程式为
的化学方程式为(2)检验圆底烧瓶中已收集满氨气的方法是
Ⅱ.探究氨气与氧化铜的反应(如图2)验证氨气的性质及部分反应产物:
(3)无水硫酸铜的作用是
 固体的球形干燥管,这样做的目的是
固体的球形干燥管,这样做的目的是(4)该实验缺少尾气吸收装置。如图中能用来吸收尾气的装置是
 粉末变红,b中无水硫酸铜变蓝,并收集到一种单质气体。则该反应的化学方程式为
粉末变红,b中无水硫酸铜变蓝,并收集到一种单质气体。则该反应的化学方程式为(6)①如图是进行氨气喷泉实验的装置,氨气使烧杯中溶液由无色变为红色,其原因是(用方程式表示)
②在上图的烧瓶中充满干燥气体,胶头滴管及烧杯中分别盛有液体。下列组合中不可能形成喷泉的是
 和
和 B.
B. 和氢氧化钠溶液 C.
和氢氧化钠溶液 C. 和饱和食盐水 D.
和饱和食盐水 D. 和烧碱溶液
和烧碱溶液
您最近一年使用:0次
解题方法
4 . Ⅰ.实验室欲用NaOH固体配制490mL 0.25mol·L−1的NaOH溶液。
回答下列问题:
(1)称取NaOH质量为___________ g。
(2)在配制的过程中一定不需要使用到的仪器是___________  填字母
填字母 ,还缺少的仪器有
,还缺少的仪器有___________ (填仪器名称)
A.烧杯 B.药匙 C.玻璃棒 D.托盘天平 E.锥形瓶 F.胶头滴管
(3)下列的实验操作可能导致配制的溶液浓度偏低的是___________  填字母
填字母 。
。
A.容量瓶内原来存有少量的水未进行干燥
B. 称量固体时,所用砝码已生锈
C. NaOH固体溶解后,未冷却至室温就开始进行转移
D. 定容时仰视视刻度线
E.定容时液面超过刻度线,用胶头滴管吸出
Ⅱ.某学习小组为探究CO2与过氧化钠反应时是否需要与水接触,设计了如下实验装置
步骤1:先打开K2,关闭K1,然后打开分液漏斗活塞加入盐酸,一段时间后,将带火星的木条放在a处。
步骤2:先打开K1,关闭K2,然后打开分液漏斗活塞加入盐酸,一段时间后,将带火星的木条放在a处。
(4)装置②是为了除去CO2中的HCl气体,所选试剂是___________ (填字母)。
A.浓H2SO4 B.饱和Na2CO3溶液 C.饱和NaHCO3溶液
(5)从上述试剂中选择,装置③中的试剂是___________ (填字母),其作用为___________ 。
(6)甲同学根据实验现象认为:CO2与过氧化钠反应时需要与水接触。据此推断他观察到的步骤1和步骤2的a处的实验现象分别是___________ 。
(7)乙同学对此结论提出质疑,他认为:上述实验不足以证明“有水存在时,过氧化钠与CO2发生了化学反应”。用化学方程式表示乙同学的理由___________ 。
回答下列问题:
(1)称取NaOH质量为
(2)在配制的过程中一定不需要使用到的仪器是
 填字母
填字母 ,还缺少的仪器有
,还缺少的仪器有A.烧杯 B.药匙 C.玻璃棒 D.托盘天平 E.锥形瓶 F.胶头滴管
(3)下列的实验操作可能导致配制的溶液浓度偏低的是
 填字母
填字母 。
。A.容量瓶内原来存有少量的水未进行干燥
B. 称量固体时,所用砝码已生锈
C. NaOH固体溶解后,未冷却至室温就开始进行转移
D. 定容时仰视视刻度线
E.定容时液面超过刻度线,用胶头滴管吸出
Ⅱ.某学习小组为探究CO2与过氧化钠反应时是否需要与水接触,设计了如下实验装置

步骤1:先打开K2,关闭K1,然后打开分液漏斗活塞加入盐酸,一段时间后,将带火星的木条放在a处。
步骤2:先打开K1,关闭K2,然后打开分液漏斗活塞加入盐酸,一段时间后,将带火星的木条放在a处。
(4)装置②是为了除去CO2中的HCl气体,所选试剂是
A.浓H2SO4 B.饱和Na2CO3溶液 C.饱和NaHCO3溶液
(5)从上述试剂中选择,装置③中的试剂是
(6)甲同学根据实验现象认为:CO2与过氧化钠反应时需要与水接触。据此推断他观察到的步骤1和步骤2的a处的实验现象分别是
(7)乙同学对此结论提出质疑,他认为:上述实验不足以证明“有水存在时,过氧化钠与CO2发生了化学反应”。用化学方程式表示乙同学的理由
您最近一年使用:0次
5 . 某小组学习了盐类水解,对 溶液与
溶液与 溶液的反应产生了兴趣,进行如下探究。
溶液的反应产生了兴趣,进行如下探究。
(1)理论预测
甲同学认为两溶液的水解平衡相互促进并完全水解,实验中会观察到___________ 并闻到臭鸡蛋气味;
乙同学认为会发生氧化还原反应,并预测了还原产物为___________ (填化学式)。
(2)实验探究
已知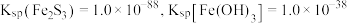 。
。
①实验中生成黑色沉淀 的反应类型是
的反应类型是___________ ; 溶解生成的黄色固体为
溶解生成的黄色固体为___________ 。
②实验中首先观察到黑色沉淀出现,可能的原因是___________ ; 溶液滴加至一定量时,
溶液滴加至一定量时, 溶解的原因是
溶解的原因是___________ 。
③针对实验过程中未观察到红褐色沉淀,甲同学认为可能是产生的量比较少,被黑色所遮盖。乙同学根据 数据分析,认为就算产生红褐色沉淀,也会转化为黑色沉淀,写出沉淀转化的离子方程式
数据分析,认为就算产生红褐色沉淀,也会转化为黑色沉淀,写出沉淀转化的离子方程式___________ 。
④丙同学设计实验证明③中乙同学的猜想,方案是:向洁净试管中加入新制并洗净的 沉淀,若
沉淀,若___________ (填实验操作及现象)则证明猜想正确。
 溶液与
溶液与 溶液的反应产生了兴趣,进行如下探究。
溶液的反应产生了兴趣,进行如下探究。(1)理论预测
甲同学认为两溶液的水解平衡相互促进并完全水解,实验中会观察到
乙同学认为会发生氧化还原反应,并预测了还原产物为
(2)实验探究
| 实验操作 | 实验现象 |
向稀的 溶液中逐滴加入 溶液中逐滴加入 稀溶液,直至过量 稀溶液,直至过量 | 立即产生黑色沉淀并逐渐增加, 溶液过量后黑色沉淀部分溶解,观察到黄褐色浑浊 溶液过量后黑色沉淀部分溶解,观察到黄褐色浑浊 |
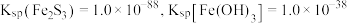 。
。①实验中生成黑色沉淀
 的反应类型是
的反应类型是 溶解生成的黄色固体为
溶解生成的黄色固体为②实验中首先观察到黑色沉淀出现,可能的原因是
 溶液滴加至一定量时,
溶液滴加至一定量时, 溶解的原因是
溶解的原因是③针对实验过程中未观察到红褐色沉淀,甲同学认为可能是产生的量比较少,被黑色所遮盖。乙同学根据
 数据分析,认为就算产生红褐色沉淀,也会转化为黑色沉淀,写出沉淀转化的离子方程式
数据分析,认为就算产生红褐色沉淀,也会转化为黑色沉淀,写出沉淀转化的离子方程式④丙同学设计实验证明③中乙同学的猜想,方案是:向洁净试管中加入新制并洗净的
 沉淀,若
沉淀,若
您最近一年使用:0次
解题方法
6 . 化学小组同学为研究氯气制备和氯水的成分及性质进行了如下实验。
【实验1】制备氯气。如图1是实验室制取纯净、干燥氯气装置图。
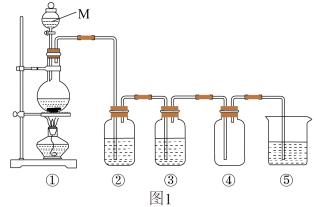
(1)M的名称是_______ ,①中反应的反应的离子方程式是_______ 。
(2)③中存放的试剂是_______ 。
(3)⑤中反应的离子方程式是_______ 。
【实验2】研究氯水性质。实验操作及现象如下表。
(4)实验2﹣1结论是_______ 。
(5)实验2﹣2中溶液变红是由于溶液中含有_______ ;使溶液褪色的粒子是_______ 。
(6)证明氯水中含有氯离子的方案是_______ 。
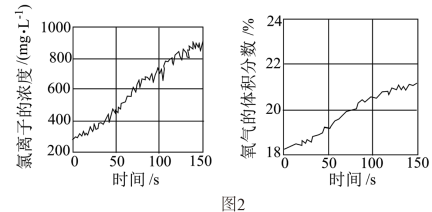
(7)同学们发现久置的氯水会失去漂白性,溶液由黄绿色变为无色。为探究氯水失效的原因,进行实验:用强光照射盛有氯水的密闭广口瓶,并用传感器测定广口瓶中数据,得到如图2曲线。图中曲线变化的原因是_______ 。若在上述整个实验过程中测定溶液的pH,pH的变化是_______ 。
【实验1】制备氯气。如图1是实验室制取纯净、干燥氯气装置图。

(1)M的名称是
(2)③中存放的试剂是
(3)⑤中反应的离子方程式是
【实验2】研究氯水性质。实验操作及现象如下表。
| 实验2﹣1 | 实验2﹣2 | |
| 实验操作(氯水均为新制) |  |  |
| 实验现象 | 溶液变蓝 | 石蕊溶液先变红,后褪色 |
(5)实验2﹣2中溶液变红是由于溶液中含有
(6)证明氯水中含有氯离子的方案是
(7)同学们发现久置的氯水会失去漂白性,溶液由黄绿色变为无色。为探究氯水失效的原因,进行实验:用强光照射盛有氯水的密闭广口瓶,并用传感器测定广口瓶中数据,得到如图2曲线。图中曲线变化的原因是

您最近一年使用:0次
2023-01-29更新
|
167次组卷
|
2卷引用:四川省宜宾市叙州区第二中学校2023-2024学年高一上学期1月期末化学试题
7 . 某同学用如图所示的装置进行铜与浓硫酸反应的实验。
(1)铜与浓硫酸反应的化学方程式是___________ 。
(2)实验过程中,观察到品红溶液褪色,石蕊溶液_________ (填现象),说明SO2________ (填选项)。
a.有氧化性 b.有还原性 c.有漂白性 d.水溶液显酸性
(3)为进一步确认产生的气体是二氧化硫气体,还应补充的操作是___________ 。
(4)结合离子方程式 说明试管D中氢氧化钠溶液的作用是___________ 。
(5)反应结束后取D中溶液进行以下实验:___________ 性。
②ⅱ中产生淡黄色沉淀的离子方程式为___________ 。
③ⅲ中无明显现象,甲同学通过检测 的生成证明Na2SO3和H2O2发生反应:取1 mL ⅲ中溶液于试管中,
的生成证明Na2SO3和H2O2发生反应:取1 mL ⅲ中溶液于试管中,___________ (填试剂和操作),产生白色沉淀。
乙同学认为甲同学的实验没有排除O2的影响,设计对比实验:___________ 。
综合甲、乙同学的实验可知,H2O2能将Na2SO3氧化。
(6)将装置C替换为下图所示装置,并用来比较碳和硅的非金属性。
已知:①酸性:H2SO3>H2CO3。
②硅酸为玻璃状无色透明的无定形颗粒,难溶于水和醇。___________ ,其作用是___________ 。
②能说明碳的非金属性比硅强的实验现象是___________ 。
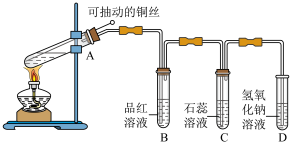
(1)铜与浓硫酸反应的化学方程式是
(2)实验过程中,观察到品红溶液褪色,石蕊溶液
a.有氧化性 b.有还原性 c.有漂白性 d.水溶液显酸性
(3)为进一步确认产生的气体是二氧化硫气体,还应补充的操作是
(4)
(5)反应结束后取D中溶液进行以下实验:
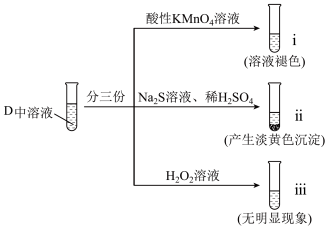
②ⅱ中产生淡黄色沉淀的离子方程式为
③ⅲ中无明显现象,甲同学通过检测
 的生成证明Na2SO3和H2O2发生反应:取1 mL ⅲ中溶液于试管中,
的生成证明Na2SO3和H2O2发生反应:取1 mL ⅲ中溶液于试管中,乙同学认为甲同学的实验没有排除O2的影响,设计对比实验:
综合甲、乙同学的实验可知,H2O2能将Na2SO3氧化。
(6)将装置C替换为下图所示装置,并用来比较碳和硅的非金属性。
已知:①酸性:H2SO3>H2CO3。
②硅酸为玻璃状无色透明的无定形颗粒,难溶于水和醇。
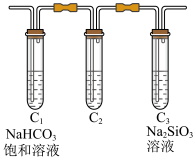
②能说明碳的非金属性比硅强的实验现象是
您最近一年使用:0次
2023-05-19更新
|
193次组卷
|
3卷引用:四川省华蓥中学2023-2024学年高一下学期4月月考化学试题



