名校
解题方法
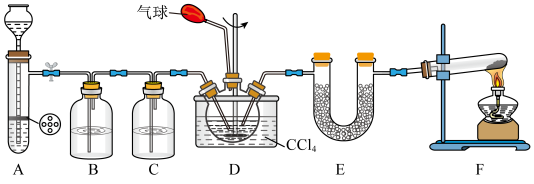
1 . 氨基甲酸铵(NH2COONH4)受热易分解,易与水反应分解,难溶于CCl4,设计如图所示装置制备氨基甲酸铵。已知: 。下列说法错误的是
。下列说法错误的是
 。下列说法错误的是
。下列说法错误的是
| A.A装置的优点是能够随时控制反应的发生和停止 |
| B.装置B、C、E中试剂可分别为饱和碳酸氢钠溶液、浓硫酸、CaCl2固体 |
| C.装置D使用热水浴 |
| D.装置F中所用试剂可为NH4Cl与熟石灰 |
您最近半年使用:0次
解题方法
2 . 实验室用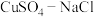 混合液与
混合液与 溶液反应制取
溶液反应制取 (装置如下图),已知溶液
(装置如下图),已知溶液 时产率最高,
时产率最高, 可发生反应:
可发生反应: ,
, 。
。

下列叙述正确的是
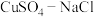 混合液与
混合液与 溶液反应制取
溶液反应制取 (装置如下图),已知溶液
(装置如下图),已知溶液 时产率最高,
时产率最高, 可发生反应:
可发生反应: ,
, 。
。
下列叙述正确的是
A.仪器2中所加试剂应为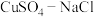 混合液或 混合液或 溶液 溶液 |
B. 与 与 溶液反应的离子方程式为 溶液反应的离子方程式为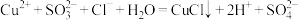 |
C.实验过程中用 混合溶液代替 混合溶液代替 溶液,可保证 溶液,可保证 产率较高 产率较高 |
| D.反应完成后需经稀释、过滤、洗涤、干燥后才可获得产品 |
您最近半年使用:0次
3 . 食盐补碘剂KIO₃的工业生产流程如图所示:
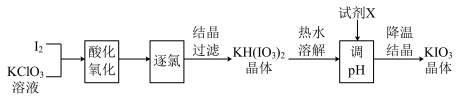
已知:“酸化氧化”后,溶液中主要含有 、
、 、
、 、
、 及少量氯气。下列说法正确的是
及少量氯气。下列说法正确的是

已知:“酸化氧化”后,溶液中主要含有
 、
、 、
、 、
、 及少量氯气。下列说法正确的是
及少量氯气。下列说法正确的是A.参与反应的 和 和 的物质的量之比为3∶5 的物质的量之比为3∶5 |
| B.“逐氯”可采用加热的方法,原理是气体的溶解度随温度升高而降低 |
| C.试剂X最适宜选用NaOH溶液 |
| D.实验室中进行过滤操作时,用到的硅酸盐仪器有烧杯、漏斗和玻璃棒 |
您最近半年使用:0次
名校
解题方法
4 . 一种以镉废渣(含CdO及少量ZnO、CuO和FeO)为原料制备镉(Cd)的流程如下:
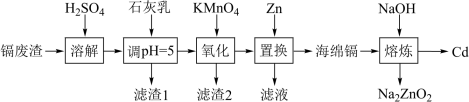
已知: 在酸性环境中被还原为
在酸性环境中被还原为 ,在弱酸性、弱碱性溶液中被还原为
,在弱酸性、弱碱性溶液中被还原为 ,在碱性环境中被还原为
,在碱性环境中被还原为 ;部分阳离子以氢氧化物形式沉淀时溶液pH如下。
;部分阳离子以氢氧化物形式沉淀时溶液pH如下。
下列说法正确的是

已知:
 在酸性环境中被还原为
在酸性环境中被还原为 ,在弱酸性、弱碱性溶液中被还原为
,在弱酸性、弱碱性溶液中被还原为 ,在碱性环境中被还原为
,在碱性环境中被还原为 ;部分阳离子以氢氧化物形式沉淀时溶液pH如下。
;部分阳离子以氢氧化物形式沉淀时溶液pH如下。 |  |  | |
| 开始沉淀时的pH | 2.7 | 6.3 | 3.8 |
| 完全沉淀时的pH | 3.2 | 8.3 | 5.0 |
| A.“调pH=5”可除去Fe和Cu等杂质 |
B.滤渣2的成分中含有 |
C.“置换”后滤液溶质主要成分是 和 和 |
| D.“熔炼”过程中有气体产生 |
您最近半年使用:0次
5 . 以电石渣[主要成分为Ca(OH)2和CaCO3]为原料制备KClO3的步骤如下:
步骤1:将电石渣与水混合,形成浆料。
步骤2:控制电石渣过量,75℃时向浆料中通入Cl2,该过程生成Ca(ClO)2,Ca(ClO)2进一步转化为Ca(ClO3)2,少量Ca(ClO)2分解为CaCl2和O2。氯化过程中Cl2转化为Ca(ClO3)2的总反应方程式为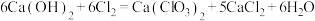 。充分反应后过滤。
。充分反应后过滤。
步骤3:向滤液中加入稍过量KCl固体,蒸发浓缩、冷却至25℃结晶,得KClO3。
下列说法正确的是
步骤1:将电石渣与水混合,形成浆料。
步骤2:控制电石渣过量,75℃时向浆料中通入Cl2,该过程生成Ca(ClO)2,Ca(ClO)2进一步转化为Ca(ClO3)2,少量Ca(ClO)2分解为CaCl2和O2。氯化过程中Cl2转化为Ca(ClO3)2的总反应方程式为
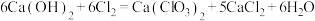 。充分反应后过滤。
。充分反应后过滤。步骤3:向滤液中加入稍过量KCl固体,蒸发浓缩、冷却至25℃结晶,得KClO3。
下列说法正确的是
A.控制通入 的速率,可以提高 的速率,可以提高 的利用率 的利用率 |
B.25℃时, 的溶解度比 的溶解度比 的溶解度大 的溶解度大 |
C.步骤2中,过滤所得滤液中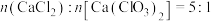 |
D.生成 的化学方程式为 的化学方程式为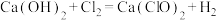 |
您最近半年使用:0次
2023-12-24更新
|
105次组卷
|
2卷引用:江苏省徐州市沛县四校联考2023-2024学年高一上学期12月月考化学试题
名校
解题方法
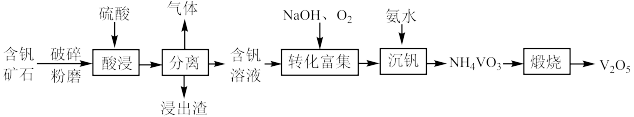
6 . 某含钒矿石(主要成分为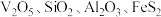 等)制取
等)制取 的流程如下:
的流程如下:
已知:①
②强酸性溶液中钒以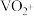 形式存在
形式存在
③ 易溶于水、
易溶于水、 难溶于水
难溶于水
下列说法错误的是
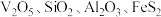 等)制取
等)制取 的流程如下:
的流程如下:
已知:①

②强酸性溶液中钒以
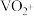 形式存在
形式存在③
 易溶于水、
易溶于水、 难溶于水
难溶于水下列说法错误的是
| A.破碎粉磨含钒矿石的目的是加快酸浸速率和溶出率 |
B.浸出渣的主要成分为 |
C.转化富集的目的是除去含钒溶液中的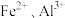 |
D.沉钒过程中发生反应的离子方程式为 |
您最近半年使用:0次
解题方法
7 . 以印刷线路板酸性蚀刻废液(含有 、
、 、
、 )为原料制备纳米CuO的流程如图:
)为原料制备纳米CuO的流程如图:
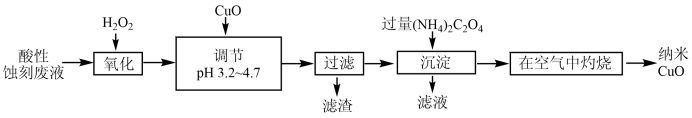
下列说法正确的是
 、
、 、
、 )为原料制备纳米CuO的流程如图:
)为原料制备纳米CuO的流程如图:
下列说法正确的是
A.“氧化”步骤发生的离子反应为: |
| B.“调节pH”步骤中不可用铁粉代替CuO |
| C.“过滤”步骤为加快速度可以用玻璃棒适当搅拌 |
D.“沉淀”步骤产生的沉淀 可不洗涤直接灼烧,不会影响产品质量 可不洗涤直接灼烧,不会影响产品质量 |
您最近半年使用:0次
名校
解题方法
8 . 铬和钒具有广泛用途。铬钒渣中铬和钒以低价态含氧酸盐形式存在,主要杂质为铁、铝、硅等的氧化物,从铬钒渣中分离提取铬和钒的一种流程如图所示。下列说法正确的是
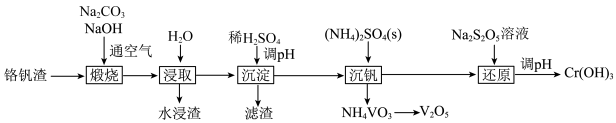
已知:①“煅烧”时铬、铝和硅的氧化物均转化为可溶性钠盐:
② 。
。

已知:①“煅烧”时铬、铝和硅的氧化物均转化为可溶性钠盐:
②
 。
。A.“煅烧”后的含铬化合物是 |
B.“滤渣”中只含有 |
C.“沉钒”时 固体可增大 固体可增大 的浓度,有利于沉淀的生成 的浓度,有利于沉淀的生成 |
D.“还原”工序中氧化剂和还原剂的物质的量之比为 |
您最近半年使用:0次
2023-12-03更新
|
355次组卷
|
2卷引用:山东省菏泽市2023-2024学年高三上学期期中化学试题
9 . 实验室利用SO2和Cl2在活性炭作用下制取SO2Cl2,原理为SO2(g)+Cl2(g)  SO2Cl2(l) ΔH=-97.3 kJ/mol。装置如图所示(部分装置已省略)。已知SO2Cl2的熔点为-54.1 ℃,沸点为69.1 ℃,遇水能发生剧烈反应并产生白雾。下列说法正确的是
SO2Cl2(l) ΔH=-97.3 kJ/mol。装置如图所示(部分装置已省略)。已知SO2Cl2的熔点为-54.1 ℃,沸点为69.1 ℃,遇水能发生剧烈反应并产生白雾。下列说法正确的是
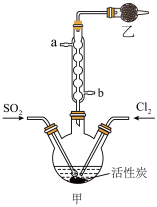
 SO2Cl2(l) ΔH=-97.3 kJ/mol。装置如图所示(部分装置已省略)。已知SO2Cl2的熔点为-54.1 ℃,沸点为69.1 ℃,遇水能发生剧烈反应并产生白雾。下列说法正确的是
SO2Cl2(l) ΔH=-97.3 kJ/mol。装置如图所示(部分装置已省略)。已知SO2Cl2的熔点为-54.1 ℃,沸点为69.1 ℃,遇水能发生剧烈反应并产生白雾。下列说法正确的是
| A.乙装置中盛放的试剂为无水氯化钙 | B.制备过程中需要将装置甲置于冰水浴中 |
| C.冷却水应该从b口进,a口出 | D.可用硝酸与亚硫酸钠反应制备二氧化硫 |
您最近半年使用:0次
名校
解题方法
10 . 锰酸钾(K2MnO4)在浓强碱溶液中可稳定存在,碱性减弱时易发生反应: 。利用Cl2氧化K2MnO4制备KMnO4的装置如图所示(夹持装置略)。下列说法错误的是
。利用Cl2氧化K2MnO4制备KMnO4的装置如图所示(夹持装置略)。下列说法错误的是
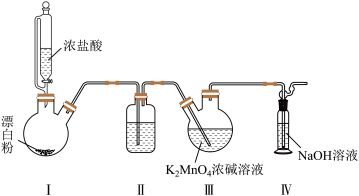
 。利用Cl2氧化K2MnO4制备KMnO4的装置如图所示(夹持装置略)。下列说法错误的是
。利用Cl2氧化K2MnO4制备KMnO4的装置如图所示(夹持装置略)。下列说法错误的是
| A.在强碱性环境下,氧化性:Cl2>KMnO4 |
| B.装置Ⅰ中的漂白粉可以用MnO2代替 |
| C.装置Ⅱ中盛放浓硫酸,以提高KMnO4的产率 |
| D.装置Ⅳ不需要防倒吸的原因是氢氧化钠溶液与氯气反应速率较慢 |
您最近半年使用:0次
2023-11-11更新
|
228次组卷
|
4卷引用:山东省青岛市第五十八中学2023-2024学年高一上学期10月月考化学试题



