解题方法
1 .  溶液在酸性条件下能与氧气反应。现有以下实验记录,回答下列问题:
溶液在酸性条件下能与氧气反应。现有以下实验记录,回答下列问题:
(1)该反应的离子方程式为_____________ 。
(2)该实验的目的是探究___________ 对反应速率的影响。
(3)实验试剂除了 溶液、
溶液、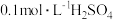 溶液外,还需要的指示剂是
溶液外,还需要的指示剂是________ 。实验仪器除了试管、试剂瓶、胶头滴管、温度计外,还需要的仪器是___________ 。
(4)上述实验操作中除了需要(3)的条件外,还必须控制不变的是________ (填字母)。
A.温度 B.指示剂的浓度 C.试剂的用量(体积) D.试剂添加的顺序
(5)由上述实验记录可得出的结论是温度每升高 ,反应速率增大为原来的
,反应速率增大为原来的____ 倍。
(6)若要进行酸性强弱对反应速率的影响的探究实验,你会采取的措施是_______ 。
 溶液在酸性条件下能与氧气反应。现有以下实验记录,回答下列问题:
溶液在酸性条件下能与氧气反应。现有以下实验记录,回答下列问题:| 实验编号 | ① | ② | ③ | ④ | ⑤ |
| 温度/℃ | 30 | 40 | 50 | 60 | 70 |
| 显色时间/s | 160 | 80 | 40 | 20 | 10 |
(2)该实验的目的是探究
(3)实验试剂除了
 溶液、
溶液、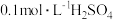 溶液外,还需要的指示剂是
溶液外,还需要的指示剂是(4)上述实验操作中除了需要(3)的条件外,还必须控制不变的是
A.温度 B.指示剂的浓度 C.试剂的用量(体积) D.试剂添加的顺序
(5)由上述实验记录可得出的结论是温度每升高
 ,反应速率增大为原来的
,反应速率增大为原来的(6)若要进行酸性强弱对反应速率的影响的探究实验,你会采取的措施是
您最近一年使用:0次
名校
解题方法
2 . 装置甲、乙、丙都是铁与水蒸气反应的实验装置,下列说法不正确的是
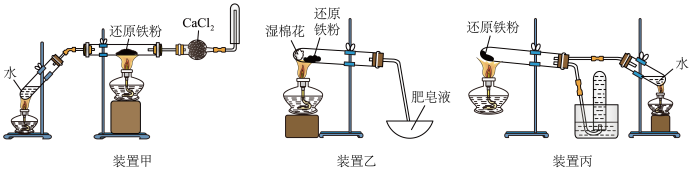

| A.选用丙装置,实验结束时先移去酒精灯,再将导气管拿出水面 |
| B.甲装置中氯化钙的作用是除去氢气中混有的水蒸气 |
| C.用乙装置实验时,蒸发皿中产生大量肥皂泡,点燃肥皂泡发出爆鸣声 |
| D.三个装置相比较,乙装置简单、操作简便、节约原料、安全性好 |
您最近一年使用:0次
2020-04-26更新
|
383次组卷
|
5卷引用:【校级联考】安徽省滁州市定远县西片区2018-2019学年高一上学期期中考试化学试题
3 . 下列有关实验的叙述完全正确的是
选项 | 实验用其或实验操作 | 目的或结论 |
A | 点燃插入到由MnO2、Al组成的铝热剂(混合物上有少量KClO3)上的镁条 | 证明还原性Al>Mn |
B | 将含有HCl、H2O(g)的Cl2依次通过盛有浓硫酸、饱和食盐水的洗气瓶 | 除去Cl2的杂质 |
C | 向某盐溶液X中先滴加几滴氯水、再滴2滴KSCN溶液 | 确定盐溶液X中是否含有Fe3+ |
D | 向某Na2SO3溶液中加入用盐酸酸化的Ba(NO3)2溶液 | 检验Na2SO3是否变质 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2019-12-04更新
|
164次组卷
|
2卷引用:河南省中原名校2020届高三上学期第四次质量考评化学试题
名校
4 . 下列实验装置、选用的试剂或实验操作中都正确的是( )
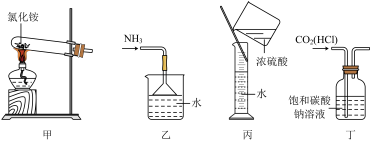

| A.实验室用装置甲制取氨 |
| B.用装置乙吸收氨,并防止倒吸 |
| C.用装置丙稀释浓硫酸 |
| D.用装置丁除去CO2中的HCl |
您最近一年使用:0次
2019-06-14更新
|
119次组卷
|
11卷引用:2016届河南省陕州中学高三上学期第一次月考化学试卷
2016届河南省陕州中学高三上学期第一次月考化学试卷2014-2015学年福建省晋江市季延中学高一下学期期中考试化学试卷2016届山东省华侨中学高三上学期开学考试化学试卷2016届山东省山东师范大学附属中学高三上学期一模化学试卷2016-2017学年山东省济南市历城区第二中学高一下学期开学考试化学试卷【全国名校大联考】2017-2018学年度高三第三次联考化学试题云南省文山州2018届高三毕业生复习统一检测理综化学试题陕西省榆林市高新完全中学2018-2019学年高一上学期第二次月考化学试题吉林省乾安县第七中学2018-2019学年高二下学期第三次质量检测化学试题山东省新泰二中2020届高三上学期第一阶段性测试化学试题甘肃省永昌县第一高级中学2021-2022学年高三上学期期中考试化学试题
名校
5 . 下列有关实验装置进行的相应实验,不能达到实验目的的是( )
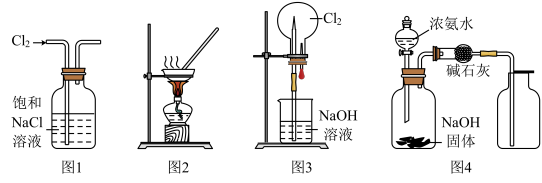

| A.用图1所示装置除去Cl2中含有的少量HCl |
| B.用图2所示装置蒸发KCl溶液制备无水KCl |
| C.用图3所示装置可以完成“喷泉”实验 |
| D.用图4所示装置制取干燥纯净的NH3 |
您最近一年使用:0次
2019-06-11更新
|
366次组卷
|
4卷引用:河南省商丘市第一高级中学2020届高三上学期期中考试化学试题
名校
6 . 实验室用Ca与H2反应制取氢化钙(CaH2)。下列实验装置和原理不能达到实验目的的是( )
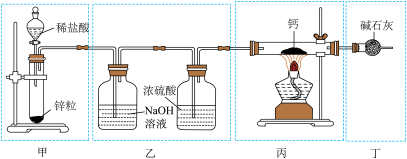

| A.装置甲制取H2 | B.装置乙净化干燥H2 |
| C.装置丙制取CaH2 | D.装置丁吸收尾气 |
您最近一年使用:0次
2019-05-24更新
|
1182次组卷
|
10卷引用:河南省洛阳市新安县第一高级中学2021届高三入学测试化学试题
河南省洛阳市新安县第一高级中学2021届高三入学测试化学试题【市级联考】江苏省苏锡常镇四市2019届高三下学期第三次模拟考试化学试题江苏省扬州中学2020届高三下学期4月考化学试题河南省洛阳市2021届高三5月第三次统一考试理综化学试题广东省广州市天河中学2021届高三上学期1月月考化学试题广东省汕头市金山中学2021届高三下学期学科素养测试化学试题(已下线)押全国卷理综第9题 化学实验基础-备战2021年高考化学临考题号押题(课标全国卷)天津市南开中学2021届高三年级高考模拟考试化学试题(已下线)卷12 化学综合实验选择题-【小题小卷】冲刺2022年高考化学小题限时集训(新高考专用)湖南省益阳市沅江市第一中学2022届高三下学期第二次模拟考试试题
名校
7 . 用下列实验方案及所选玻璃容器就能实现相应实验目的的是
| 选项 | 实验目的 | 实验方案 | 所选玻璃仪器 |
| A | 分离乙醇、乙酸乙酯混合物 | 向混合物中加入水,混合后振荡,然后静置分液 | 分液漏斗、烧杯 |
| B | 检验蔗糖是否水解 | 向蔗糖溶液中加入几滴稀硫酸,水浴加热几分钟,再向其中加入新制的银氨溶液,并水浴加热 | 试管、烧杯、酒精灯、胶头滴管 |
| C | 证明乙醇发生消去反应生成乙烯 | 将乙醇与浓硫酸混合加热到170 ℃,将产生的气体通入溴水 | 酒精灯、圆底烧瓶、导管、 试管 |
| D | 分离乙醇和苯酚 | 向混合物中加入NaOH溶液,混合后振荡,然后静置分液 | 分液漏斗、烧杯 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
12-13高一上·吉林长春·期末
名校
8 . 下列方法中,不能用于实验室里制取氨气的是
| A.在试管中将熟石灰和氯化铵混合后加热 |
| B.加热试管中的氯化铵固体 |
| C.将烧瓶中的浓氨水加热 |
| D.将分液漏斗中的浓氨水滴入装有生石灰的烧瓶中 |
您最近一年使用:0次
2019-04-23更新
|
534次组卷
|
14卷引用:河南省永城市实验高级中学2018-2019学年高一下学期3月月考化学试题
河南省永城市实验高级中学2018-2019学年高一下学期3月月考化学试题(已下线)2011-2012学年吉林省长春外国语学校高一上学期期末考试文科化学试卷(已下线)2011-2012学年河北省石家庄市高一上学期期末考试化学试卷2016届河北省衡水市冀州中学高三复习班上月考化学试卷2015-2016学年广东省佛山一中高一下期中化学试卷2016-2017学年广西桂林市第十八中学高一下学期开学考化学试卷2016-2017学年河北省邯郸市成安县第一中学高一下学期第一次月考化学试卷【全国百强校】黑龙江省哈尔滨市第三中学2018-2019学年高一下学期第一次阶段性测试化学试题吉林省辉南县第一中学2018-2019学年高一下学期第一次月考化学试题【全国百强校】内蒙古自治区杭锦后旗奋斗中学2018-2019学年高一下学期期中考试化学试题【校级联考】黑龙江省哈尔滨市呼兰一中、阿城二中、宾县三中、尚志五中四校2018-2019学年高一下学期期中考试(呼兰用卷)化学试题新疆巴楚县第一中学2019-2020学年高一上学期期末考试化学试题(已下线)5.2.2 氨和铵盐——同步学习必备知识四川省甘孜州康定中学2022-2023学年高一下学期3月月考化学试题
9 . 实验室欲用Cu片和浓HNO3反应制取适量NO2气体,下图中最适合完成该实验的简易装置是
A.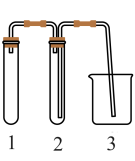 | B.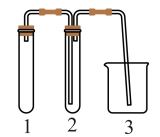 |
C.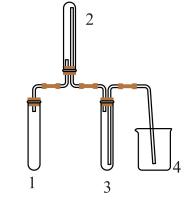 | D.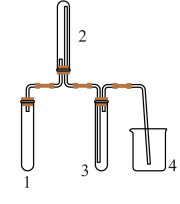 |
您最近一年使用:0次
10 . 某化学实验小组从商店买回的浓硫酸试剂标签的部分内容破损。由于试剂瓶口密封签已破损,他们怀疑该硫酸的质量分数与标签不符,决定开展研究。部分破损标签内容为硫酸:化学纯(CP) 品名:硫酸, 化学式:H2SO4相对分子质量:98,质量分数:98% 密度:1.84g/cm3。甲同学认为,可以用一种精密仪器测量该溶液的c(H+),若c(H+)=36.8 mol·L-1,则该溶液的质量分数为98%。乙同学认为,即使有精密的仪器,甲同学的方案也不行,建议用重量分析法来测定。具体设想:取一定体积的该硫酸与足量氯化钡溶液反应,过滤、洗涤、干燥沉淀,称量沉淀的质量。丙同学则建议用中和滴定法进行测定,设想如下:①准确量取一定体积的硫酸,用适量的水稀释;②往稀释后的溶液中滴入几滴指示剂;③用碱式滴定管量取标准浓度的氢氧化钠溶液滴定,直到出现滴定终点为止;④记录消耗的氢氧化钠溶液的体积。
请回答下列问题:
(1)乙同学推测甲同学的方案不可行的理由是_____________________________________
(2)乙同学的方案的关键操作有两点:①确保SO42-完全沉淀;②洗涤沉淀,确保沉淀不含杂质。在实际中,请设计简单实验检验SO42-是否完全沉淀:____________________________
检验沉淀是否洗净的操作方法是__________________________________________________ ;
(3)在丙同学的方案中步骤②用到的指示剂是____________ ;达到滴定终点的标志是______________________________________________________________________________ 。
(4)丙同学的方案中,下列操作使测定结果偏小的是_____________ 。
①在滴定前未用NaOH标准溶液润洗滴定管,②滴定前滴定管尖嘴部分有气泡,滴定后滴定管尖嘴部分仍有气泡,③锥形瓶用蒸馏水洗净后,没有用待测液润洗,④滴定前,仰视读数,滴定后,仍仰视读数,⑤滴定前,仰视读数,滴定后,俯视读数
(5)丙同学在实验中,分别取等体积原硫酸,用NaOH溶液滴定三次,终点时,得到的NaOH溶液体积如下表所示:
通过计算,该浓硫酸物质的量浓度为____________________________________________ 。是否与标签上表示的溶质质量分数相同___________ (填“是”或“否”)
请回答下列问题:
(1)乙同学推测甲同学的方案不可行的理由是
(2)乙同学的方案的关键操作有两点:①确保SO42-完全沉淀;②洗涤沉淀,确保沉淀不含杂质。在实际中,请设计简单实验检验SO42-是否完全沉淀:
检验沉淀是否洗净的操作方法是
(3)在丙同学的方案中步骤②用到的指示剂是
(4)丙同学的方案中,下列操作使测定结果偏小的是
①在滴定前未用NaOH标准溶液润洗滴定管,②滴定前滴定管尖嘴部分有气泡,滴定后滴定管尖嘴部分仍有气泡,③锥形瓶用蒸馏水洗净后,没有用待测液润洗,④滴定前,仰视读数,滴定后,仍仰视读数,⑤滴定前,仰视读数,滴定后,俯视读数
(5)丙同学在实验中,分别取等体积原硫酸,用NaOH溶液滴定三次,终点时,得到的NaOH溶液体积如下表所示:
| 实验序号 | 硫酸体积 | NaOH溶液体积 | NaOH溶液浓度 |
| ① | 5.00 mL | 35.65 mL | 5.00 mol·L-1 |
| ② | 5.00 mL | 39.65 mL | 5.00 mol·L-1 |
| ③ | 5.00 mL | 35.55 mL | 5.00mol·L-1 |
您最近一年使用:0次
2019-02-14更新
|
135次组卷
|
2卷引用:河南省南阳市2020-2021学年高二上学期期末考试化学试题



