20. 碳、氮及其化合物在生产中有重要应用。
(1)700℃时,若向2L体积恒定的密闭容器中充入一定量N
2和CO
2发生反应:N
2(g)+CO
2(g)

C(s)+2NO(g);其中N
2、NO物质的量随时间变化的曲线如下图所示。
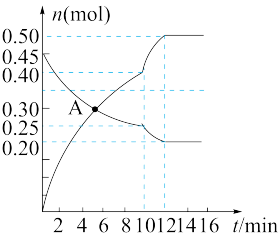
请回答下列问题。
①0~10min内的CO
2平均反应速率
v=
______。
②第10 min时,外界改变的条件可能是
______。
A.加催化剂
B.增大C(s)的物质的量
C.减小CO
2的物质的量
D.升温
E.降温
(2)100kPa时,反应2NO(g)+O
2(g)

2NO
2(g)中NO的平衡转化率与温度的关系曲线如图1,反应2NO
2(g)

N
2O
4(g)中NO
2的平衡转化率与温度的关系曲线如图2。
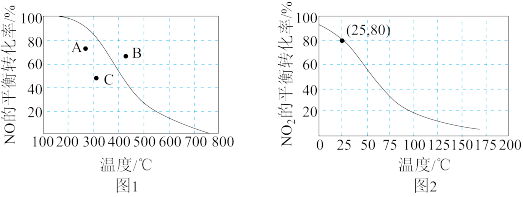
①图1中A、B、C三点表示不同温度、压强下,2NO(g)+O
2(g)

2NO
2(g)达到平衡时NO的转化率,则
_______点对应的压强最大。
②100kPa、25℃时,2NO
2(g)

N
2O
4(g),计算平衡常数
Kp=
______。(
Kp用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)
③100kPa、25℃时,VmLNO与0.5VmLO
2混合后最终气体的体积为
__________mL。
(3)室温下,用注射器吸入一定量NO
2气体,将针头插入胶塞密封(如图3),
然后迅速将气体体积压缩为原来的一半并使活塞固定,此时手握针筒有热感,继续放置一段时间。从活塞固定时开始观察,气体颜色逐渐
_______________(填“变深”或“变浅”)。[已知:2NO
2(g)

N
2O
4(g)在几微秒内即可达到化学平衡]
(4)在压强为0.1MPa条件,将CO和H
2的混合气体在催化剂作用下转化为甲醇的反应为CO(g)+2H
2(g)

CH
3OH(g) Δ
H<0
①下列能说明该反应达到平衡状态的是
________________。
A.混合气体的密度不再变化
B.CO和H
2的物质的量之比不再变化
C.
v(CO)=
v(CH
3OH) D.CO在混合气中的质量分数保持不变
②
T1℃时,在一个体积为5L的恒压容器中充入1molCO、2molH
2,经过5min达到平衡,CO的转化率为0.75,则
T1℃时,CO(g)+2H
2(g)

CH
3OH(g)的平衡常数
K=
_______。