10. 绿色能源是未来能源发展的重要方向,氢能是重要的绿色能源,利用生物乙醇来制取氢气的部分反应过程如下图所示。

(1)已知:CH
3CH
2OH(g)+3H
2O(g)=2CO
2(g)+6H
2(g) ΔH
1=+173.5kJ·mol
-1反应Ⅱ:CO(g)+H
2O(g)=CO
2(g)+H
2(g) ΔH
2=-41.2kJ·mol
-1则反应Ⅰ的热化学方程式为
___________。
(2)反应Ⅱ在不同进气比[n(CO)∶n(H
2O)]、不同温度下,测得相应的CO平衡转化率见下表(各点对应的其他反应条件都相同)。
| 平衡点 | a | b | c | d |
| n(CO)∶n(H2O) | 0.5 | 0.5 | 1 | 1 |
| CO平衡转化率/% | 50 | 66.7 | 50 | 60 |
①a点平衡混合物中H
2的体积分数为
___________,a、c两点对应的反应温度T
a___________T
c(填“<”“=”或“>”),d点对应的平衡常数K=
___________。
②有利于提高CO平衡转化率的是
___________(填标号)。
A.增大压强
B.降低温度
C.增大进气比[n(CO)∶n(H
2O)] D.分离出CO
2(3)反应Ⅱ在工业上称为一氧化碳的催化变换反应,若用[K]表示催化剂,则反应历程可用下式表示:
第一步:[K]+H
2O(g)=[K]O+H
2第二步:[K]O+CO=[K]+CO
2第二步比第一步反应慢,则第二步反应的活化能比第一步反应
___________。反应过程中,相对能量最高的中间产物是催化剂吸附态的
___________(填标号)。
A.水蒸气
B.氧原子
C.一氧化碳
D.二氧化碳
(4)研究表明,CO催化变换反应的速率方程为v=k(

)式中,

分别表示相应的物质的量分数,K
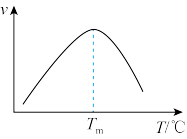
p为平衡常数,k为反应的速率常数,温度升高时k值增大。在气体组成和催化剂一定的情况下,反应速率随温度变化的曲线如图所示。温度升高时,CO催化变换反应的K
p___________(填“增大”“减小”)。根据速率方程分析,T>T
m时v逐渐减小的原因是
___________。