湖南省长沙市明达中学2022届高三上学期入学考试化学试题
湖南
高三
开学考试
2021-12-13
195次
整体难度:
适中
考查范围:
常见无机物及其应用、化学与STSE、认识化学科学、化学实验基础、化学反应原理、有机化学基础、物质结构与性质
湖南省长沙市明达中学2022届高三上学期入学考试化学试题
湖南
高三
开学考试
2021-12-13
195次
整体难度:
适中
考查范围:
常见无机物及其应用、化学与STSE、认识化学科学、化学实验基础、化学反应原理、有机化学基础、物质结构与性质
一、单选题 添加题型下试题
单选题
|
较易(0.85)
解题方法
1. 近年来,中国在探索太空、开发深海、高铁和桥梁建设、5G技术研发和推广等方面取得举世瞩目的成就。它们与化学有着密切联系。下列说法不正确的是
| A.5G手机上使用的7nm芯片的主要成分是晶体硅 |
| B.“蛟龙号”深海探测器外表面使用的是钛合金材料,钛合金属于金属材料 |
| C.“天问一号”探测器搭载的太阳能帆板,是一种将光能转化为电能的原电池装置 |
| D.高铁车厢的制造采用了大量先进复合材料,使车厢轻量化并具有优异的耐腐蚀特性 |
您最近一年使用:0次
2020-10-18更新
|
164次组卷
|
2卷引用:吉林省梅河口市第五中学、辽源市第五中学、四平市第四中学2021届高三上学期第一次联考化学试题
单选题
|
容易(0.94)
解题方法
2. 化学与生活密切相关。下列应用中与氧化还原反应有关的是
| A.“84”消毒液消毒 | B.明矾净水 |
| C.熟石灰改良酸性土壤 | D.木炭作冰箱除味剂 |
您最近一年使用:0次
2020-10-18更新
|
133次组卷
|
2卷引用:吉林省梅河口市第五中学、辽源市第五中学、四平市第四中学2021届高三上学期第一次联考化学试题
二、多选题 添加题型下试题
多选题
|
较易(0.85)
3. 实验室以石灰石为原料,制备CO2并获得CaCl2·6H2O晶体。下列装置使用不正确的是
A. | B. |
C. | D. |
您最近一年使用:0次
三、单选题 添加题型下试题
单选题
|
较易(0.85)
4. 制备少量羟基乙酸钠的反应为ClCH2COOH+2NaOH→HOCH2COONa+NaCl+H2O。下列表示相关微粒的化学用语不正确的是
A.中子数为20的氯原子: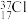 |
B.Na+的结构示意图: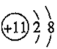 |
C.ClCH2COOH的结构式: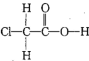 |
D.H2O的电子式: |
您最近一年使用:0次
单选题
|
较易(0.85)
解题方法
5. 下表中物质的分类组合完全正确的是
选项 | A | B | C | D |
强电解质 | Ca(OH)2 | 盐酸 | HClO4 | BaSO4 |
弱电解质 | HF | Ca(ClO)2 | CH3COOH | NH4Cl |
非电解质 | SO3 | H2S | Cl2 | 乙醇 |
| A.A | B.B | C.C | D.D |
【知识点】 非电解质、电解质物质类别判断解读 强电解质与弱电解质解读
您最近一年使用:0次
2020-10-18更新
|
168次组卷
|
2卷引用:吉林省梅河口市第五中学、辽源市第五中学、四平市第四中学2021届高三上学期第一次联考化学试题
单选题
|
较难(0.4)
解题方法
6. 下列描述中所发生化学反应对应的离子方程式正确的是
A.KClO的碱性溶液与Fe(OH)3反应:3ClO-+2Fe(OH)3=2 +3Cl-+4H++H2O +3Cl-+4H++H2O |
B.将二氧化硫通入氯化铁溶液中:SO2+2Fe3++2H2O= +2Fe2++4H+ +2Fe2++4H+ |
| C.向溴化亚铁溶液中通入足量氯气:2Fe2++Cl2=2Fe3++2Cl- |
D.用酸性高锰酸钾标准溶液滴定草酸:2 +16H++5 +16H++5 =2Mn2++10CO2↑+8H2O =2Mn2++10CO2↑+8H2O |
您最近一年使用:0次
2020-10-18更新
|
405次组卷
|
2卷引用:吉林省梅河口市第五中学、辽源市第五中学、四平市第四中学2021届高三上学期第一次联考化学试题
单选题
|
适中(0.65)
7. 下表所列各组物质中,能一步实现如图所示转化关系的是
| 选项 | X | Y | Z | W | 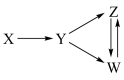 |
| A | NH3 | N2 | HNO3 | NO2 | |
| B | Al | Al2O3 | Al(OH)3 | AlCl3 | |
| C | Na | Na2O2 | NaOH | Na2CO3 | |
| D | H2S | S | SO2 | SO3 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
较易(0.85)
8. NA为阿伏加 德罗常数的值,下列叙述正确的是
| A.40g正丁烷和18g异丁烷的混合物中共价键数目为13NA |
| B.NA个NH3分子溶于1L水中,所得溶液的物质的量浓度为1mol·L-1 |
| C.标准状况下,22.4LCHCl3中所含的分子数为NA |
| D.25℃时,1LpH=2的H2SO4溶液中含有H+的数目为0.02NA |
您最近一年使用:0次
2020-10-18更新
|
80次组卷
|
2卷引用:吉林省梅河口市第五中学、辽源市第五中学、四平市第四中学2021届高三上学期第一次联考化学试题
单选题
|
较易(0.85)
解题方法
9. 下列有关物质的性质和应用对应不正确的是
| 性质 | 应用 | |
| A | 阿司匹林含有羧基,显酸性 | 服用阿司匹林出现水杨酸反应时,可用小苏打溶液解毒 |
| B | BaSO4不溶于水,不溶于酸 | 在医疗上进行胃部造影前,BaSO4用作患者服用的“钡餐” |
| C | K2FeO4具有强氧化性,还原产物Fe3+易水解生成Fe(OH)3胶体 | 可作新型净水剂 |
| D | 福尔马林是35%-40%的甲醛水溶液,能使蛋白质变性 | 可用于食品保鲜 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
较易(0.85)
解题方法
10. 前四周期元素X、Y、Z、W、T的原子序数依次增大,Y、Z、W位于同—周期,通常用X元素的某种同位素来确定文物的年代,Y的原子半径在同周期元素中最大,在同周期元素的简单离子中,元素Z形成的离子半径最小,W的常见单质为气体,T元素的单质是目前用量最大的金属。下列说法不正确的是
| A.X的氢化物的沸点一定比W的氢化物的沸点低 |
| B.Y、Z、W的最高价氧化物对应的水化物相互间能反应 |
| C.T的单质在W2中点燃可得化合物TW3 |
| D.Y的氧化物均可溶于水且所得水溶液显碱性 |
【知识点】 元素周期律、元素周期表的推断
您最近一年使用:0次
四、多选题 添加题型下试题
多选题
|
较易(0.85)
解题方法
11. 某研究以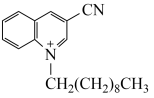 为有机光催化剂,对甲苯进行了二氧两相光催化氧化以获取苯甲醛和苯甲醇,同时还可以制备较高浓度的H2O2溶液,反应过程如图所示。下列说法正确的是
为有机光催化剂,对甲苯进行了二氧两相光催化氧化以获取苯甲醛和苯甲醇,同时还可以制备较高浓度的H2O2溶液,反应过程如图所示。下列说法正确的是
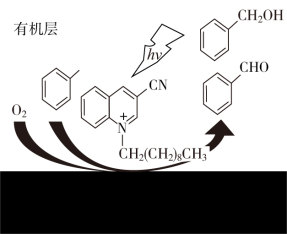
 为有机光催化剂,对甲苯进行了二氧两相光催化氧化以获取苯甲醛和苯甲醇,同时还可以制备较高浓度的H2O2溶液,反应过程如图所示。下列说法正确的是
为有机光催化剂,对甲苯进行了二氧两相光催化氧化以获取苯甲醛和苯甲醇,同时还可以制备较高浓度的H2O2溶液,反应过程如图所示。下列说法正确的是
A.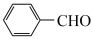 属于芳香烃 属于芳香烃 |
| B.该反应不适宜在高温条件下进行 |
C.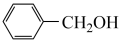 分子中所有原子均在同一平面内 分子中所有原子均在同一平面内 |
D.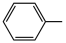 的一氯代物有4种 的一氯代物有4种 |
【知识点】 同分异构体的数目的确定解读 有机分子中原子共面的判断解读
您最近一年使用:0次
12. 水热法制备Fe3O4纳米颗粒的反应:3Fe2++2S2O32-+O2+xOH-=Fe3O4+S4O62-+2H2O,下列说法正确的是:
| A.反应方程式中x=4 |
| B.此反应中,氧化剂为O2,将Fe元素全部氧化 |
| C.每生成1 mol Fe3O4,该反应共转移电子4 mol |
| D.反应中S元素的价态未发生变化 |
【知识点】 氧化还原反应有关计算 氧化还原反应方程式的配平解读
您最近一年使用:0次
2019-12-05更新
|
129次组卷
|
2卷引用:山东省德州市2020届高三上学期期中考试化学试题
多选题
|
较难(0.4)
名校
13. 某科学课题小组通过在催化剂作用下,使用K2S2O8、Ce(NH4)2(NO3)6等氧化剂实现了甲烷向乙烷的转化(CH3COCH3为溶剂,总量几乎不变)。下列说法不正确的是


| A.该催化循环中Pd的成键数目没有发生变化 |
| B.氧化剂Ce(NH4)2(NO3)6中Ce的化合价为+2价 |
| C.在还原消除反应中,有CH3COCH3生成 |
D. 为中间产物 为中间产物 |
您最近一年使用:0次
2021-11-06更新
|
492次组卷
|
3卷引用:湖南省长沙市明达中学2022届高三上学期入学考试化学试题
五、单选题 添加题型下试题
单选题
|
适中(0.65)
14. 常温下,往饱和H2S溶液中滴加NaOH溶液,H2S、HS-、S2-三种微粒的物质的量分数[ ]随溶液pH变化的关系如图所示。下列说法正确的是
]随溶液pH变化的关系如图所示。下列说法正确的是

 ]随溶液pH变化的关系如图所示。下列说法正确的是
]随溶液pH变化的关系如图所示。下列说法正确的是
| A.在同一溶液中,H2S、HS-、S2-可以大量共存 |
B.反应2H++S2- H2S K=10-6.1 H2S K=10-6.1 |
| C.在滴加NaOH溶液的过程中,始终存在c(Na+)>c(HS-)>c(H+)>c(S2-)>c(OH-) |
| D.加入NaOH溶液的过程中,始终有c(Na+)+c(H+)=c(OH-)+2c(S2-)+c(HS-) |
您最近一年使用:0次
六、解答题 添加题型下试题
解答题-工业流程题
|
适中(0.65)
15. 钯属于稀有贵金属(铂族金属),钯在工业上的主要用途是作为催化剂,从含钯电子废料直接制备钯精细化工产品的工艺流程图如下:

已知:Ksp(AgCl)=1.8×10-10.回答下列问题:
(1)含钯电子废料的预处理包括筛选和焚烧等必要步骤,焚烧的目的是___________ 。
(2)钯易溶于硝酸,溶解时既要考虑浸出速率和浸出率,又要注意成本。使用25%的硝酸,浸取2h,钯的浸出率与温度的关系如图所示,则选择浸出的温度为___________ ℃。酸浸”后过滤,洗净滤渣,滤渣中可能含有铂、铑和金等其他贵金属,应___________ 。

(3)“除银赶硝”后的溶液中Cl-的浓度为0.15mol·L-1,则溶液中Ag+的浓度为___________ 。
(4)“除银赶硝”后的溶液中含钯成分为H2PdCl4,加热溶液到80~90℃,不断搅拌并滴加氨水,控制溶液的pH<7.5,使溶液中的钯变成肉红色的氯亚钯酸四氨络合亚钯[Pd(NH3)4·PdCl4]沉淀,写出反应的化学方程式:___________ 。
(5)在搅拌下滴加浓盐酸至溶液pH=1~1.5,此时溶液中出现大量黄色絮状沉淀,继续搅拌1h,静置沉降,过滤,用去离子水反复清洗沉淀,所得固体即为二氯化二氨合钯(Ⅱ)[Pd(NH3)2Cl2],用去离子水反复清洗沉淀的原因是___________ 。

已知:Ksp(AgCl)=1.8×10-10.回答下列问题:
(1)含钯电子废料的预处理包括筛选和焚烧等必要步骤,焚烧的目的是
(2)钯易溶于硝酸,溶解时既要考虑浸出速率和浸出率,又要注意成本。使用25%的硝酸,浸取2h,钯的浸出率与温度的关系如图所示,则选择浸出的温度为

(3)“除银赶硝”后的溶液中Cl-的浓度为0.15mol·L-1,则溶液中Ag+的浓度为
(4)“除银赶硝”后的溶液中含钯成分为H2PdCl4,加热溶液到80~90℃,不断搅拌并滴加氨水,控制溶液的pH<7.5,使溶液中的钯变成肉红色的氯亚钯酸四氨络合亚钯[Pd(NH3)4·PdCl4]沉淀,写出反应的化学方程式:
(5)在搅拌下滴加浓盐酸至溶液pH=1~1.5,此时溶液中出现大量黄色絮状沉淀,继续搅拌1h,静置沉降,过滤,用去离子水反复清洗沉淀,所得固体即为二氯化二氨合钯(Ⅱ)[Pd(NH3)2Cl2],用去离子水反复清洗沉淀的原因是
您最近一年使用:0次
解答题-原理综合题
|
较难(0.4)
名校
解题方法
16. C、N、S的氧化物常会造成一些环境问题,科研工作者正在研究用各种化学方法来消除这些物质对环境的影响。
(1)CO2的重整用CO2和H2为原料可得到CH4燃料。
已知:①CH4(g)+CO2(g)=2CO(g)+2H2(g) ΔH1=+247kJ/mol
②CH4(g)+H2O(g)=CO(g)+3H2(g) ΔH2=+205kJ/mol
写出CO2重整的热化学方程式:___________ 。
(2)“亚硫酸盐法”吸收烟气中的SO2
①将烟气通入1.0mol/L的Na2SO3溶液,若此过程中溶液体积不变,则溶液的pH不断___________ (填“减小”“不变”或“增大)。当溶液pH约为6时,吸收SO2的能力显著下降,应更换吸收剂,此时溶液中c(SO )=0.2mol/L,则溶液中c(HSO
)=0.2mol/L,则溶液中c(HSO )=
)=___________ 。
②室温条件下,将烟气通入(NH4)2SO3溶液中,测得溶液pH与各组分物质的量分数的变化关系如图:
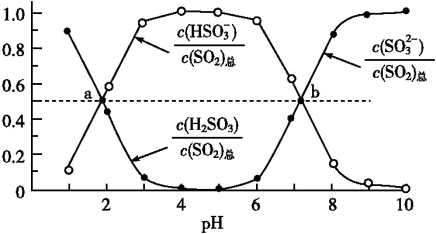
b点时溶液pH=7,则n(NH )∶n(HSO
)∶n(HSO )=
)=___________ 。
(3)催化氧化法去除NO。一定条件下,用NH3消除NO污染,其反应原理:4NH3+6NO 5N2+6H2O。不同温度条件下,n(NH3)∶n(NO)的物质的量之比分别为4∶1,3∶1,1∶3时,得到NO脱除率曲线如图所示:
5N2+6H2O。不同温度条件下,n(NH3)∶n(NO)的物质的量之比分别为4∶1,3∶1,1∶3时,得到NO脱除率曲线如图所示:
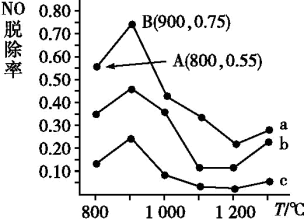
①曲线a中,NO的起始浓度为6×10−4mg·m−3,从A点到B点经过0.8s,该时间段内NO的脱除速率为___________ mg·m−3·s−1。
②曲线b对应NH3与NO的物质的量之比是___________ 。
(4)间接电化学法除NO。其原理如图所示:

写出阴极的电极反应式(阴极室溶液呈酸性):___________
(1)CO2的重整用CO2和H2为原料可得到CH4燃料。
已知:①CH4(g)+CO2(g)=2CO(g)+2H2(g) ΔH1=+247kJ/mol
②CH4(g)+H2O(g)=CO(g)+3H2(g) ΔH2=+205kJ/mol
写出CO2重整的热化学方程式:
(2)“亚硫酸盐法”吸收烟气中的SO2
①将烟气通入1.0mol/L的Na2SO3溶液,若此过程中溶液体积不变,则溶液的pH不断
 )=0.2mol/L,则溶液中c(HSO
)=0.2mol/L,则溶液中c(HSO )=
)=②室温条件下,将烟气通入(NH4)2SO3溶液中,测得溶液pH与各组分物质的量分数的变化关系如图:

b点时溶液pH=7,则n(NH
 )∶n(HSO
)∶n(HSO )=
)=(3)催化氧化法去除NO。一定条件下,用NH3消除NO污染,其反应原理:4NH3+6NO
 5N2+6H2O。不同温度条件下,n(NH3)∶n(NO)的物质的量之比分别为4∶1,3∶1,1∶3时,得到NO脱除率曲线如图所示:
5N2+6H2O。不同温度条件下,n(NH3)∶n(NO)的物质的量之比分别为4∶1,3∶1,1∶3时,得到NO脱除率曲线如图所示:
①曲线a中,NO的起始浓度为6×10−4mg·m−3,从A点到B点经过0.8s,该时间段内NO的脱除速率为
②曲线b对应NH3与NO的物质的量之比是
(4)间接电化学法除NO。其原理如图所示:

写出阴极的电极反应式(阴极室溶液呈酸性):
【知识点】 化学反应原理综合考查解读
您最近一年使用:0次
2021-11-06更新
|
179次组卷
|
2卷引用:湖南省长沙市明达中学2022届高三上学期入学考试化学试题
解答题-实验探究题
|
适中(0.65)
解题方法
17. ClCH2COOH(氯乙酸,熔点为50℃)是一种化工原料,实验室制备氯乙酸的装置如图:

按下列实验步骤回答问题:
(1)在500mL三颈烧瓶中放置300g冰醋酸和15g催化剂乙酸酐。加热至105℃时,开始徐徐通入干燥纯净的氯气。加热的方法是___________ ,仪器X的名称是___________ 。
(2)氯气通入冰醋酸中呈黄色随即黄色褪去,用化学方程式解释黄色褪去的原因:___________ ,控制通入氯气速率的方法是___________ ,NaOH溶液的主要作用是___________ 。
(3)反应约需10小时,每隔2小时向三颈烧瓶中加入5g乙酸酐,当取出样品测得其___________ 时,停止通入氯气。
(4)将熔融的生成物移至蒸馏瓶中进行蒸馏纯化,收集186~188℃馏分。蒸馏操作最好选择装置b,原因是___________ 。
a. b.
b.

按下列实验步骤回答问题:
(1)在500mL三颈烧瓶中放置300g冰醋酸和15g催化剂乙酸酐。加热至105℃时,开始徐徐通入干燥纯净的氯气。加热的方法是
(2)氯气通入冰醋酸中呈黄色随即黄色褪去,用化学方程式解释黄色褪去的原因:
(3)反应约需10小时,每隔2小时向三颈烧瓶中加入5g乙酸酐,当取出样品测得其
(4)将熔融的生成物移至蒸馏瓶中进行蒸馏纯化,收集186~188℃馏分。蒸馏操作最好选择装置b,原因是
a.
 b.
b.
您最近一年使用:0次
解答题-结构与性质
|
适中(0.65)
名校
18. 铜是人类知道最早的金属之一,也是广泛使用的第一种金属。回答下列问题:
(1)镍白铜(铜镍合金)可用于制作仿银饰品。第二电离能I2(Cu)___________ (填“>”或“<”)I2(Ni),其原因为___________ 。
(2)向[Cu(NH3)2]Cl溶液中通入乙炔(C2H2)气体,可生成红棕色沉淀Cu2C2。
①C2H2分子中σ键与π键的数目之比为___________ ;碳原子的杂化方式为___________ ;
②写出与Cu2C2中阴离子C 互为等电子体的一种分子:
互为等电子体的一种分子:___________ 。
(3)乙二胺(H2N-CH2CH2-NH2)易与Cu2+形成络合物,用于Cu2+的定量测定。
①形成的络合物中提供孤对电子的原子为___________ (填元素符号)。
②乙二胺中所含元素的电负性由大到小的顺序为___________ 。
(4)铜与氧构成的某种化合物的立方晶胞如图甲所示,图乙是沿晶胞对角面取得的截图,晶胞中所有原子均在对角面上。氧原子的配位数为___________ ,若Cu原子之间最短距离为dpm,阿伏加德罗常数的值为NA,该晶体的密度为___________ g•cm-3(列出计算式即可)。

(1)镍白铜(铜镍合金)可用于制作仿银饰品。第二电离能I2(Cu)
(2)向[Cu(NH3)2]Cl溶液中通入乙炔(C2H2)气体,可生成红棕色沉淀Cu2C2。
①C2H2分子中σ键与π键的数目之比为
②写出与Cu2C2中阴离子C
 互为等电子体的一种分子:
互为等电子体的一种分子:(3)乙二胺(H2N-CH2CH2-NH2)易与Cu2+形成络合物,用于Cu2+的定量测定。
①形成的络合物中提供孤对电子的原子为
②乙二胺中所含元素的电负性由大到小的顺序为
(4)铜与氧构成的某种化合物的立方晶胞如图甲所示,图乙是沿晶胞对角面取得的截图,晶胞中所有原子均在对角面上。氧原子的配位数为

您最近一年使用:0次
2021-11-06更新
|
100次组卷
|
2卷引用:湖南省长沙市明达中学2022届高三上学期入学考试化学试题
解答题-有机推断题
|
适中(0.65)
19. 某抗肿瘤药物的有效成分为E,其一种合成路线如图所示:

回答下列问题:
(1)质谱图显示有机物A的最大质荷比为___________ 。
(2)C分子中官能团的名称是___________ ;A→B的反应类型包括___________ 。
(3)常温下,下列试剂不能与E反应的是___________(填标号)。
(4)在冰水浴条件下,E与乙酸酐[(CH3CO)2O]反应生成一种香料M,1个M分子中含2个酯基。由E合成M的化学方程式为___________ 。
(5)T是C的同系物,T的相对分子质量比C多28,则满足下列条件的T的同分异构体有___________ 种(不考虑立体异构)。①属于芳香族化合物;②既能发生水解反应又能发生银镜反应。其中核磁共振氢谱有4组峰且峰面积之比为1∶1∶2∶6的T的同分异构体的所有可能结构为___________ 。
(6)由化合物E与乙二酸恰好完全反应生成1mol单一聚合度的 ,若生成H2O的质量为378g,则该聚合物的n值理论上应等于
,若生成H2O的质量为378g,则该聚合物的n值理论上应等于___________ 。

回答下列问题:
(1)质谱图显示有机物A的最大质荷比为
(2)C分子中官能团的名称是
(3)常温下,下列试剂不能与E反应的是___________(填标号)。
| A.H2 | B.FeCl3溶液 | C.溴水 | D.NaHCO3 |
(5)T是C的同系物,T的相对分子质量比C多28,则满足下列条件的T的同分异构体有
(6)由化合物E与乙二酸恰好完全反应生成1mol单一聚合度的
 ,若生成H2O的质量为378g,则该聚合物的n值理论上应等于
,若生成H2O的质量为378g,则该聚合物的n值理论上应等于
您最近一年使用:0次
试卷分析
整体难度:适中
考查范围:常见无机物及其应用、化学与STSE、认识化学科学、化学实验基础、化学反应原理、有机化学基础、物质结构与性质
试卷题型(共 19题)
题型
数量
单选题
10
多选题
4
解答题
5
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、单选题 | |||
| 1 | 0.85 | 硅的物理性质与用途 金属与合金性能比较 金属材料的应用 光导纤维与硅芯片 | |
| 2 | 0.94 | 氧化还原反应在生活、生产中的应用 明矾的净水作用及原理 化学科学对人类文明发展的意义 化学在农业中的应用 | |
| 4 | 0.85 | 化学用语综合判断 原子结构示意图、离子结构示意图 共价型分子结构式、电子式 | |
| 5 | 0.85 | 非电解质、电解质物质类别判断 强电解质与弱电解质 | |
| 6 | 0.4 | 离子反应的发生及书写 离子方程式的正误判断 氧化还原反应方程式的配平 | |
| 7 | 0.65 | 氨的还原性 含硫化合物之间的转化 过氧化钠 铝三角转化 | |
| 8 | 0.85 | 结合气体物质与NA相关推算 根据n=m/M进行相关计算 结合物质结构基础知识与NA相关推算 依据物质的量浓度公式的基础计算 | |
| 9 | 0.85 | 胶体的性质和应用 蛋白质的变性 化学科学对人类文明发展的意义 药物的合理使用 | |
| 10 | 0.85 | 元素周期律、元素周期表的推断 | |
| 14 | 0.65 | 弱电解质的电离平衡 弱电解质的电离方程式 电离平衡常数及影响因素 盐溶液中微粒间的电荷守恒、物料守恒、质子守恒原理 | |
| 二、多选题 | |||
| 3 | 0.85 | 仪器使用与实验安全 常用仪器及使用 化学实验基础操作 物质分离、提纯综合应用 | |
| 11 | 0.85 | 同分异构体的数目的确定 有机分子中原子共面的判断 | |
| 12 | 0.65 | 氧化还原反应有关计算 氧化还原反应方程式的配平 | |
| 13 | 0.4 | 氧化还原反应的应用 氧化还原反应方程式的配平 氧化还原反应的规律 | |
| 三、解答题 | |||
| 15 | 0.65 | 溶度积常数相关计算 物质分离、提纯综合应用 常见无机物的制备 | 工业流程题 |
| 16 | 0.4 | 化学反应原理综合考查 | 原理综合题 |
| 17 | 0.65 | 氯气的实验室制法 常用仪器及使用 化学实验基础操作 蒸馏与分馏 | 实验探究题 |
| 18 | 0.65 | 电离能变化规律 利用杂化轨道理论判断化学键杂化类型 简单配合物的成键 晶胞的有关计算 | 结构与性质 |
| 19 | 0.65 | 有机反应类型 有机物分子式的确定 常见官能团名称、组成及结构 根据要求书写同分异构体 | 有机推断题 |



