已知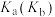 、
、 、
、 、
、 分别表示弱酸的电离平衡常数(弱碱的电离平衡常数)、水的离子积常数、盐的水解平衡常数、难溶电解质的溶度积常数。通过查阅资料获得温度为25℃时以下数据:
分别表示弱酸的电离平衡常数(弱碱的电离平衡常数)、水的离子积常数、盐的水解平衡常数、难溶电解质的溶度积常数。通过查阅资料获得温度为25℃时以下数据: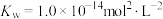 ,
, ,
,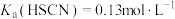 ,
,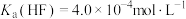 ,
,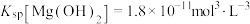 ,
,
(1)有关上述常数的说法正确的是_______ (填字母)。
a.它们都能反映一定条件下对应变化进行的程度
b.所有弱电解质的电离常数和难溶电解质的 p都随温度的升高而增大
p都随温度的升高而增大
c.常温下, 在水中的
在水中的 大于在饱和
大于在饱和 溶液中的
溶液中的
d.一定温度下,在 溶液中,
溶液中,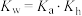
(2)25℃时,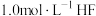 溶液的
溶液的 约等于
约等于_____ (已知 )。将浓度相等的
)。将浓度相等的 与
与 溶液等体积混合,判断溶液呈
溶液等体积混合,判断溶液呈_____ (填“酸”“碱”或“中”)性,并结合有关数据解释原因:______ 。
(3)已知 溶液为中性,又知
溶液为中性,又知 溶液加到
溶液加到 溶液中有气体放出,现有25℃时等浓度的四种溶液:
溶液中有气体放出,现有25℃时等浓度的四种溶液:
A. B.
B. C.
C. D.
D.
回答下列问题:
①试推断 溶液的
溶液的
_______ (填“>”“<”或“=”)7。
②将四种溶液按 浓度由大到小的顺序排列:
浓度由大到小的顺序排列:_______ (填字母)。
③ 溶液中所有离子浓度由大到小的顺序为
溶液中所有离子浓度由大到小的顺序为_______ 。
(4)为探究 在酸中的溶解性,利用以上数据可以计算出反应:
在酸中的溶解性,利用以上数据可以计算出反应: 在25℃时的平衡常数
在25℃时的平衡常数
_______ ,并据此推断
_______ (填“能”或“不能”)溶解于醋酸。(已知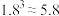 )。
)。
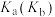 、
、 、
、 、
、 分别表示弱酸的电离平衡常数(弱碱的电离平衡常数)、水的离子积常数、盐的水解平衡常数、难溶电解质的溶度积常数。通过查阅资料获得温度为25℃时以下数据:
分别表示弱酸的电离平衡常数(弱碱的电离平衡常数)、水的离子积常数、盐的水解平衡常数、难溶电解质的溶度积常数。通过查阅资料获得温度为25℃时以下数据: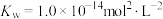 ,
, ,
,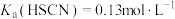 ,
,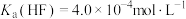 ,
,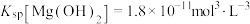 ,
,(1)有关上述常数的说法正确的是
a.它们都能反映一定条件下对应变化进行的程度
b.所有弱电解质的电离常数和难溶电解质的
 p都随温度的升高而增大
p都随温度的升高而增大c.常温下,
 在水中的
在水中的 大于在饱和
大于在饱和 溶液中的
溶液中的
d.一定温度下,在
 溶液中,
溶液中,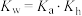
(2)25℃时,
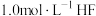 溶液的
溶液的 约等于
约等于 )。将浓度相等的
)。将浓度相等的 与
与 溶液等体积混合,判断溶液呈
溶液等体积混合,判断溶液呈(3)已知
 溶液为中性,又知
溶液为中性,又知 溶液加到
溶液加到 溶液中有气体放出,现有25℃时等浓度的四种溶液:
溶液中有气体放出,现有25℃时等浓度的四种溶液:A.
 B.
B. C.
C. D.
D.
回答下列问题:
①试推断
 溶液的
溶液的
②将四种溶液按
 浓度由大到小的顺序排列:
浓度由大到小的顺序排列:③
 溶液中所有离子浓度由大到小的顺序为
溶液中所有离子浓度由大到小的顺序为(4)为探究
 在酸中的溶解性,利用以上数据可以计算出反应:
在酸中的溶解性,利用以上数据可以计算出反应: 在25℃时的平衡常数
在25℃时的平衡常数

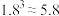 )。
)。
2020·湖北荆州·模拟预测 查看更多[4]
湖北省荆州市2020届高三上学期质量检测(一) 化学试题(已下线)第26讲 难溶电解质的溶解平衡(精练)-2022年高考化学一轮复习讲练测山东省枣庄市第三中学2022-2023学年高二上学期12月月考化学试题(已下线)第八章 水溶液中的离子反应与平衡 第54讲 水溶液中四大平衡常数的综合应用
更新时间:2022-12-12 21:36:23
|
相似题推荐
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐1】用正确的化学语言回答下列问题
(1)有1mol/L NaHCO3和Al2(SO4)3溶液,NaHCO3溶液滴入酚酞后变红,用离子方程式解释________ ;两溶液混合,可作为泡沫灭火剂的起泡剂,发生反应的离子方程式是____
(2)已知室温时,0.1mol/L某酸HA在水中有0.1%发生电离,HA的电离常数约为_________ ;HA电离出的c(H+)约为水电离出的c(H+)的______ 倍。
(3)浓度均为0.01mol/L的CH3COOH和CH3COONa混和溶液中,c(CH3COO-)+c(CH3COOH)=_____ mol/L。
(4)25 ℃时,将a mol·L-1氨水与0.01 mol·L-1盐酸等体积混合,反应平衡时溶液中c(NH )=c(Cl-)。用含a的代数式表示NH3·H2O的电离常数Kb=
)=c(Cl-)。用含a的代数式表示NH3·H2O的电离常数Kb=_______________ 。
(5)燃料电池是一种高效、环境友好的供电装置,CH4燃料电池,电解质为KOH,写出负极电极反应方程式_______________________________________ 。
(1)有1mol/L NaHCO3和Al2(SO4)3溶液,NaHCO3溶液滴入酚酞后变红,用离子方程式解释
(2)已知室温时,0.1mol/L某酸HA在水中有0.1%发生电离,HA的电离常数约为
(3)浓度均为0.01mol/L的CH3COOH和CH3COONa混和溶液中,c(CH3COO-)+c(CH3COOH)=
(4)25 ℃时,将a mol·L-1氨水与0.01 mol·L-1盐酸等体积混合,反应平衡时溶液中c(NH
 )=c(Cl-)。用含a的代数式表示NH3·H2O的电离常数Kb=
)=c(Cl-)。用含a的代数式表示NH3·H2O的电离常数Kb=(5)燃料电池是一种高效、环境友好的供电装置,CH4燃料电池,电解质为KOH,写出负极电极反应方程式
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】实验室常用氯化铵与氢氧化钙的固体混合加热制取氨气,实验室提供的有关装置见下表:
完成下列填空:
(1)从上图中选择实验室制取氨气的发生装置_____ (选填编号)、收集装置____ (选填编号)。
(2)用注射器收集50 mL纯净的氨气,然后再抽取10 mL滴有酚酞试液的蒸馏水,并用橡皮塞封闭针头。充分振荡后注射器内_______ (选填“有”“无”)气体剩余,液体呈___ 色,用化学方程式解释液体颜色变化的原因_____________________ 。
(3)工业合成氨的简易流程如下:
通过循环Ⅰ可利用的气态物质是_______
a.催化剂 b.只有N2 c.只有H2 d.N2和H2
(4)将 CO2通入到氨化的饱和食盐水中制备NaHCO3固体,反应的化学方程式__________ 。
(5)NH3、PH3、AsH3三种氢化物热稳定性由强到弱的顺序是_______ ,理由是___________ 。
(6)工业上用氨水吸收SO2尾气,最终得到化肥 (NH4)2SO4。(NH4)2SO4溶液呈_______ 性,用离子方程式解释原因__________________ ;该溶液中存在多种守恒,用离子浓度表示其中一种守恒关系________________________ 。
气体发生装置 |
a |
b |
c |
气体收集装置 |
|
|
|
完成下列填空:
(1)从上图中选择实验室制取氨气的发生装置
(2)用注射器收集50 mL纯净的氨气,然后再抽取10 mL滴有酚酞试液的蒸馏水,并用橡皮塞封闭针头。充分振荡后注射器内
(3)工业合成氨的简易流程如下:
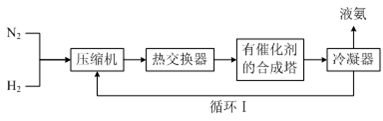
通过循环Ⅰ可利用的气态物质是
a.催化剂 b.只有N2 c.只有H2 d.N2和H2
(4)将 CO2通入到氨化的饱和食盐水中制备NaHCO3固体,反应的化学方程式
(5)NH3、PH3、AsH3三种氢化物热稳定性由强到弱的顺序是
(6)工业上用氨水吸收SO2尾气,最终得到化肥 (NH4)2SO4。(NH4)2SO4溶液呈
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐3】乙二酸(H2C2O4)俗称草酸,为无色晶体,是二元弱酸,广泛分布于植物、动物和真菌体中,在实验研究和化学工业中应用广泛。请回答下列问题:
(1)工业上由以下反应制取乙二酸: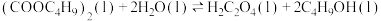 能够说明该反应已经达到平衡状态的是___________(填序号)。
能够说明该反应已经达到平衡状态的是___________(填序号)。
(2)乙二酸溶液中微粒的物质的量分数随溶液pH变化如图所示:
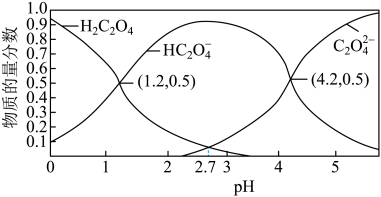
①向乙二酸溶液中滴加KOH溶液,pH由2.5至5.5过程中发生的主要反应的离子方程式是___________ 。
②向10 mL0.1 mol/LH2C2O4溶液中逐滴加入10 mL0.1 mol/LNaOH溶液,此时溶液中c(Na+)___________  (填“>”、“=”或“<”),若加入NaOH溶液体积为20mL,此时溶液中阴离子浓度的大小顺序为
(填“>”、“=”或“<”),若加入NaOH溶液体积为20mL,此时溶液中阴离子浓度的大小顺序为___________ ;当pH=2.7时,溶液中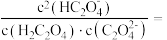
___________ 。
(3)设计实验证明乙二酸的酸性比碳酸的强___________ 。
(1)工业上由以下反应制取乙二酸:
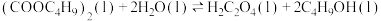 能够说明该反应已经达到平衡状态的是___________(填序号)。
能够说明该反应已经达到平衡状态的是___________(填序号)。| A.平衡常数K保持不变 | B.溶液的pH保持不变 |
| C.反应液的总质量保持不变 | D.丁醇的物质的量保持不变 |

①向乙二酸溶液中滴加KOH溶液,pH由2.5至5.5过程中发生的主要反应的离子方程式是
②向10 mL0.1 mol/LH2C2O4溶液中逐滴加入10 mL0.1 mol/LNaOH溶液,此时溶液中c(Na+)
 (填“>”、“=”或“<”),若加入NaOH溶液体积为20mL,此时溶液中阴离子浓度的大小顺序为
(填“>”、“=”或“<”),若加入NaOH溶液体积为20mL,此时溶液中阴离子浓度的大小顺序为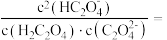
(3)设计实验证明乙二酸的酸性比碳酸的强
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐1】请回答下列问题:
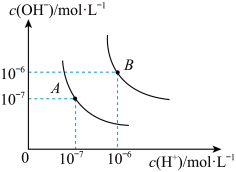
(1)水的电离平衡曲线如图所示,若A点表示 时水的电离达平衡时的离子浓度,B点表示
时水的电离达平衡时的离子浓度,B点表示 时水的电离达平衡时的离子浓度。
时水的电离达平衡时的离子浓度。
① 时
时 的
的 溶液中,由水电离出的
溶液中,由水电离出的
_______  。
。
② 时,向水的电离平衡体系中加入少量
时,向水的电离平衡体系中加入少量 固体,对水的电离平衡的影响是
固体,对水的电离平衡的影响是_______ (填“促进”、“抑制”或“不影响”)
(2)电离平衡常数是衡量弱电解质电离程度强弱的量,已知如表数据,
 时,有等浓度的a.
时,有等浓度的a. 溶液 b.
溶液 b. 溶液 c.
溶液 c. 溶液,三种溶液的
溶液,三种溶液的 由大到小的顺序为
由大到小的顺序为_______ (填序号)。
(3) 是重要的化工产品,可应用于造纸业。
是重要的化工产品,可应用于造纸业。 溶液的
溶液的 ,用离子方程式表示原因
,用离子方程式表示原因_______ 。
(4)写出将少量 通入
通入 中的化学方程式:
中的化学方程式:_______ 。
(5)已知在常温下测得浓度均为 的下列4种溶液的
的下列4种溶液的 :
:
则下列离子 ,
, ,
, ,
, 结合质子
结合质子 的能力最强的是
的能力最强的是_______ 。
(6) 时,
时, 的
的 溶液与
溶液与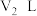
 的
的 溶液混合,混合后
溶液混合,混合后 ,求
,求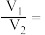
_______ 。
(7)在 下,将
下,将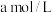 的氨水与
的氨水与 的盐酸等体积混合,反应平衡时溶液中
的盐酸等体积混合,反应平衡时溶液中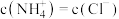 ,用含a的代数式表示
,用含a的代数式表示 的电离常数
的电离常数
_______ 。
(1)水的电离平衡曲线如图所示,若A点表示
 时水的电离达平衡时的离子浓度,B点表示
时水的电离达平衡时的离子浓度,B点表示 时水的电离达平衡时的离子浓度。
时水的电离达平衡时的离子浓度。
①
 时
时 的
的 溶液中,由水电离出的
溶液中,由水电离出的
 。
。②
 时,向水的电离平衡体系中加入少量
时,向水的电离平衡体系中加入少量 固体,对水的电离平衡的影响是
固体,对水的电离平衡的影响是(2)电离平衡常数是衡量弱电解质电离程度强弱的量,已知如表数据,
| 化学式 | 电离平衡常数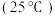 |
 | 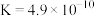 |
 |  |
 | 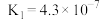 、 、 |
 | 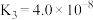 |
 时,有等浓度的a.
时,有等浓度的a. 溶液 b.
溶液 b. 溶液 c.
溶液 c. 溶液,三种溶液的
溶液,三种溶液的 由大到小的顺序为
由大到小的顺序为(3)
 是重要的化工产品,可应用于造纸业。
是重要的化工产品,可应用于造纸业。 溶液的
溶液的 ,用离子方程式表示原因
,用离子方程式表示原因(4)写出将少量
 通入
通入 中的化学方程式:
中的化学方程式:(5)已知在常温下测得浓度均为
 的下列4种溶液的
的下列4种溶液的 :
:| 溶质 |  |  |  |  |
 | 8.8 | 9.7 | 10.3 | 11.1 |
 ,
, ,
, ,
, 结合质子
结合质子 的能力最强的是
的能力最强的是(6)
 时,
时, 的
的 溶液与
溶液与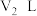
 的
的 溶液混合,混合后
溶液混合,混合后 ,求
,求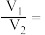
(7)在
 下,将
下,将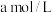 的氨水与
的氨水与 的盐酸等体积混合,反应平衡时溶液中
的盐酸等体积混合,反应平衡时溶液中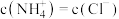 ,用含a的代数式表示
,用含a的代数式表示 的电离常数
的电离常数
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】I.乙二酸俗称草酸,是一种二元弱酸(结构简式为HOOC-COOH,可简写为H2C2O4),它是一种重要的化工原料。(常温下0.01mL的H2C2O4、KHC2O4、K2C2O4溶液的pH如表所示)填空:
(1)KHC2O4溶液显酸性的原因是_______ 。
(2)向0.1 mol∙L-1的草酸氢钾溶液里滴加NaOH溶液至中性,此时溶液里各粒子浓度关系正确的是_______
Ⅱ.化学学习小组探究反应速率的影响因素,设计了如下的方案并记录实验结果(忽略溶液混合体积变化)。限选试剂和仪器:0.20 mol∙L-1H2C2O4溶液、0.010 mol∙L-1KMnO4溶液(酸性)、蒸馏水、试管、量筒、秒表、恒温水浴槽。
(3)上述实验②、③是探究浓度对化学反应速率的影响,则a为_______ ;“乙”是该实验需要测量的量及单位是_______ 。
| H2C2O4 | KHC2O4 | K2C2O4 | |
| pH | 2.1 | 3.1 | 8.1 |
(2)向0.1 mol∙L-1的草酸氢钾溶液里滴加NaOH溶液至中性,此时溶液里各粒子浓度关系正确的是_______
A.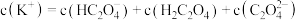 |
B.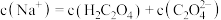 |
C.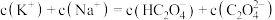 |
D.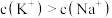 |
Ⅱ.化学学习小组探究反应速率的影响因素,设计了如下的方案并记录实验结果(忽略溶液混合体积变化)。限选试剂和仪器:0.20 mol∙L-1H2C2O4溶液、0.010 mol∙L-1KMnO4溶液(酸性)、蒸馏水、试管、量筒、秒表、恒温水浴槽。
| 物理量 | V(0.200mol∙L-1 H2C2O4溶液)/mL | V(蒸馏水)/mL | V(0.010mol∙L-1 KMnO4溶液)/mL | T/℃ | 乙 |
| ① | 2.0 | 0 | 4.0 | 50 | |
| ② | 2.0 | 0 | 4.0 | 25 | |
| ③ | 1.0 | a | 4.0 | 25 |
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐3】醋酸是日常生活中最常见的调味剂和重要的化工原料,醋酸钠是其常见的盐(已知:25℃,Ka(CH3COOH)=1.69×10-5)。
(1)醋酸钠溶液呈碱性的原因是_______________ (写出有关的离子方程式)
(2)在CH3COONa溶液中离子浓度由大到小的顺序为_____________________ (用c(Bn+)表示相应离子浓度);
(3)25℃时,0.10mol/L的醋酸溶液的pH约为___________ ( 已知:lg1.3=0.114);
(4)对于醋酸溶液和醋酸钠溶液的下列说法正确的是____________ ;
A.稀释醋酸溶液,醋酸的电离程度增大,而稀释醋酸钠溶液则醋酸钠的水解程度减小.
B.升高温度可以促进醋酸电离,也可以促进醋酸钠水解.
C.醋酸和醋酸钠混合液中,醋酸抑制醋酸钠的水解、醋酸钠也抑制醋酸的电离.
D.醋酸和醋酸钠混合液中,醋酸促进醋酸钠的水解、醋酸钠也促进醋酸的电离.
(5)物质的量浓度均为0.1mol/L的CH3COONa和CH3COOH溶液等体积混合(注:混合前后溶液体积变化忽略不计),混合液中的下列关系式正确的是_______ ;
A.c(CH3COOH)+2c(H+)=c(CH3COO-)+2c(OH-)
B.c(Na+)+c(H+)=c(CH3COO-)+c(OH-)
C.c(CH3COO-)+c(CH3COOH)=0.1mol/L
(6)常温时,有以下3种溶液,其中pH最小的是____________ ;
A.0.02mol•L-1CH3COOH与0.02mol•L-1NaOH溶液等体积混合液
B.0.03mol•L-1CH3COOH与0.01mol•L-1NaOH溶液等体积混合液
C.pH=2的CH3COOH与pH=12的NaOH溶液等体积混合液
(7)用pH试纸在常温下分别测定0.10mol/L的醋酸钠溶液和0.10mol/L的碳酸钠溶液,则pH(CH3COONa)_______ pH(Na2CO3).(填:“>”、“<”或“=”)
(1)醋酸钠溶液呈碱性的原因是
(2)在CH3COONa溶液中离子浓度由大到小的顺序为
(3)25℃时,0.10mol/L的醋酸溶液的pH约为
(4)对于醋酸溶液和醋酸钠溶液的下列说法正确的是
A.稀释醋酸溶液,醋酸的电离程度增大,而稀释醋酸钠溶液则醋酸钠的水解程度减小.
B.升高温度可以促进醋酸电离,也可以促进醋酸钠水解.
C.醋酸和醋酸钠混合液中,醋酸抑制醋酸钠的水解、醋酸钠也抑制醋酸的电离.
D.醋酸和醋酸钠混合液中,醋酸促进醋酸钠的水解、醋酸钠也促进醋酸的电离.
(5)物质的量浓度均为0.1mol/L的CH3COONa和CH3COOH溶液等体积混合(注:混合前后溶液体积变化忽略不计),混合液中的下列关系式正确的是
A.c(CH3COOH)+2c(H+)=c(CH3COO-)+2c(OH-)
B.c(Na+)+c(H+)=c(CH3COO-)+c(OH-)
C.c(CH3COO-)+c(CH3COOH)=0.1mol/L
(6)常温时,有以下3种溶液,其中pH最小的是
A.0.02mol•L-1CH3COOH与0.02mol•L-1NaOH溶液等体积混合液
B.0.03mol•L-1CH3COOH与0.01mol•L-1NaOH溶液等体积混合液
C.pH=2的CH3COOH与pH=12的NaOH溶液等体积混合液
(7)用pH试纸在常温下分别测定0.10mol/L的醋酸钠溶液和0.10mol/L的碳酸钠溶液,则pH(CH3COONa)
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐1】含硅元素的化合物广泛存在于自然界中,与其他矿物共同构成岩石.晶体硅(熔点 1410℃)用途广泛,制取与提纯方法有多种.
(1)炼钢开始和结束阶段都可能发生反应:Si+2FeO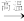 2Fe+SiO2,其目的是
2Fe+SiO2,其目的是________________ .
A.得到副产品硅酸盐水泥 B.制取SiO2,提升钢的硬度
C.除去生铁中过多的Si杂质 D.除过量FeO,防止钢变脆
(2)一种由粗硅制纯硅过程如下:Si(粗)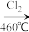 SiCl4
SiCl4 SiCl4(纯)
SiCl4(纯)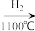 Si(纯),在上述由SiCl4制纯硅的反应中,测得每生成 1.12kg纯硅需吸收a kJ热量,写出该反应的热化学方程式:
Si(纯),在上述由SiCl4制纯硅的反应中,测得每生成 1.12kg纯硅需吸收a kJ热量,写出该反应的热化学方程式:________________ .
对于钠的卤化物(NaX)和硅的卤化物(SiX4)下列叙述正确的是________________
A.NaX易水解
B.SiX4是共价化合物
C.NaX的熔点一般高于SiX4
D.SiF4晶体是由共价键形成的空间网状结构
(3)粗硅经系列反应可生成硅烷(SiH4),硅烷分解也可以生成高纯硅.硅烷的热稳定性弱于甲烷,所以Si元素的非金属性弱于C元素,用原子结构解释其原因:________________ .
(4)此外,还可以将粗硅转化成三氯氢硅(SiHCl3),通过反应:SiHCl3(g)+H2(g)⇌Si(s)+3HCl(g)制得高纯硅.不同温度下,SiHCl3的平衡转化率随反应物的投料比(反应初始时,各反应物的物质的量之比)的变化关系如图所示.下列说法正确的是________________ (填字母序号).
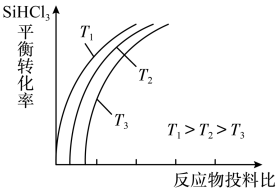
a.该反应的平衡常数随温度升高而增大
b.横坐标表示的投料比应该是
c.实际生产中为提高SiHCl3的利用率,可适当降低压强
(5)硅元素最高价氧化物对应的水化物是H2SiO3.室温下,0.1mol/L的硅酸钠溶液和0.1mol/L的碳酸钠溶液,碱性更强的是___________ ,其原因是________________ .已知:H2SiO3:Ka1=2.0×10﹣10、Ka2=1.0×10﹣12,H2CO3:Ka1=4.3×10﹣7Ka2=5.6×10 ﹣11.
(1)炼钢开始和结束阶段都可能发生反应:Si+2FeO
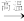 2Fe+SiO2,其目的是
2Fe+SiO2,其目的是A.得到副产品硅酸盐水泥 B.制取SiO2,提升钢的硬度
C.除去生铁中过多的Si杂质 D.除过量FeO,防止钢变脆
(2)一种由粗硅制纯硅过程如下:Si(粗)
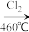 SiCl4
SiCl4 SiCl4(纯)
SiCl4(纯)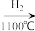 Si(纯),在上述由SiCl4制纯硅的反应中,测得每生成 1.12kg纯硅需吸收a kJ热量,写出该反应的热化学方程式:
Si(纯),在上述由SiCl4制纯硅的反应中,测得每生成 1.12kg纯硅需吸收a kJ热量,写出该反应的热化学方程式:对于钠的卤化物(NaX)和硅的卤化物(SiX4)下列叙述正确的是
A.NaX易水解
B.SiX4是共价化合物
C.NaX的熔点一般高于SiX4
D.SiF4晶体是由共价键形成的空间网状结构
(3)粗硅经系列反应可生成硅烷(SiH4),硅烷分解也可以生成高纯硅.硅烷的热稳定性弱于甲烷,所以Si元素的非金属性弱于C元素,用原子结构解释其原因:
(4)此外,还可以将粗硅转化成三氯氢硅(SiHCl3),通过反应:SiHCl3(g)+H2(g)⇌Si(s)+3HCl(g)制得高纯硅.不同温度下,SiHCl3的平衡转化率随反应物的投料比(反应初始时,各反应物的物质的量之比)的变化关系如图所示.下列说法正确的是

a.该反应的平衡常数随温度升高而增大
b.横坐标表示的投料比应该是

c.实际生产中为提高SiHCl3的利用率,可适当降低压强
(5)硅元素最高价氧化物对应的水化物是H2SiO3.室温下,0.1mol/L的硅酸钠溶液和0.1mol/L的碳酸钠溶液,碱性更强的是
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐2】已知:草酸H2C2O4的Ka1=5.0×10-2, Ka2=5.4×10-5; Ksp(CaC2O4)=4.8×10-8
(1)在此溶液中逐滴滴加0.2mol/L的NaOH溶液,n( )的变化趋势是
)的变化趋势是_________________ 。
(2)用Ka1 、 Ka2、Kw 表示对应的K
① +2H+ =H2C2O4 K=
+2H+ =H2C2O4 K=____________ ② +OH- =
+OH- = +H2O K=
+H2O K=____________
③H2C2O4+ =2
=2 K=
K=____________
(3)0.1mol/L的Na2C2O4溶液100mL,该溶液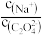
______ 2(填“>”、“<”或“=”,下同),向此溶液中加入草酸(H2C2O4)固体至pH=7,溶液中c( )
)_______ c( )。
)。
(4)在某温度下向含有草酸钙(CaC2O4)固体的CaC2O4饱和溶液中加入少量草酸(H2C2O4)固体,则CaC2O4的溶解量________ (填“增大”、“减小”或“不变”,下同),Ksp(CaC2O4)__________ ,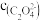
__________ 。
(5)将0.2mol/L的H2C2O4溶液与0.2mol/L的CaCl2溶液等体积混合,通过计算说明溶液中是否有沉淀生成_______ 。
(1)在此溶液中逐滴滴加0.2mol/L的NaOH溶液,n(
 )的变化趋势是
)的变化趋势是(2)用Ka1 、 Ka2、Kw 表示对应的K
①
 +2H+ =H2C2O4 K=
+2H+ =H2C2O4 K= +OH- =
+OH- = +H2O K=
+H2O K=③H2C2O4+
 =2
=2 K=
K=(3)0.1mol/L的Na2C2O4溶液100mL,该溶液
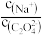
 )
) )。
)。(4)在某温度下向含有草酸钙(CaC2O4)固体的CaC2O4饱和溶液中加入少量草酸(H2C2O4)固体,则CaC2O4的溶解量
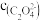
(5)将0.2mol/L的H2C2O4溶液与0.2mol/L的CaCl2溶液等体积混合,通过计算说明溶液中是否有沉淀生成
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐3】请回答下列问题:
(1)25℃时,pH=5的CH3COOH溶液中.加入少量NaOH固体,则溶液中
_______ (填“增大”、“减小”或“不变”)。
(2)25℃下,向某Na2CO3溶液中加入稀盐酸,其中含碳元素的各种微粒物质的量分数(φ)随溶液pH变化的部分情况如图所示。
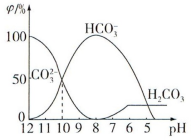
①在同一溶液中H2CO3、HCO3-、CO32-______ (填“能”或“不能”)大量共存。
②当pH =7时,溶液中含碳元素的微粒主要为________ 。溶液中各种离子的物质的量浓度大小关系为___________________________ 。
③反应的CO32-+H2O HCO3-+OH-的平衡常数Kh值为
HCO3-+OH-的平衡常数Kh值为_________ 。
(3)生物脱H2S的原理为:H2S+Fe2(SO4)3=S↓+2FeSO4+H2SO4、4FeSO4+O2+2H2SO4 2Fe2(SO4)3+2H2O。
2Fe2(SO4)3+2H2O。
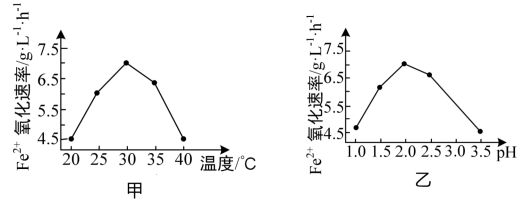
①硫杆菌存在时,FeSO4被氧化的速率是无菌时的5×105倍,该菌的作用是___________ 。
②由图甲和图乙判断使用硫杆菌的最佳条件为____________ 。在最佳条件下,该反应的加热
方式为_________ 。
(1)25℃时,pH=5的CH3COOH溶液中.加入少量NaOH固体,则溶液中

(2)25℃下,向某Na2CO3溶液中加入稀盐酸,其中含碳元素的各种微粒物质的量分数(φ)随溶液pH变化的部分情况如图所示。

①在同一溶液中H2CO3、HCO3-、CO32-
②当pH =7时,溶液中含碳元素的微粒主要为
③反应的CO32-+H2O
 HCO3-+OH-的平衡常数Kh值为
HCO3-+OH-的平衡常数Kh值为(3)生物脱H2S的原理为:H2S+Fe2(SO4)3=S↓+2FeSO4+H2SO4、4FeSO4+O2+2H2SO4
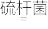 2Fe2(SO4)3+2H2O。
2Fe2(SO4)3+2H2O。
①硫杆菌存在时,FeSO4被氧化的速率是无菌时的5×105倍,该菌的作用是
②由图甲和图乙判断使用硫杆菌的最佳条件为
方式为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐1】三盐基硫酸铅(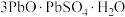 ,其相对分子质量为990)简称“三盐”,不溶于水及有机溶剂。主要适用于不透明的聚氯乙烯硬质管、注射成型制品,也可用于人造革等软质制品。以铅泥(主要成分为
,其相对分子质量为990)简称“三盐”,不溶于水及有机溶剂。主要适用于不透明的聚氯乙烯硬质管、注射成型制品,也可用于人造革等软质制品。以铅泥(主要成分为 、
、 及
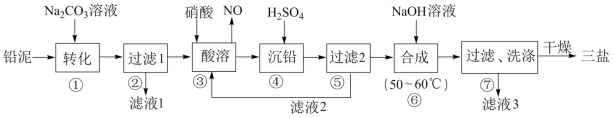
及 等)为原料制备三盐的工艺流程如下图所示。
等)为原料制备三盐的工艺流程如下图所示。

已知: ,
,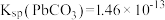 请回答下列问题:
请回答下列问题:
(1)写出步骤①“转化”的离子方程式___________ 。
(2)根据上图解度曲线(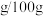 水),由滤液Ⅰ得到
水),由滤液Ⅰ得到 固体的操作为:将“滤液1”
固体的操作为:将“滤液1”___________ 、___________ 、用乙醇洗涤后干燥。
(3)步骤③“酸溶”,为提高酸溶速率,可采取的措施是___________ (任意写出一条)
(4)若步骤④“沉铅”后的滤液中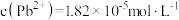 ,则此时
,则此时
___________  。
。
(5)步骤⑥“合成”三盐的化学方程式为___________ 。
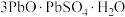 ,其相对分子质量为990)简称“三盐”,不溶于水及有机溶剂。主要适用于不透明的聚氯乙烯硬质管、注射成型制品,也可用于人造革等软质制品。以铅泥(主要成分为
,其相对分子质量为990)简称“三盐”,不溶于水及有机溶剂。主要适用于不透明的聚氯乙烯硬质管、注射成型制品,也可用于人造革等软质制品。以铅泥(主要成分为 、
、 及
及 等)为原料制备三盐的工艺流程如下图所示。
等)为原料制备三盐的工艺流程如下图所示。

已知:
 ,
,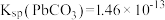 请回答下列问题:
请回答下列问题:(1)写出步骤①“转化”的离子方程式
(2)根据上图解度曲线(
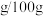 水),由滤液Ⅰ得到
水),由滤液Ⅰ得到 固体的操作为:将“滤液1”
固体的操作为:将“滤液1”(3)步骤③“酸溶”,为提高酸溶速率,可采取的措施是
(4)若步骤④“沉铅”后的滤液中
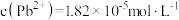 ,则此时
,则此时
 。
。(5)步骤⑥“合成”三盐的化学方程式为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐2】金属钛(Ti)因其硬度大、熔点高、常温时耐酸碱腐蚀而被广泛用作高新科技材料,被誉为“未来金属”。以钛铁矿(主要成分钛酸亚铁)为主要原料冶炼金属钛同时获得副产品甲的工业生产流程如下。请回答下列问题。
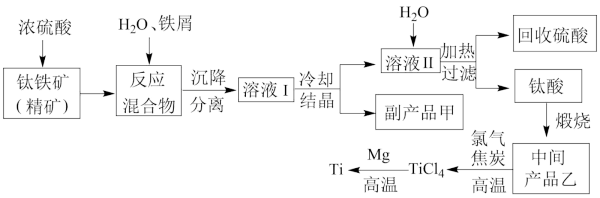
(1)钛酸亚铁(用R表示)与碳在高温下发生反应:2R+C=2Fe+2TiO2+CO2↑,钛酸亚铁的化学式为___________ ;钛酸亚铁和浓H2SO4反应的产物之一是TiOSO4,反应中无气体生成,该反应的化学方程式为___________ 。
(2)上述生产流程中溶液Ⅰ中含有Fe2+、TiO2+和少量Mg2+等阳离子。常温下,其对应氢氧化物的Ksp如下表所示。
①常温下,若所得溶液中Mg2+的物质的量浓度为0.0018mol·L-1,当溶液的pH等于___________ 时,Mg(OH)2开始沉淀。
②若将含有Fe2+、TiO2+和Mg2+的溶液加水稀释,立即析出大量白色沉淀,该反应的离子方程式为___________ 。
(3)中间产品乙与焦炭(二者按物质的量比1∶2参加反应)、氯气在高温下发生反应制取TiCl4的方程式为___________ ,Mg还原TiCl4过程中必须在1070K的温度下进行,你认为还应该控制的反应条件是___________ 。

(1)钛酸亚铁(用R表示)与碳在高温下发生反应:2R+C=2Fe+2TiO2+CO2↑,钛酸亚铁的化学式为
(2)上述生产流程中溶液Ⅰ中含有Fe2+、TiO2+和少量Mg2+等阳离子。常温下,其对应氢氧化物的Ksp如下表所示。
| 氢氧化物 | Fe(OH)2 | TiO(OH)2 | Mg(OH)2 |
| Ksp | 8.0×10-16 | 1.0×10-29 | 1.8×10-11 |
①常温下,若所得溶液中Mg2+的物质的量浓度为0.0018mol·L-1,当溶液的pH等于
②若将含有Fe2+、TiO2+和Mg2+的溶液加水稀释,立即析出大量白色沉淀,该反应的离子方程式为
(3)中间产品乙与焦炭(二者按物质的量比1∶2参加反应)、氯气在高温下发生反应制取TiCl4的方程式为
您最近一年使用:0次
【推荐3】工业上利用钴渣[主要成分为Co2O3、Co(OH)3,含少量Fe2O3、Al2O3、MnO、MgO、CaO等]制备钴氧化物的工艺流程如下。
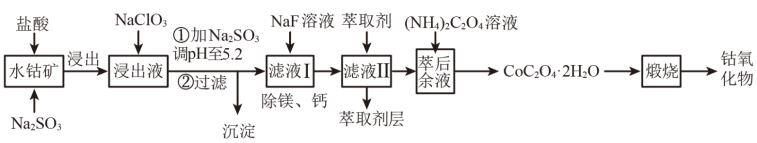
已知:部分阳离子以氢氧化物形式沉淀时溶液的 pH 见下表。
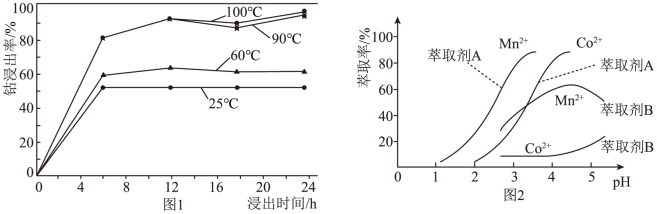
(1)钴的浸出率随酸浸时间、温度的变化关系如图1,应选择的最佳工艺条件为______ 。金属离子在萃取剂中的萃取率随pH变化关系如图2,据此分析pH的最佳范围是______ 。
A.5~5.5 B. 4~4.5 C. 3~3.5 D. 2~2.5
(2)Fe2+、Co2+、 SO 三种离子的还原性由强到弱的顺序是
三种离子的还原性由强到弱的顺序是______ 。氧化过程中加NaClO3被还原,产物中的氯元素处在最低价态,反应的离子方程式为______ 。
(3)25℃ Ksp(MgF2)=7.4×10-11,Ksp(CaF2)=1.5×10-10。除钙、镁工艺中加过量NaF溶液,滤液中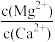 =
=______ (保留两位有效数字)。
(4)已知常温下Kb(NH3·H2O)=1.8×10-5,Kh(C2O )=1.8×10-10,(NH4)2C2O4溶液显
)=1.8×10-10,(NH4)2C2O4溶液显______ (填“酸性” 或“中性”或“碱性”)。在“萃后余液”中加入(NH4)2C2O4溶液后析出晶体,再过滤、洗涤,洗涤时应选用的试剂为______ (填字母代号)。
A.蒸馏水 B.自来水 C.饱和的(NH4)2C2O4溶液 D.稀盐酸
(5)取一定质量煅烧后产生的钴氧化物(Co为+2、+3价),用100 mL 8 mol·L-1的盐酸恰好完全溶解,得到CoCl2溶液和标准状况2.24 L黄绿色气体。则该钴氧化物中+2价的Co与+3价Co元素的物质的量之比为______ 。

已知:部分阳离子以氢氧化物形式沉淀时溶液的 pH 见下表。
| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Co(OH)2 | Al(OH)3 | Mn(OH)2 |
| 开始沉淀 | 2.7 | 7.6 | 7.6 | 4.0 | 7.7 |
| 完全沉淀 | 3.7 | 9.6 | 9.2 | 5.2 | 9.8 |
(1)钴的浸出率随酸浸时间、温度的变化关系如图1,应选择的最佳工艺条件为
A.5~5.5 B. 4~4.5 C. 3~3.5 D. 2~2.5

(2)Fe2+、Co2+、 SO
 三种离子的还原性由强到弱的顺序是
三种离子的还原性由强到弱的顺序是(3)25℃ Ksp(MgF2)=7.4×10-11,Ksp(CaF2)=1.5×10-10。除钙、镁工艺中加过量NaF溶液,滤液中
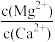 =
=(4)已知常温下Kb(NH3·H2O)=1.8×10-5,Kh(C2O
 )=1.8×10-10,(NH4)2C2O4溶液显
)=1.8×10-10,(NH4)2C2O4溶液显A.蒸馏水 B.自来水 C.饱和的(NH4)2C2O4溶液 D.稀盐酸
(5)取一定质量煅烧后产生的钴氧化物(Co为+2、+3价),用100 mL 8 mol·L-1的盐酸恰好完全溶解,得到CoCl2溶液和标准状况2.24 L黄绿色气体。则该钴氧化物中+2价的Co与+3价Co元素的物质的量之比为
您最近一年使用:0次





 水
水

