1 . 实验是学习化学、探究化学过程的重要途径。下列装置不能达到相应实验目的的是
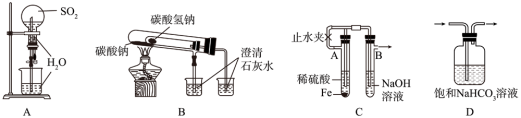

| A.进行喷泉实验 | B.比较 与 与 的热稳定性 的热稳定性 |
C.制备 沉淀 沉淀 | D.除去 中混有的 中混有的 气体 气体 |
您最近一年使用:0次
解题方法
2 . Ⅰ.漂白液是一种常用的消毒剂,通常可将 通入
通入 溶液中制取,某化学兴趣小组想用下列装置制备漂白液并探究漂白液的化学性质。
溶液中制取,某化学兴趣小组想用下列装置制备漂白液并探究漂白液的化学性质。

(1)写出制取漂白液的化学反应方程式___________ ,为完成该制备实验请将上述装置的接口按照合理的顺序连接:___________ 。
(2)为了探究漂白液的性质,各取少量制备的漂白液于3支试管中,进行下列实验(已知淀粉遇碘变蓝),根据要求完善表格。
Ⅱ.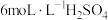 溶液的配制
溶液的配制
若实验室没有配制好的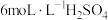 溶液,需要利用图片中的信息自行配制
溶液,需要利用图片中的信息自行配制
(3)该浓硫酸的物质的量浓度为___________ 。
(4)若本实验需要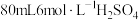 溶液溶液,配制步骤为:
溶液溶液,配制步骤为:
a:将容量瓶塞紧,充分摇匀;
b:待烧杯中的溶液冷却到室温后,转入___________;
c:用量筒量取___________mL浓硫酸慢慢注入盛有少量水的烧杯中,进行稀释;
d:用少量蒸馏水洗涤玻璃棒和烧杯2~3次,每次洗涤的溶液都转入容量瓶,并轻轻摇匀。
e:继续加蒸馏水至液面距刻度线1~2cm处,改用胶头滴管滴加蒸馏水至溶液凹液面与刻度线相切;回答下列问题:
①步骤c中用量筒量取___________ mL浓硫酸。
②实验步骤中使用的仪器b为___________ 。
③本实验正确的操作顺序为___________ (填序号)。
④下列操作会导致所配溶液浓度偏高的是___________ (填字母)。
a.定容时俯视刻度线
b.将烧杯中的溶液转移到容量瓶时不慎洒到容量瓶外
c.摇匀后发现液面低于容量瓶刻度线,再滴加蒸馏水至刻度线
d.转移洗涤液时洒到容量瓶外,继续用未清洗的该容量瓶重新配制
 通入
通入 溶液中制取,某化学兴趣小组想用下列装置制备漂白液并探究漂白液的化学性质。
溶液中制取,某化学兴趣小组想用下列装置制备漂白液并探究漂白液的化学性质。
(1)写出制取漂白液的化学反应方程式
(2)为了探究漂白液的性质,各取少量制备的漂白液于3支试管中,进行下列实验(已知淀粉遇碘变蓝),根据要求完善表格。
| 实验操作 | 试剂X | 实验现象 | 推论 |
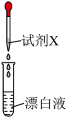 | 紫色石蕊试液 | 先变蓝,后褪色 | ①后褪色说明漂白液具有 |
| 含淀粉的碘化钾溶液 | ② | ③漂白液具有 | |
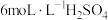 溶液 溶液 | 产生黄绿色气体 | ④溶液中发生反应的离子方程式为 |
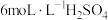 溶液的配制
溶液的配制若实验室没有配制好的
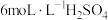 溶液,需要利用图片中的信息自行配制
溶液,需要利用图片中的信息自行配制浓H2SO4 相对分子质量:98 密度:1.84g/mL 质量分数:98% |
(4)若本实验需要
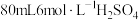 溶液溶液,配制步骤为:
溶液溶液,配制步骤为:a:将容量瓶塞紧,充分摇匀;
b:待烧杯中的溶液冷却到室温后,转入___________;
c:用量筒量取___________mL浓硫酸慢慢注入盛有少量水的烧杯中,进行稀释;
d:用少量蒸馏水洗涤玻璃棒和烧杯2~3次,每次洗涤的溶液都转入容量瓶,并轻轻摇匀。
e:继续加蒸馏水至液面距刻度线1~2cm处,改用胶头滴管滴加蒸馏水至溶液凹液面与刻度线相切;回答下列问题:
①步骤c中用量筒量取
②实验步骤中使用的仪器b为
③本实验正确的操作顺序为
④下列操作会导致所配溶液浓度偏高的是
a.定容时俯视刻度线
b.将烧杯中的溶液转移到容量瓶时不慎洒到容量瓶外
c.摇匀后发现液面低于容量瓶刻度线,再滴加蒸馏水至刻度线
d.转移洗涤液时洒到容量瓶外,继续用未清洗的该容量瓶重新配制
您最近一年使用:0次
3 . 研究性学习小组对Fe及其化合物的相关性质进行探究。
探究一:设计如图所示装置进行“铁与水蒸气反应”的实验(夹持仪器略)。

(1)A中放碎瓷片的目的是_______ 。
(2)硬质玻璃管b中发生反应的化学方程式为:_______ 。
(3)装置D的作用是_______ 。
(4)装置E中可观察的现象是_______ 。
探究二:确定探究一反应后硬质玻璃管B中黑色固体的成分。
(5)将硬质玻璃管中反应后的固体混合物全部取出置于烧杯中,加入足量的盐酸溶解并过滤,进行如下实验,请将下表补充完整:
探究三:利用如下图所示装置制备 。
。

(6)试剂X可选用植物油,其主要作用是_______ 。
(7)实验开始时,打开分液漏斗塞子,关闭 ,依次打开
,依次打开 、
、 的目的是
的目的是_______ 。一段时间后关闭 ,打开
,打开 ,可观察到的现象是
,可观察到的现象是_______ 。
探究一:设计如图所示装置进行“铁与水蒸气反应”的实验(夹持仪器略)。

(1)A中放碎瓷片的目的是
(2)硬质玻璃管b中发生反应的化学方程式为:
(3)装置D的作用是
(4)装置E中可观察的现象是
探究二:确定探究一反应后硬质玻璃管B中黑色固体的成分。
(5)将硬质玻璃管中反应后的固体混合物全部取出置于烧杯中,加入足量的盐酸溶解并过滤,进行如下实验,请将下表补充完整:
| 步骤 | 现象 | 解释(用离子方程式表示) | 结论 |
| Ⅰ.取少量滤液,滴加KSCN溶液 | 溶液不变红,为浅绿色 | 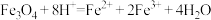 ; ; | 滤液中的阳离子为 |
| Ⅱ.取少量滤液,滴加NaOH溶液 | 刚开始无明显现象,一段时间后先出现白色沉淀,迅速变为灰绿色,最终变为红褐色 |  (白色); (白色);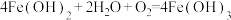 |
探究三:利用如下图所示装置制备
 。
。
(6)试剂X可选用植物油,其主要作用是
(7)实验开始时,打开分液漏斗塞子,关闭
 ,依次打开
,依次打开 、
、 的目的是
的目的是 ,打开
,打开 ,可观察到的现象是
,可观察到的现象是
您最近一年使用:0次
解题方法
4 . 高铁酸钠( )为紫色固体,易溶于水,微溶于NaOH溶液,具有强氧化性,可以杀菌消毒,是一种新型、高效、多功能的水处理剂。某化学实验小组利用NaClO在碱性介质中与
)为紫色固体,易溶于水,微溶于NaOH溶液,具有强氧化性,可以杀菌消毒,是一种新型、高效、多功能的水处理剂。某化学实验小组利用NaClO在碱性介质中与 溶液的反应制备
溶液的反应制备 并探究其性质,实验装置如下图所示。
并探究其性质,实验装置如下图所示。
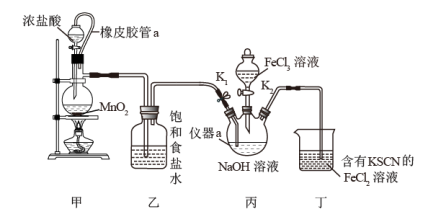
请回答下列问题:
(1)橡皮管a的作用是___________ ,装置甲中反应的化学方程式为___________ 。
(2)若去掉装置乙,其不足之处为___________ 。
(3)当装置丁中出现___________ 现象时,关闭 ;此时向装置丙中加入
;此时向装置丙中加入 溶液。
溶液。
(4)装置丙中生成 的离子方程式为
的离子方程式为___________ 。
(5)反应后,向装置丙中加入饱和的___________ (填化学式)溶液,析出紫色晶体,过滤、洗涤、干燥。
(6)取少量 晶体加入浑浊的泥浆水很快澄清,同时产生气体。请结合化学方程分析
晶体加入浑浊的泥浆水很快澄清,同时产生气体。请结合化学方程分析 的净水原理为
的净水原理为___________ 。
 )为紫色固体,易溶于水,微溶于NaOH溶液,具有强氧化性,可以杀菌消毒,是一种新型、高效、多功能的水处理剂。某化学实验小组利用NaClO在碱性介质中与
)为紫色固体,易溶于水,微溶于NaOH溶液,具有强氧化性,可以杀菌消毒,是一种新型、高效、多功能的水处理剂。某化学实验小组利用NaClO在碱性介质中与 溶液的反应制备
溶液的反应制备 并探究其性质,实验装置如下图所示。
并探究其性质,实验装置如下图所示。
请回答下列问题:
(1)橡皮管a的作用是
(2)若去掉装置乙,其不足之处为
(3)当装置丁中出现
 ;此时向装置丙中加入
;此时向装置丙中加入 溶液。
溶液。(4)装置丙中生成
 的离子方程式为
的离子方程式为(5)反应后,向装置丙中加入饱和的
(6)取少量
 晶体加入浑浊的泥浆水很快澄清,同时产生气体。请结合化学方程分析
晶体加入浑浊的泥浆水很快澄清,同时产生气体。请结合化学方程分析 的净水原理为
的净水原理为
您最近一年使用:0次
5 . 如图为实验室用二氧化锰制取纯净、干燥的氯气,并验证氯气性质的装置。其中E瓶放有干燥红色布条;F中为沾有湿润淀粉碘化钾的棉花。请据图回答下列问题:

(1)A仪器的名称是___________ 。
(2)B中发生反应的离子方程式为___________ 。
(3)D中试剂的作用是___________ ,E中的现象为___________ 。
(4)F中反应的化学反应方程式:___________ 。
(5)装置H中盛装的溶液是___________ ,工业上常用廉价的石灰乳吸收工业氯气尾气制得漂粉精,漂粉精的有效成分是___________ 。
(6)实验室也常用如下反应制备Cl2,请根据反应回答下列问题:
___________KMnO4 +___________HCl(浓) → ___________KCl +___________MnCl2 +___________Cl2↑+___________H2O
①请在题中横线内填入适当的系数___________ 。
② 若反应中转移了0.3mol电子,则生成的Cl2在标准状况下的体积为___________ 。

(1)A仪器的名称是
(2)B中发生反应的离子方程式为
(3)D中试剂的作用是
(4)F中反应的化学反应方程式:
(5)装置H中盛装的溶液是
(6)实验室也常用如下反应制备Cl2,请根据反应回答下列问题:
___________KMnO4 +___________HCl(浓) → ___________KCl +___________MnCl2 +___________Cl2↑+___________H2O
①请在题中横线内填入适当的系数
② 若反应中转移了0.3mol电子,则生成的Cl2在标准状况下的体积为
您最近一年使用:0次
名校
解题方法
6 . 某化学小组在实验室制备KMnO4,并利用其性质测定血液中钙的含量。请回答:
(一)KMnO4的制备,分步骤Ⅰ、Ⅱ两步进行。
步骤Ⅰ.将软锰矿(主要成分MnO2)和KOH固体混合后装入图所示装置A中,在空气中加热,并不断用B搅拌最终得到K2MnO4。
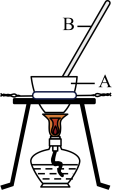
(1)仪器A、B分别是_______ (填序号)。
A.瓷坩埚、玻璃棒B.石英坩埚、玻璃棒C.铁坩埚、玻璃棒D.铁坩埚、铁棒
(2)装置A处反应生成K2MnO4的化学方程式为_______ 。
步骤Ⅱ.KMnO4的制备。
已知:锰酸钾(K2MnO4)在浓强碱溶液中可稳定存在,碱性减弱时易发生反应:3 +2H2O═2
+2H2O═2 +MnO2↓+4OH﹣。
+MnO2↓+4OH﹣。
(3)甲同学利用Cl2在碱性条件下氧化K2MnO4制备KMnO4其装置如图所示(夹持和加热装置略)。
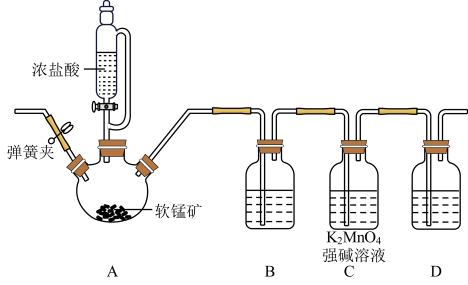
回答下列问题:
①装置B中的试剂为_______ ;若没有B装置则产率会_______ (填“增大”“减小”或“不变”)。
②当C中反应结束后,后续操作是熄灭酒精灯,_______ ,拆除装置。
③请写出D中的生成物在生活中的一个应用:_______ 。
(4)乙同学利用已知信息和部分物质溶解度数据表,提出另一种新的制备方法:向上述K2MnO4溶液中加入_______ (请从下列物质中选出一种最合适的物质),充分反应,然后过滤,再将滤液蒸发浓缩、降温结晶、过滤、洗涤、干燥,得KMnO4晶体。
A.亚硫酸氢钾B.硫酸氢钠C.稀盐酸D.稀醋酸
(二)人体血液里Ca2+含量的测定。
抽取血样20.00mL,加适量的草酸铵[(NH4)2C2O4]溶液;可析出草酸钙(CaC2O4)沉淀,将此草酸钙沉淀洗涤后溶于强酸可得草酸(H2C2O4),再用0.0020mol/L酸性KMnO4溶液滴定,共消耗9.00mL酸性KMnO4溶液。
(1)滴定时,当出现_______ 现象,即可确定反应达到终点。
(2)经过计算,血液样品中Ca2+的浓度为_______ mg/cm3。
(一)KMnO4的制备,分步骤Ⅰ、Ⅱ两步进行。
步骤Ⅰ.将软锰矿(主要成分MnO2)和KOH固体混合后装入图所示装置A中,在空气中加热,并不断用B搅拌最终得到K2MnO4。

(1)仪器A、B分别是
A.瓷坩埚、玻璃棒B.石英坩埚、玻璃棒C.铁坩埚、玻璃棒D.铁坩埚、铁棒
(2)装置A处反应生成K2MnO4的化学方程式为
步骤Ⅱ.KMnO4的制备。
已知:锰酸钾(K2MnO4)在浓强碱溶液中可稳定存在,碱性减弱时易发生反应:3
 +2H2O═2
+2H2O═2 +MnO2↓+4OH﹣。
+MnO2↓+4OH﹣。(3)甲同学利用Cl2在碱性条件下氧化K2MnO4制备KMnO4其装置如图所示(夹持和加热装置略)。

回答下列问题:
①装置B中的试剂为
②当C中反应结束后,后续操作是熄灭酒精灯,
③请写出D中的生成物在生活中的一个应用:
(4)乙同学利用已知信息和部分物质溶解度数据表,提出另一种新的制备方法:向上述K2MnO4溶液中加入
| 物质 | KMnO4 | K2SO4 | CH3COOK | Na2SO4 |
| 20℃溶解度 | 6.4 | 11.1 | 217 | 30 |
(二)人体血液里Ca2+含量的测定。
抽取血样20.00mL,加适量的草酸铵[(NH4)2C2O4]溶液;可析出草酸钙(CaC2O4)沉淀,将此草酸钙沉淀洗涤后溶于强酸可得草酸(H2C2O4),再用0.0020mol/L酸性KMnO4溶液滴定,共消耗9.00mL酸性KMnO4溶液。
(1)滴定时,当出现
(2)经过计算,血液样品中Ca2+的浓度为
您最近一年使用:0次
2020-11-15更新
|
543次组卷
|
3卷引用:陕西省汉中市龙岗学校2021届高三上学期第二次月考化学试题
陕西省汉中市龙岗学校2021届高三上学期第二次月考化学试题江西省南昌市南昌县莲塘第一中学2021届高三上学期12月质量检测化学试题(已下线)培优02 无机制备类实验 提高训练-2021年高考化学大题培优练(新高考地区专用)
7 . 下列装置或操作能达到相应实验目的的是
| 选项 | A | B | C | D |
| 装置或操作 |  |  |  | 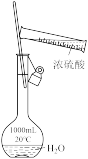 |
| 实验目的 | 排水集气法收集 | 实验室制取氨气 | 测定镁铝合金中铝排水的质量分数 | 配制稀硫酸 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
8 . 某兴趣小组用如图装置研究溶液的导电性,把X溶液逐滴加入含少量酚酞的 溶液中。下列说法不正确的是
溶液中。下列说法不正确的是
 溶液中。下列说法不正确的是
溶液中。下列说法不正确的是序号 | 装置 | X溶液 | 现象 |
I |
| 盐酸 | 溶液红色褪去,无沉淀,灯泡亮度稍微变暗 |
II |
| 溶液红色不变,有白色沉淀生成,灯泡亮度稍微变暗 | |
III |
| 溶液红色褪去,有白色沉淀生成,灯泡亮度:变暗→熄灭→变亮 |
A.实验I中溶液红色褪去,说明发生了反应 |
B.实验II中溶液红色不变,灯泡亮度稍微变暗,说明溶液中依然存在大量的 与 与 |
C.实验III中溶液红色褪去,有白色沉淀生成,灯泡由暗→灭→亮,说明发生了反应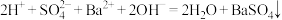 |
D.将实验II中 溶液换成 溶液换成 溶液,现象与原实验Ⅱ中的现象相同 溶液,现象与原实验Ⅱ中的现象相同 |
您最近一年使用:0次
2023-02-18更新
|
124次组卷
|
2卷引用:陕西省渭南市临渭区2022-2023学年高一上学期期末考试化学试题
解题方法
9 . 下图是实验室制备 的实验装置图,其中甲为氯气的发生装置,丙装置中反应的离子方程式为
的实验装置图,其中甲为氯气的发生装置,丙装置中反应的离子方程式为 (未配平)。(资料:
(未配平)。(资料: 为紫色固体,微溶于
为紫色固体,微溶于 ,在碱性环境中稳定,具有强氧化性)下列说法不正确的是
,在碱性环境中稳定,具有强氧化性)下列说法不正确的是

 的实验装置图,其中甲为氯气的发生装置,丙装置中反应的离子方程式为
的实验装置图,其中甲为氯气的发生装置,丙装置中反应的离子方程式为 (未配平)。(资料:
(未配平)。(资料: 为紫色固体,微溶于
为紫色固体,微溶于 ,在碱性环境中稳定,具有强氧化性)下列说法不正确的是
,在碱性环境中稳定,具有强氧化性)下列说法不正确的是
A.B装置的作用是干燥水,所用试剂为浓 |
| B.工业上利用D中所发生的反应原理制备漂白液 |
| C.三颈烧瓶中使用搅拌器的目的是加快反应速率,增大反应物的利用率 |
D.A中浓盐酸中的 在该反应中既失电子又为反应提供所需的酸性环境 在该反应中既失电子又为反应提供所需的酸性环境 |
您最近一年使用:0次
10 . 草酸亚铁晶体(FeC2O4·2H2O)是一种黄色难溶于水可溶于稀硫酸的固体,具有较强还原性,受热易分解,是生产电池、涂料以及感光材料的原材料。某化学活动小组分别设计了相应装置进行草酸亚铁的制备及其性质实验。回答下列问题:
Ⅰ.制备草酸亚铁晶体(装置如图所示):

(1)盛装稀硫酸的仪器名称为_____________________ 。
(2)实验过程:待 中反应一段时间后,需要对开关进行的操作是
中反应一段时间后,需要对开关进行的操作是_________ 。
(3)装置 的作用
的作用 _________________________ 。
Ⅱ.草酸亚铁晶体热分解产物的探究:

(4)装置C和D可以可以合并为一个盛有_________________ 的球形干燥管。
(5)从绿色化学考虑,该套装置存在的明显缺陷是_________________ 。
(6)实验结束后,E中黑色固体变为红色,B、F中澄清石灰水变浑浊,a中无水硫酸变为蓝色,A中残留FeO,则A处反应管中发生反应的化学方程式为__________ 。
Ⅲ. 运用热重分析法推测产物
称取3.60g草酸亚铁晶体加热分解,得到剩余固体质量随温度变化的曲线如图所示:

(7)当剩余固体质量为1.60g时,,剩余固体物质的化学式为__________ 。
Ⅰ.制备草酸亚铁晶体(装置如图所示):

(1)盛装稀硫酸的仪器名称为
(2)实验过程:待
 中反应一段时间后,需要对开关进行的操作是
中反应一段时间后,需要对开关进行的操作是(3)装置
 的作用
的作用 Ⅱ.草酸亚铁晶体热分解产物的探究:

(4)装置C和D可以可以合并为一个盛有
(5)从绿色化学考虑,该套装置存在的明显缺陷是
(6)实验结束后,E中黑色固体变为红色,B、F中澄清石灰水变浑浊,a中无水硫酸变为蓝色,A中残留FeO,则A处反应管中发生反应的化学方程式为
Ⅲ. 运用热重分析法推测产物
称取3.60g草酸亚铁晶体加热分解,得到剩余固体质量随温度变化的曲线如图所示:

(7)当剩余固体质量为1.60g时,,剩余固体物质的化学式为
您最近一年使用:0次


 溶液
溶液 溶液
溶液

