1 . 次磷酸钠(NaH2PO2)在食品工业中用作防腐剂、抗氧化剂,也是一种很好的化学镀剂。
(1)NaH2PO2中P的化合价为___________ 价。
(2)将待镀零件浸泡在NiSO4和NaH2PO2的混合溶液中,可达到化学镀镍(在待镀零件表面形成一层金属镍)的目的,该过程中 被氧化为二元弱酸H3PO3,写出该反应的离子方程式
被氧化为二元弱酸H3PO3,写出该反应的离子方程式___________ 。
(3)次磷酸钠的制备
将黄磷(P4)和过量烧碱溶液混合加热,生成NaH2PO2和PH3(气体),PH3与NaClO溶液反应可生成次磷酸(H3PO2),实验装置如图:

①装置A中盛放烧碱溶液的仪器名称为___________ 。
②由装置A中发生化学反应可知,次磷酸(H3PO2)属于___________ 元弱酸。
③装置C中发生反应的化学方程式为___________ 。
④已知相关物质的溶解度如表:
充分反应后,将A、C中溶液混合,再将混合液(含极少量NaOH)加热浓缩,有大量杂质晶体析出,然后___________ (填操作名称),得到含NaH2PO2的溶液,进一步处理得到粗产品。
⑤反应结束后,向装置内通入N2的目的是___________ 。
(4)次磷酸钠的纯度测定
先取1.0g粗产品配成100mL溶液,再取25.00mL所配溶液于锥形瓶中,酸化后加入过量的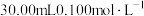 碘水。充分反应后,剩余碘水恰好可消耗
碘水。充分反应后,剩余碘水恰好可消耗 溶液(相关反应方程式为:
溶液(相关反应方程式为: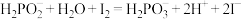 ,
, ),则产品纯度为
),则产品纯度为___________ 。(已知:NaH2PO2相对分子质量为88)
(1)NaH2PO2中P的化合价为
(2)将待镀零件浸泡在NiSO4和NaH2PO2的混合溶液中,可达到化学镀镍(在待镀零件表面形成一层金属镍)的目的,该过程中
 被氧化为二元弱酸H3PO3,写出该反应的离子方程式
被氧化为二元弱酸H3PO3,写出该反应的离子方程式(3)次磷酸钠的制备
将黄磷(P4)和过量烧碱溶液混合加热,生成NaH2PO2和PH3(气体),PH3与NaClO溶液反应可生成次磷酸(H3PO2),实验装置如图:

①装置A中盛放烧碱溶液的仪器名称为
②由装置A中发生化学反应可知,次磷酸(H3PO2)属于
③装置C中发生反应的化学方程式为
④已知相关物质的溶解度如表:
| 25℃ | 100℃ | |
| NaCl | 37g | 39g |
| NaH2PO2 | 100g | 667g |
⑤反应结束后,向装置内通入N2的目的是
(4)次磷酸钠的纯度测定
先取1.0g粗产品配成100mL溶液,再取25.00mL所配溶液于锥形瓶中,酸化后加入过量的
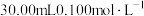 碘水。充分反应后,剩余碘水恰好可消耗
碘水。充分反应后,剩余碘水恰好可消耗 溶液(相关反应方程式为:
溶液(相关反应方程式为: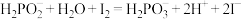 ,
, ),则产品纯度为
),则产品纯度为
您最近一年使用:0次
真题
名校
2 . 利用如图所示的装置(夹持及加热装置略)制备高纯白磷的流程如下:

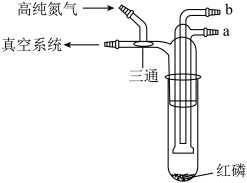
| A.红磷使用前洗涤以除去表面杂质 |
| B.将红磷转入装置,抽真空后加热外管以去除水和氧气 |
| C.从a口通入冷凝水,升温使红磷转化 |
| D.冷凝管外壁出现白磷,冷却后在氮气氛围下收集 |
您最近一年使用:0次
2023-06-14更新
|
7066次组卷
|
12卷引用:2023年高考湖北卷化学真题
2023年高考湖北卷化学真题(已下线)专题10 物质的反应及转化(已下线)T13-化学实验基础(已下线)专题10 物质的反应及转化(已下线)专题10 物质的反应及转化(已下线)考点巩固卷12 化学实验基础(一)(3大考点67题)-2024年高考化学一轮复习考点通关卷(新高考通用)(已下线)专题11 化学实验(选择题)-2023年高考化学真题题源解密(新高考专用)(已下线)第13讲氮及其化合物(已下线)第6讲 硝酸 含氮化合物之间的转化(已下线)专题05 化学实验基础-2023年高考化学真题题源解密(全国通用)吉林省长春外国语学校2023-2024学年高三上学期9月月考化学试题江苏省南菁高中、常州市第一中学2023-2024学年高二下学期3月月考化学试题
解题方法
3 . 一种化合物的结构如图所示,Q、X、Y、Z、W为相邻两个短周期主族元素,原子序数依次增大,W元素的最外层电子数等于其电子总数的三分之一。下列说法正确的是
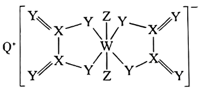

| A.通常所用的农药中含有Z、W等元素 |
| B.氢化物的沸点一定是Y>Z>X |
| C.由Q、Y、W形成的正盐只有一种 |
| D.Q的单质在空气中燃烧的产物具有强氧化性 |
您最近一年使用:0次
4 . 碳酸锂是制备各种锂化合物的关键原料。一种以磷酸锂渣(主要成分Li3PO4)为原料制备碳酸锂的工艺流程示意图如下。
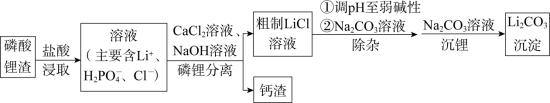
已知:部分物质的溶解性表(20℃)
(1)写出浸取时Li3PO4与盐酸反应的化学方程式:_______ 。
(2)加入盐酸的量不宜过多的原因是_______ 。
(3)钙渣的主要成分是_______ 。
(4)磷锂分离时,需要不断加入适量NaOH溶液以维持溶液的pH基本不变。结合离子方程式解释其原因是_______ 。
(5)沉锂时,反应的离子方程式是_______ 。

已知:部分物质的溶解性表(20℃)
| 阳离子 | 阴离子 | ||
 |  | 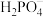 | |
| Li+ | 难溶 | 可溶 | 易溶 |
| Ca2+ | 难溶 | 难溶 | 可溶 |
(2)加入盐酸的量不宜过多的原因是
(3)钙渣的主要成分是
(4)磷锂分离时,需要不断加入适量NaOH溶液以维持溶液的pH基本不变。结合离子方程式解释其原因是
(5)沉锂时,反应的离子方程式是
您最近一年使用:0次
5 .  为正盐,能将溶液中的
为正盐,能将溶液中的 还原为
还原为 ,可用于化学镀银。反应的离子方程式为
,可用于化学镀银。反应的离子方程式为 。下列说法正确的是
。下列说法正确的是
 为正盐,能将溶液中的
为正盐,能将溶液中的 还原为
还原为 ,可用于化学镀银。反应的离子方程式为
,可用于化学镀银。反应的离子方程式为 。下列说法正确的是
。下列说法正确的是A.上述反应中,氧化产物是 |
| B.该反应氧化剂与还原剂的物质的量之比为1∶4 |
C. 中含有离子键、极性共价键和非极性共价键 中含有离子键、极性共价键和非极性共价键 |
D. 是三元酸,与 是三元酸,与 反应可生成三种盐 反应可生成三种盐 |
您最近一年使用:0次
名校
解题方法
6 . 我国磷资源储量丰富。回答下列问题:
(1)已知亚磷酸(H3PO3)为二元弱酸,写出亚磷酸与过量 反应的化学方程式
反应的化学方程式___________ ;
(2)磷酸为磷的最高价含氧酸,其空间结构如图1所示:
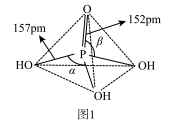
①键能大小比较:磷氧双键___________ (填“大于”“等于”或“小于”)磷氧单键。
②键角大小比较:
___________  (填“大于”“等于”或“小于”)。
(填“大于”“等于”或“小于”)。
③纯净的磷酸黏度极大,随温度升高黏度迅速下降,原因是___________ 。
(3)磷化硼(BP)是一种超硬耐磨涂层材料,其立方晶胞如图2所示
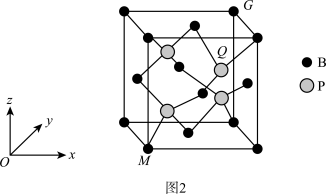
①固态磷化硼属于___________ (填“分子”“离子”或“共价”)晶体。
②以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子的分数坐标。已知原子分数坐标:M点为(0,0,0)、G点为(1,1,1),则Q点的原子分数坐标为___________ 。
③若晶胞参数为acm,则B与P之间的最短距离为___________ cm(用含a的代数式表示)。
(1)已知亚磷酸(H3PO3)为二元弱酸,写出亚磷酸与过量
 反应的化学方程式
反应的化学方程式(2)磷酸为磷的最高价含氧酸,其空间结构如图1所示:

①键能大小比较:磷氧双键
②键角大小比较:

 (填“大于”“等于”或“小于”)。
(填“大于”“等于”或“小于”)。③纯净的磷酸黏度极大,随温度升高黏度迅速下降,原因是
(3)磷化硼(BP)是一种超硬耐磨涂层材料,其立方晶胞如图2所示

①固态磷化硼属于
②以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子的分数坐标。已知原子分数坐标:M点为(0,0,0)、G点为(1,1,1),则Q点的原子分数坐标为
③若晶胞参数为acm,则B与P之间的最短距离为
您最近一年使用:0次
名校
解题方法
7 . 关于非金属含氧酸及其盐的性质,下列说法正确的是
A.浓 具有强吸水性,能吸收糖类化合物中的水分并使其炭化 具有强吸水性,能吸收糖类化合物中的水分并使其炭化 |
B. 等氯的含氧酸盐均可用于制取氯气 等氯的含氧酸盐均可用于制取氯气 |
C.加热 与浓 与浓 混合物可制备 混合物可制备 ,说明 ,说明 比 比 酸性强 酸性强 |
D.浓 和稀 和稀 与 与 反应的还原产物分别为 反应的还原产物分别为 和 和 ,故稀 ,故稀 氧化性更强 氧化性更强 |
您最近一年使用:0次
8 . 实验室利用红磷(P)与Cl2反应可制取少量PCl3或PCl5。
I.利用如图所示装置制取少量PCl3(部分夹持装置已略去)。
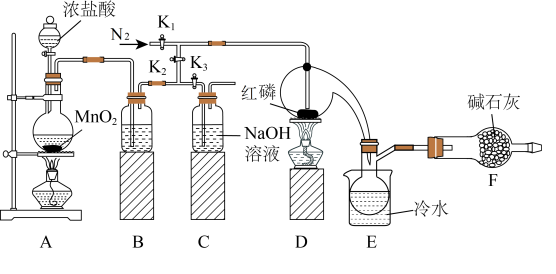
(1)组装好装置,在放入试剂前应先_____ 。
(2)A中发生反应的离子方程式为_____ 。
(3)B中所装试剂为_____ 。
(4)实验开始前,打开K1通入一段时间氮气来除去装置中的空气,除去空气的目的是_____ ;除去装置A、B中空气的具体方法是_____ 。
(5)除去产物中PCl5杂质的化学反应方程式是_____ 。
II.测定产品中PCl3的质量分数
实验步骤:
①迅速称取mg产品,加水反应后配成100mL溶液。
②取上述溶液10.00mL,向其中加入V1mLc1mol/L碘水(足量),充分反应。
③向②所得溶液中加入几滴淀粉溶液,逐滴滴加c2mol/L的Na2S2O3溶液并振荡,当溶液恰好由蓝色变为无色时,记录所消耗Na2S2O3溶液的体积。
④重复②、③操作3次,平均消耗Na2S2O3溶液V2mL。
(6)第①步溶于水的化学反应方程式是_____ 。
(7)逐滴滴加Na2S2O3溶液使用的仪器是_____ 。(已知:H2S2O3是弱酸)。
(8)根据上述数据测得该产品中PCl3的质量分数为_____ 。(已知:H3PO3+I2+H2O=H3PO4+2HI,I2+2Na2S2O3=2NaI+Na2S4O6)
| 物质 | 熔点/℃ | 沸点/℃ | 性质 |
| PCl3 | -112 | 75.5 | 遇水生成H3PO3和HCl,与O2反应生成POCl3 |
| PCl5 | — | 约100℃升华 | 遇水生成H3PO4和HCl,与红磷反应生成PCl3 |

(1)组装好装置,在放入试剂前应先
(2)A中发生反应的离子方程式为
(3)B中所装试剂为
| A.饱和碳酸氢钠溶液 | B.饱和氯化钠溶液 |
| C.氢氧化钠溶液 | D.浓硫酸 |
(5)除去产物中PCl5杂质的化学反应方程式是
II.测定产品中PCl3的质量分数
实验步骤:
①迅速称取mg产品,加水反应后配成100mL溶液。
②取上述溶液10.00mL,向其中加入V1mLc1mol/L碘水(足量),充分反应。
③向②所得溶液中加入几滴淀粉溶液,逐滴滴加c2mol/L的Na2S2O3溶液并振荡,当溶液恰好由蓝色变为无色时,记录所消耗Na2S2O3溶液的体积。
④重复②、③操作3次,平均消耗Na2S2O3溶液V2mL。
(6)第①步溶于水的化学反应方程式是
(7)逐滴滴加Na2S2O3溶液使用的仪器是
(8)根据上述数据测得该产品中PCl3的质量分数为
您最近一年使用:0次
名校
解题方法
9 .  为正盐,其中P为
为正盐,其中P为 价O为
价O为 价,能将溶液中的
价,能将溶液中的 还原为
还原为 ,可用于化学镀银。反应的离子方程式为
,可用于化学镀银。反应的离子方程式为 。下列说法正确的是
。下列说法正确的是
 为正盐,其中P为
为正盐,其中P为 价O为
价O为 价,能将溶液中的
价,能将溶液中的 还原为
还原为 ,可用于化学镀银。反应的离子方程式为
,可用于化学镀银。反应的离子方程式为 。下列说法正确的是
。下列说法正确的是A.上述反应中,氧化产物是 |
| B.该反应氧化剂与还原剂的物质的量之比为1∶4 |
C. 溶于水破坏离子键、极性共价键和非极性共价键 溶于水破坏离子键、极性共价键和非极性共价键 |
D. 是三元酸,与 是三元酸,与 反应可生成三种盐 反应可生成三种盐 |
您最近一年使用:0次
2023-03-23更新
|
204次组卷
|
3卷引用: 山东省青岛第五十八中学2022-2023学年高一下学期3月月考化学试题
名校
10 . 根据物质类别预测物质性质是常用的方法之一,下列预测正确的是
| 选项 | 已知性质 | 性质预测 |
| A | Fe能置换出 溶液中的Cu 溶液中的Cu | Na也能置换出 溶液中的Cu 溶液中的Cu |
| B | 氮气与氧气不容易化合 | 磷单质与氧气也不容易化合 |
| C |  能使澄清石灰水变浑浊 能使澄清石灰水变浑浊 |  也能使澄清石灰水变浑浊 也能使澄清石灰水变浑浊 |
| D |  通入氯化钡溶液,溶液不变浑浊 通入氯化钡溶液,溶液不变浑浊 |  通入硝酸钡溶液,溶液也不变浑浊 通入硝酸钡溶液,溶液也不变浑浊 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-02-18更新
|
222次组卷
|
2卷引用:广东省汕尾市2022-2023学年高一上学期期末考试化学试题



