解题方法
1 . 实验小组用废铁屑(含少量 、FeS和
、FeS和 )和硫酸制备
)和硫酸制备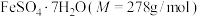 晶体。
晶体。
② 的密度1.19g/mL。
的密度1.19g/mL。
(1)步骤II过程中产生气体成分为___________ (填化学式)。
(2)下列说法不正确的是___________。
(3)为获得较多产品,步骤III一系列操作如下:
滤液B转移至蒸发血,加入适量3mol/L硫酸→70℃蒸发至溶液析出适量的晶体,停止加热→操作X→过滤→用冷蒸馏水洗涤→滤纸吸干。
①加入适量硫酸作用是抑制 水解和
水解和___________ 。
②操作X的名称为___________ 。
(4) 产品纯度测定:
产品纯度测定:
用 标准溶液滴定
标准溶液滴定 (所含杂质不含亚铁及其他还原性物质)溶液,3次平行滴定,若每次滴定的锥形瓶中含样品2.93g,平均消耗
(所含杂质不含亚铁及其他还原性物质)溶液,3次平行滴定,若每次滴定的锥形瓶中含样品2.93g,平均消耗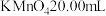 。
。
①产品纯度为___________ %(保留值小数点后1位)。
②下列操作会使得测定结果偏大的是___________ 。
A.滴定用的酸式滴定管用蒸馏水洗后未用标准液润洗
B.移取硫酸亚铁溶液时,待液体全部流出后,立即取出移液管
C.滴定终点时,酸式滴定管读数时没有等液体回落
D.滴定前酸式滴定管尖嘴处无气泡,到达滴定终点时有气泡
 、FeS和
、FeS和 )和硫酸制备
)和硫酸制备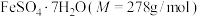 晶体。
晶体。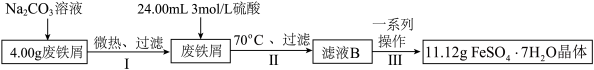
| 温度/℃ | 0 | 10 | 30 | 56 | 64 | 80 | 90 | ||
| 溶解度/g | 14.0 | 17.0 | 25.0 | 35.2 | 35.6 | 30.5 | 27.0 | ||
| 析出晶体 |  |  |  | ||||||
 的密度1.19g/mL。
的密度1.19g/mL。(1)步骤II过程中产生气体成分为
(2)下列说法不正确的是___________。
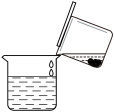
| A.步骤I的目的是去除废铁屑表面的油脂 |
| B.步骤I的过滤可用如图所示操作代替 |
| C.步骤II水浴加热至无气泡产生、溶液颜色呈灰绿色停止反应 |
| D.步骤II需要在通风橱中进行,等溶液冷却至室温后过滤 |
(3)为获得较多产品,步骤III一系列操作如下:
滤液B转移至蒸发血,加入适量3mol/L硫酸→70℃蒸发至溶液析出适量的晶体,停止加热→操作X→过滤→用冷蒸馏水洗涤→滤纸吸干。
①加入适量硫酸作用是抑制
 水解和
水解和②操作X的名称为
(4)
 产品纯度测定:
产品纯度测定:用
 标准溶液滴定
标准溶液滴定 (所含杂质不含亚铁及其他还原性物质)溶液,3次平行滴定,若每次滴定的锥形瓶中含样品2.93g,平均消耗
(所含杂质不含亚铁及其他还原性物质)溶液,3次平行滴定,若每次滴定的锥形瓶中含样品2.93g,平均消耗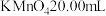 。
。①产品纯度为
②下列操作会使得测定结果偏大的是
A.滴定用的酸式滴定管用蒸馏水洗后未用标准液润洗
B.移取硫酸亚铁溶液时,待液体全部流出后,立即取出移液管
C.滴定终点时,酸式滴定管读数时没有等液体回落
D.滴定前酸式滴定管尖嘴处无气泡,到达滴定终点时有气泡
您最近一年使用:0次
2 . 氟单质及其化合物在生产、生活和科研中应用广泛。回答下列问题:
(1)基态F原子价电子的电子排布式为___________ 。
(2)范德华半径是指分子晶体中共价分子之间的最短距离。图1中可看成氟单质的范德华半径的是___________ (填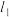 、
、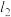 或
或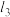 )。
)。___________ (填元素符号)。
(4)液态HF存在自耦电离: ,试解释形成
,试解释形成 的原因
的原因___________ , 的VSEPR模型的名称为
的VSEPR模型的名称为___________ 。
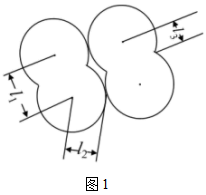
(5)1962年,青年化学家N。Bartlett用Xe和 合成了氙的第一个化合物—
合成了氙的第一个化合物—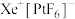 ,震惊了化学界,
,震惊了化学界, 、
、 、
、 也随之合成。下列说法不正确的是___________
也随之合成。下列说法不正确的是___________
(6)由Xe和F构成的化合物的晶体属四方晶系,晶胞参数如图2所示,晶胞棱边夹角均为90°。已知Xe和F原子的共价半径分别为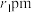 和
和 ,空间利用率是指构成晶体的原子在整个晶体空间中所占有的体积百分比。
,空间利用率是指构成晶体的原子在整个晶体空间中所占有的体积百分比。___________ 。(用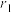 、
、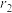 、a、c表示)
、a、c表示)
(1)基态F原子价电子的电子排布式为
(2)范德华半径是指分子晶体中共价分子之间的最短距离。图1中可看成氟单质的范德华半径的是
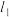 、
、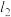 或
或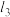 )。
)。
(4)液态HF存在自耦电离:
 ,试解释形成
,试解释形成 的原因
的原因 的VSEPR模型的名称为
的VSEPR模型的名称为(5)1962年,青年化学家N。Bartlett用Xe和
 合成了氙的第一个化合物—
合成了氙的第一个化合物—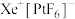 ,震惊了化学界,
,震惊了化学界, 、
、 、
、 也随之合成。下列说法不正确的是___________
也随之合成。下列说法不正确的是___________A.该化合物中基态阳离子的价电子排布式为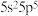 |
| B.合成过程中Xe为还原剂 |
C.可推测Ne也会和 化合 化合 |
D.Xe属于p区元素, 中心原子杂化方式是 中心原子杂化方式是 |
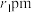 和
和 ,空间利用率是指构成晶体的原子在整个晶体空间中所占有的体积百分比。
,空间利用率是指构成晶体的原子在整个晶体空间中所占有的体积百分比。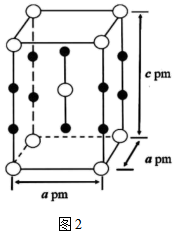
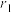 、
、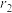 、a、c表示)
、a、c表示)
您最近一年使用:0次
3 . 某小组采用如下实验流程制备难溶于水的白色BiOCl: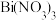 极易水解产生难溶的
极易水解产生难溶的 固体,
固体,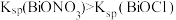 。
。
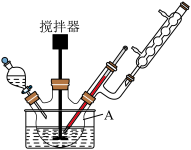
(1)下图为步骤Ⅰ的实验装置图(夹持仪器和尾气处理装置已省略),仪器A的名称是_______ 。
(3)写出 水解离子方程式
水解离子方程式_______ 。
①简述实验室配制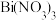 溶液方法
溶液方法_______ 。
②请结合浓度商和平衡常数 解释 可抑制
可抑制 的水解
的水解_______ 。
(4)利用 溶液与NaOH溶液测定中和反应反应热,从下列选项中选择合适的操作补全测定步骤(有些步骤可重复使用):
溶液与NaOH溶液测定中和反应反应热,从下列选项中选择合适的操作补全测定步骤(有些步骤可重复使用):_______ 。
用量筒量取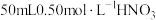 →(_______)→(_______)→(_______)→(_______)→用另一个量筒量取
→(_______)→(_______)→(_______)→(_______)→用另一个量筒量取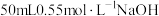 溶液→(_______)→(_______)→(_______)→打开杯盖,将NaOH溶液倒入量热计的内筒,盖上杯盖→(a)→(e)→测量并记录温度→重复上述步骤两次。
溶液→(_______)→(_______)→(_______)→打开杯盖,将NaOH溶液倒入量热计的内筒,盖上杯盖→(a)→(e)→测量并记录温度→重复上述步骤两次。
a.插入温度计
b.测量并记录温度
c.打开杯盖,将硝酸倒入量热计的内筒,盖上杯盖
d.用蒸馏水把温度计上的溶液冲洗干净,擦干备用
e.搅拌器匀速搅拌
(5)测定产品的纯度:称取产品0.1200g于锥形瓶中,加盐酸溶解,加入饱和硫脲(简写为TU)与Bi3+形成黄色溶液,再用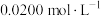 的EDTA滴定至终点,三次滴定消耗EDTA溶液的平均体积为20.50 mL,则产品的纯度为
的EDTA滴定至终点,三次滴定消耗EDTA溶液的平均体积为20.50 mL,则产品的纯度为_______ (已知形成无色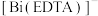 远比形成黄色
远比形成黄色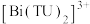 容易,
容易,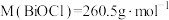 )。
)。

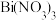 极易水解产生难溶的
极易水解产生难溶的 固体,
固体,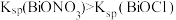 。
。(1)下图为步骤Ⅰ的实验装置图(夹持仪器和尾气处理装置已省略),仪器A的名称是
| A.步骤Ⅰ:加热温度越高,溶解速率越快,产率越高 |
| B.步骤Ⅱ:可加适量的NaOH溶液调节pH |
| C.步骤Ⅲ:在通风橱中浓缩至蒸发皿中大量晶体析出 |
| D.步骤Ⅳ:试剂X选用HCl、NaCl,组合使用更有利于制备BiOCl |
 水解离子方程式
水解离子方程式①简述实验室配制
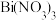 溶液方法
溶液方法②
 可抑制
可抑制 的水解
的水解(4)利用
 溶液与NaOH溶液测定中和反应反应热,从下列选项中选择合适的操作补全测定步骤(有些步骤可重复使用):
溶液与NaOH溶液测定中和反应反应热,从下列选项中选择合适的操作补全测定步骤(有些步骤可重复使用):用量筒量取
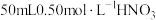 →(_______)→(_______)→(_______)→(_______)→用另一个量筒量取
→(_______)→(_______)→(_______)→(_______)→用另一个量筒量取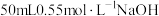 溶液→(_______)→(_______)→(_______)→打开杯盖,将NaOH溶液倒入量热计的内筒,盖上杯盖→(a)→(e)→测量并记录温度→重复上述步骤两次。
溶液→(_______)→(_______)→(_______)→打开杯盖,将NaOH溶液倒入量热计的内筒,盖上杯盖→(a)→(e)→测量并记录温度→重复上述步骤两次。a.插入温度计
b.测量并记录温度
c.打开杯盖,将硝酸倒入量热计的内筒,盖上杯盖
d.用蒸馏水把温度计上的溶液冲洗干净,擦干备用
e.搅拌器匀速搅拌
(5)测定产品的纯度:称取产品0.1200g于锥形瓶中,加盐酸溶解,加入饱和硫脲(简写为TU)与Bi3+形成黄色溶液,再用
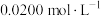 的EDTA滴定至终点,三次滴定消耗EDTA溶液的平均体积为20.50 mL,则产品的纯度为
的EDTA滴定至终点,三次滴定消耗EDTA溶液的平均体积为20.50 mL,则产品的纯度为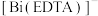 远比形成黄色
远比形成黄色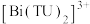 容易,
容易,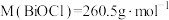 )。
)。
您最近一年使用:0次
名校
4 . 某手机电池采用了石墨烯电池,可充电5分钟,通话2小时。一种石墨烯锂硫电池(2Li+S8=Li2S8)工作原理示意图如图。已知参与电极反应的单位质量的电极材料放出电能的大小称为该电池的比能量。下列有关该电池说法不正确的是
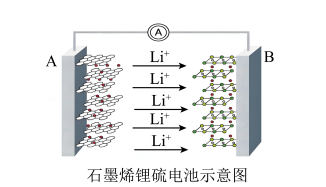
| A.金属锂是所有金属中比能量最高的电极材料 |
| B.电子从A电极经过外电路流向B电极,再经过电解质流回A电极 |
| C.A电极为该电源的负极,发生氧化反应 |
| D.B电极的反应:2Li++S8+2e-=Li2S8 |
您最近一年使用:0次
2024-09-11更新
|
115次组卷
|
4卷引用:浙江省衢州市2017届高三1月教学质量检测化学试题
5 . 在 溶液中加入
溶液中加入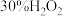 溶液,能得到紫色的
溶液,能得到紫色的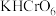 溶液,继续加入稀硫酸,立即有蓝色的
溶液,继续加入稀硫酸,立即有蓝色的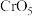 生成,该蓝色物质能被乙醚萃取,下列说法
生成,该蓝色物质能被乙醚萃取,下列说法不正确 的是
 溶液中加入
溶液中加入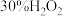 溶液,能得到紫色的
溶液,能得到紫色的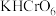 溶液,继续加入稀硫酸,立即有蓝色的
溶液,继续加入稀硫酸,立即有蓝色的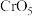 生成,该蓝色物质能被乙醚萃取,下列说法
生成,该蓝色物质能被乙醚萃取,下列说法A.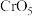 结构为: 结构为: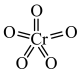 |
B.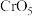 在酸性溶液继续反应可能会生成 在酸性溶液继续反应可能会生成 |
C.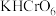 和 和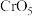 均能氧化 均能氧化 |
D.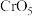 与 与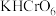 晶体类型不同,后者难以被乙醚萃取 晶体类型不同,后者难以被乙醚萃取 |
您最近一年使用:0次
6 . 硫脲(CS(NH2)2)是一种有机合成中常用的试剂,对于反应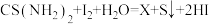 ,下列说法正确的是
,下列说法正确的是
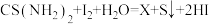 ,下列说法正确的是
,下列说法正确的是| A.X的化学式为HCONH2 | B.氧化产物与还原产物物质的量之比为2:1 |
| C.氧化性I2>S | D.每产生32gS单质,转移NA个电子 |
您最近一年使用:0次
解题方法
7 . 某研究小组按下列路线合成一种治疗慢性便秘药品的中间体。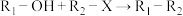
(1)B中的官能团名称为___________ 。
(2)E的结构简式为___________ 。
(3)下列说法正确的是___________。
(4)F→G有一种分子式为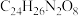 的副产物生成,写出生成该副产物的反应方程式
的副产物生成,写出生成该副产物的反应方程式___________ 。
(5)设计以苯,1,3-丁二烯为原料合成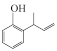 的路线(用流程图表示,无机试剂、有机溶剂任选)
的路线(用流程图表示,无机试剂、有机溶剂任选)___________ 。
(6)写出同时符合下列条件的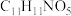 的同分异构体的结构简式
的同分异构体的结构简式___________ 。
①不能与 发生显色反应,但能发生银镜反应
发生显色反应,但能发生银镜反应
②1mol最多能与 溶液恰好完全反应
溶液恰好完全反应
③核磁共振氢谱有4组吸收峰
④分子中没有两个甲基连在同一个碳原子上
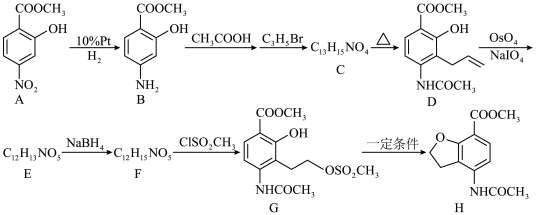
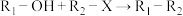
②克莱森重排反应: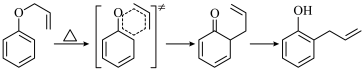
(1)B中的官能团名称为
(2)E的结构简式为
(3)下列说法正确的是___________。
A.C能与 发生显色反应 发生显色反应 |
B.1mol E最多能与 发生加成反应 发生加成反应 |
| C.B分子中所有碳原子可能共平面 |
| D.图示流程中没有发生克莱森重排反应 |
(4)F→G有一种分子式为
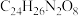 的副产物生成,写出生成该副产物的反应方程式
的副产物生成,写出生成该副产物的反应方程式(5)设计以苯,1,3-丁二烯为原料合成
 的路线(用流程图表示,无机试剂、有机溶剂任选)
的路线(用流程图表示,无机试剂、有机溶剂任选)(6)写出同时符合下列条件的
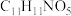 的同分异构体的结构简式
的同分异构体的结构简式①不能与
 发生显色反应,但能发生银镜反应
发生显色反应,但能发生银镜反应②1mol最多能与
 溶液恰好完全反应
溶液恰好完全反应③核磁共振氢谱有4组吸收峰
④分子中没有两个甲基连在同一个碳原子上
您最近一年使用:0次
解题方法
8 . 下列说法正确的是
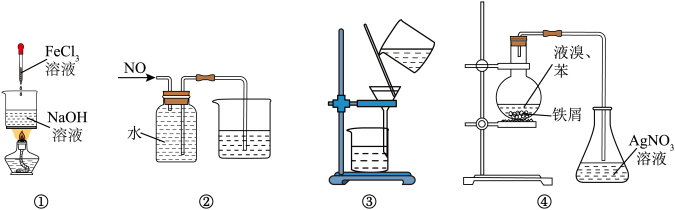
| A.图①装置可用于制备氢氧化铁胶体 |
B.图②装置可用于收集 |
| C.图③装置可用于常温下分离苯酚和水的混合物 |
| D.图④装置可证明苯与液溴发生了取代反应 |
您最近一年使用:0次
解题方法
9 . 室温下,用含少量 的
的 溶液制备
溶液制备 的过程如题图所示:
的过程如题图所示: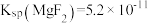 ,
,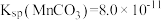 ;
;
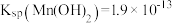 ,
,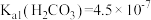 ,
,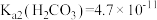
下列说法正确的是
 的
的 溶液制备
溶液制备 的过程如题图所示:
的过程如题图所示:
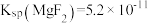 ,
,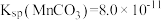 ;
;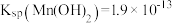 ,
,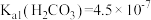 ,
,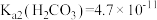
下列说法正确的是
A. 饱和溶液中: 饱和溶液中: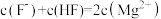 |
B.为提高 的产率,使用 的产率,使用 溶液“沉锰”效果更好 溶液“沉锰”效果更好 |
C.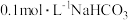 溶液中, 溶液中,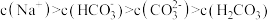 |
D.反应 的平衡常数为 的平衡常数为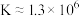 |
您最近一年使用:0次
解题方法
10 . 某研究团队通过膜电解法制得纯碱,甘氨酸(H2NCH2COOH)和高浓度烧碱,其装置如图所示。其中膜a、b为离子交换膜,双极膜c在直流电的作用下,中间界面层水发生解离产生H+和OH-。下列说法正确的是

| A.膜a为阴离子交换膜 |
| B.制得7.5g甘氨酸,盐室1增重2.2g |
| C.碱室2反应式:2H2O-4e-=O2↑+4H+ |
| D.一段时间后,碱室1浓度变小,碱室2浓度变大 |
您最近一年使用:0次



