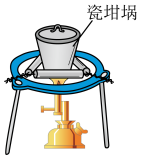
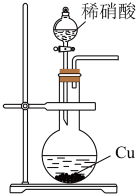
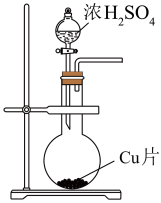
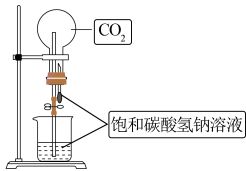
1 . 用下列装置及药品能达到实验目的的是
| |
| A.熔化NaOH | B.制备NO |
|
|
| C.制备SO2 | D.作喷泉实验 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
2 . 为了除去粗盐中的Ca2+、Mg2+、 以及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如下(用于沉淀的试剂均过量)
以及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如下(用于沉淀的试剂均过量)
 以及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如下(用于沉淀的试剂均过量)
以及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如下(用于沉淀的试剂均过量)
| A.第⑤步操作用到的玻璃仪器只有烧杯、漏斗和玻璃棒 |
| B.“?”处的试剂可以是NaOH溶液也可以是KOH溶液 |
| C.步骤②和④顺序可以颠倒 |
| D.第④发生的反应只有CaCl2+Na2CO3=CaCO3↓+2NaCl |
您最近一年使用:0次
名校
3 . 向容积为1.00L的密闭容器中通入一定量的N2O4和NO2的混合气体,发生反应:N2O4(g)⇌2NO2(g),体系中各物质浓度随时间变化如图。下列有关说法不正确的是

| A.到达化学平衡前,混合气体的颜色逐渐变深 |
| B.64s时N2O4和NO2的反应速率一定相等 |
| C.当v正(NO2)=2v逆(N2O4),反应达到化学平衡状态 |
| D.前100s内,用NO2浓度的变化表示的化学反应速率是0.008mol·L-1·s-1 |
您最近一年使用:0次
名校
解题方法
4 . 请用所学知识填空。
(1)相对分子质量为128的烷烃习惯性命名为:_______ 。
(2)硝酸是重要的化工原料,下图为合成氨以及氨氧化制硝酸的流程图,请结合你所学的知识回答以下问题:_______ (填序号)。
b.②反应的化学方程式为_______ 。
(3)①若A、B电极材料分别为铜和锌,溶液C为稀硫酸溶液,电流表指针发生偏转,则B电极上发生的电极反应为_______ 。
②若A、B电极材料分别为铜和银,溶液C为氯化铁溶液,则B电极上发生的电极反应为_______ ;若有0.2mol电子通过导线,则负极减轻_______ g。
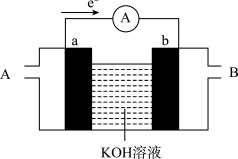
(4)某种燃料电池的工作原理示意如图所示,a、b均为惰性电极。_______ (填“A”或“B”)口通入。假设使用的“燃料”是H2,a极的电极反应式为_______ 。
(1)相对分子质量为128的烷烃习惯性命名为:
(2)硝酸是重要的化工原料,下图为合成氨以及氨氧化制硝酸的流程图,请结合你所学的知识回答以下问题:
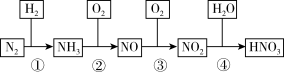
b.②反应的化学方程式为
(3)①若A、B电极材料分别为铜和锌,溶液C为稀硫酸溶液,电流表指针发生偏转,则B电极上发生的电极反应为
②若A、B电极材料分别为铜和银,溶液C为氯化铁溶液,则B电极上发生的电极反应为
(4)某种燃料电池的工作原理示意如图所示,a、b均为惰性电极。
您最近一年使用:0次
名校
解题方法
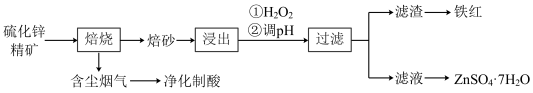
5 . 某硫化锌精矿的主要成分为ZnS(还含一定量FeS),以其为原料制备七水合硫酸锌(ZnSO4·7H2O)与铁红的工艺流程如图所示:
①焙砂的成分是ZnO和FeO
②相关金属离子形成氢氧化物沉淀的pH范围如下:
回答下列问题:
(1)“焙烧”时为了加快反应速率,可以采取的措施是_______ ,其中ZnS发生反应的化学方程式为_______ 。“净化制酸”所得的产品可用于后续的_______ 操作。
(2)“浸出”后加入H2O2发生反应的离子方程式为_______ ,调pH的目的是将Fe3+完全转化为Fe(OH)3沉淀并与Zn2+分离,为达到该目的,调节pH的范围是_______ 。
(3)“滤渣”的化学式是_______ ,由“滤液”得到ZnSO4·7H2O的操作是蒸发浓缩、_______ 、过滤洗涤。
①焙砂的成分是ZnO和FeO
②相关金属离子形成氢氧化物沉淀的pH范围如下:
| 金属离子 | Fe3+ | Fe2+ | Zn2+ |
| 开始沉淀的pH | 1.5 | 6.3 | 6.2 |
| 沉淀完全的pH | 2.8 | 8.3 | 8.2 |
(1)“焙烧”时为了加快反应速率,可以采取的措施是
(2)“浸出”后加入H2O2发生反应的离子方程式为
(3)“滤渣”的化学式是
您最近一年使用:0次
名校
6 . 实验室可用如图装置(略去部分夹持仪器)制取SO2并验证其性质。_______ ,仪器组装完成后,关闭两端活塞,向装置B的长颈漏斗内注入液体至形成段液柱,若_______ 则整个装置气密性良好。
(2)A中如果用浓硫酸和铜反应,也可制得 进行实验,反应的化学方程式为
进行实验,反应的化学方程式为_______ 。
(3)C试管中的试剂可以验证二氧化硫的氧化性,现象为_______ 。
(4)为验证二氧化硫的还原性,充分反应后,取试管D中的溶液分成三份,分别进行实验:
方案Ⅰ:向第一份溶液中加入 溶液,有白色沉淀生成;
溶液,有白色沉淀生成;
方案Ⅱ:向第二份溶液中加入品红溶液,红色褪去;
方案Ⅲ:向第三份溶液中加入 溶液,产生白色沉淀
溶液,产生白色沉淀
上述方案合理的是方案_______ (填“Ⅰ”“Ⅱ”或“Ⅲ”); 通入KMnO4溶液中发生的主要反应的离子方程式为
通入KMnO4溶液中发生的主要反应的离子方程式为_______ 。
(5)装置E的作用是做安全瓶,防止F中的液体倒吸入D中,装置F中为_______ 溶液。

(2)A中如果用浓硫酸和铜反应,也可制得
 进行实验,反应的化学方程式为
进行实验,反应的化学方程式为(3)C试管中的试剂可以验证二氧化硫的氧化性,现象为
(4)为验证二氧化硫的还原性,充分反应后,取试管D中的溶液分成三份,分别进行实验:
方案Ⅰ:向第一份溶液中加入
 溶液,有白色沉淀生成;
溶液,有白色沉淀生成;方案Ⅱ:向第二份溶液中加入品红溶液,红色褪去;
方案Ⅲ:向第三份溶液中加入
 溶液,产生白色沉淀
溶液,产生白色沉淀上述方案合理的是方案
 通入KMnO4溶液中发生的主要反应的离子方程式为
通入KMnO4溶液中发生的主要反应的离子方程式为(5)装置E的作用是做安全瓶,防止F中的液体倒吸入D中,装置F中为
您最近一年使用:0次
名校
7 . 一定温度下,把2.5molA和2.5molB混合盛入容积为2L的密闭容器里,发生如下反应:3A(g)+B(s)⇌xC(g)+2D(g),经5s反应达平衡,在此5s内C的平均反应速率为0.2mol·L-1·s-1,同时生成1molD,下列叙述中不正确的是
| A.反应达到平衡状态时A的转化率为60% |
| B.x=4 |
| C.反应达到平衡状态时,相同条件下容器内气体的压强与起始时压强比为8∶5 |
| D.某条件下,该反应的v(A)=0.6mol·L-1·s-1,v(D)=24mol·L-1·min-1,此时D表示的反应速率更快 |
您最近一年使用:0次
名校
解题方法
8 . 油气开采的废气含有H2S,一种处理方法是高温将其分解:2H2S(g) S2(g)+2H2(g)(吸热反应),在2L恒容密闭容器中充入1molH2S发生该反应。下列说法正确的是
S2(g)+2H2(g)(吸热反应),在2L恒容密闭容器中充入1molH2S发生该反应。下列说法正确的是
 S2(g)+2H2(g)(吸热反应),在2L恒容密闭容器中充入1molH2S发生该反应。下列说法正确的是
S2(g)+2H2(g)(吸热反应),在2L恒容密闭容器中充入1molH2S发生该反应。下列说法正确的是| A.充入Ne后气体总压强增大,反应速率加快 |
| B.调控反应温度,可使S2(g)浓度达到0.25mol/L |
| C.达到平衡时,c(H2S):c(S2):c(H2)=2:1:2 |
| D.当气体的平均摩尔质量不变时,反应达平衡 |
您最近一年使用:0次
名校
解题方法
9 . 自然界中臭氧形成反应3O2(g)=2O3(g)的能量变化如图所示。下列说法中错误的是

| A.2O3(g)=3O2(g)为放热反应 |
| B.氧气比臭氧稳定 |
| C.反应物断键吸收的总能量高于生成物成键放出的总能量 |
| D.反应消耗3molO2时吸收的总能量为E3-E1 |
您最近一年使用:0次
名校
解题方法
10 . NA代表阿伏加德罗常数的值。下列说法正确的是
| A.50mL18.4mol·L-1的浓硫酸与足量的铜在加热条件下反应,生成SO2分子的数目为0.46NA |
| B.5.6g铁粉与1L1mol·L-1的HCl溶液充分反应,产生的气体分子数目为0.1NA |
| C.标准状况下,2.24LSO2与1.12LO2充分反应,生成的SO3分子数目为0.1NA |
| D.1.7gNH3完全溶于1LH2O所得溶液中,NH3·H2O微粒数目为0.1NA |
您最近一年使用:0次