1 . 下列叙述正确的是
| A.电解饱和氯化钠溶液可得金属钠 |
| B.工业上可利用铝热反应制取钒、铬、锰 |
| C.煤的干馏属于物理变化 |
| D.食品添加剂可用于掩盖食品的腐败变质 |
您最近一年使用:0次
2 . 糖类、油脂和蛋白质是维持人体生命活动所必需的三大营养物质。以下叙述错误的是
| A.糖类、油脂、蛋白质都是天然高分子化合物 |
B.可以用新制的 悬浊液鉴别蔗糖和葡萄糖 悬浊液鉴别蔗糖和葡萄糖 |
| C.用灼烧的方法可以鉴别织物是真丝还是人造丝 |
| D.利用油脂的皂化反应可以制备甘油和肥皂 |
您最近一年使用:0次
名校
解题方法
3 . 某α,β-不饱和烯醛是一种药物中间体,其合成路线如下:
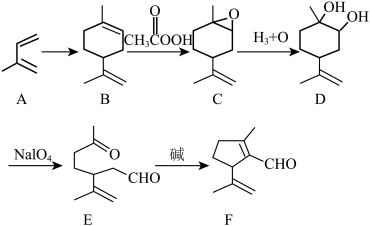
(1)F中含氧官能团名称为___________ ,检验该官能团可用的化学试剂为___________ 。
(2)B→C的反应类型为___________ 。
(3)A化学名称为___________ ,NaIO4中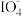 的空间结构为
的空间结构为___________ 。
(4)每个D分子中手性碳原子的数目为___________ 。
(5)F的一种同分异构体同时满足下列条件,写出该同分异构体的一种结构简式___________ 。
①分子中含有苯环,能与FeCl3溶液发生显色反应;
②分子中只有5种不同化学环境的氢。
(6)结合题中信息写出 在NaIO4作用下所得产物的结构简式
在NaIO4作用下所得产物的结构简式_______ 。

(1)F中含氧官能团名称为
(2)B→C的反应类型为
(3)A化学名称为
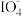 的空间结构为
的空间结构为(4)每个D分子中手性碳原子的数目为
(5)F的一种同分异构体同时满足下列条件,写出该同分异构体的一种结构简式
①分子中含有苯环,能与FeCl3溶液发生显色反应;
②分子中只有5种不同化学环境的氢。
(6)结合题中信息写出
 在NaIO4作用下所得产物的结构简式
在NaIO4作用下所得产物的结构简式
您最近一年使用:0次
2023-07-12更新
|
96次组卷
|
3卷引用:甘肃省定西市临洮县临洮中学2022-2023学年高二下学期期末考试化学试题
4 . 2020年12月17日,我国“嫦娥五号”返回器携月壤成功着陆。根据已经发表的研究成果可知,月壤中存在天然的铁、金、银、铅、锌、铜、锑、铼等矿物颗粒。
(1)写出铜的基态原子的电子排布式___________ 。
(2)Fe在周期表中位于第___________ 周期第___________ 族,属于___________ 区。
(3)基态Fe原子有___________ 个未成对电子,Fe3+的电子排布式为___________ 。
(4)基态Al3+核外共有___________ 种不同运动状态的电子。
(5)采取的月壤中未发现钒(V)元素,其价层电子的轨道表示式为___________ 。钒(V)的某种氧化物的晶胞结构如图(1)所示。该晶体的化学式为___________ 。
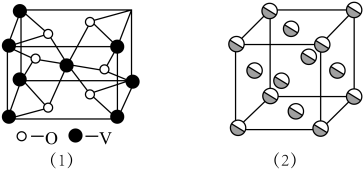
(6)金晶体的晶胞结构如图(2)所示。设金原子的直径为dcm,用NA表示阿伏加德罗常数,M表示金的摩尔质量,金的密度为___________ g/cm3(用d、M、NA表示)。
(1)写出铜的基态原子的电子排布式
(2)Fe在周期表中位于第
(3)基态Fe原子有
(4)基态Al3+核外共有
(5)采取的月壤中未发现钒(V)元素,其价层电子的轨道表示式为

(6)金晶体的晶胞结构如图(2)所示。设金原子的直径为dcm,用NA表示阿伏加德罗常数,M表示金的摩尔质量,金的密度为
您最近一年使用:0次
2023-07-12更新
|
98次组卷
|
2卷引用:甘肃省定西市临洮县临洮中学2022-2023学年高二下学期期末考试化学试题
名校
5 . 勒夏特列通过深入研究高炉炼铁后发现了该过程的主要反应为可逆反应。某科研小组进行类似的研究,以Fe3O4为原料炼铁,主要发生如下反应:
反应I:Fe3O4(s)+CO(g)⇌3FeO(s)+CO2(g) △H1=Q1(Q1>0)
反应II:Fe3O4(s)+4CO(g)⇌3Fe(s)+4CO2(g) △H2=Q2
将一定体积CO通入装有Fe3O4粉末的反应器,其它条件不变,反应达平衡,测得CO的体积分数随温度的变化关系如图所示。

回答下列问题:
(1)判断Q2的正、负值,并说明理由___________ 。
(2)温度升高,反应器中CO体积分数降低,分析可能的原因为___________ 。
(3)1040℃时,反应一段时间后,体系内2个反应均达成平衡,试计算各自的平衡常数Kp___________ 。
(4)炉温不变,扩大炼铁反应器的容积,通过分析说明等量的还原剂能否提升铁矿石的平衡转化率___________ ,能否提升平衡前铁矿石的单位时间转化率___________ 。
(5)将Fe2O3、铁粉和NaOH溶液置于反应器中,在温度大于100℃下搅拌反应半小时以上,反应产物经过一次过滤、水洗、二次过滤、干燥、研磨,可直接得到黑色的Fe3O4细末。试写出该过程的总反应方程式___________ 。
反应I:Fe3O4(s)+CO(g)⇌3FeO(s)+CO2(g) △H1=Q1(Q1>0)
反应II:Fe3O4(s)+4CO(g)⇌3Fe(s)+4CO2(g) △H2=Q2
将一定体积CO通入装有Fe3O4粉末的反应器,其它条件不变,反应达平衡,测得CO的体积分数随温度的变化关系如图所示。

回答下列问题:
(1)判断Q2的正、负值,并说明理由
(2)温度升高,反应器中CO体积分数降低,分析可能的原因为
(3)1040℃时,反应一段时间后,体系内2个反应均达成平衡,试计算各自的平衡常数Kp
(4)炉温不变,扩大炼铁反应器的容积,通过分析说明等量的还原剂能否提升铁矿石的平衡转化率
(5)将Fe2O3、铁粉和NaOH溶液置于反应器中,在温度大于100℃下搅拌反应半小时以上,反应产物经过一次过滤、水洗、二次过滤、干燥、研磨,可直接得到黑色的Fe3O4细末。试写出该过程的总反应方程式
您最近一年使用:0次
2023-07-12更新
|
235次组卷
|
2卷引用:甘肃省定西市临洮县临洮中学2022-2023学年高二下学期期末考试化学试题
名校
6 . 实验室变色硅胶是在硅酸凝胶中添加了CoCl2。一种从水钴矿(主要成分:Co2O3,少量的Fe2O3、CaO、MgO、Al2O3、MnO))制取CoCl2·6H2O工艺流程如下:
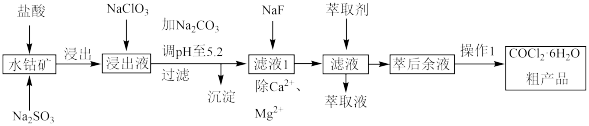
已知:阳离子的氢氧化物沉淀时溶液的pH如下表:
(1)水钴矿在浸取前需要粉碎,目的是___________ 。
(2)Na2SO3在浸取过程中作___________ 剂,写出浸取时Na2SO3与Fe2O3反应的离子方程式___________ 。
(3)写出NaClO3加入浸取后溶液的离子方程式___________ 。
(4)加入碳酸钠调节pH为5.2步骤获得沉淀的成分为___________ 。
(5)“萃取”时发生反应:Co2++n(HA)2⇌CoA2·(n-1)(HA)2+2H+,通过调节pH,设计萃取、反萃取。简述该步骤的原理和目的___________ 。
(6)CoCl2为蓝色,CoC2·6H2O为粉红色。实验室变色硅胶是在硅酸凝胶中添加CoCl2用于指示吸湿程度。请说明CoCl2用于指示吸湿程度的原理___________ 。

已知:阳离子的氢氧化物沉淀时溶液的pH如下表:
| 沉淀物 | Fe(OH)3 | Al(OH)3 | Co(OH)2 | Fe(OH)2 | Mn(OH)2 |
| 开始沉淀 | 2.7 | 4.0 | 7.6 | 7.6 | 7.7 |
| 完全沉淀 | 3.7 | 5.2 | 9.2 | 9.6 | 9.8 |
(2)Na2SO3在浸取过程中作
(3)写出NaClO3加入浸取后溶液的离子方程式
(4)加入碳酸钠调节pH为5.2步骤获得沉淀的成分为
(5)“萃取”时发生反应:Co2++n(HA)2⇌CoA2·(n-1)(HA)2+2H+,通过调节pH,设计萃取、反萃取。简述该步骤的原理和目的
(6)CoCl2为蓝色,CoC2·6H2O为粉红色。实验室变色硅胶是在硅酸凝胶中添加CoCl2用于指示吸湿程度。请说明CoCl2用于指示吸湿程度的原理
您最近一年使用:0次
2023-07-12更新
|
76次组卷
|
2卷引用:甘肃省定西市临洮县临洮中学2022-2023学年高二下学期期末考试化学试题
名校
解题方法
7 . 食品添加剂柠檬酸三钠,使用时必须符合国家标准。用标准的盐酸和电导率仪测得滴加盐酸体积与待测溶液(10mL)电导率的关系如图所示,溶液的浓度均为0.01mol/L。已知:柠檬酸( 分子式为C6H8O7)属于三元弱酸,25℃其电离平衡常数的pKa=-1gKa,pKa1=3.14,pKa2=4.77,pKa3=6.39。下列说法错误的是
分子式为C6H8O7)属于三元弱酸,25℃其电离平衡常数的pKa=-1gKa,pKa1=3.14,pKa2=4.77,pKa3=6.39。下列说法错误的是

 分子式为C6H8O7)属于三元弱酸,25℃其电离平衡常数的pKa=-1gKa,pKa1=3.14,pKa2=4.77,pKa3=6.39。下列说法错误的是
分子式为C6H8O7)属于三元弱酸,25℃其电离平衡常数的pKa=-1gKa,pKa1=3.14,pKa2=4.77,pKa3=6.39。下列说法错误的是
| A.a点代表正盐溶液,c(H+)的数量级为10-10 |
| B.b点溶液显酸性 |
C.c点溶液满足:c(Cl-)>2[c( )+c( )+c( )+c( )+c( )] )] |
| D.电导率与离子浓度有关,与离子所带电荷无关 |
您最近一年使用:0次
2023-07-12更新
|
51次组卷
|
2卷引用:甘肃省定西市临洮县临洮中学2022-2023学年高二下学期期末考试化学试题
名校
8 . 某著名运动员使用了可能有兴奋作用违禁药物事件闹得沸沸扬扬。该药物的结构简式如下图所示,有关该物质的说法正确的是
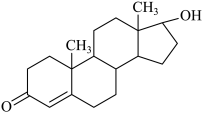
| A.该有机物的分子式为C19H26O2 |
| B.该物质所有的碳原子一定在同一个平面上 |
| C.lmol该化合物最多可与2molH2发生反应 |
| D.该化合物有两种官能团 |
您最近一年使用:0次
2023-07-12更新
|
151次组卷
|
4卷引用:甘肃省定西市临洮县临洮中学2022-2023学年高二下学期期末考试化学试题
9 . 常压下利用可逆反应Ni(s)+4CO(g)⇌Ni(CO)4(g)精炼镍。已知230℃时,该反应的平衡常数K=2×10-5(L/mol)3,Ni(CO)4的沸点为42.2℃,粗镍中固体杂质不参与反应。下列说法错误的是
| A.恒容体系下,增加c[Ni(CO)4],体系压强增大,平衡常数增大 |
| B.50℃时将粗镍与CO反应,可以获得相应的气态产物便于与粗镍杂质分离 |
| C.测量某温度下反应体系中Ni(CO)4体积分数不变时,反应达到平衡 |
| D.230℃,Ni(CO)4平衡分解率较高 |
您最近一年使用:0次
2023-07-12更新
|
113次组卷
|
2卷引用:甘肃省定西市临洮县临洮中学2022-2023学年高二下学期期末考试化学试题
名校
解题方法
10 . 病毒核酸采样管中的红色液体是一种样本保护液,其中含有胍盐,作用于病毒核酸保存。已知胍是有机一元碱,碱性与氢氧化钠相近;胍盐易水解为氨和尿素。以下说法错误的是
| A.核酸和蛋白质都是生物大分子 |
| B.核酸水解最终产物中含有磷酸、六碳糖和碱基 |
| C.胍保存不当时易吸收空气中的CO2而变质 |
| D.合理使用尿素可以促进农作物的生长,提高粮食产量 |
您最近一年使用:0次
2023-07-12更新
|
128次组卷
|
5卷引用:甘肃省定西市临洮县临洮中学2022-2023学年高二下学期期末考试化学试题
甘肃省定西市临洮县临洮中学2022-2023学年高二下学期期末考试化学试题甘肃省兰州市等5地2022-2023学年高二下学期期末化学试题(已下线)4.3核酸(基础)名校期末好题汇编-生物大分子(选择题)(已下线)专题04 生物大分子 合成高分子-【好题汇编】备战2023-2024学年高二化学下学期期末真题分类汇编(人教版2019)



