名校
解题方法
1 . 高锰酸钾溶液常用于物质的定性检验与定量分析。
(1)实验室里欲用KMnO4固体来配制250.00 mL 0.1000 mol•L-1的KMnO4酸性溶液。
①需用的仪器有天平、药匙、烧杯、玻璃棒、量筒、_________ 、_________ 。
②下列关于“容量瓶及其使用”的叙述中正确的是_________ (填序号)。
A.使用前必须检查是否漏水 B.能配制一定体积准确浓度的标准溶液
C.可用来长期贮存溶液 D.能用作溶解固体、稀释浓溶液的容器
③下列操作对实验结果的影响偏高的是_________ (填序号)。
A.加水定容时俯视刻度线
B.未洗涤溶解后的烧杯和玻璃棒
C.颠倒摇匀后发现凹液面低于刻度线,没有加水补到刻度线
D.未经冷却趁热将溶液注入容量瓶中并进行定容
(2)用上述酸性KMnO4溶液来测定FeSO4溶液中Fe2+的物质的量浓度。原理如下:FeSO4 + KMnO4 + H2SO4 — K2SO4 + MnSO4 + Fe2(SO4)3 + H2O (未配平),实验时应测定的数据有:量取FeSO4溶液的体积和__________________ 。该反应中还原剂与氧化剂的物质的量之比为_________ 。
(3)维生素C的水溶液能使高锰酸钾溶液褪色,根据这一原理,常用高锰酸钾测定蔬菜或水果中的维生素C的含量。上述实验原理体现了维生素C具有_____ (填氧化性、还原性)。
(1)实验室里欲用KMnO4固体来配制250.00 mL 0.1000 mol•L-1的KMnO4酸性溶液。
①需用的仪器有天平、药匙、烧杯、玻璃棒、量筒、
②下列关于“容量瓶及其使用”的叙述中正确的是
A.使用前必须检查是否漏水 B.能配制一定体积准确浓度的标准溶液
C.可用来长期贮存溶液 D.能用作溶解固体、稀释浓溶液的容器
③下列操作对实验结果的影响偏高的是
A.加水定容时俯视刻度线
B.未洗涤溶解后的烧杯和玻璃棒
C.颠倒摇匀后发现凹液面低于刻度线,没有加水补到刻度线
D.未经冷却趁热将溶液注入容量瓶中并进行定容
(2)用上述酸性KMnO4溶液来测定FeSO4溶液中Fe2+的物质的量浓度。原理如下:FeSO4 + KMnO4 + H2SO4 — K2SO4 + MnSO4 + Fe2(SO4)3 + H2O (未配平),实验时应测定的数据有:量取FeSO4溶液的体积和
(3)维生素C的水溶液能使高锰酸钾溶液褪色,根据这一原理,常用高锰酸钾测定蔬菜或水果中的维生素C的含量。上述实验原理体现了维生素C具有
您最近一年使用:0次
2023-01-06更新
|
208次组卷
|
2卷引用:新疆塔城地区第一高级中学2022-2023学年高一下学期开学考试化学试题
名校
解题方法
2 . 下面四个反应都可以生成氯气,有关说法不正确的是
①4HCl(浓)
②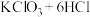 (浓)
(浓)
③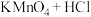 (浓)
(浓)
④
①4HCl(浓)

②
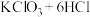 (浓)
(浓)
③
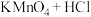 (浓)
(浓)
④

| A.四个反应中盐酸均表现还原性和酸性 |
B.反应②中,氧化产物与还原产物的质量比为 |
C.反应③的离子方程式为 |
D.根据①反应可知,物质氧化性由强到弱的顺序为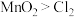 |
您最近一年使用:0次
名校
解题方法
3 .  是一种高效,安全的消毒剂,可用于取代
是一种高效,安全的消毒剂,可用于取代 。实验室制备
。实验室制备 的原理是用亚氯酸钠固体与纯净干燥的氯气反应:
的原理是用亚氯酸钠固体与纯净干燥的氯气反应: 。如图是实验室用于制备和收集一定量纯净
。如图是实验室用于制备和收集一定量纯净 的装置(某些夹持装置省略)。
的装置(某些夹持装置省略)。

(1)圆底烧瓶装有 ,发生反应的化学方程式为:
,发生反应的化学方程式为:_______ ,在该反应中浓盐酸表现的性质是_______ (填序号)。
a.只有还原性 b.还原性和酸性 c.只有氧化性 d.氧化性和酸性
(2)实验中相关气体在不同溶剂中的溶解性如下表所示:
B、E装置中的试剂依次是_______ 、_______ (填序号)。
a.NaOH溶液 b.浓硫酸 c.饱和食盐水 d. e.饱和石灰水
e.饱和石灰水
(3)F处应选用的收集装置是_______ (填序号),其中与E装置导管相连的导管口是_______ (填接口字母)。

(4)装置G的作用_______ 。
(5)家用的二氧化氯 泡腾消毒片由
泡腾消毒片由 、固体酸及辅助剂混合制得,使用时只需将泡腾片放入水中,5~10分钟即可完全溶解,释放出
、固体酸及辅助剂混合制得,使用时只需将泡腾片放入水中,5~10分钟即可完全溶解,释放出 。
。
补全泡腾片在水中发生反应的离子方程式:_______ 。

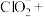



 ↑+
↑+ _______+
_______+ _______
_______
 是一种高效,安全的消毒剂,可用于取代
是一种高效,安全的消毒剂,可用于取代 。实验室制备
。实验室制备 的原理是用亚氯酸钠固体与纯净干燥的氯气反应:
的原理是用亚氯酸钠固体与纯净干燥的氯气反应: 。如图是实验室用于制备和收集一定量纯净
。如图是实验室用于制备和收集一定量纯净 的装置(某些夹持装置省略)。
的装置(某些夹持装置省略)。
(1)圆底烧瓶装有
 ,发生反应的化学方程式为:
,发生反应的化学方程式为:a.只有还原性 b.还原性和酸性 c.只有氧化性 d.氧化性和酸性
(2)实验中相关气体在不同溶剂中的溶解性如下表所示:
 |  | HCl | |
| 水 | 极易溶 | 可溶 | 极易溶 |
 | 难溶 | 易溶 | 难溶 |
a.NaOH溶液 b.浓硫酸 c.饱和食盐水 d.
 e.饱和石灰水
e.饱和石灰水(3)F处应选用的收集装置是

(4)装置G的作用
(5)家用的二氧化氯
 泡腾消毒片由
泡腾消毒片由 、固体酸及辅助剂混合制得,使用时只需将泡腾片放入水中,5~10分钟即可完全溶解,释放出
、固体酸及辅助剂混合制得,使用时只需将泡腾片放入水中,5~10分钟即可完全溶解,释放出 。
。补全泡腾片在水中发生反应的离子方程式:

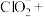



 ↑+
↑+ _______+
_______+ _______
_______
您最近一年使用:0次
名校
4 . 硫酸亚锡(SnSO4)是一种重要的硫酸盐,广泛应用于镀锡工业。某研究小组设计SnSO4制备路线如图:
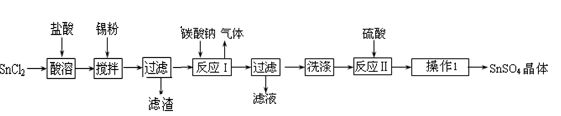
查阅资料:Ⅰ.酸性条件下,锡在水溶液中有Sn2+、Sn4+两种主要存在形式,Sn2+易被氧化。
Ⅱ.SnCl2易水解生成碱式氯化亚锡。请回答下列问题:
(1)SnCl2粉末需加浓盐酸进行溶解,请用平衡移动原理解释原因___ 。
(2)加入Sn粉的作用有两个:调节溶液pH和___ 。
(3)反应Ⅰ得到沉淀是SnO,得到该沉淀的离子反应方程式是___ 。
(4)酸性条件下,SnSO4还可以用作双氧水去除剂,发生反应的离子方程式是__ 。
(5)该小组通过下列方法测定所用锡粉的纯度(杂质不参与反应):
①将试样溶于盐酸中,发生的反应为:Sn+2HCl=SnCl2+H2↑;
②加入过量的FeCl3溶液;
③用已知浓度的K2Cr2O7滴定②中生成的Fe2+,发生的反应为:6FeCl2+K2Cr2O7+14HCl=6FeCl3+2KCl+2CrCl3+7H2O
取1.190g锡粉,经上述各步反应后,共用去0.100mol/LK2Cr2O7溶液25.00mL。锡粉中锡的质量分数是___ 。

查阅资料:Ⅰ.酸性条件下,锡在水溶液中有Sn2+、Sn4+两种主要存在形式,Sn2+易被氧化。
Ⅱ.SnCl2易水解生成碱式氯化亚锡。请回答下列问题:
(1)SnCl2粉末需加浓盐酸进行溶解,请用平衡移动原理解释原因
(2)加入Sn粉的作用有两个:调节溶液pH和
(3)反应Ⅰ得到沉淀是SnO,得到该沉淀的离子反应方程式是
(4)酸性条件下,SnSO4还可以用作双氧水去除剂,发生反应的离子方程式是
(5)该小组通过下列方法测定所用锡粉的纯度(杂质不参与反应):
①将试样溶于盐酸中,发生的反应为:Sn+2HCl=SnCl2+H2↑;
②加入过量的FeCl3溶液;
③用已知浓度的K2Cr2O7滴定②中生成的Fe2+,发生的反应为:6FeCl2+K2Cr2O7+14HCl=6FeCl3+2KCl+2CrCl3+7H2O
取1.190g锡粉,经上述各步反应后,共用去0.100mol/LK2Cr2O7溶液25.00mL。锡粉中锡的质量分数是
您最近一年使用:0次
名校
5 . 公元前9世纪,二氧化硫就被用于消毒和漂白。实验室可用下列装置(部分夹持仪器略去)制取 并验证其性质。
并验证其性质。
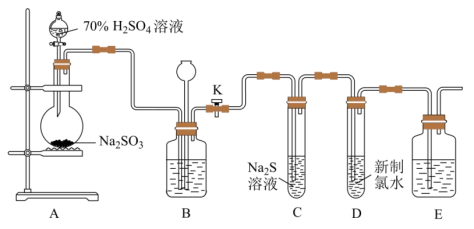
(1)检查装置A、B气密性的操作为:先关闭装置A中分液漏斗活塞和装置B中止水夹K,往长颈漏斗中注水至水柱高于广口瓶液面,若观察到_______ ,则气密性良好。
(2)装置A中反应的化学方程_______ 。
(3)实验时,通气一段时间后,C中试管中出现大量淡黄色浑浊现象,证明二氧化硫具有_______ (填“还原性”、“氧化性”或“漂白性”)。经测定,产物中含有一种摩尔质量为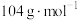 的盐,该盐的化学式为
的盐,该盐的化学式为_______ 。
(4)实验结束时,关闭止水夹K,装置B所起的作用是_______
(5)取少量试管D中的溶液,加入 溶液,产生白色沉淀。
溶液,产生白色沉淀。
①该白色沉淀为_______ (写化学式)。
②原试管D中反应的化学方程式为_______ 。
 并验证其性质。
并验证其性质。
(1)检查装置A、B气密性的操作为:先关闭装置A中分液漏斗活塞和装置B中止水夹K,往长颈漏斗中注水至水柱高于广口瓶液面,若观察到
(2)装置A中反应的化学方程
(3)实验时,通气一段时间后,C中试管中出现大量淡黄色浑浊现象,证明二氧化硫具有
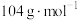 的盐,该盐的化学式为
的盐,该盐的化学式为(4)实验结束时,关闭止水夹K,装置B所起的作用是
(5)取少量试管D中的溶液,加入
 溶液,产生白色沉淀。
溶液,产生白色沉淀。①该白色沉淀为
②原试管D中反应的化学方程式为
您最近一年使用:0次
名校
解题方法
6 . 依据图中氮元素及其化合物的转化关系,回答问题:
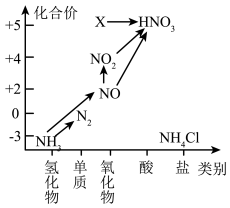
(1)图中X的化学式为_______ 。
(2)实验室常用NH4C1与Ca(OH)2制取氨气,该反应的化学方程式为_______ 。
(3)实验室收集NH3方法_______ 。
A.向上排空法 B.向下排空法 C.排水法
(4)如何检验NH4Cl溶液中阳离子_______ 。
(5)写出NH3 → NO的化学方程式:_______ 。
(6)久置浓硝酸呈黄色的原因是_______ ,(用化学方程式解释)。
(7)预测N2O可能有_______ 性质。
A.仅有还原性
B.仅有氧化性
C.既有氧化性又有还原性

(1)图中X的化学式为
(2)实验室常用NH4C1与Ca(OH)2制取氨气,该反应的化学方程式为
(3)实验室收集NH3方法
A.向上排空法 B.向下排空法 C.排水法
(4)如何检验NH4Cl溶液中阳离子
(5)写出NH3 → NO的化学方程式:
(6)久置浓硝酸呈黄色的原因是
(7)预测N2O可能有
A.仅有还原性
B.仅有氧化性
C.既有氧化性又有还原性
您最近一年使用:0次
名校
7 . 铝和铝合金是一类重要的金属材料。回答下列问题:
(1)除去镁粉中混有的少量铝粉,加入某试剂后反应的离子方程式为_______
(2)某同学在实验室用铝土矿(含有 和
和 ),不考虑其他杂质)制取金属铝的流程如下:
),不考虑其他杂质)制取金属铝的流程如下:
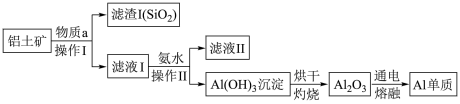
①操作I所加物质a为_______ (选填 或NaOH),
或NaOH), 与a反应的离子方程式为
与a反应的离子方程式为_______ 。
②滤液II中溶质的用途之一是_______ 。
③工业上冶炼铝的化学反应方程式_______
(3)铝与 在酸性或碱性条件下均可反应,为了降低饮用水中
在酸性或碱性条件下均可反应,为了降低饮用水中 的浓度,可以在碱性条件下用铝粉将
的浓度,可以在碱性条件下用铝粉将 还原为
还原为 ,完善并配平该反应:
,完善并配平该反应:_______ 。

(4)已知:CCl4与水不相溶且密度比水大,Cl2的CCl4溶液呈黄绿色,Br2的CCl4溶液呈橙红色,且Br2易从水溶液中溶入CCl4中。Cl2既能氧化 ,也能氧化
,也能氧化 。
。
①取 溶液,向其中滴加几滴新制的氯水,振荡后溶液呈黄色。取少量反应后的溶液加入KSCN溶液,溶液变为红色。另取少量反应后的溶液加入CCl4,振荡后,下层为无色液体。以上实验结论表明还原性:
溶液,向其中滴加几滴新制的氯水,振荡后溶液呈黄色。取少量反应后的溶液加入KSCN溶液,溶液变为红色。另取少量反应后的溶液加入CCl4,振荡后,下层为无色液体。以上实验结论表明还原性: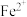
_______  (填“>”或“<”)。
(填“>”或“<”)。
②若在 溶液中通入标准状况下672mL的Cl2,取少量反应后的溶液加入CCl4,振荡后下层液体呈
溶液中通入标准状况下672mL的Cl2,取少量反应后的溶液加入CCl4,振荡后下层液体呈_______ 色,写出该反应的离子方程式_______ 。
(1)除去镁粉中混有的少量铝粉,加入某试剂后反应的离子方程式为
(2)某同学在实验室用铝土矿(含有
 和
和 ),不考虑其他杂质)制取金属铝的流程如下:
),不考虑其他杂质)制取金属铝的流程如下:
①操作I所加物质a为
 或NaOH),
或NaOH), 与a反应的离子方程式为
与a反应的离子方程式为②滤液II中溶质的用途之一是
③工业上冶炼铝的化学反应方程式
(3)铝与
 在酸性或碱性条件下均可反应,为了降低饮用水中
在酸性或碱性条件下均可反应,为了降低饮用水中 的浓度,可以在碱性条件下用铝粉将
的浓度,可以在碱性条件下用铝粉将 还原为
还原为 ,完善并配平该反应:
,完善并配平该反应:
(4)已知:CCl4与水不相溶且密度比水大,Cl2的CCl4溶液呈黄绿色,Br2的CCl4溶液呈橙红色,且Br2易从水溶液中溶入CCl4中。Cl2既能氧化
 ,也能氧化
,也能氧化 。
。①取
 溶液,向其中滴加几滴新制的氯水,振荡后溶液呈黄色。取少量反应后的溶液加入KSCN溶液,溶液变为红色。另取少量反应后的溶液加入CCl4,振荡后,下层为无色液体。以上实验结论表明还原性:
溶液,向其中滴加几滴新制的氯水,振荡后溶液呈黄色。取少量反应后的溶液加入KSCN溶液,溶液变为红色。另取少量反应后的溶液加入CCl4,振荡后,下层为无色液体。以上实验结论表明还原性: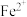
 (填“>”或“<”)。
(填“>”或“<”)。②若在
 溶液中通入标准状况下672mL的Cl2,取少量反应后的溶液加入CCl4,振荡后下层液体呈
溶液中通入标准状况下672mL的Cl2,取少量反应后的溶液加入CCl4,振荡后下层液体呈
您最近一年使用:0次
名校
8 . (1)当光束通过下列物质时,会出现丁达尔效应的是_______ 。
①Fe(OH)3胶体,②水,③蔗糖溶液,④Ca(OH)2悬浊液
(2)维生素C又称“抗坏血酸”,在人体内有重要的功能。例如,能帮助人体将食物中摄取的、不易吸收的Fe3+转变为易吸收的Fe2+,这说明维生素C具有_______ (填“氧化性”或“还原性”)。
(3)下列各组混合物的分离或提纯选用哪种方法最合适?(把选用的标号填入括号内)
A.萃取 B.分液 C.过滤 D.加热分解 E.蒸发 F.蒸馏 H.升华
①把溴水中的溴提取出来_______
②分离柴油和水的混合物_______
③分离四氯化碳(沸点为 76.75℃)和甲苯(沸点为 110.6℃)的混合物_______
(4)现有以下物质:①Ba(OH)2晶体,②盐酸,③冰醋酸(固态醋酸),④石墨,⑤酒精(C2H5OH),请回答下列问题(填序号):
Ⅰ、以上物质中属于电解质的是_______ 。
Ⅱ、以上物质中属于非电解质的是_______ 。
Ⅲ、请写出①在水溶液中的电离方程式_______ 。
(5)某学校实验室有一瓶浓硫酸试剂,标签上标有密度1.84g·cm-3,质量分数98%,现用该浓硫酸配制480 mL 1mol·L﹣1的稀硫酸。可供选用的仪器有:①胶头滴管;②烧瓶;③烧杯;④药匙;⑤量筒;⑥托盘天平;⑦玻璃棒。请回答下列问题:
a.配制稀硫酸时,除了上述仪器,还缺少的仪器有_______ (写仪器名称)。
b.经计算,配制480mL 1mol·L-1的稀硫酸,需要用量筒量取上述浓硫酸的体积为_______ mL。
①Fe(OH)3胶体,②水,③蔗糖溶液,④Ca(OH)2悬浊液
(2)维生素C又称“抗坏血酸”,在人体内有重要的功能。例如,能帮助人体将食物中摄取的、不易吸收的Fe3+转变为易吸收的Fe2+,这说明维生素C具有
(3)下列各组混合物的分离或提纯选用哪种方法最合适?(把选用的标号填入括号内)
A.萃取 B.分液 C.过滤 D.加热分解 E.蒸发 F.蒸馏 H.升华
①把溴水中的溴提取出来
②分离柴油和水的混合物
③分离四氯化碳(沸点为 76.75℃)和甲苯(沸点为 110.6℃)的混合物
(4)现有以下物质:①Ba(OH)2晶体,②盐酸,③冰醋酸(固态醋酸),④石墨,⑤酒精(C2H5OH),请回答下列问题(填序号):
Ⅰ、以上物质中属于电解质的是
Ⅱ、以上物质中属于非电解质的是
Ⅲ、请写出①在水溶液中的电离方程式
(5)某学校实验室有一瓶浓硫酸试剂,标签上标有密度1.84g·cm-3,质量分数98%,现用该浓硫酸配制480 mL 1mol·L﹣1的稀硫酸。可供选用的仪器有:①胶头滴管;②烧瓶;③烧杯;④药匙;⑤量筒;⑥托盘天平;⑦玻璃棒。请回答下列问题:
a.配制稀硫酸时,除了上述仪器,还缺少的仪器有
b.经计算,配制480mL 1mol·L-1的稀硫酸,需要用量筒量取上述浓硫酸的体积为
您最近一年使用:0次
名校
解题方法
9 . 某化学兴趣小组为探究氧化性强弱的影响因素进行如下实验。
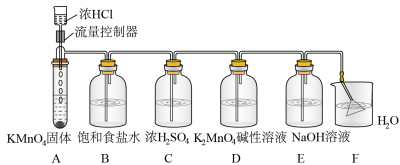
(1)饱和食盐水的作用是______________ 。装置F可吸收微量氯气制得氯水,使用倒置漏斗的目的是_________________________ 。
(2)装置A中产生Cl2的化学方程式为________ ,可推知氧化性:Cl2____  (填“>”或“<”)。
(填“>”或“<”)。
(3)装置D中可观察到溶液变紫红色,则该反应的离子方程式为_________ ,可推知氧化性Cl2____  (填“>”或“<”)。
(填“>”或“<”)。
(4)通过对比(2)和(3)可判断的氧化性强弱的影响因素是__________ 。利用本实验充分反应所得溶液设计实验验证你的判断。实验方案为____________________________ 。
(5)有同学认为无需流量控制器,你是否认可?并简要说明理由_______________ 。

(1)饱和食盐水的作用是
(2)装置A中产生Cl2的化学方程式为
 (填“>”或“<”)。
(填“>”或“<”)。(3)装置D中可观察到溶液变紫红色,则该反应的离子方程式为
 (填“>”或“<”)。
(填“>”或“<”)。(4)通过对比(2)和(3)可判断的氧化性强弱的影响因素是
(5)有同学认为无需流量控制器,你是否认可?并简要说明理由
您最近一年使用:0次
2020-08-12更新
|
179次组卷
|
2卷引用:新疆维吾尔自治区塔城地区第二中学2022-2023学年高三上学期11月月考化学试题(B)
名校
10 . 下列对卤素的说法不符合递变规律的是( )
| A.F2、Cl2、Br2、I2的氧化性逐渐减弱 | B.HF、HCl、HBr、HI的热稳定性逐渐减弱 |
| C.F-、Cl-、Br-、I-的还原性逐渐增强 | D.卤素单质按F2、Cl2、Br2、I2的顺序颜色变浅,密度增大 |
您最近一年使用:0次
2017-03-28更新
|
293次组卷
|
8卷引用:新疆塔城地区第一高级中学2022-2023学年高一下学期开学考试化学试题



