1 . 通过电化学、热化学等方法,将 转化为
转化为 等化学品,是实现“双碳”目标的途径之一。请回答:
等化学品,是实现“双碳”目标的途径之一。请回答:
(1)某研究小组采用电化学方法将 转化为
转化为 ,装置如图。电极B上的电极反应式是
,装置如图。电极B上的电极反应式是_______ 。
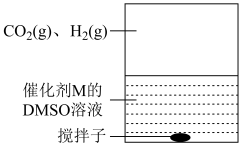
 :
: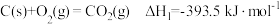
Ⅱ:
Ⅲ: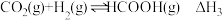
①
_______  。
。
②反应Ⅲ在恒温、恒容的密闭容器中进行, 和
和 的投料浓度均为
的投料浓度均为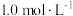 ,平衡常数
,平衡常数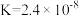 ,则
,则 的平衡转化率为
的平衡转化率为_______ 。
③用氨水吸收 ,得到
,得到 氨水和
氨水和 甲酸铵的混合溶液,
甲酸铵的混合溶液,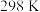 时该混合溶液的
时该混合溶液的
_______ 。[已知: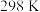 时,电离常数
时,电离常数 、
、 ]
]
(3)为提高效率,该研究小组参考文献优化热化学方法,在如图密闭装置中充分搅拌催化剂M的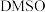 (有机溶剂)溶液,
(有机溶剂)溶液, 和
和 在溶液中反应制备
在溶液中反应制备 ,反应过程中保持
,反应过程中保持 和
和 的压强不变,总反应
的压强不变,总反应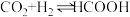 的反应速率为v,反应机理如下列三个基元反应,各反应的活化能
的反应速率为v,反应机理如下列三个基元反应,各反应的活化能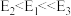 (不考虑催化剂活性降低或丧失)。
(不考虑催化剂活性降低或丧失)。
Ⅳ:

V: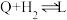

VI: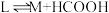

_______ 。
A.v与 的压强无关 B.v与溶液中溶解
的压强无关 B.v与溶液中溶解 的浓度无关
的浓度无关
C.温度升高,v不一定增大 D.在溶液中加入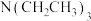 ,可提高
,可提高 转化率
转化率
②实验测得: ,
, 下,v随催化剂M浓度c变化如图。
下,v随催化剂M浓度c变化如图。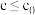 时,v随c增大而增大:
时,v随c增大而增大: 时,v不再显著增大。请解释原因
时,v不再显著增大。请解释原因_______ 。
 转化为
转化为 等化学品,是实现“双碳”目标的途径之一。请回答:
等化学品,是实现“双碳”目标的途径之一。请回答:(1)某研究小组采用电化学方法将
 转化为
转化为 ,装置如图。电极B上的电极反应式是
,装置如图。电极B上的电极反应式是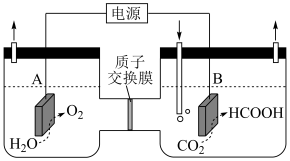
 :
: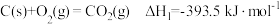
Ⅱ:

Ⅲ:
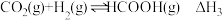
①

 。
。②反应Ⅲ在恒温、恒容的密闭容器中进行,
 和
和 的投料浓度均为
的投料浓度均为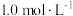 ,平衡常数
,平衡常数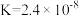 ,则
,则 的平衡转化率为
的平衡转化率为③用氨水吸收
 ,得到
,得到 氨水和
氨水和 甲酸铵的混合溶液,
甲酸铵的混合溶液,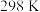 时该混合溶液的
时该混合溶液的
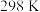 时,电离常数
时,电离常数 、
、 ]
](3)为提高效率,该研究小组参考文献优化热化学方法,在如图密闭装置中充分搅拌催化剂M的
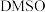 (有机溶剂)溶液,
(有机溶剂)溶液, 和
和 在溶液中反应制备
在溶液中反应制备 ,反应过程中保持
,反应过程中保持 和
和 的压强不变,总反应
的压强不变,总反应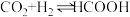 的反应速率为v,反应机理如下列三个基元反应,各反应的活化能
的反应速率为v,反应机理如下列三个基元反应,各反应的活化能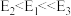 (不考虑催化剂活性降低或丧失)。
(不考虑催化剂活性降低或丧失)。Ⅳ:


V:
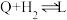

VI:
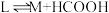

A.v与
 的压强无关 B.v与溶液中溶解
的压强无关 B.v与溶液中溶解 的浓度无关
的浓度无关C.温度升高,v不一定增大 D.在溶液中加入
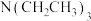 ,可提高
,可提高 转化率
转化率②实验测得:
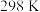 ,
, 下,v随催化剂M浓度c变化如图。
下,v随催化剂M浓度c变化如图。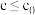 时,v随c增大而增大:
时,v随c增大而增大: 时,v不再显著增大。请解释原因
时,v不再显著增大。请解释原因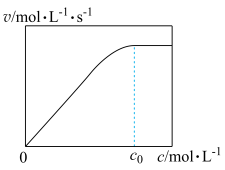
您最近一年使用:0次
2024-02-02更新
|
2081次组卷
|
3卷引用:2024年浙江高考真题化学(1月)
2 . 某温度下,两种难溶盐 的饱和溶液中
的饱和溶液中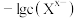 或
或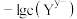 与
与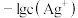 的关系如图所示。下列说法错误的是
的关系如图所示。下列说法错误的是
 的饱和溶液中
的饱和溶液中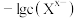 或
或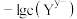 与
与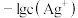 的关系如图所示。下列说法错误的是
的关系如图所示。下列说法错误的是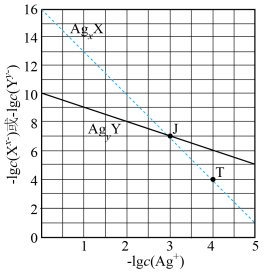
A. |
B.若混合溶液中各离子浓度如J点所示,加入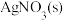 ,则平衡时 ,则平衡时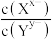 变小 变小 |
C.向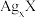 固体中加入 固体中加入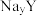 溶液,可发生 溶液,可发生 的转化 的转化 |
D.若混合溶液中各离子起始浓度如T点所示,待平衡时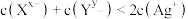 |
您最近一年使用:0次
2023-11-29更新
|
4448次组卷
|
7卷引用:2023年河北省高考化学试卷
2023年河北省高考化学试卷河南省信阳高级中学2023-2024学年高三上学期1月月考理综试题(已下线)专题06 沉淀溶解平衡-【寒假自学课】2024年高二化学寒假提升学与练(人教版2019)宁夏银川一中2023-2024学年高二上学期期末考试化学试题(已下线)题型14 电解质溶液-2024年高考化学二轮热点题型归纳与变式演练(新高考通用)题型15 沉淀溶解平衡及图像分析-2024年高考化学二轮热点题型归纳与变式演练(新高考通用)(已下线)选择题11-14
3 . 银及其化合物在催化与电化学等领域中具有重要应用。
(1)在银催化下,乙烯与氧气反应生成环氧乙烷(EO)和乙醛(AA)。根据图所示,回答下列问题:

①中间体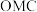 生成吸附态
生成吸附态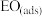 的活化能为
的活化能为_______  。
。
②由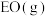 生成
生成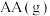 的热化学方程式为
的热化学方程式为_______ 。
(2)一定条件下,银催化剂表面上存在反应: ,该反应平衡压强
,该反应平衡压强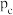 与温度
与温度 的关系如下:
的关系如下:
①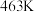 时的平衡常数
时的平衡常数
_______ 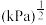 。
。
②起始状态Ⅰ中有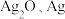 和
和 ,经下列过程达到各平衡状态:
,经下列过程达到各平衡状态:

已知状态Ⅰ和Ⅲ的固体质量相等,下列叙述正确的是_______ (填字母)。
A.从Ⅰ到Ⅱ的过程
B.
C.平衡常数: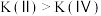
D.若体积 ,则
,则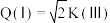
E.逆反应的速率: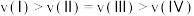
③某温度下,向恒容容器中加入 ,分解过程中反应速率
,分解过程中反应速率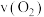 与压强
与压强 的关系为
的关系为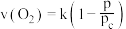 ,k为速率常数(定温下为常数)。当固体质量减少
,k为速率常数(定温下为常数)。当固体质量减少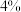 时,逆反应速率最大。若转化率为
时,逆反应速率最大。若转化率为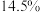 ,则
,则
_______ (用 表示)。
表示)。
(3) 可用作固体离子导体,能通过加热
可用作固体离子导体,能通过加热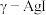 制得。上述两种晶体的晶胞示意图如图所示(为了简化,只画出了碘离子在晶胞中的位置)。
制得。上述两种晶体的晶胞示意图如图所示(为了简化,只画出了碘离子在晶胞中的位置)。

①测定晶体结构最常用的仪器是_______ (填字母)。
A.质谱仪 B.红外光谱仪 C.核磁共振仪 D. 射线衍射仪
射线衍射仪
②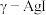 与
与 晶胞的体积之比为
晶胞的体积之比为_______ 。
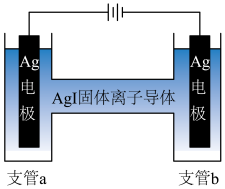
③测定 中导电离子类型的实验装置如图所示。实验测得支管a中
中导电离子类型的实验装置如图所示。实验测得支管a中 质量不变,可判定导电离子是
质量不变,可判定导电离子是 而不是
而不是 ,依据是
,依据是_______ 。
(1)在银催化下,乙烯与氧气反应生成环氧乙烷(EO)和乙醛(AA)。根据图所示,回答下列问题:

①中间体
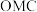 生成吸附态
生成吸附态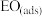 的活化能为
的活化能为 。
。②由
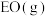 生成
生成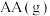 的热化学方程式为
的热化学方程式为(2)一定条件下,银催化剂表面上存在反应:
 ,该反应平衡压强
,该反应平衡压强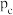 与温度
与温度 的关系如下:
的关系如下: | 401 | 443 | 463 |
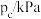 | 10 | 51 | 100 |
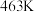 时的平衡常数
时的平衡常数
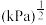 。
。②起始状态Ⅰ中有
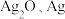 和
和 ,经下列过程达到各平衡状态:
,经下列过程达到各平衡状态:
已知状态Ⅰ和Ⅲ的固体质量相等,下列叙述正确的是
A.从Ⅰ到Ⅱ的过程

B.

C.平衡常数:
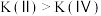
D.若体积
 ,则
,则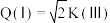
E.逆反应的速率:
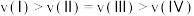
③某温度下,向恒容容器中加入
 ,分解过程中反应速率
,分解过程中反应速率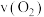 与压强
与压强 的关系为
的关系为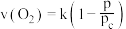 ,k为速率常数(定温下为常数)。当固体质量减少
,k为速率常数(定温下为常数)。当固体质量减少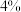 时,逆反应速率最大。若转化率为
时,逆反应速率最大。若转化率为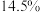 ,则
,则
 表示)。
表示)。(3)
 可用作固体离子导体,能通过加热
可用作固体离子导体,能通过加热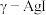 制得。上述两种晶体的晶胞示意图如图所示(为了简化,只画出了碘离子在晶胞中的位置)。
制得。上述两种晶体的晶胞示意图如图所示(为了简化,只画出了碘离子在晶胞中的位置)。
①测定晶体结构最常用的仪器是
A.质谱仪 B.红外光谱仪 C.核磁共振仪 D.
 射线衍射仪
射线衍射仪②
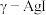 与
与 晶胞的体积之比为
晶胞的体积之比为③测定
 中导电离子类型的实验装置如图所示。实验测得支管a中
中导电离子类型的实验装置如图所示。实验测得支管a中 质量不变,可判定导电离子是
质量不变,可判定导电离子是 而不是
而不是 ,依据是
,依据是
您最近一年使用:0次
2023-09-28更新
|
5401次组卷
|
7卷引用:2023年重庆市高考化学试卷
真题
名校
4 . 我国科学家发现一种钒配合物Ⅰ可以充当固氮反应的催化剂,反应过程中经历的中间体包括Ⅱ和Ⅲ。
(1)配合物Ⅰ中钒的配位原子有4种,它们是_______ 。
(2)配合物Ⅰ中,R′代表芳基, 空间结构呈角形,原因是
空间结构呈角形,原因是_______ 。
(3)配合物Ⅱ中,第一电离能最大的配位原子是_______ 。
(4)配合物Ⅱ和Ⅲ中,钒的化合价分别为 和
和 ,配合物Ⅱ、Ⅲ和
,配合物Ⅱ、Ⅲ和 三者中,两个氮原子间键长最长的是
三者中,两个氮原子间键长最长的是_______ 。
(5)近年来,研究人员发现含钒的锑化物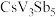 在超导方面表现出潜在的应用前景。
在超导方面表现出潜在的应用前景。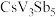 晶胞如图1所示,晶体中包含由V和Sb组成的二维平面(见图2)。
晶胞如图1所示,晶体中包含由V和Sb组成的二维平面(见图2)。_______ 。锑和磷同族,锑原子基态的价层电子排布式为_______ 。
②晶体中少部分钒原子被其它元素(包括Ti、Nb、Cr、Sn)原子取代,可得到改性材料。下列有关替代原子说法正确的是_______ 。
a.有 或
或 价态形式 b.均属于第四周期元素
价态形式 b.均属于第四周期元素
c.均属于过渡元素 d.替代原子与原离子的离子半径相近
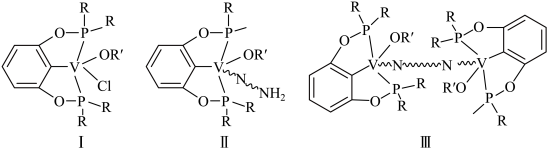
( 代表单键、双键或叁键)
代表单键、双键或叁键)
(1)配合物Ⅰ中钒的配位原子有4种,它们是
(2)配合物Ⅰ中,R′代表芳基,
 空间结构呈角形,原因是
空间结构呈角形,原因是(3)配合物Ⅱ中,第一电离能最大的配位原子是
(4)配合物Ⅱ和Ⅲ中,钒的化合价分别为
 和
和 ,配合物Ⅱ、Ⅲ和
,配合物Ⅱ、Ⅲ和 三者中,两个氮原子间键长最长的是
三者中,两个氮原子间键长最长的是(5)近年来,研究人员发现含钒的锑化物
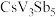 在超导方面表现出潜在的应用前景。
在超导方面表现出潜在的应用前景。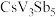 晶胞如图1所示,晶体中包含由V和Sb组成的二维平面(见图2)。
晶胞如图1所示,晶体中包含由V和Sb组成的二维平面(见图2)。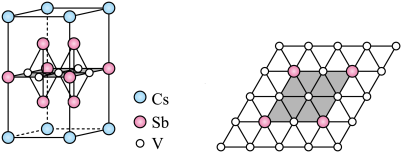
②晶体中少部分钒原子被其它元素(包括Ti、Nb、Cr、Sn)原子取代,可得到改性材料。下列有关替代原子说法正确的是
a.有
 或
或 价态形式 b.均属于第四周期元素
价态形式 b.均属于第四周期元素c.均属于过渡元素 d.替代原子与原离子的离子半径相近
您最近一年使用:0次
2023-08-03更新
|
4517次组卷
|
4卷引用:2023年高考海南卷化学真题
真题
5 . 25℃下, 水溶液的pH随其浓度的变化关系如图所示。下列说法正确的是
水溶液的pH随其浓度的变化关系如图所示。下列说法正确的是
 水溶液的pH随其浓度的变化关系如图所示。下列说法正确的是
水溶液的pH随其浓度的变化关系如图所示。下列说法正确的是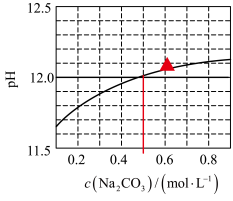
A.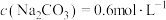 时,溶液中 时,溶液中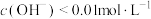 |
B. 水解程度随其浓度增大而减小 水解程度随其浓度增大而减小 |
C.在水中 的 的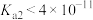 |
D. 的 的 溶液和 溶液和 的 的 溶液等体积混合,得到的溶液 溶液等体积混合,得到的溶液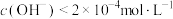 |
您最近一年使用:0次
2023-08-03更新
|
4515次组卷
|
6卷引用:2023年高考海南卷化学真题
2023年高考海南卷化学真题(已下线)不定项选择题(已下线)实验05 盐类水解的应用-【同步实验课】2023-2024学年高二化学教材实验大盘点(人教版2019选择性必修1)(已下线)第31讲盐类的水解(已下线)考点3 盐类水解(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(新高考专用)【精品卷】3.3.1 盐类的水解课堂例题-人教版2023-2024学年选择性必修1
6 . 工业上煅烧含硫矿物产生的 可以按如下流程脱除或利用。
可以按如下流程脱除或利用。
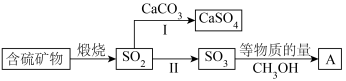
已知: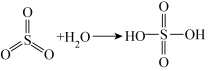
请回答:
(1)富氧煅烧燃煤产生的低浓度的 可以在炉内添加
可以在炉内添加 通过途径Ⅰ脱除,写出反应方程式
通过途径Ⅰ脱除,写出反应方程式___________ 。
(2)煅烧含硫量高的矿物得到高浓度的 ,通过途径Ⅱ最终转化为化合物A。
,通过途径Ⅱ最终转化为化合物A。
①下列说法正确的是___________ 。
A.燃煤中的有机硫主要呈正价 B.化合物A具有酸性
C.化合物A是一种无机酸酯 D.工业上途径Ⅱ产生的 也可用浓
也可用浓 吸收
吸收
②一定压强下,化合物A的沸点低于硫酸的原因是___________ 。
(3)设计实验验证化合物A中含有S元素_____ ;写出实验过程中涉及的反应方程式____ 。
 可以按如下流程脱除或利用。
可以按如下流程脱除或利用。
已知:
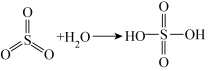
请回答:
(1)富氧煅烧燃煤产生的低浓度的
 可以在炉内添加
可以在炉内添加 通过途径Ⅰ脱除,写出反应方程式
通过途径Ⅰ脱除,写出反应方程式(2)煅烧含硫量高的矿物得到高浓度的
 ,通过途径Ⅱ最终转化为化合物A。
,通过途径Ⅱ最终转化为化合物A。①下列说法正确的是
A.燃煤中的有机硫主要呈正价 B.化合物A具有酸性
C.化合物A是一种无机酸酯 D.工业上途径Ⅱ产生的
 也可用浓
也可用浓 吸收
吸收②一定压强下,化合物A的沸点低于硫酸的原因是
(3)设计实验验证化合物A中含有S元素
您最近一年使用:0次
7 . 卤素可形成许多结构和性质特殊的化合物。回答下列问题:
(1)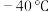 时,
时, 与冰反应生成
与冰反应生成 和
和 。常温常压下,
。常温常压下, 为无色气体,固态
为无色气体,固态 的晶体类型为
的晶体类型为_____ , 水解反应的产物为
水解反应的产物为_____ (填化学式)。
(2) 中心原子为
中心原子为 ,
, 中心原子为
中心原子为 ,二者均为
,二者均为 形结构,但
形结构,但 中存在大
中存在大 键
键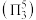 。
。 中
中 原子的轨道杂化方式
原子的轨道杂化方式_____ ;为 键角
键角_____  键角(填“>”“ <”或“=”)。比较
键角(填“>”“ <”或“=”)。比较 与
与 中
中 键的键长并说明原因
键的键长并说明原因_____ 。
(3)一定条件下, 和
和 反应生成
反应生成 和化合物
和化合物 。已知
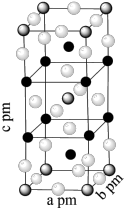
。已知 属于四方晶系,晶胞结构如图所示(晶胞参数
属于四方晶系,晶胞结构如图所示(晶胞参数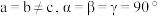 ),其中
),其中 化合价为
化合价为 。上述反应的化学方程式为
。上述反应的化学方程式为_____ 。若阿伏伽德罗常数的值为 ,化合物
,化合物 的密度
的密度
_____  (用含
(用含 的代数式表示)。
的代数式表示)。
(1)
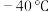 时,
时, 与冰反应生成
与冰反应生成 和
和 。常温常压下,
。常温常压下, 为无色气体,固态
为无色气体,固态 的晶体类型为
的晶体类型为 水解反应的产物为
水解反应的产物为(2)
 中心原子为
中心原子为 ,
, 中心原子为
中心原子为 ,二者均为
,二者均为 形结构,但
形结构,但 中存在大
中存在大 键
键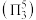 。
。 中
中 原子的轨道杂化方式
原子的轨道杂化方式 键角
键角 键角(填“>”“ <”或“=”)。比较
键角(填“>”“ <”或“=”)。比较 与
与 中
中 键的键长并说明原因
键的键长并说明原因(3)一定条件下,
 和
和 反应生成
反应生成 和化合物
和化合物 。已知
。已知 属于四方晶系,晶胞结构如图所示(晶胞参数
属于四方晶系,晶胞结构如图所示(晶胞参数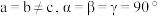 ),其中
),其中 化合价为
化合价为 。上述反应的化学方程式为
。上述反应的化学方程式为 ,化合物
,化合物 的密度
的密度
 (用含
(用含 的代数式表示)。
的代数式表示)。
您最近一年使用:0次
2023-06-19更新
|
10473次组卷
|
10卷引用:2023年高考山东卷化学真题
2023年高考山东卷化学真题(已下线)2023年高考山东卷化学真题变式题(结构与性质)(已下线)专题20 结构与性质(已下线)专题20 结构与性质(已下线)第11讲 氯气和卤族元素(已下线)专题17 物质结构与性质综合题-2023年高考化学真题题源解密(新高考专用)(已下线)专题16 物质结构与性质综合题-2023年高考化学真题题源解密(全国通用)(已下线)第20讲化学键(已下线)考点14 氯及其化合物(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(新高考专用) 河南省南阳市第一中学校2024届高三上学期阶段检测化学试题(12月)
真题
解题方法
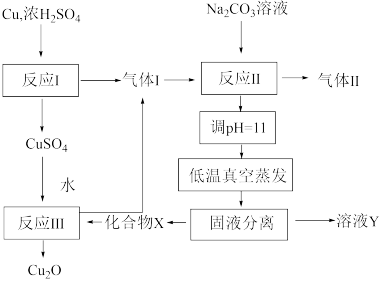
8 . 一种制备 的工艺路线如图所示,反应Ⅱ所得溶液
的工艺路线如图所示,反应Ⅱ所得溶液 在3~4之间,反应Ⅲ需及时补加
在3~4之间,反应Ⅲ需及时补加 以保持反应在
以保持反应在 条件下进行。常温下,
条件下进行。常温下, 的电离平衡常数
的电离平衡常数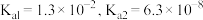 。下列说法正确的是
。下列说法正确的是
 的工艺路线如图所示,反应Ⅱ所得溶液
的工艺路线如图所示,反应Ⅱ所得溶液 在3~4之间,反应Ⅲ需及时补加
在3~4之间,反应Ⅲ需及时补加 以保持反应在
以保持反应在 条件下进行。常温下,
条件下进行。常温下, 的电离平衡常数
的电离平衡常数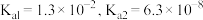 。下列说法正确的是
。下列说法正确的是
| A.反应Ⅰ、Ⅱ、Ⅲ均为氧化还原反应 |
B.低温真空蒸发主要目的是防止 被氧化 被氧化 |
| C.溶液Y可循环用于反应Ⅱ所在操作单元吸收气体Ⅰ |
D.若 产量不变,参与反应Ⅲ的 产量不变,参与反应Ⅲ的 与 与 物质的量之比 物质的量之比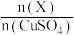 增大时,需补加 增大时,需补加 的量减少 的量减少 |
您最近一年使用:0次
真题
解题方法
9 . 氨是最重要的化学品之一,我国目前氨的生产能力位居世界首位。回答下列问题:
(1)根据图1数据计算反应 的
的
_______  。
。
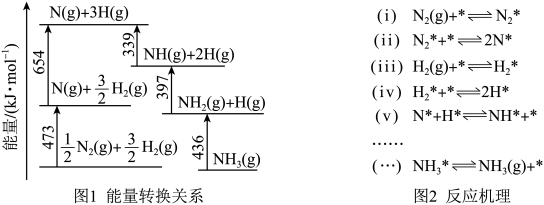
(2)研究表明,合成氨反应在 催化剂上可能通过图2机理进行(*表示催化剂表面吸附位,
催化剂上可能通过图2机理进行(*表示催化剂表面吸附位,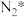 表示被吸附于催化剂表面的
表示被吸附于催化剂表面的 )。判断上述反应机理中,速率控制步骤(即速率最慢步骤)为
)。判断上述反应机理中,速率控制步骤(即速率最慢步骤)为_______ (填步骤前的标号),理由是_______ 。
(3)合成氨催化剂前驱体(主要成分为 )使用前经
)使用前经 还原,生成
还原,生成 包裹的
包裹的 。已知
。已知 属于立方晶系,晶胞参数
属于立方晶系,晶胞参数 ,密度为
,密度为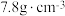 ,则
,则 晶胞中含有
晶胞中含有 的原子数为
的原子数为_______ (列出计算式,阿伏加德罗常数的值为 )。
)。
(4)在不同压强下,以两种不同组成进料,反应达平衡时氨的摩尔分数与温度的计算结果如下图所示。其中一种进料组成为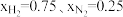 ,另一种为
,另一种为 。(物质i的摩尔分数:
。(物质i的摩尔分数: )
)

①图中压强由小到大的顺序为_______ ,判断的依据是_______ 。
②进料组成中含有惰性气体 的图是
的图是_______ 。
③图3中,当 、
、 时,氮气的转化率
时,氮气的转化率
_______ 。该温度时,反应 的平衡常数
的平衡常数
_______  (化为最简式)。
(化为最简式)。
(1)根据图1数据计算反应
 的
的
 。
。
(2)研究表明,合成氨反应在
 催化剂上可能通过图2机理进行(*表示催化剂表面吸附位,
催化剂上可能通过图2机理进行(*表示催化剂表面吸附位,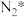 表示被吸附于催化剂表面的
表示被吸附于催化剂表面的 )。判断上述反应机理中,速率控制步骤(即速率最慢步骤)为
)。判断上述反应机理中,速率控制步骤(即速率最慢步骤)为(3)合成氨催化剂前驱体(主要成分为
 )使用前经
)使用前经 还原,生成
还原,生成 包裹的
包裹的 。已知
。已知 属于立方晶系,晶胞参数
属于立方晶系,晶胞参数 ,密度为
,密度为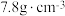 ,则
,则 晶胞中含有
晶胞中含有 的原子数为
的原子数为 )。
)。(4)在不同压强下,以两种不同组成进料,反应达平衡时氨的摩尔分数与温度的计算结果如下图所示。其中一种进料组成为
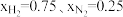 ,另一种为
,另一种为 。(物质i的摩尔分数:
。(物质i的摩尔分数: )
)
①图中压强由小到大的顺序为
②进料组成中含有惰性气体
 的图是
的图是③图3中,当
 、
、 时,氮气的转化率
时,氮气的转化率
 的平衡常数
的平衡常数
 (化为最简式)。
(化为最简式)。
您最近一年使用:0次
真题
解题方法
10 . 光伏组件封装胶膜是太阳能电池的重要材料,经由如图反应路线可分别制备封装胶膜基础树脂Ⅰ和Ⅱ(部分试剂及反应条件略)。
反应路线Ⅰ: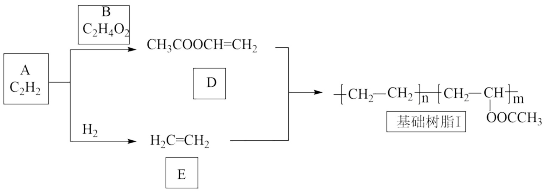
反应路线Ⅱ: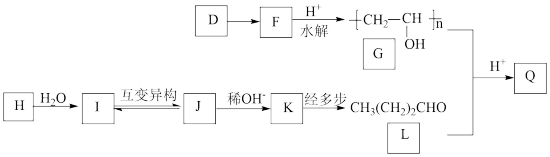
已知以下信息:
①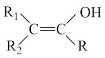
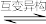
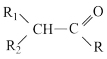

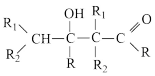 (R、R1、R2为H或烃基)
(R、R1、R2为H或烃基)
② +2ROH
+2ROH
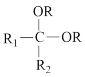 +H2O
+H2O
(1)A+B→D的反应类型为______ 。
(2)基础树脂Ⅰ中官能团的名称为______ 。
(3)F的结构简式为_____ 。
(4)从反应路线Ⅰ中选择某种化合物作为原料H,且H与H2O反应只生成一种产物Ⅰ,则H的化学名称为_____ 。
(5)K与银氨溶液反应的化学方程式为_____ ;K可发生消去反应,其有机产物R的分子式为C4H6O,R及R的同分异构体同时满足含有碳碳双键和碳氧双键的有______ 个(不考虑立体异构),其中核磁共振氢谱只有一组峰的结构简式为______ 。
(6)L与G反应制备非体型结构的Q的化学方程式为_______ 。
(7)为满足性能要求,实际生产中可控制反应条件使F的支链不完全水解,生成的产物再与少量L发生反应,得到含三种链节的基础树脂Ⅱ,其结构简式可表示为_____ 。
反应路线Ⅰ:

反应路线Ⅱ:

已知以下信息:
①

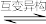
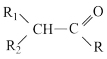

 (R、R1、R2为H或烃基)
(R、R1、R2为H或烃基)②
 +2ROH
+2ROH
 +H2O
+H2O(1)A+B→D的反应类型为
(2)基础树脂Ⅰ中官能团的名称为
(3)F的结构简式为
(4)从反应路线Ⅰ中选择某种化合物作为原料H,且H与H2O反应只生成一种产物Ⅰ,则H的化学名称为
(5)K与银氨溶液反应的化学方程式为
(6)L与G反应制备非体型结构的Q的化学方程式为
(7)为满足性能要求,实际生产中可控制反应条件使F的支链不完全水解,生成的产物再与少量L发生反应,得到含三种链节的基础树脂Ⅱ,其结构简式可表示为
您最近一年使用:0次



