1 . 葡萄糖酸钙是一种可促进骨骼生长的营养物质。葡萄糖酸钙可通过以下反应制得:
C6H12O6(葡萄糖)+Br2+H2O→C6H12O7(葡萄糖酸)+2HBr
2C6H12O7(葡萄糖酸)+CaCO3→Ca(C6H11O7)2(葡萄糖酸钙)+H2O+CO2
相关物质的溶解性见下表:
实验流程如下:


请回答下列问题:
(1)第①步中溴水氧化葡萄糖时,下列装置最合适的是________ 。

制备葡萄糖酸钙的过程中,葡萄糖的氧化也可用其它试剂,下列物质中最适合的是________ 。
A.新制Cu(OH)2悬浊液 B.酸性KMnO4溶液
C.O2/葡萄糖氧化酶 D.[Ag(NH3)2]OH溶液
(2)第②步充分反应后CaCO3固体需有剩余,其目的是________ ;本实验中不宜用CaCl2替代CaCO3,理由是________ 。
(3)第③步需趁热过滤,其原因是________ 。
(4)第④步加入乙醇的作用是________ 。
(5)第⑥步中,下列洗涤剂最合适的是________ 。
A.冷水 B.热水 C.乙醇 D.乙醇-水混合溶液
C6H12O6(葡萄糖)+Br2+H2O→C6H12O7(葡萄糖酸)+2HBr
2C6H12O7(葡萄糖酸)+CaCO3→Ca(C6H11O7)2(葡萄糖酸钙)+H2O+CO2
相关物质的溶解性见下表:
| 物质名称 | 葡萄糖酸钙 | 葡萄糖酸 | 溴化钙 | 氯化钙 |
| 水中的溶解性 | 可溶于冷水 易溶于热水 | 可溶 | 易溶 | 易溶 |
| 乙醇中的溶解性 | 微溶 | 微溶 | 可溶 | 可溶 |


请回答下列问题:
(1)第①步中溴水氧化葡萄糖时,下列装置最合适的是

制备葡萄糖酸钙的过程中,葡萄糖的氧化也可用其它试剂,下列物质中最适合的是
A.新制Cu(OH)2悬浊液 B.酸性KMnO4溶液
C.O2/葡萄糖氧化酶 D.[Ag(NH3)2]OH溶液
(2)第②步充分反应后CaCO3固体需有剩余,其目的是
(3)第③步需趁热过滤,其原因是
(4)第④步加入乙醇的作用是
(5)第⑥步中,下列洗涤剂最合适的是
A.冷水 B.热水 C.乙醇 D.乙醇-水混合溶液
您最近一年使用:0次
2016-12-09更新
|
2104次组卷
|
7卷引用:2014年全国普通高等学校招生统一考试理科综合能力测试化学(浙江卷)
2014年全国普通高等学校招生统一考试理科综合能力测试化学(浙江卷)2014-2015学年广东省汕头市普通高中高二下学期教学测试化学试卷山东省滕州市第一中学2015-2016学年高一4月竞赛化学试题浙江省诸暨中学2017-2018学年高二上学期第二阶段考试化学试题(已下线)二轮复习 专题14 化学实验综合 押题专练【全国百强校】海南省海南中学2018届高三第五次月考化学试题(已下线)解密12 实验化学(讲义)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(浙江专版)
2 . 实验室制备1,2-二溴乙烷的反应原理如下:
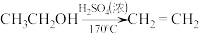
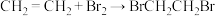
可能存在的主要副反应有:乙醇在浓硫酸的存在下在l40℃脱水生成乙醚。
用少量的溴和足量的乙醇制备1,2—二溴乙烷的装置如下图所示:

有关数据列表如下:
回答下列问题:
(1)在此制备实验中,要尽可能迅速地把反应温度提高到170℃左右,其最主要目的是_____ ;(填正确选项前的字母)
a.引发反应 b.加快反应速度 c.防止乙醇挥发 d.减少副产物乙醚生成
(2)在装置C中应加入______ ,其目的是吸收反应中可能生成的酸性气体:(填正确选项前的字母)
a.水 b.浓硫酸 c.氢氧化钠溶液 d.饱和碳酸氢钠溶液
(3)判断该制备反应已经结束的最简单方法是__________________ ;
(4)将1,2-二溴乙烷粗产品置于分液漏斗中加水,振荡后静置,产物应在___ 层(填“上”、“下”);
(5)若产物中有少量未反应的Br2,最好用____ 洗涤除去;(填正确选项前的字母)
a.水 b.氢氧化钠溶液 c.碘化钠溶液 d.乙醇
(6)若产物中有少量副产物乙醚.可用_______ 的方法除去;
(7)反应过程中应用冷水冷却装置D,其主要目的是___________ ;但又不能过度冷却(如用冰水),其原因是_______________________ 。
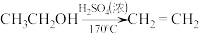
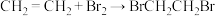
可能存在的主要副反应有:乙醇在浓硫酸的存在下在l40℃脱水生成乙醚。
用少量的溴和足量的乙醇制备1,2—二溴乙烷的装置如下图所示:

有关数据列表如下:
| 乙醇 | 1,2-二溴乙烷 | 乙醚 | |
| 状态 | 色液体 | 无色液体 | 无色液体 |
| 密度/g·cm-3 | 0.79 | 2.2 | 0.71 |
| 沸点/℃ | 78.5 | 132 | 34.6 |
| 熔点/℃ | 一l30 | 9 | -1l6 |
回答下列问题:
(1)在此制备实验中,要尽可能迅速地把反应温度提高到170℃左右,其最主要目的是
a.引发反应 b.加快反应速度 c.防止乙醇挥发 d.减少副产物乙醚生成
(2)在装置C中应加入
a.水 b.浓硫酸 c.氢氧化钠溶液 d.饱和碳酸氢钠溶液
(3)判断该制备反应已经结束的最简单方法是
(4)将1,2-二溴乙烷粗产品置于分液漏斗中加水,振荡后静置,产物应在
(5)若产物中有少量未反应的Br2,最好用
a.水 b.氢氧化钠溶液 c.碘化钠溶液 d.乙醇
(6)若产物中有少量副产物乙醚.可用
(7)反应过程中应用冷水冷却装置D,其主要目的是
您最近一年使用:0次
2016-12-09更新
|
2828次组卷
|
25卷引用:2012年普通高等学校招生全国统一考试化学(海南卷)
2012年普通高等学校招生全国统一考试化学(海南卷)(已下线)2012-2013学年山西省晋中市昔阳中学高二下学期期末考试化学试卷(已下线)2013-2014学年浙江省金华一中高二下学期期中考试化学试卷2014-2015江苏省扬州中学高二12月月考化学试题2015-2016河北石家庄第一中学高二上期中考试化学试卷2015-2016学年江苏省清江中学高二上期末选修化学试卷2015-2016学年福建省连江尚德中学高二下学期期中化学试卷2015-2016学年贵州省铜仁一中高二下期末化学试卷2014-2015学年辽宁省锦州市高二下学期期末化学试卷(已下线)同步君 选修五 第三章 第一节 第一课时 醇天津市和平区2017届高三第三次质量调查(三模)化学试题2018版化学(苏教版)高考总复习专题十二课时跟踪训练--常见的烃和卤代烃高中化学人教版 选修五 第三章 第一节 醇广东省北京师范大学东莞石竹附属学校2018-2019学年高二下学期期中考试化学试题河南省驻马店市2019-2020学年高三下学期模拟考试理科综合化学试题江苏省上冈高级中学2019-2020学年高二上学期期中考试化学(选修)试题宁夏回族自治区银川市长庆高级中学2021届高三上学期第一次月考化学试题江苏省苏州市吴江汾湖高级中学2020-2021学年高二上学期10月月考化学试题海南省海口市琼山中学2019-2020学年高二下学期期中考试化学试题河南省滑县实验学校2020-2021学年高二下学期4月月考化学试题(清北实验卷)江苏省昆山市陆家高级中学、柏庐高级中学、周市高级中学2020-2021学年高一下学期6月联合考试化学试题广东省佛山市禅城区2020-2021学年高二下学期期末统考化学试题宁夏石嘴山市第三中学2020-2021学年高二下学期期末考试化学试题广东省佛山市顺德区罗定邦中学2021-2022学年高二下学期期中教学质量监测化学试题(已下线)专题十一 有机化学基础 能力提升检测卷(测)-2023年高考化学一轮复习讲练测(新教材新高考)
真题
3 . 某研究性学习小组为合成1-丁醇,查阅资料得知一条合成路线:
CH3CH=CH+CO+H2 CH3CH2CH2CHO
CH3CH2CH2CHO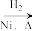 CH3CH2CH2CH2OH
CH3CH2CH2CH2OH
CO的制备原理:HCOOH CO↑+H2O,并设计出原料气的制备装置如图:
CO↑+H2O,并设计出原料气的制备装置如图:
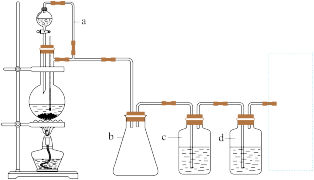
请填写下列空白:
(1)实验室现有锌粒、稀硝酸、稀盐酸、浓硫酸、2-丙醇,从中选择合适的试剂制备氢气,丙烯。写出化学方程式:______ ,______ 。
(2)若用以上装置制备干燥纯净的CO,装置中a和b的作用分别是______ ,______ ;
c和d中盛装的试剂分别是______ ,______ 。若用以上装置制备H2, 气体发生装置中必需的玻璃仪器名称是 ______ ;在虚线框内画出收集H2干燥的装置图_____ 。
(3)制丙烯时,还产生少量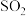 ,
, 及水蒸气,该小组用以下试剂检验这四种气体,混合气体通过试剂的顺序是
及水蒸气,该小组用以下试剂检验这四种气体,混合气体通过试剂的顺序是______ (填序号)
①饱和 溶液 ②酸性
溶液 ②酸性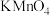 溶液 ③石灰水
溶液 ③石灰水
④无水 ⑤品红溶液
⑤品红溶液
(4)合成正丁醛的反应为正向放热的可逆反应,为增大反应速率和提高原料气的转化率,你认为应该采用的适宜反应条件是______ 。
a. 低温、高压、催化剂 b. 适当的温度、高压、催化剂
c. 常温、常压、催化剂 d. 适当的温度、常压、催化剂
(5)正丁醛经催化剂加氢得到含少量正丁醛的1-丁醇粗品,为纯化10-丁醇,该小组查阅文献得知:①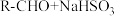 (饱和)→
(饱和)→ ↓;②沸点:乙醚34°C,1-丁醇118°C,并设计出如下提纯路线:
↓;②沸点:乙醚34°C,1-丁醇118°C,并设计出如下提纯路线:

试剂1为______ ,操作1为______ ,操作2为______ ,操作3为______ 。
CH3CH=CH+CO+H2
 CH3CH2CH2CHO
CH3CH2CH2CHO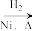 CH3CH2CH2CH2OH
CH3CH2CH2CH2OHCO的制备原理:HCOOH
 CO↑+H2O,并设计出原料气的制备装置如图:
CO↑+H2O,并设计出原料气的制备装置如图:
请填写下列空白:
(1)实验室现有锌粒、稀硝酸、稀盐酸、浓硫酸、2-丙醇,从中选择合适的试剂制备氢气,丙烯。写出化学方程式:
(2)若用以上装置制备干燥纯净的CO,装置中a和b的作用分别是
c和d中盛装的试剂分别是
(3)制丙烯时,还产生少量
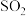 ,
, 及水蒸气,该小组用以下试剂检验这四种气体,混合气体通过试剂的顺序是
及水蒸气,该小组用以下试剂检验这四种气体,混合气体通过试剂的顺序是①饱和
 溶液 ②酸性
溶液 ②酸性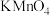 溶液 ③石灰水
溶液 ③石灰水④无水
 ⑤品红溶液
⑤品红溶液(4)合成正丁醛的反应为正向放热的可逆反应,为增大反应速率和提高原料气的转化率,你认为应该采用的适宜反应条件是
a. 低温、高压、催化剂 b. 适当的温度、高压、催化剂
c. 常温、常压、催化剂 d. 适当的温度、常压、催化剂
(5)正丁醛经催化剂加氢得到含少量正丁醛的1-丁醇粗品,为纯化10-丁醇,该小组查阅文献得知:①
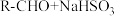 (饱和)→
(饱和)→ ↓;②沸点:乙醚34°C,1-丁醇118°C,并设计出如下提纯路线:
↓;②沸点:乙醚34°C,1-丁醇118°C,并设计出如下提纯路线:
试剂1为
您最近一年使用:0次
真题
4 .  广泛存在于自然界,是一种重要的化工原料。大理石主要成分为
广泛存在于自然界,是一种重要的化工原料。大理石主要成分为 ,另外有少量的含硫化合物。实验室用大理石和稀盐酸反应制备
,另外有少量的含硫化合物。实验室用大理石和稀盐酸反应制备 气体。下列装置可用于
气体。下列装置可用于 气体的提纯和干燥。
气体的提纯和干燥。
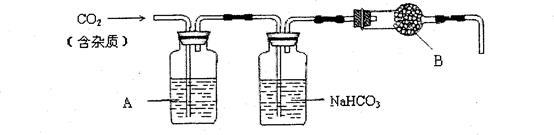
完成下列填空:
1)用浓盐酸配制1:1(体积比)的稀盐酸(约6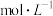 ),应选用的仪器是
),应选用的仪器是_____ 。
a.烧杯 b.玻璃棒 c.量筒d.容量瓶
2)上述装置中,A是____ 溶液,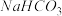 溶液可以吸收
溶液可以吸收_____ 。
3)上述装置中,b物质是_____ 。用这个实验得到的气体测定 的分子量,如果B物质失效,测定结果
的分子量,如果B物质失效,测定结果____ (填“偏高”、“偏低”或“不受影响”)。
4)一次性饭盒中石蜡(高级烷烃)和 在食物中的溶出量是评价饭盒质量的指标之 一,测定溶出量的主要实验步骤设计如下:
在食物中的溶出量是评价饭盒质量的指标之 一,测定溶出量的主要实验步骤设计如下:
剪碎、称重→浸泡溶解→过滤→残渣烘干→冷却、称重→恒重
为了将石蜡和碳酸钙溶出,应选用的试剂是______ 。
a.氯化钠溶液 b.稀醋酸 c.稀硫酸d 正己烷
5)在溶出量测定实验中,为了获得石蜡和碳酸钙的最大溶出量,应先溶出_____ 后溶出_______ 。
6)上述测定实验中,连续_______ ,说明样品已经恒重。
 广泛存在于自然界,是一种重要的化工原料。大理石主要成分为
广泛存在于自然界,是一种重要的化工原料。大理石主要成分为 ,另外有少量的含硫化合物。实验室用大理石和稀盐酸反应制备
,另外有少量的含硫化合物。实验室用大理石和稀盐酸反应制备 气体。下列装置可用于
气体。下列装置可用于 气体的提纯和干燥。
气体的提纯和干燥。
完成下列填空:
1)用浓盐酸配制1:1(体积比)的稀盐酸(约6
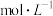 ),应选用的仪器是
),应选用的仪器是a.烧杯 b.玻璃棒 c.量筒d.容量瓶
2)上述装置中,A是
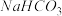 溶液可以吸收
溶液可以吸收3)上述装置中,b物质是
 的分子量,如果B物质失效,测定结果
的分子量,如果B物质失效,测定结果4)一次性饭盒中石蜡(高级烷烃)和
 在食物中的溶出量是评价饭盒质量的指标之 一,测定溶出量的主要实验步骤设计如下:
在食物中的溶出量是评价饭盒质量的指标之 一,测定溶出量的主要实验步骤设计如下:剪碎、称重→浸泡溶解→过滤→残渣烘干→冷却、称重→恒重
为了将石蜡和碳酸钙溶出,应选用的试剂是
a.氯化钠溶液 b.稀醋酸 c.稀硫酸d 正己烷
5)在溶出量测定实验中,为了获得石蜡和碳酸钙的最大溶出量,应先溶出
6)上述测定实验中,连续
您最近一年使用:0次
2016-12-09更新
|
32次组卷
|
2卷引用:2010年全国普通高等学校招生统一考试上海卷化学试题
真题
5 . N2O5—是一种新型硝化剂,其性质和制备受到人们的关注.
(1)N2O5与苯发生硝化反应生成的硝基苯的结构简式是_______________ 。
(2)2N2O5(g)→4NO2(g)+O2(g);ΔH>0
①反应达平衡后,若再通入一定量氮气,则N2O5的转化率将___________ 填“增大”、“减小”、“不变”)。
②下表为反应在T1温度下的部分实验数据:
则500 s内N2O5的分解速率为____________ 。
③在T2温度下,反应1 000 s时测得NO2的浓度为4.98 mol·L-1,则T2_________ T1。
(3)如图所示装置可用于制备N2O5,则N2O5在电解池的_________ 区生成,其电极反应式为______________________________ 。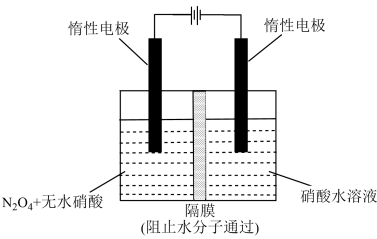
(1)N2O5与苯发生硝化反应生成的硝基苯的结构简式是
(2)2N2O5(g)→4NO2(g)+O2(g);ΔH>0
①反应达平衡后,若再通入一定量氮气,则N2O5的转化率将
②下表为反应在T1温度下的部分实验数据:
| t/s | 0 | 500 | 1000 |
| e(N2O5)/mol·L-1 | 5.00 | 3.52 | 2.48 |
则500 s内N2O5的分解速率为
③在T2温度下,反应1 000 s时测得NO2的浓度为4.98 mol·L-1,则T2
(3)如图所示装置可用于制备N2O5,则N2O5在电解池的

您最近一年使用:0次
真题
6 . X、Y、Z、W为含有相同电子数的分子或离子,均由原子序数小于10的元素组成,X有5个原子核。通常状况下,W为无色液体。
已知:X+Y Z+W
Z+W
(1)Y的电子式是_________________________ 。
(2)液态Z和W的电离相似,都可电离出电子数相同的两种离子,液态Z的电离方程式是_________________________________ 。
(3)用图示装置制备NO并验证其还原性。有下列主要操作:
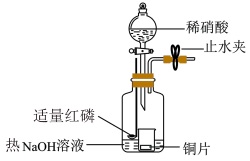
a.向广口瓶内注入足量热NaOH溶液,将盛有铜片的小烧杯放入瓶中。
b.关闭止水夹,点燃红磷,伸入瓶中,塞好胶塞。
c.待红磷充分燃烧,一段时间后打开分液漏斗旋塞,向烧杯中滴入少量稀硝酸。
①步骤c后还缺少的一步主要操作是_______________________________________ 。
②红磷充分燃烧的产物与NaOH溶液反应的离子方程式是____________________________________________________________________ 。
③步骤c滴入稀硝酸后烧杯中的现象是______________________________________ 。
反应的离子方程式是____________________________________________________ 。
(4)一定温度下,将1 mol N2O4置于密闭容器中,保持压强不变,升高温度至T1的过程中,气体由无色逐渐变为红棕色。温度由T1继续升高到T2的过程中,气体逐渐变为无色。若保持T2,增大压强,气体逐渐变为红棕色。气体的物质的量n随温度T变化的关系如图所示。

①温度在T1-T2之间,反应的化学方程式是_________________________ 。
②温度在T2-T3之间,气体的平均相对分子质量是(保留1位小数)______________ 。
已知:X+Y
 Z+W
Z+W(1)Y的电子式是
(2)液态Z和W的电离相似,都可电离出电子数相同的两种离子,液态Z的电离方程式是
(3)用图示装置制备NO并验证其还原性。有下列主要操作:

a.向广口瓶内注入足量热NaOH溶液,将盛有铜片的小烧杯放入瓶中。
b.关闭止水夹,点燃红磷,伸入瓶中,塞好胶塞。
c.待红磷充分燃烧,一段时间后打开分液漏斗旋塞,向烧杯中滴入少量稀硝酸。
①步骤c后还缺少的一步主要操作是
②红磷充分燃烧的产物与NaOH溶液反应的离子方程式是
③步骤c滴入稀硝酸后烧杯中的现象是
反应的离子方程式是
(4)一定温度下,将1 mol N2O4置于密闭容器中,保持压强不变,升高温度至T1的过程中,气体由无色逐渐变为红棕色。温度由T1继续升高到T2的过程中,气体逐渐变为无色。若保持T2,增大压强,气体逐渐变为红棕色。气体的物质的量n随温度T变化的关系如图所示。

①温度在T1-T2之间,反应的化学方程式是
②温度在T2-T3之间,气体的平均相对分子质量是(保留1位小数)
您最近一年使用:0次
真题
名校
7 . 某小组以CoCl2·6H2O、NH4Cl、H2O2、液氨、氯化铵为原料,在活性炭催化下合成了橙黄色晶体X。为测定其组成,进行如下实验。
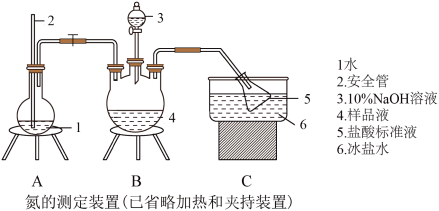
①氨的测定:精确称取wgX,加适量水溶解,注入如图所示的三颈瓶中,然后逐滴加入足量10%NaOH溶液,通入水蒸气,将样品溶液中的氨全部蒸出,用V1mLc1mol·L—1的盐酸溶液吸收。蒸氨结束后取下接收瓶,用c2mol·L—1NaOH标准溶液滴定过剩的HCl,到终点时消耗V2mLNaOH溶液。
②氯的测定:准确称取样品X,配成溶液后用AgNO3标准溶液滴定,K2CrO4溶液为指示剂,至出现砖红色沉淀不再消失为终点(Ag2CrO4为砖红色)。
回答下列问题:
(1)装置中安全管的作用原理是_________ 。
(2)用NaOH标准溶液滴定过剩的HCl时,应使用_____ 式滴定管,可使用的指示剂为________ 。
(3)样品中氨的质量分数表达式为____________ 。
(4)测定氨前应该对装置进行气密性检验,若气密性不好测定结果将___ (填“偏高”或“偏低”)。
(5)测定氯的过程中,使用棕色滴定管的原因是___________ ;滴定终点时,若溶液中c(Ag+)=2.0×10—5mol·L—1,c(CrO42—)为______ mol·L—1。(已知:Ksp(Ag2CrO4)=1.12×10—12)
(6)经测定,样品X中钴、氨、氯的物质的量之比为1:6:3,钴的化合价为______ ,制备X的化学方程式为____________________ ;X的制备过程中温度不能过高的原因是__________________ 。

①氨的测定:精确称取wgX,加适量水溶解,注入如图所示的三颈瓶中,然后逐滴加入足量10%NaOH溶液,通入水蒸气,将样品溶液中的氨全部蒸出,用V1mLc1mol·L—1的盐酸溶液吸收。蒸氨结束后取下接收瓶,用c2mol·L—1NaOH标准溶液滴定过剩的HCl,到终点时消耗V2mLNaOH溶液。
②氯的测定:准确称取样品X,配成溶液后用AgNO3标准溶液滴定,K2CrO4溶液为指示剂,至出现砖红色沉淀不再消失为终点(Ag2CrO4为砖红色)。
回答下列问题:
(1)装置中安全管的作用原理是
(2)用NaOH标准溶液滴定过剩的HCl时,应使用
(3)样品中氨的质量分数表达式为
(4)测定氨前应该对装置进行气密性检验,若气密性不好测定结果将
(5)测定氯的过程中,使用棕色滴定管的原因是
(6)经测定,样品X中钴、氨、氯的物质的量之比为1:6:3,钴的化合价为
您最近一年使用:0次
2016-12-09更新
|
3788次组卷
|
11卷引用:2014年全国普通高等学校招生统一考试理科综合能力测试化学(新课标Ⅱ卷)
2014年全国普通高等学校招生统一考试理科综合能力测试化学(新课标Ⅱ卷)2016届黑龙江省哈尔滨第六中学高三上期中测试化学试卷2016届山东省泰安一中高三5月模拟一理综化学试卷2016届山东省泰安一中高三5月高考拉练一模理综化学试卷四川省成都市龙泉第二中学2019-2020学年高三上学期1月月考理科综合化学试题2020届高考化学二轮复习大题精准训练——定量分析实验中成分的测定【懂做原理题】2020届高三化学选修4二轮专题练——沉淀溶解平衡常数及相关计算【精编25题】甘肃省西北师范大学附属中学2019-2020学年高二上学期期中考试化学试题云南省玉溪市通海县第三中学2021-2022学年高二上学期期末考试化学试题云南省玉溪市峨山县第一中学2022-2023学年高二上学期期中考试化学试题(已下线)实验综合题
真题
名校
8 . Na2S2O3是重要的化工原料,易溶于水。在中性或碱性环境中稳定。
I.制备Na2S2O3•5H2O
反应原理:Na2SO3(aq)+S(s) Na2S2O3(aq)
Na2S2O3(aq)
实验步骤:
①称取15g Na2SO3加入圆底烧瓶中,再加入80ml蒸馏水。另取5g研细的硫粉,用3ml 乙醇润湿,加入上述溶液中。
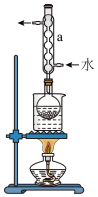
②安装实验装置(如图所示,部分加持装置略去),水浴加热,微沸60分钟。
③趁热过滤,将滤液水浴加热浓缩,冷却析出Na2S2O3•5H2O,经过滤,洗涤,干燥,得到产品。
回答问题:
(1)硫粉在反应前用乙醇润湿的目的是_______________________________________________ 。
(2)仪器a的名称是___________ ,其作用是_________________________________________ 。
(3)产品中除了有未反应的Na2SO3外,最可能存在的无机杂质是______________________________ ,检验是否存在该杂质的方法是_______________________________________________________ 。
(4)该实验一般控制在碱性环境下进行,否则产品发黄,用离子方程式表示其原因:_____________________________________________________________________________________________________ 。
II.测定产品纯度
准确称取Wg产品,用适量蒸馏水溶解,以淀粉作指示剂,用0.1000 mol•L‾1碘的标准溶液滴定。
反应原理为:2S2O32‾+I2=S4O62-+2I‾
(5)滴定至终点时,溶液颜色的变化:___________________________________ 。
(6)滴定起始和终点的液面位置如图,则消耗碘的标准溶液体积为________ mL。产品的纯度为(设Na2S2O3•5H2O相对分子质量为M)___________ 。

III.Na2S2O3的应用
(7)Na2S2O3还原性较强,在溶液中易被Cl2氧化成SO42‾,常用作脱氧剂,该反应的离子方程式为_____________________________________________________________ 。
I.制备Na2S2O3•5H2O
反应原理:Na2SO3(aq)+S(s)
 Na2S2O3(aq)
Na2S2O3(aq)实验步骤:
①称取15g Na2SO3加入圆底烧瓶中,再加入80ml蒸馏水。另取5g研细的硫粉,用3ml 乙醇润湿,加入上述溶液中。
②安装实验装置(如图所示,部分加持装置略去),水浴加热,微沸60分钟。

③趁热过滤,将滤液水浴加热浓缩,冷却析出Na2S2O3•5H2O,经过滤,洗涤,干燥,得到产品。
回答问题:
(1)硫粉在反应前用乙醇润湿的目的是
(2)仪器a的名称是
(3)产品中除了有未反应的Na2SO3外,最可能存在的无机杂质是
(4)该实验一般控制在碱性环境下进行,否则产品发黄,用离子方程式表示其原因:
II.测定产品纯度
准确称取Wg产品,用适量蒸馏水溶解,以淀粉作指示剂,用0.1000 mol•L‾1碘的标准溶液滴定。
反应原理为:2S2O32‾+I2=S4O62-+2I‾
(5)滴定至终点时,溶液颜色的变化:
(6)滴定起始和终点的液面位置如图,则消耗碘的标准溶液体积为

III.Na2S2O3的应用
(7)Na2S2O3还原性较强,在溶液中易被Cl2氧化成SO42‾,常用作脱氧剂,该反应的离子方程式为
您最近一年使用:0次
2016-12-09更新
|
1829次组卷
|
2卷引用:2014年全国普通高等学校招生统一考试理科综合能力测试化学(天津卷)
9 . [14分]实验室制备苯乙酮的化学方程式为:
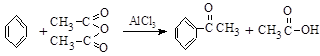
制备过程中还有
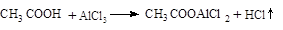 等副反应。
等副反应。
主要实验装置和步骤如下:
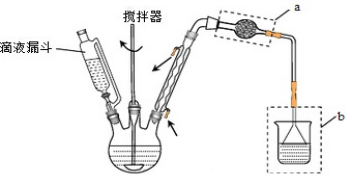
(I)合成:在三颈瓶中加入20 g无水AlCl3和30 mL无水苯。为避免反应液升温过快,边搅拌边慢慢滴加6 mL乙酸酐和10 mL无水苯的混合液,控制滴加速率,使反应液缓缓回流。滴加完毕后加热回流1小时。
(Ⅱ)分离与提纯:
①边搅拌边慢慢滴加一定量浓盐酸与冰水混合液,分离得到有机层
②水层用苯萃取,分液
③将①②所得有机层合并,洗涤、干燥、蒸去苯,得到苯乙酮粗产品
④蒸馏粗产品得到苯乙酮。回答下列问题:
(1)仪器a的名称:____________ ;装置b的作用:________________________ 。
(2)合成过程中要求无水操作,理由是___________________________ 。
(3)若将乙酸酐和苯的混合液一次性倒入三颈瓶,可能导致_________________ 。
(4)分离和提纯操作②的目的是__________________ 。该操作中是否可改用乙醇萃取?_____ (填“是”或“否”),原因是___________________________________ 。
(5)分液漏斗使用前须___________________ 并洗净备用。萃取时,先后加入待萃取液和萃取剂,经振摇并________________ 后,将分液漏斗置于铁架台的铁圈上静置片刻,分层。分离上下层液体时,应先________________ ,然后打开活塞放出下层液体,上层液体从上口倒出。
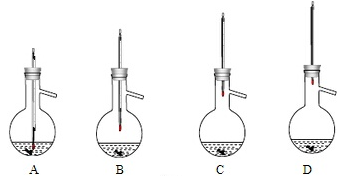
(6)粗产品蒸馏提纯时,下面装置中温度计位置正确的是________________ ,可能会导致收集到的产品中混有低沸点杂质的装置是________________ 。
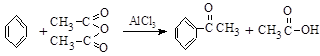
制备过程中还有

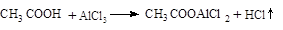 等副反应。
等副反应。主要实验装置和步骤如下:

(I)合成:在三颈瓶中加入20 g无水AlCl3和30 mL无水苯。为避免反应液升温过快,边搅拌边慢慢滴加6 mL乙酸酐和10 mL无水苯的混合液,控制滴加速率,使反应液缓缓回流。滴加完毕后加热回流1小时。
(Ⅱ)分离与提纯:
①边搅拌边慢慢滴加一定量浓盐酸与冰水混合液,分离得到有机层
②水层用苯萃取,分液
③将①②所得有机层合并,洗涤、干燥、蒸去苯,得到苯乙酮粗产品
④蒸馏粗产品得到苯乙酮。回答下列问题:
(1)仪器a的名称:
(2)合成过程中要求无水操作,理由是
(3)若将乙酸酐和苯的混合液一次性倒入三颈瓶,可能导致
| A.反应太剧烈 | B.液体太多搅不动 | C.反应变缓慢 | D.副产物增多 |
(4)分离和提纯操作②的目的是
(5)分液漏斗使用前须
(6)粗产品蒸馏提纯时,下面装置中温度计位置正确的是

您最近一年使用:0次
真题
名校
10 . 实验室采用MgCl2、AlCl3的混合溶液与过量氨水反应制备MgAl2O4,主要流程如下 :

(1)为使Mg2+、Al3+同时生成沉淀,应先向沉淀反应器中加入____________ (填“A”或“B”),再滴加另一反应物。
(2)如右图所示,过滤操作中的一处错误是_______________________________ 。
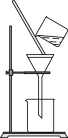
(3)判断流程中沉淀是否洗净所用的试剂是_____________________________ ;高温焙烧时,用于盛放固体的仪器名称是________________ 。
(4)无水AlCl3(183°C升华)遇潮湿空气即产生大量白雾,实验室可用下列装置制备。
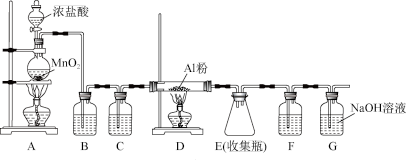
装置 B中盛放饱和NaCl溶液,该装置的主要作用是_________________________ 。F中试剂的作用是________________ ;用一件仪器装填适当试剂后也可起到F和G的作用;所装填的试剂为________________ 。

(1)为使Mg2+、Al3+同时生成沉淀,应先向沉淀反应器中加入
(2)如右图所示,过滤操作中的一处错误是

(3)判断流程中沉淀是否洗净所用的试剂是
(4)无水AlCl3(183°C升华)遇潮湿空气即产生大量白雾,实验室可用下列装置制备。

装置 B中盛放饱和NaCl溶液,该装置的主要作用是
您最近一年使用:0次
2016-12-09更新
|
820次组卷
|
13卷引用:2012年普通高等学校招生全国统一考试化学(山东卷)
2012年普通高等学校招生全国统一考试化学(山东卷)(已下线)2013届新课标高三配套月考(四)化学试卷(B卷)(已下线)2012-2013学年山西大学附属中学高二暑假8月考试化学试卷(已下线)2014高考名师推荐化学--预测42014-2015福建省福州一中高三1月综合训练理综化学试卷2017届河北省武安三中高三上学期第一次月考化学试卷2017届福建省漳州市八校高三下学期3月联考化学试卷河南省新野县第一高级中学2018届高三上学期第一次月考化学试题贵州省毕节梁才学校2018届高三上学期第一次月考理综化学试题陕西省西安市第八十三中学高三年级2017-2018学年第三阶段考试化学试题【全国校级联考】河南省商丘市九校2017-2018学年高二下学期期末联考化学试题(已下线)2019高考热点题型和提分秘籍 第三章 金属及其化合物 第2讲 铝及其化合物 (题型专练)山东省微山县第二中学2019届高三上学期第三学段教学质量监测化学试题



