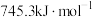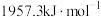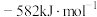真题
解题方法
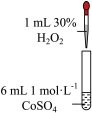
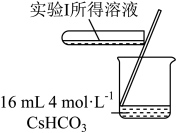
1 . 学习小组为探究 、
、 能否催化
能否催化 的分解及相关性质,室温下进行了实验I~Ⅳ。
的分解及相关性质,室温下进行了实验I~Ⅳ。
已知: 为粉红色、
为粉红色、 为蓝色、
为蓝色、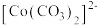 为红色、
为红色、 为墨绿色。回答下列问题:
为墨绿色。回答下列问题:
(1)配制 的
的 溶液,需要用到下列仪器中的
溶液,需要用到下列仪器中的_______ (填标号)。
_______ (填“能”或“不能”)催化 的分解。实验Ⅱ中
的分解。实验Ⅱ中 大大过量的原因是
大大过量的原因是_______ 。实验Ⅲ初步表明 能催化
能催化 的分解,写出
的分解,写出 在实验Ⅲ中所发生反应的离子方程式
在实验Ⅲ中所发生反应的离子方程式_______ 、_______ 。
(3)实验I表明,反应 难以正向进行,利用化学平衡移动原理,分析
难以正向进行,利用化学平衡移动原理,分析 、
、 分别与
分别与 配位后,正向反应能够进行的原因
配位后,正向反应能够进行的原因_______ 。_______ 、_______ 。
 、
、 能否催化
能否催化 的分解及相关性质,室温下进行了实验I~Ⅳ。
的分解及相关性质,室温下进行了实验I~Ⅳ。| 实验I | 实验Ⅱ | 实验Ⅲ |
|
|
|
| 无明显变化 | 溶液变为红色,伴有气泡产生 | 溶液变为墨绿色,并持续产生能使带火星木条复燃的气体 |
 为粉红色、
为粉红色、 为蓝色、
为蓝色、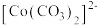 为红色、
为红色、 为墨绿色。回答下列问题:
为墨绿色。回答下列问题:(1)配制
 的
的 溶液,需要用到下列仪器中的
溶液,需要用到下列仪器中的a.  b.
b. 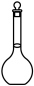 c.
c.  d.
d.

 的分解。实验Ⅱ中
的分解。实验Ⅱ中 大大过量的原因是
大大过量的原因是 能催化
能催化 的分解,写出
的分解,写出 在实验Ⅲ中所发生反应的离子方程式
在实验Ⅲ中所发生反应的离子方程式(3)实验I表明,反应
 难以正向进行,利用化学平衡移动原理,分析
难以正向进行,利用化学平衡移动原理,分析 、
、 分别与
分别与 配位后,正向反应能够进行的原因
配位后,正向反应能够进行的原因实验Ⅳ:
您最近一年使用:0次
名校
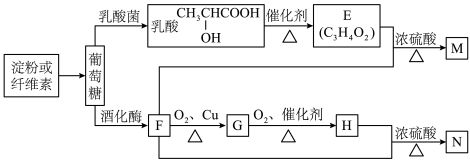
2 . 以富含淀粉或纤维素的农林产品为原料,制备生活中的某些有机物。
(1)葡萄糖的分子式为_______ ,乳酸分子中的官能团的名称为_______ 。
(2)下列说法正确的是_______。
(3)G在一定条件下可转化为F,则该反应的反应类型是_______ 。
(4)久置的M自身会发生聚合反应得到弹性较好的聚合物,请写出该聚合物的结构简式:_______ 。
(5)写出“F→G”、“E+F→M”两个反应的化学方程式(有机物用结构简式表示)
“F→G”:_______
“E+F→M”:_______
(1)葡萄糖的分子式为
(2)下列说法正确的是_______。
| A.淀粉和纤维素互为同分异构体 |
| B.E和H属于同系物、M和N也属于同系物 |
| C.E、F和G均能使酸性高锰酸钾溶液褪色 |
| D.乳酸、F和H均能与钠、氢氧化钠溶液发生反应 |
(3)G在一定条件下可转化为F,则该反应的反应类型是
(4)久置的M自身会发生聚合反应得到弹性较好的聚合物,请写出该聚合物的结构简式:
(5)写出“F→G”、“E+F→M”两个反应的化学方程式(有机物用结构简式表示)
“F→G”:
“E+F→M”:
您最近一年使用:0次
名校
3 . 请回答下列问题:
(1)冷敷袋俗称冰袋,在日常生活中有降温、保鲜和镇痛等多种用途。
①制作冷敷袋常利用吸热的化学变化来实现,以下组合最能满足的是___________ 。(填字母)
A.冰 B.硝酸铵+水 C.硝酸铵+水合碳酸钠
②下列过程中的热量变化与冰袋一致的有___________ 。(填字母)
a. b.盐酸和镁条
b.盐酸和镁条
c.盐酸和碳酸氢钠 d. 和氯化铵
和氯化铵
e. 分解
分解
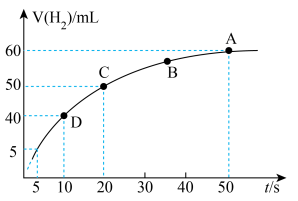
③某课外实验小组利用压强传感器、温度传感器、数据采集器和计算机等数字化实验设备,探究镁与一定量盐酸的反应速率,测得产生 的体积与反应时间的关系曲线如图所示,结合所学知识分析速率变化的原因为
的体积与反应时间的关系曲线如图所示,结合所学知识分析速率变化的原因为___________ ;在20s内用H+浓度表示的平均反应速率
___________ (20s时溶液体积为50mL,气体摩尔体积为25L/mol)。 ,是一个常见的放热反应。回答下列问题。
,是一个常见的放热反应。回答下列问题。
t℃时,向填充有催化剂、体积为2L的刚性容器中充入一定量的 和
和 合成氨,实验中测得
合成氨,实验中测得 随时间的变化如表所示:
随时间的变化如表所示:
①4-6min内 的平均反应速率
的平均反应速率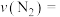
___________ 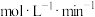
②下列情况能说明反应达到平衡状态的是___________ (填标号)。
A.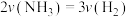 B.混合气体的平均相对分子质量不再变化
B.混合气体的平均相对分子质量不再变化
C. 体积分数不再变化 D.混合气体的密度保持不变
体积分数不再变化 D.混合气体的密度保持不变
③如表列出了在不同温度和压强下,反应达到平衡时 的百分含量
的百分含量 。
。
从表中数据得出,合成氨最优的条件是___________ 。
(1)冷敷袋俗称冰袋,在日常生活中有降温、保鲜和镇痛等多种用途。
①制作冷敷袋常利用吸热的化学变化来实现,以下组合最能满足的是
A.冰 B.硝酸铵+水 C.硝酸铵+水合碳酸钠
②下列过程中的热量变化与冰袋一致的有
a.
 b.盐酸和镁条
b.盐酸和镁条c.盐酸和碳酸氢钠 d.
 和氯化铵
和氯化铵e.
 分解
分解③某课外实验小组利用压强传感器、温度传感器、数据采集器和计算机等数字化实验设备,探究镁与一定量盐酸的反应速率,测得产生
 的体积与反应时间的关系曲线如图所示,结合所学知识分析速率变化的原因为
的体积与反应时间的关系曲线如图所示,结合所学知识分析速率变化的原因为
 ,是一个常见的放热反应。回答下列问题。
,是一个常见的放热反应。回答下列问题。t℃时,向填充有催化剂、体积为2L的刚性容器中充入一定量的
 和
和 合成氨,实验中测得
合成氨,实验中测得 随时间的变化如表所示:
随时间的变化如表所示:①4-6min内
 的平均反应速率
的平均反应速率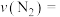
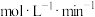
| 时间/min | 2 | 4 | 6 | 8 | 10 | 12 |
 / / | 0.04 | 0.10 | 0.14 | 0.16 | 0.16 | 0.16 |
A.
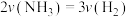 B.混合气体的平均相对分子质量不再变化
B.混合气体的平均相对分子质量不再变化C.
 体积分数不再变化 D.混合气体的密度保持不变
体积分数不再变化 D.混合气体的密度保持不变③如表列出了在不同温度和压强下,反应达到平衡时
 的百分含量
的百分含量 。
。压强/MPa % %温度/℃ | 0.1 | 10 | 20 | 30 | 60 | 100 |
| 200 | 15.3 | 81.5 | 86.4 | 89.9 | 95.4 | 98.8 |
| 300 | 2.2 | 52.0 | 64.2 | 71.0 | 84.2 | 92.6 |
| 400 | 0.4 | 25.1 | 38.2 | 47.0 | 65.5 | 79.8 |
| 500 | 0.1 | 10.6 | 19.1 | 26.4 | 42.2 | 57.5 |
| 600 | 0.05 | 4.5 | 9.1 | 13.8 | 23.1 | 31.4 |
您最近一年使用:0次
名校
4 . 铜及其化合物在生活、生产中用途广泛。回答下列问题:
(1)基态铁原子的价层电子的轨道表示式为__________ ,其原子核外电子的空间运动状态有__________ 种。
(2)高温下CuO能转化为 ,说明高温下
,说明高温下 比
比 稳定,原因是
稳定,原因是__________ 。
(3)在水溶液中 则不如
则不如 稳定,因为
稳定,因为 在水溶液中可以
在水溶液中可以 的形式存在。请结合表中信息加以解释
的形式存在。请结合表中信息加以解释__________ 。
(注:水合能指的是气态基态离子与水分子结合生成 水合离子时所释放的能量。)
水合离子时所释放的能量。)
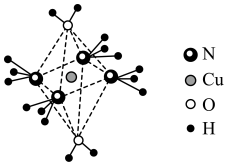
(4)H、N、O与Cu能形成一种阳离子M,呈轴向狭长的八面体结构(如下图所示)。__________ ,加热时,M首先失去的组分分子空间结构名称为__________ 。
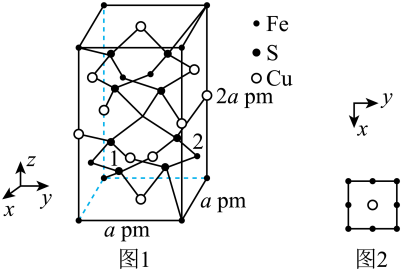
(5) 晶体的晶胞结构如图1所示。晶胞中Fe的投影位置如图2所示。以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子的分数坐标,例如图1中原子1(铜原子)的分数坐标为
晶体的晶胞结构如图1所示。晶胞中Fe的投影位置如图2所示。以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子的分数坐标,例如图1中原子1(铜原子)的分数坐标为 ,则原子2(铁原子)的分数坐标为
,则原子2(铁原子)的分数坐标为__________ 。晶胞参数分别为 ,
, 、
、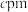 ,晶胞棱边夹角均为90°,该晶体的密度为
,晶胞棱边夹角均为90°,该晶体的密度为__________  (列出计算表达式,设阿伏加德罗常数的值为
(列出计算表达式,设阿伏加德罗常数的值为 )。
)。
(1)基态铁原子的价层电子的轨道表示式为
(2)高温下CuO能转化为
 ,说明高温下
,说明高温下 比
比 稳定,原因是
稳定,原因是(3)在水溶液中
 则不如
则不如 稳定,因为
稳定,因为 在水溶液中可以
在水溶液中可以 的形式存在。请结合表中信息加以解释
的形式存在。请结合表中信息加以解释第一电离能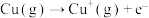 | 第二电离能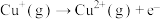 | 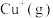 水合能( 水合能( ) ) | 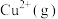 水合能( 水合能( ) ) |
|
|
|
|
 水合离子时所释放的能量。)
水合离子时所释放的能量。)(4)H、N、O与Cu能形成一种阳离子M,呈轴向狭长的八面体结构(如下图所示)。
(5)
 晶体的晶胞结构如图1所示。晶胞中Fe的投影位置如图2所示。以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子的分数坐标,例如图1中原子1(铜原子)的分数坐标为
晶体的晶胞结构如图1所示。晶胞中Fe的投影位置如图2所示。以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子的分数坐标,例如图1中原子1(铜原子)的分数坐标为 ,则原子2(铁原子)的分数坐标为
,则原子2(铁原子)的分数坐标为 ,
, 、
、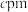 ,晶胞棱边夹角均为90°,该晶体的密度为
,晶胞棱边夹角均为90°,该晶体的密度为 (列出计算表达式,设阿伏加德罗常数的值为
(列出计算表达式,设阿伏加德罗常数的值为 )。
)。
您最近一年使用:0次
名校
解题方法
5 . 碲(Te)常用于冶金工业,也是石油裂解的催化剂。工业上常以碲铜废料(主要成分是 )为原料提取碲,其工艺流程如下:
)为原料提取碲,其工艺流程如下: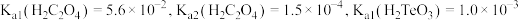 ,
,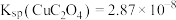 。
。
(1) 中碲元素的化合价为
中碲元素的化合价为_______ 。碲在元素周期表中的位置为_______ 。
(2)“氧化酸浸”得到 和
和 ,该反应的化学方程式为
,该反应的化学方程式为_______ 。
(3) 可溶于
可溶于 ,反应
,反应 的平衡常数为
的平衡常数为_______ 。(保留两位有效数字){已知:反应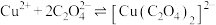 的平衡常数
的平衡常数 }
}
(4)“还原”在 50 ℃条件下进行: ,反应中还原产物和氧化产物的物质的量之比为
,反应中还原产物和氧化产物的物质的量之比为_______ 。
(5)“还原”时, 的实际投入量大于理论量,其可能原因有
的实际投入量大于理论量,其可能原因有_______ 。
(6)将一定质量的 置于
置于 气中热解,测得剩余固体的质量与原始固体的质量的比值约为
气中热解,测得剩余固体的质量与原始固体的质量的比值约为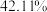 ,则剩余固体的化学式为
,则剩余固体的化学式为_______ 。
 )为原料提取碲,其工艺流程如下:
)为原料提取碲,其工艺流程如下:
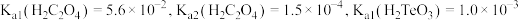 ,
,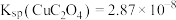 。
。(1)
 中碲元素的化合价为
中碲元素的化合价为(2)“氧化酸浸”得到
 和
和 ,该反应的化学方程式为
,该反应的化学方程式为(3)
 可溶于
可溶于 ,反应
,反应 的平衡常数为
的平衡常数为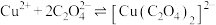 的平衡常数
的平衡常数 }
}(4)“还原”在 50 ℃条件下进行:
 ,反应中还原产物和氧化产物的物质的量之比为
,反应中还原产物和氧化产物的物质的量之比为(5)“还原”时,
 的实际投入量大于理论量,其可能原因有
的实际投入量大于理论量,其可能原因有(6)将一定质量的
 置于
置于 气中热解,测得剩余固体的质量与原始固体的质量的比值约为
气中热解,测得剩余固体的质量与原始固体的质量的比值约为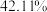 ,则剩余固体的化学式为
,则剩余固体的化学式为
您最近一年使用:0次
6 . 从“钛磁铁矿”冶炼金属铁后的“含钛高炉渣”中提取金属钛的工艺流程如下:
②“水浸”溶液的 。
。
请回答下列问题:
(1)“熔融”时,为了使反应物充分受热融化反应,可以采取的措施有___________ 。
(2)某实验小组模拟“熔融”过程的反应,将固体 与
与 按物质的量1:2混合反应生成
按物质的量1:2混合反应生成 反应过程的热重曲线如图所示。
反应过程的热重曲线如图所示。 的方程式为
的方程式为___________ 。
②“水浸”后滤渣主要有___________ 。
(3)整合剂EDTA(乙二胺四乙酸三钠, )能够与金属阳离子按1:1反应形成非常稳定的整合物(
)能够与金属阳离子按1:1反应形成非常稳定的整合物(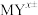 )。已知
)。已知 ,
,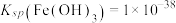
①“水解”步骤加入EDTA的目的是___________ 。
②常温下,某溶液中 和Fe3+浓度均为:
和Fe3+浓度均为: 的溶液中,用氨水调pH至4时溶液中的
的溶液中,用氨水调pH至4时溶液中的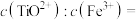
___________ 。
(4)一种 晶体结构如图(黑球表示
晶体结构如图(黑球表示 ,白球表示
,白球表示 ),其熔点为1850℃。
),其熔点为1850℃。 的配位数为
的配位数为___________ 。
②“电解”时,以覆盖氮化硼的石墨电极为阳极,电解 的共熔物得到金属钛,
的共熔物得到金属钛,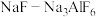 的作用是
的作用是___________ 。
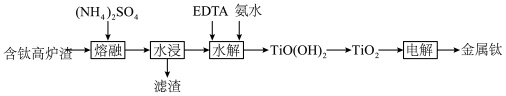
| 组分 |  |  |  |  |  |  | 其他 |
| 质量分数% | 34 | 6~16 | 17~19 | 14~16 | 8.0~9.0 | 3.0~4.2 | 0.8 |
 。
。请回答下列问题:
(1)“熔融”时,为了使反应物充分受热融化反应,可以采取的措施有
(2)某实验小组模拟“熔融”过程的反应,将固体
 与
与 按物质的量1:2混合反应生成
按物质的量1:2混合反应生成 反应过程的热重曲线如图所示。
反应过程的热重曲线如图所示。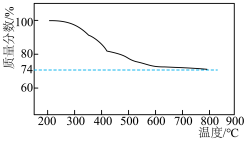
 的方程式为
的方程式为②“水浸”后滤渣主要有
(3)整合剂EDTA(乙二胺四乙酸三钠,
 )能够与金属阳离子按1:1反应形成非常稳定的整合物(
)能够与金属阳离子按1:1反应形成非常稳定的整合物(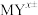 )。已知
)。已知 ,
,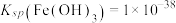
①“水解”步骤加入EDTA的目的是
②常温下,某溶液中
 和Fe3+浓度均为:
和Fe3+浓度均为: 的溶液中,用氨水调pH至4时溶液中的
的溶液中,用氨水调pH至4时溶液中的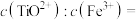
(4)一种
 晶体结构如图(黑球表示
晶体结构如图(黑球表示 ,白球表示
,白球表示 ),其熔点为1850℃。
),其熔点为1850℃。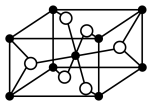
 的配位数为
的配位数为②“电解”时,以覆盖氮化硼的石墨电极为阳极,电解
 的共熔物得到金属钛,
的共熔物得到金属钛,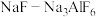 的作用是
的作用是
您最近一年使用:0次
名校
解题方法
7 . 人体摄入少量氟可预防龋齿,增强免疫力,但摄入过量会导致氟斑牙、氟骨症和肿瘤的发生,因此需要对氟离子进行定量检测。化合物J可以定量检测氟离子,其合成路线如下
(1)按照系统命名法,B的名称为_______ 。
(2)D中所含官能团的名称为_______ 。
(3)G的结构简式为_______ 。
(4)已知RCN在酸性条件下水解生成RCOOH,I在酸性条件下充分水解的离子方程式为____ 。
(5)H→J分2步进行,反应类型依次为_______ 、_______ 。
(6)I的同分异构体中,同时满足下列条件的共有____ 种(不考虑立体异构)。其中,含有手性碳的异构体的结构简式为_____ 。
①具有链状结构且含有硝基。②碳原子不全在一条直线上。
(7)J检测氟离子时,J转化为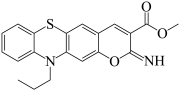 释放出较强的荧光信号,同时生成氟硅烷,从结构的角度分析Si-O转换为Si-F的原因:
释放出较强的荧光信号,同时生成氟硅烷,从结构的角度分析Si-O转换为Si-F的原因:_______ 。
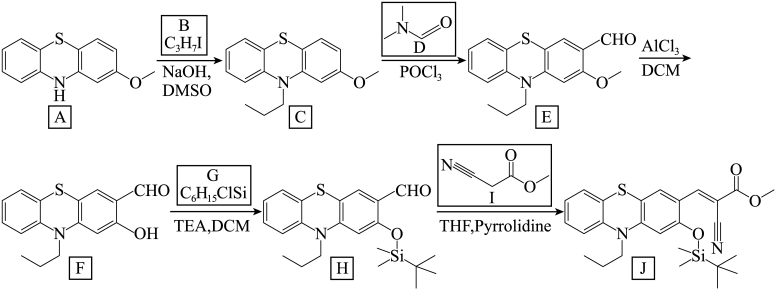
(1)按照系统命名法,B的名称为
(2)D中所含官能团的名称为
(3)G的结构简式为
(4)已知RCN在酸性条件下水解生成RCOOH,I在酸性条件下充分水解的离子方程式为
(5)H→J分2步进行,反应类型依次为
(6)I的同分异构体中,同时满足下列条件的共有
①具有链状结构且含有硝基。②碳原子不全在一条直线上。
(7)J检测氟离子时,J转化为
 释放出较强的荧光信号,同时生成氟硅烷,从结构的角度分析Si-O转换为Si-F的原因:
释放出较强的荧光信号,同时生成氟硅烷,从结构的角度分析Si-O转换为Si-F的原因:
您最近一年使用:0次
解题方法
8 . 铜(Ⅱ)氨基酸配合物在医药、食品、农业等领域具有广泛的应用,甘氨酸( ,以HL代表甘氨酸)在约70℃的条件下可与氢氧化铜反应制备二甘氨酸合铜(Ⅱ)水合物,其反应的化学方程式为
,以HL代表甘氨酸)在约70℃的条件下可与氢氧化铜反应制备二甘氨酸合铜(Ⅱ)水合物,其反应的化学方程式为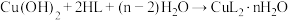 。
。
Ⅰ.氢氧化铜的制备
①向烧杯中加入适量 和20mL水。
和20mL水。
②完全溶解后,边滴加氨水边搅拌至最初产生的沉淀完全溶解。
③加入 溶液至不再生成沉淀,过滤,用水洗涤。
溶液至不再生成沉淀,过滤,用水洗涤。
(1)步骤②沉淀溶解过程中反应的离子方程式为___________ 。
(2)步骤③中检验沉淀洗涤干净的操作及现象为___________ 。
Ⅱ.二甘氨酸合铜(Ⅱ)水合物的制备
④称取适量甘氨酸,溶于150mL水中。
⑤在65~70℃的条件下加热,边搅拌边加入新制的 ,至
,至 全部溶解。
全部溶解。
⑥热抽滤,向滤液加入10mL无水乙醇。
⑦抽滤,用乙醇溶液洗涤晶体,再用丙酮洗涤,抽干。
⑧将产品烘干。
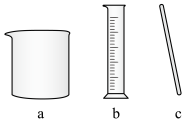
(3)步骤④中使用的部分仪器如下。仪器a的名称是___________ 。加快甘氨酸溶解的操作为___________ 。___________ 。
(5)步骤⑦中用乙醇溶液洗涤晶体后再用丙酮洗涤的原因为___________ 。
Ⅲ.产品中铜含量的测定
称取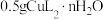 产品,加入水和稀硫酸溶解,配制成250mL溶液。取20.00mL该溶液,加入足量KI固体和50mL水,以淀粉为指示剂,立即用
产品,加入水和稀硫酸溶解,配制成250mL溶液。取20.00mL该溶液,加入足量KI固体和50mL水,以淀粉为指示剂,立即用 标准溶液滴定至终点,消耗
标准溶液滴定至终点,消耗 溶液1.60mL。
溶液1.60mL。
已知:在酸性介质中,配合物中的 被质子化,配合物被破坏;
被质子化,配合物被破坏;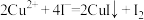 ,
, 。
。
(6)滴定终点溶液颜色的变化为___________ 。
(7)产品中铜元素的质量分数为___________ 。
 ,以HL代表甘氨酸)在约70℃的条件下可与氢氧化铜反应制备二甘氨酸合铜(Ⅱ)水合物,其反应的化学方程式为
,以HL代表甘氨酸)在约70℃的条件下可与氢氧化铜反应制备二甘氨酸合铜(Ⅱ)水合物,其反应的化学方程式为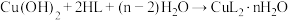 。
。Ⅰ.氢氧化铜的制备
①向烧杯中加入适量
 和20mL水。
和20mL水。②完全溶解后,边滴加氨水边搅拌至最初产生的沉淀完全溶解。
③加入
 溶液至不再生成沉淀,过滤,用水洗涤。
溶液至不再生成沉淀,过滤,用水洗涤。(1)步骤②沉淀溶解过程中反应的离子方程式为
(2)步骤③中检验沉淀洗涤干净的操作及现象为
Ⅱ.二甘氨酸合铜(Ⅱ)水合物的制备
④称取适量甘氨酸,溶于150mL水中。
⑤在65~70℃的条件下加热,边搅拌边加入新制的
 ,至
,至 全部溶解。
全部溶解。⑥热抽滤,向滤液加入10mL无水乙醇。
⑦抽滤,用乙醇溶液洗涤晶体,再用丙酮洗涤,抽干。
⑧将产品烘干。
(3)步骤④中使用的部分仪器如下。仪器a的名称是
(5)步骤⑦中用乙醇溶液洗涤晶体后再用丙酮洗涤的原因为
Ⅲ.产品中铜含量的测定
称取
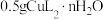 产品,加入水和稀硫酸溶解,配制成250mL溶液。取20.00mL该溶液,加入足量KI固体和50mL水,以淀粉为指示剂,立即用
产品,加入水和稀硫酸溶解,配制成250mL溶液。取20.00mL该溶液,加入足量KI固体和50mL水,以淀粉为指示剂,立即用 标准溶液滴定至终点,消耗
标准溶液滴定至终点,消耗 溶液1.60mL。
溶液1.60mL。已知:在酸性介质中,配合物中的
 被质子化,配合物被破坏;
被质子化,配合物被破坏;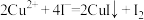 ,
, 。
。(6)滴定终点溶液颜色的变化为
(7)产品中铜元素的质量分数为
您最近一年使用:0次
名校
解题方法
9 . 苯及其同系物是一类重要的有机化工原料。
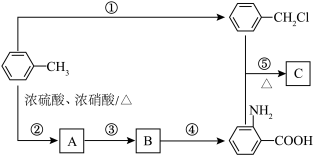
(1)B生成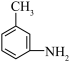 的反应类型为:
的反应类型为:________ ,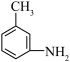 分子中最多有
分子中最多有________ 个原子共面。
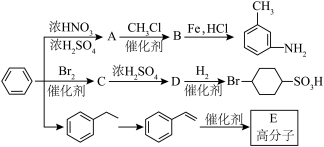
(2)由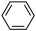 生成A温度控制在50~60℃,温度不宜过高或者过低,理由是
生成A温度控制在50~60℃,温度不宜过高或者过低,理由是________ 。
(3)已知: (R表示烃基),苯酚易被氧化。苯环上原有的取代基对新导入的取代基进入苯环的位置有显著的影响,根据上述转化关系,若以苯为原料有以下合成路线,则G的结构简式为
(R表示烃基),苯酚易被氧化。苯环上原有的取代基对新导入的取代基进入苯环的位置有显著的影响,根据上述转化关系,若以苯为原料有以下合成路线,则G的结构简式为________ 。
(4)反应②的副产物D与A互为同分异构体,写出生成D结构简式:________ 。
(5)反应④的条件为________ 。
(6)邻氨基苯甲酸在一定条件下可发生取代反应,生成酰胺类化合物,请写出由两个邻氨基苯甲酸分子生成的环状酰胺类化合物的结构简式________ 。
已知:①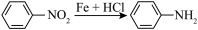 (苯胺,弱碱性,易被氧化)
(苯胺,弱碱性,易被氧化)
②苯的同系物能被酸性高锰酸钾氧化,如: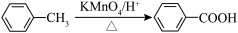
(1)B生成
 的反应类型为:
的反应类型为: 分子中最多有
分子中最多有(2)由
 生成A温度控制在50~60℃,温度不宜过高或者过低,理由是
生成A温度控制在50~60℃,温度不宜过高或者过低,理由是(3)已知:
 (R表示烃基),苯酚易被氧化。苯环上原有的取代基对新导入的取代基进入苯环的位置有显著的影响,根据上述转化关系,若以苯为原料有以下合成路线,则G的结构简式为
(R表示烃基),苯酚易被氧化。苯环上原有的取代基对新导入的取代基进入苯环的位置有显著的影响,根据上述转化关系,若以苯为原料有以下合成路线,则G的结构简式为 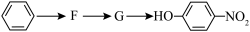
(4)反应②的副产物D与A互为同分异构体,写出生成D结构简式:
(5)反应④的条件为
(6)邻氨基苯甲酸在一定条件下可发生取代反应,生成酰胺类化合物,请写出由两个邻氨基苯甲酸分子生成的环状酰胺类化合物的结构简式
您最近一年使用:0次
解题方法
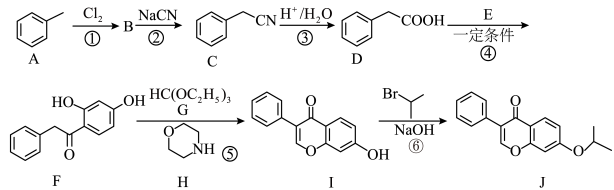
10 . 化合物J是一种抗骨质疏松药,俗称依普黄酮,以化合物A为原料合成该化合物的路线如下:
(1)A中最多有___________ 个原子共平面。
(2)化合物E的名称是___________ 。
(3)反应⑥反应类型为___________ ,J中无氧官能团的名称为___________ 。
(4)H为催化剂,F和G反应生成I和另一种有机物X,该反应的化学方程式为___________ 。
(5)F的同系物K,相对分子质量比F大28,满足下列条件的K的同分异构体有___________ 种,写出上述同分异构体的水解产物核磁共振峰面积比为6:2:1:1的结构简式___________ (写出一种即可)。
①能发生水解反应,水解后只生成两种产物;
②水解产物均只有4种不同化学环境的等效氢原子,且都能与 溶液发生显紫色反应。
溶液发生显紫色反应。
(6)一种制备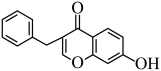 的合成路线如下:
的合成路线如下:___________ 。
已知: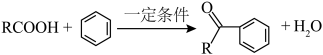
(1)A中最多有
(2)化合物E的名称是
(3)反应⑥反应类型为
(4)H为催化剂,F和G反应生成I和另一种有机物X,该反应的化学方程式为
(5)F的同系物K,相对分子质量比F大28,满足下列条件的K的同分异构体有
①能发生水解反应,水解后只生成两种产物;
②水解产物均只有4种不同化学环境的等效氢原子,且都能与
 溶液发生显紫色反应。
溶液发生显紫色反应。(6)一种制备
 的合成路线如下:
的合成路线如下:
您最近一年使用:0次