真题
解题方法
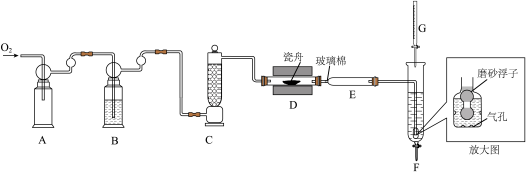
1 . 利用“燃烧—碘酸钾滴定法”测定钢铁中硫含量的实验装置如下图所示(夹持装置略)。
①加样,将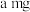 样品加入管式炉内瓷舟中(瓷舟两端带有气孔且有盖),聚四氟乙烯活塞滴定管G内预装
样品加入管式炉内瓷舟中(瓷舟两端带有气孔且有盖),聚四氟乙烯活塞滴定管G内预装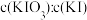 略小于
略小于 的
的 碱性标准溶液,吸收管F内盛有盐酸酸化的淀粉水溶液。向F内滴入适量
碱性标准溶液,吸收管F内盛有盐酸酸化的淀粉水溶液。向F内滴入适量 碱性标准溶液,发生反应:
碱性标准溶液,发生反应: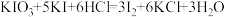 ,使溶液显浅蓝色。
,使溶液显浅蓝色。
②燃烧:按一定流速通入 ,一段时间后,加热并使样品燃烧。
,一段时间后,加热并使样品燃烧。
③滴定:当F内溶液浅蓝色消退时(发生反应: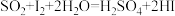 ),立即用
),立即用 碱性标准溶液滴定至浅蓝色复现。随
碱性标准溶液滴定至浅蓝色复现。随 不断进入F,滴定过程中溶液颜色“消退-变蓝”不断变换,直至终点。
不断进入F,滴定过程中溶液颜色“消退-变蓝”不断变换,直至终点。
回答下列问题:
(1)取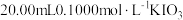 的碱性溶液和一定量的
的碱性溶液和一定量的 固体,配制
固体,配制
 碱性标准溶液,下列仪器必须用到的是_______(填标号)。
碱性标准溶液,下列仪器必须用到的是_______(填标号)。
(2)装置B和C的作用是充分干燥 ,B中的试剂为
,B中的试剂为_______ 。装置F中通气管末端多孔玻璃泡内置一密度小于水的磨砂浮子(见放大图),目的是_______ 。
(3)该滴定实验达终点的现象是_______ ;滴定消耗 碱性标准溶液
碱性标准溶液 ,样品中硫的质量分数是
,样品中硫的质量分数是_______ (用代数式表示)。
(4)若装置D中瓷舟未加盖,会因燃烧时产生粉尘而促进 的生成,粉尘在该过程中的作用是
的生成,粉尘在该过程中的作用是_______ ;若装置E冷却气体不充分,可能导致测定结果偏大,原因是_______ ;若滴定过程中,有少量 不经
不经 直接将
直接将 氧化成
氧化成 ,测定结果会
,测定结果会_______ (填“偏大”“偏小”或“不变”)。
①加样,将
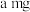 样品加入管式炉内瓷舟中(瓷舟两端带有气孔且有盖),聚四氟乙烯活塞滴定管G内预装
样品加入管式炉内瓷舟中(瓷舟两端带有气孔且有盖),聚四氟乙烯活塞滴定管G内预装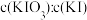 略小于
略小于 的
的 碱性标准溶液,吸收管F内盛有盐酸酸化的淀粉水溶液。向F内滴入适量
碱性标准溶液,吸收管F内盛有盐酸酸化的淀粉水溶液。向F内滴入适量 碱性标准溶液,发生反应:
碱性标准溶液,发生反应: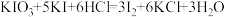 ,使溶液显浅蓝色。
,使溶液显浅蓝色。②燃烧:按一定流速通入
 ,一段时间后,加热并使样品燃烧。
,一段时间后,加热并使样品燃烧。③滴定:当F内溶液浅蓝色消退时(发生反应:
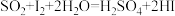 ),立即用
),立即用 碱性标准溶液滴定至浅蓝色复现。随
碱性标准溶液滴定至浅蓝色复现。随 不断进入F,滴定过程中溶液颜色“消退-变蓝”不断变换,直至终点。
不断进入F,滴定过程中溶液颜色“消退-变蓝”不断变换,直至终点。回答下列问题:
(1)取
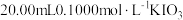 的碱性溶液和一定量的
的碱性溶液和一定量的 固体,配制
固体,配制
 碱性标准溶液,下列仪器必须用到的是_______(填标号)。
碱性标准溶液,下列仪器必须用到的是_______(填标号)。| A.玻璃棒 | B. 锥形瓶 锥形瓶 | C.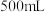 容量瓶 容量瓶 | D.胶头滴管 |
(2)装置B和C的作用是充分干燥
 ,B中的试剂为
,B中的试剂为(3)该滴定实验达终点的现象是
 碱性标准溶液
碱性标准溶液 ,样品中硫的质量分数是
,样品中硫的质量分数是(4)若装置D中瓷舟未加盖,会因燃烧时产生粉尘而促进
 的生成,粉尘在该过程中的作用是
的生成,粉尘在该过程中的作用是 不经
不经 直接将
直接将 氧化成
氧化成 ,测定结果会
,测定结果会
您最近一年使用:0次
解题方法
2 . 苯并咪唑是一类杂环化合物,其结构与天然存在的核苷酸的结构相似,具有较强的生物活性。以 ,
,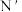 -二苄基邻苯二胺为原料,在二甲亚砜(DMSO)溶剂中,加入氧化剂DDQ,可制备1-苄基-2-苯基苯并咪唑,转化关系如图1所示:
-二苄基邻苯二胺为原料,在二甲亚砜(DMSO)溶剂中,加入氧化剂DDQ,可制备1-苄基-2-苯基苯并咪唑,转化关系如图1所示:
①称取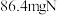 ,
,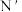 -二苄基邻苯二胺
-二苄基邻苯二胺 ,取足量氧化剂DDQ备用。
,取足量氧化剂DDQ备用。
②向 三颈烧瓶中依次加入
三颈烧瓶中依次加入 ,
,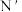 -二苄基邻苯二胺、DDQ,再加入
-二苄基邻苯二胺、DDQ,再加入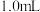 二甲亚砜。
二甲亚砜。
③将反应烧瓶移至 的油浴锅中,加热回流
的油浴锅中,加热回流 。
。
④向反应烧瓶中滴加 饱和
饱和 溶液,待反应液变色后加入
溶液,待反应液变色后加入 蒸馏水稀释反应液。将反应液转移至分液漏斗,加乙酸乙酯萃取后分液,用少量饱和食盐水洗涤有机层,分液,向有机层中加入无水硫酸镁固体,静置一段时间后,分离出液体,对分离出的液体进一步分离纯化,得到1-苄基-2-苯基苯并咪唑,称得质量为
蒸馏水稀释反应液。将反应液转移至分液漏斗,加乙酸乙酯萃取后分液,用少量饱和食盐水洗涤有机层,分液,向有机层中加入无水硫酸镁固体,静置一段时间后,分离出液体,对分离出的液体进一步分离纯化,得到1-苄基-2-苯基苯并咪唑,称得质量为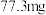 。
。
回答下列问题:
(1)仪器A的名称是______ ,冷凝水应从______ (选填“a”或“b”)口通入。
(2)从绿色化学的角度考虑,本实验不用浓硝酸做氧化剂的主要原因是______ 。
(3)步骤③中回流结束后需要进行的操作有:①停止加热,②关闭冷凝水,③移去油浴。正确的顺序是______(填字母)。
(4)步骤④中加入饱和 溶液的目的是
溶液的目的是______ 。
(5)步骤④中饱和食盐水的作用除了洗涤,还有_______ 。“进一步分离纯化”的操作是______ 。
(6)本实验中1-苄基-2-苯基苯并咪唑的产率是______ (保留一位小数)。
 ,
,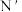 -二苄基邻苯二胺为原料,在二甲亚砜(DMSO)溶剂中,加入氧化剂DDQ,可制备1-苄基-2-苯基苯并咪唑,转化关系如图1所示:
-二苄基邻苯二胺为原料,在二甲亚砜(DMSO)溶剂中,加入氧化剂DDQ,可制备1-苄基-2-苯基苯并咪唑,转化关系如图1所示: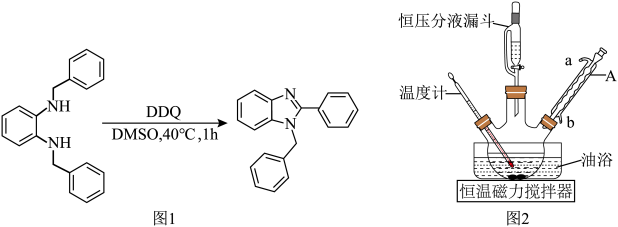
①称取
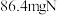 ,
,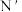 -二苄基邻苯二胺
-二苄基邻苯二胺 ,取足量氧化剂DDQ备用。
,取足量氧化剂DDQ备用。②向
 三颈烧瓶中依次加入
三颈烧瓶中依次加入 ,
,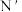 -二苄基邻苯二胺、DDQ,再加入
-二苄基邻苯二胺、DDQ,再加入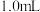 二甲亚砜。
二甲亚砜。③将反应烧瓶移至
 的油浴锅中,加热回流
的油浴锅中,加热回流 。
。④向反应烧瓶中滴加
 饱和
饱和 溶液,待反应液变色后加入
溶液,待反应液变色后加入 蒸馏水稀释反应液。将反应液转移至分液漏斗,加乙酸乙酯萃取后分液,用少量饱和食盐水洗涤有机层,分液,向有机层中加入无水硫酸镁固体,静置一段时间后,分离出液体,对分离出的液体进一步分离纯化,得到1-苄基-2-苯基苯并咪唑,称得质量为
蒸馏水稀释反应液。将反应液转移至分液漏斗,加乙酸乙酯萃取后分液,用少量饱和食盐水洗涤有机层,分液,向有机层中加入无水硫酸镁固体,静置一段时间后,分离出液体,对分离出的液体进一步分离纯化,得到1-苄基-2-苯基苯并咪唑,称得质量为 。
。回答下列问题:
(1)仪器A的名称是
(2)从绿色化学的角度考虑,本实验不用浓硝酸做氧化剂的主要原因是
(3)步骤③中回流结束后需要进行的操作有:①停止加热,②关闭冷凝水,③移去油浴。正确的顺序是______(填字母)。
| A.①②③ | B.③①② | C.②①③ | D.①③② |
(4)步骤④中加入饱和
 溶液的目的是
溶液的目的是(5)步骤④中饱和食盐水的作用除了洗涤,还有
(6)本实验中1-苄基-2-苯基苯并咪唑的产率是
您最近一年使用:0次
解题方法
3 . 阿司匹林的有效成分是乙酰水杨酸( 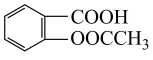 )。实验室以水杨酸(邻羟基苯甲酸)与醋酸酐[(CH3CO)2O]为主要原料合成乙酰水杨酸,制备的主要反应为:
)。实验室以水杨酸(邻羟基苯甲酸)与醋酸酐[(CH3CO)2O]为主要原料合成乙酰水杨酸,制备的主要反应为:
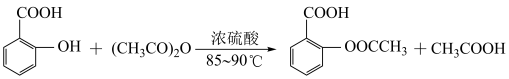
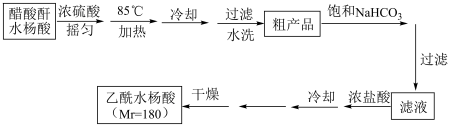
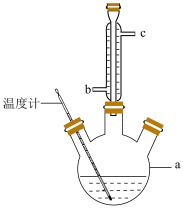
回答下列问题:
(1)合成过程中最合适的加热方法是
(2)提纯粗产品流程如下,加热回流装置如图:
①沸石的作用是
②冷凝水的流出方向是
③使用温度计的目的是
(3)检验最终产品中是否含有水杨酸的化学方法是
(4)阿司匹林药片中乙酰水杨酸含量的测定步骤(假定只含乙酰水杨酸和辅料,辅料不参与反应):
Ⅰ.称取阿司匹林样品m g;
Ⅱ.将样品研碎,溶于V1 mL a mol·L-1NaOH(过量)并加热,除去辅料等不溶物,将所得溶液移入锥形瓶;
Ⅲ.向锥形瓶中滴加几滴酚酞,用浓度为b mol·L-1的标准盐酸到滴定剩余的NaOH,消耗盐酸的体积为V2 mL。
①研碎时用到的实验仪器有
②写出乙酰水杨酸与过量NaOH溶液加热发生反应的化学方程式
③阿司匹林药片中乙酰水杨酸质量分数的表达式为
您最近一年使用:0次
名校
解题方法
4 . 新冠病毒感染者居家治疗常用药参考表中,将布洛芬列为发热症状常用药物。布洛芬(化合物J)的一种合成路线如图所示(部分反应条件省略)。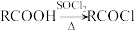
回答下列问题:
(1)D的化学名称为_____ 。I的分子式为_____ 。
(2)反应B→C、G→H的反应类型分别为_____ 、_____ 。
(3)E→F的反应方程式为_____ 。
(4)已知Q的分子式比J的分子式少C4H8,写出一种含有手性碳原子的Q的结构简式_____ 。写出符合下列条件的Q的结构简式_____ 。
①苯环上有4个取代基,其中2个取代基相同
②能发生银镜反应
③能与FeCl3溶液发生显色反应
④核磁共振氢谱显示有4组峰,且峰面积之比为1:2:6:1
(5)苄基苯是一种有机合成中间体,可用于配制皂用香精,其结构简式为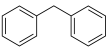 。设计以苯甲醛和苯为原料制备苄基苯的合成路线(其他试剂任选)
。设计以苯甲醛和苯为原料制备苄基苯的合成路线(其他试剂任选)_____ 。
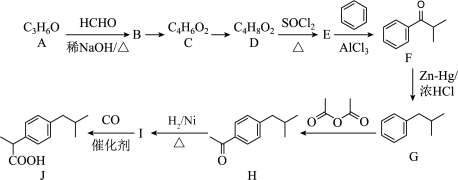
已知:①HCHO+RCH2CHO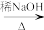
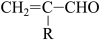
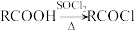
回答下列问题:
(1)D的化学名称为
(2)反应B→C、G→H的反应类型分别为
(3)E→F的反应方程式为
(4)已知Q的分子式比J的分子式少C4H8,写出一种含有手性碳原子的Q的结构简式
①苯环上有4个取代基,其中2个取代基相同
②能发生银镜反应
③能与FeCl3溶液发生显色反应
④核磁共振氢谱显示有4组峰,且峰面积之比为1:2:6:1
(5)苄基苯是一种有机合成中间体,可用于配制皂用香精,其结构简式为
 。设计以苯甲醛和苯为原料制备苄基苯的合成路线(其他试剂任选)
。设计以苯甲醛和苯为原料制备苄基苯的合成路线(其他试剂任选)
您最近一年使用:0次
名校
解题方法
5 . 香豆素又名1,2-苯并吡喃酮,是一种重要的香料。某小组以水杨醛和醋酸酐为原料,用以下方案制备香豆素。
Ⅲ.向三颈烧瓶烧中加入水杨醛、醋酸酐和醋酸钾,加热进行反应;反应时,通过温度计监测馏出温度为120-125℃,待无馏出物时,通过仪器A向烧瓶中补加预热的醋酸酐,并保持补加速度与馏出速度一致;加料完毕,反应一定时间后停止加热,将混合液趁热倒入烧杯中,用10% 溶液洗涤2次,至pH值为7;分离出香豆素粗产品,对香豆素粗产品进行减压蒸馏,在1.5kPa、145℃下收集馏分,再重结晶2次,过滤、洗涤、干燥,得到香豆素精品。回答下列问题:
溶液洗涤2次,至pH值为7;分离出香豆素粗产品,对香豆素粗产品进行减压蒸馏,在1.5kPa、145℃下收集馏分,再重结晶2次,过滤、洗涤、干燥,得到香豆素精品。回答下列问题:
(1)仪器A的名称是___________ 。
(2)从平衡移动角度分析,反应时馏出温度为120~125℃的目的是___________ 。
(3)在补加醋酸酐时,判断反应已无馏出物的方法是___________ 。
(4)反应后混合液用10% 溶液洗涤时,除去一种芳香性物质的化学方程式为
溶液洗涤时,除去一种芳香性物质的化学方程式为_________ 。
(5)控制其他因素一定,改变反应原料水杨醛和醋酸酐的投料比,探究其对转化率的影响。A、B、C、D组加入的水杨醛与醋酸酐的物质的量之比分别为1:3.0、1:3.5、1:4.0、1:4.5.在反应结束后,取水杨醛和四组混合液进行薄层色谱分析,结果如图所示。则水杨醛和醋酸酐的最佳投料比为________ 。___________ 。
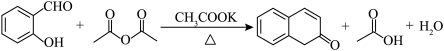
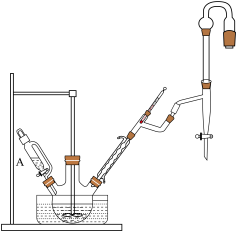
| 物质 | 分子量 | 性状 | 熔点 | 沸点 | 溶解性 |
| 水杨醛 | 122 | 无色液体 | -7℃ | 196℃ | 微溶于水,易溶于有机溶剂 |
| 醋酸酐 | 102 | 无色液体 | -73℃ | 140℃ | 微溶于水,易溶于有机溶剂 |
| 香豆素 | 146 | 白色结晶固体 | 71℃ | 302℃ | 难溶于冷水,可溶于热水,易溶于乙醇等有机溶剂 |
| 乙酸 | 60 | 无色液体 | 16℃ | 118℃ | 易溶于水,可溶于有机溶剂 |
| 乙酸钾 | 98 | 白色粉末 | 292℃ | 分解 | 易溶于水,难溶于有机溶剂 |
 溶液洗涤2次,至pH值为7;分离出香豆素粗产品,对香豆素粗产品进行减压蒸馏,在1.5kPa、145℃下收集馏分,再重结晶2次,过滤、洗涤、干燥,得到香豆素精品。回答下列问题:
溶液洗涤2次,至pH值为7;分离出香豆素粗产品,对香豆素粗产品进行减压蒸馏,在1.5kPa、145℃下收集馏分,再重结晶2次,过滤、洗涤、干燥,得到香豆素精品。回答下列问题:(1)仪器A的名称是
(2)从平衡移动角度分析,反应时馏出温度为120~125℃的目的是
(3)在补加醋酸酐时,判断反应已无馏出物的方法是
(4)反应后混合液用10%
 溶液洗涤时,除去一种芳香性物质的化学方程式为
溶液洗涤时,除去一种芳香性物质的化学方程式为(5)控制其他因素一定,改变反应原料水杨醛和醋酸酐的投料比,探究其对转化率的影响。A、B、C、D组加入的水杨醛与醋酸酐的物质的量之比分别为1:3.0、1:3.5、1:4.0、1:4.5.在反应结束后,取水杨醛和四组混合液进行薄层色谱分析,结果如图所示。则水杨醛和醋酸酐的最佳投料比为
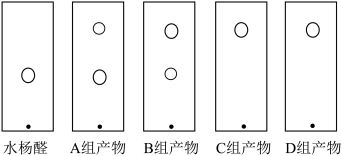
| 反应温度 | 粗产品质量 | 香豆素精品收 |
| 170℃ | 11.68g | 70.0% |
| 175℃ | 13.14g | 75.0% |
| 180℃ | 14.60g | 72.0% |
您最近一年使用:0次
6 . 催化剂的研究一直是一个重要的领域。根据所学知识,回答下列问题:
I.铁触媒是普遍使用的以铁为主体的多成分催化剂,通常还含有 、
、 、
、 、
、 、
、 等氧化物中的几种。
等氧化物中的几种。
(1)基态氧原子中,核外电子有___________ 种空间运动状态,能量最高的电子的电子云在空间有___________ 个伸展方向。
(2)原子中运动的电子有两种相反的自旋状态,若一种自旋状态用“ ”表示,与之相反的用“
”表示,与之相反的用“ ”表示,
”表示, 即称为电子的自旋磁量子数。对于基态的铁原子,其价层电子自旋磁量子数的代数和为
即称为电子的自旋磁量子数。对于基态的铁原子,其价层电子自旋磁量子数的代数和为___________ 。
Ⅱ.我国科研人员研制出了 (M为
(M为 、等金属)等催化剂,使得合成氨工业的温度、压强分别降到了
、等金属)等催化剂,使得合成氨工业的温度、压强分别降到了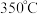 、
、 ,这是近年来合成氨反应研究中的重要突破。
,这是近年来合成氨反应研究中的重要突破。
(3) 在元素周期表中位于
在元素周期表中位于___________ 区。
(4)第三电离能:
___________ (填“ ”或“
”或“ ”)
”) ,原因是
,原因是___________ 。
Ⅲ. 、
、 、
、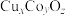 、
、 是常见的无机非贵金属光催化剂等。
是常见的无机非贵金属光催化剂等。
(5)铜元素的焰色试验呈绿色,下列三种波长为橙、黄、绿色对应的波长,则其中绿色对应的辐射波长为___________ (填标号)。
A.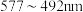 B.
B.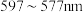 C.
C.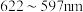
I.铁触媒是普遍使用的以铁为主体的多成分催化剂,通常还含有
 、
、 、
、 、
、 、
、 等氧化物中的几种。
等氧化物中的几种。(1)基态氧原子中,核外电子有
(2)原子中运动的电子有两种相反的自旋状态,若一种自旋状态用“
 ”表示,与之相反的用“
”表示,与之相反的用“ ”表示,
”表示, 即称为电子的自旋磁量子数。对于基态的铁原子,其价层电子自旋磁量子数的代数和为
即称为电子的自旋磁量子数。对于基态的铁原子,其价层电子自旋磁量子数的代数和为Ⅱ.我国科研人员研制出了
 (M为
(M为 、等金属)等催化剂,使得合成氨工业的温度、压强分别降到了
、等金属)等催化剂,使得合成氨工业的温度、压强分别降到了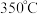 、
、 ,这是近年来合成氨反应研究中的重要突破。
,这是近年来合成氨反应研究中的重要突破。(3)
 在元素周期表中位于
在元素周期表中位于(4)第三电离能:

 ”或“
”或“ ”)
”) ,原因是
,原因是Ⅲ.
 、
、 、
、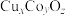 、
、 是常见的无机非贵金属光催化剂等。
是常见的无机非贵金属光催化剂等。(5)铜元素的焰色试验呈绿色,下列三种波长为橙、黄、绿色对应的波长,则其中绿色对应的辐射波长为
A.
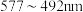 B.
B.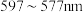 C.
C.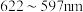
您最近一年使用:0次
名校
7 . 甲烷和甲醇 既是重要的化工原料,又是未来重要的能源物质。
既是重要的化工原料,又是未来重要的能源物质。
(1)将 和
和 通入容积为
通入容积为 的恒容密闭容器中,恒温条件下发生反应:
的恒容密闭容器中,恒温条件下发生反应: 。
。
①下列描述中能说明该反应已达到平衡状态的是_______ (填标号)。
A.断裂 键时,生成
键时,生成 键
键
B.容器内混合气体的平均摩尔质量保持不变
C.容器内混合气体的压强保持不变
D.容器内CO与H2的体积之比保持不变
②测得在 时该反应达到平衡,此时CH4的物质的量为
时该反应达到平衡,此时CH4的物质的量为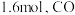 的物质的量浓度为
的物质的量浓度为 。则
。则 内,用CO表示的该反应平均反应速率
内,用CO表示的该反应平均反应速率
_______ mol•L-1•min-1,V=_______  。
。
(2)在容积为 的恒容密闭容器中通入等物质的量的
的恒容密闭容器中通入等物质的量的 和
和 ,进行反应:
,进行反应: 。
。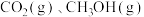 的物质的量随时间的变化关系如图所示。
的物质的量随时间的变化关系如图所示。_______ (填“a”“b”“c”或“d”);用同一物质表示反应速率时,a,c两点的正反应速率:Va_______ (填“ ”“
”“ ”或“
”或“ ”,下同)
”,下同)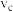 ,该反应达到平衡时,CO2的转化率
,该反应达到平衡时,CO2的转化率_______ 50%。
 既是重要的化工原料,又是未来重要的能源物质。
既是重要的化工原料,又是未来重要的能源物质。(1)将
 和
和 通入容积为
通入容积为 的恒容密闭容器中,恒温条件下发生反应:
的恒容密闭容器中,恒温条件下发生反应: 。
。①下列描述中能说明该反应已达到平衡状态的是
A.断裂
 键时,生成
键时,生成 键
键B.容器内混合气体的平均摩尔质量保持不变
C.容器内混合气体的压强保持不变
D.容器内CO与H2的体积之比保持不变
②测得在
 时该反应达到平衡,此时CH4的物质的量为
时该反应达到平衡,此时CH4的物质的量为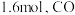 的物质的量浓度为
的物质的量浓度为 。则
。则 内,用CO表示的该反应平均反应速率
内,用CO表示的该反应平均反应速率
 。
。(2)在容积为
 的恒容密闭容器中通入等物质的量的
的恒容密闭容器中通入等物质的量的 和
和 ,进行反应:
,进行反应: 。
。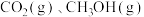 的物质的量随时间的变化关系如图所示。
的物质的量随时间的变化关系如图所示。
 ”“
”“ ”或“
”或“ ”,下同)
”,下同)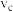 ,该反应达到平衡时,CO2的转化率
,该反应达到平衡时,CO2的转化率
您最近一年使用:0次
2024-06-16更新
|
38次组卷
|
3卷引用:山东省部分学校2023-2024学年高一下学期五月月考化学试题
名校
8 . 某实验小组用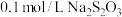 溶液和
溶液和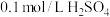 溶液为反应物,探究外界条件对化学反应速率的影响,实验记录如下表。
溶液为反应物,探究外界条件对化学反应速率的影响,实验记录如下表。
已知:实验结果: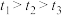 。回答下列问题:
。回答下列问题:
(1)a=___________ ml。
(2)写出Na2S2O3溶液和H2SO4溶液反应的离子方程式:___________ 。
(3)对比实验I、III可知,___________ 能加快反应速率。
(4)进行实验I、II时,依次向试管中加入Na2S2O3溶液、___________ 、___________ ,两者的顺序不可颠倒,理由是:___________ 。
(5)经查阅资料,构成原电池也能加快反应速率。某小组用一定的锌与足量的0.1 mol/L H2SO4溶液反应,下列物质即能加快反应速率,又不影响生成气体量的是:___________
a.适当升温 b.滴加几滴0.15 mol/LHCl c.滴加几滴 溶液
溶液
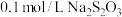 溶液和
溶液和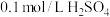 溶液为反应物,探究外界条件对化学反应速率的影响,实验记录如下表。
溶液为反应物,探究外界条件对化学反应速率的影响,实验记录如下表。| 实验序号 | 温度/℃ | Na2S2O3溶液体积/mL | H2SO4溶液体积/mL | H2O体积/mL | 出现沉淀所需的时间/s |
| I | 20 | 5.0 | 5.0 | 10.0 | t1 |
| II | 20 | 5.0 | 10.0 | a | t2 |
| III | 60 | 5.0 | 5.0 | 10.0 | t3 |
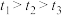 。回答下列问题:
。回答下列问题:(1)a=
(2)写出Na2S2O3溶液和H2SO4溶液反应的离子方程式:
(3)对比实验I、III可知,
(4)进行实验I、II时,依次向试管中加入Na2S2O3溶液、
(5)经查阅资料,构成原电池也能加快反应速率。某小组用一定的锌与足量的0.1 mol/L H2SO4溶液反应,下列物质即能加快反应速率,又不影响生成气体量的是:
a.适当升温 b.滴加几滴0.15 mol/LHCl c.滴加几滴
 溶液
溶液
您最近一年使用:0次
解题方法
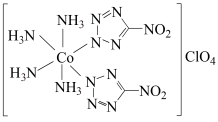
9 . 高性能炸药BNCP的结构如下所示,回答下列问题: 的基态价层电子排布图是
的基态价层电子排布图是_______ , 的配位数是
的配位数是_______ ,阴离子 的中心原子杂化类型是
的中心原子杂化类型是_______ 。
(2)
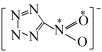 配体中的
配体中的 键的数目是
键的数目是_______ ,已知该配体是平面结构,图中标记的 原子与
原子与 原子之间的
原子之间的 键是由
键是由 原子的
原子的_______ 杂化轨道与O原子的_______ 轨道重叠形成的。
(3)比较 、
、 、
、 的键角大小:
的键角大小:_______ 。
(4)比较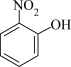 、
、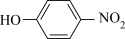 的沸点并说明理由:
的沸点并说明理由:_______ 。
(5)比较 与
与 的极性大小并说明理由:
的极性大小并说明理由:_______ 。
(6)2018年南京理工大学胡炳成团队合成全国首个全氮阴离子,全氮阴离子的盐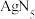 的晶体结构中:
的晶体结构中: 采取面心立方最密堆积,
采取面心立方最密堆积, 填在正四面体空隙中,从晶胞上方俯视的投影图如图所示。每个晶胞中含有的
填在正四面体空隙中,从晶胞上方俯视的投影图如图所示。每个晶胞中含有的 的数目是
的数目是_______ , 与
与 最近的距离是
最近的距离是_______ (用 表示)。
表示)。
 的基态价层电子排布图是
的基态价层电子排布图是 的配位数是
的配位数是 的中心原子杂化类型是
的中心原子杂化类型是(2)

 配体中的
配体中的 键的数目是
键的数目是 原子与
原子与 原子之间的
原子之间的 键是由
键是由 原子的
原子的(3)比较
 、
、 、
、 的键角大小:
的键角大小:(4)比较
 、
、 的沸点并说明理由:
的沸点并说明理由:(5)比较
 与
与 的极性大小并说明理由:
的极性大小并说明理由:(6)2018年南京理工大学胡炳成团队合成全国首个全氮阴离子,全氮阴离子的盐
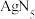 的晶体结构中:
的晶体结构中: 采取面心立方最密堆积,
采取面心立方最密堆积, 填在正四面体空隙中,从晶胞上方俯视的投影图如图所示。每个晶胞中含有的
填在正四面体空隙中,从晶胞上方俯视的投影图如图所示。每个晶胞中含有的 的数目是
的数目是 与
与 最近的距离是
最近的距离是 表示)。
表示)。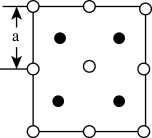
您最近一年使用:0次
10 . 氮化钒(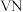 )作为一种有效、经济的合金添加剂被广泛应用。实验室探究制取氮化钒并测定所得氮化钒的纯度的实验装置如图(夹持装置略去)。
)作为一种有效、经济的合金添加剂被广泛应用。实验室探究制取氮化钒并测定所得氮化钒的纯度的实验装置如图(夹持装置略去)。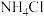 溶液与
溶液与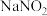 溶液反应制取
溶液反应制取 。
。
(1)检验装置的气密性方法是___________ 。
(2)制备氮化钒的一种方法为将 先用碳还原后再氮化,此法需将
先用碳还原后再氮化,此法需将 与焦炭混合放入石英管,关闭
与焦炭混合放入石英管,关闭___________ (填开关代号,下同),打开___________ 和真空泵,加热热电偶。
(3)氮化反应为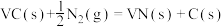 ,
,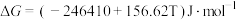 ,则此反应能自发进行的上限温度(反应截止温度)为
,则此反应能自发进行的上限温度(反应截止温度)为___________ K(T的单位为K)。氮化过程中,反应截止温度 还受氮气分压的影响,其影响如下图,则
还受氮气分压的影响,其影响如下图,则___________ (填“增大”或“减小”)氮气分压有利于氮化反应进行。 热还原时通入氮气使氮化反应同时进行,可以降低成本提高产率。此反应过程中,生成的
热还原时通入氮气使氮化反应同时进行,可以降低成本提高产率。此反应过程中,生成的 与
与 的物质的量比为3:1,则装置C中反应的化学方程式为
的物质的量比为3:1,则装置C中反应的化学方程式为___________ ,每生成 氮化钒,转移电子
氮化钒,转移电子___________  。
。
(5)向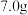 所得
所得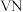 中加入足量
中加入足量 溶液,将产生的
溶液,将产生的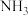 用
用 1mol/L
1mol/L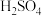 溶液恰好完全吸收生成正盐,则所得产品中
溶液恰好完全吸收生成正盐,则所得产品中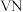 的质量分数为
的质量分数为___________ (结果保留三位有效数字)。
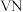 )作为一种有效、经济的合金添加剂被广泛应用。实验室探究制取氮化钒并测定所得氮化钒的纯度的实验装置如图(夹持装置略去)。
)作为一种有效、经济的合金添加剂被广泛应用。实验室探究制取氮化钒并测定所得氮化钒的纯度的实验装置如图(夹持装置略去)。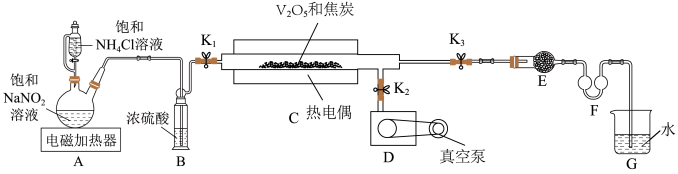
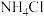 溶液与
溶液与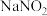 溶液反应制取
溶液反应制取 。
。(1)检验装置的气密性方法是
(2)制备氮化钒的一种方法为将
 先用碳还原后再氮化,此法需将
先用碳还原后再氮化,此法需将 与焦炭混合放入石英管,关闭
与焦炭混合放入石英管,关闭(3)氮化反应为
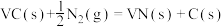 ,
,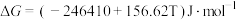 ,则此反应能自发进行的上限温度(反应截止温度)为
,则此反应能自发进行的上限温度(反应截止温度)为 还受氮气分压的影响,其影响如下图,则
还受氮气分压的影响,其影响如下图,则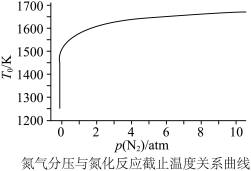
 热还原时通入氮气使氮化反应同时进行,可以降低成本提高产率。此反应过程中,生成的
热还原时通入氮气使氮化反应同时进行,可以降低成本提高产率。此反应过程中,生成的 与
与 的物质的量比为3:1,则装置C中反应的化学方程式为
的物质的量比为3:1,则装置C中反应的化学方程式为 氮化钒,转移电子
氮化钒,转移电子 。
。(5)向
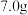 所得
所得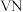 中加入足量
中加入足量 溶液,将产生的
溶液,将产生的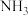 用
用 1mol/L
1mol/L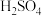 溶液恰好完全吸收生成正盐,则所得产品中
溶液恰好完全吸收生成正盐,则所得产品中 的质量分数为
的质量分数为
您最近一年使用:0次



