名校
1 . 铋酸钠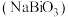 是分析化学中的重要试剂,可应用于钢铁分析中测定锰。某兴趣小组设计实验制取铋酸钠并探究其应用,其中,
是分析化学中的重要试剂,可应用于钢铁分析中测定锰。某兴趣小组设计实验制取铋酸钠并探究其应用,其中,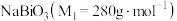 为淡黄色固体,难溶于冷水,遇沸水或酸则迅速分解;
为淡黄色固体,难溶于冷水,遇沸水或酸则迅速分解;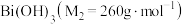 为白色固体,难溶于水。根据实验回答下列问题:
为白色固体,难溶于水。根据实验回答下列问题:_______ 。
(2)装置C中发生反应的离子方程式为_______ 。
(3)装置B的作用为_______ 。
(4)反应结束后,为从装置C中获得尽可能多的产品的操作是_______ 、过滤、洗涤、干燥。
(5) 在酸性介质中可用于
在酸性介质中可用于 的鉴定,已知
的鉴定,已知 被还原为
被还原为 ,其中氧化剂与还原剂的物质的量之比为
,其中氧化剂与还原剂的物质的量之比为_______ 。
(6)取上述 样品
样品 ,加入稀硫酸和
,加入稀硫酸和 溶液使其完全溶解,稀释至
溶液使其完全溶解,稀释至 ,取出
,取出 溶液,然后用新配制的
溶液,然后用新配制的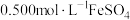 溶液进行滴定,滴定终点的颜色变化为
溶液进行滴定,滴定终点的颜色变化为_______ ,假设终点时消耗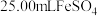 溶液。则该样品中
溶液。则该样品中 纯度为
纯度为_______ %(结果保留小数点后一位)。
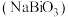 是分析化学中的重要试剂,可应用于钢铁分析中测定锰。某兴趣小组设计实验制取铋酸钠并探究其应用,其中,
是分析化学中的重要试剂,可应用于钢铁分析中测定锰。某兴趣小组设计实验制取铋酸钠并探究其应用,其中,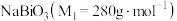 为淡黄色固体,难溶于冷水,遇沸水或酸则迅速分解;
为淡黄色固体,难溶于冷水,遇沸水或酸则迅速分解;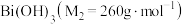 为白色固体,难溶于水。根据实验回答下列问题:
为白色固体,难溶于水。根据实验回答下列问题: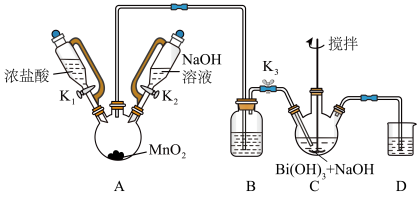
(2)装置C中发生反应的离子方程式为
(3)装置B的作用为
(4)反应结束后,为从装置C中获得尽可能多的产品的操作是
(5)
 在酸性介质中可用于
在酸性介质中可用于 的鉴定,已知
的鉴定,已知 被还原为
被还原为 ,其中氧化剂与还原剂的物质的量之比为
,其中氧化剂与还原剂的物质的量之比为(6)取上述
 样品
样品 ,加入稀硫酸和
,加入稀硫酸和 溶液使其完全溶解,稀释至
溶液使其完全溶解,稀释至 ,取出
,取出 溶液,然后用新配制的
溶液,然后用新配制的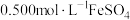 溶液进行滴定,滴定终点的颜色变化为
溶液进行滴定,滴定终点的颜色变化为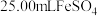 溶液。则该样品中
溶液。则该样品中 纯度为
纯度为
您最近一年使用:0次
名校
解题方法
2 . 碲(Te)常用于冶金工业,也是石油裂解的催化剂。工业上常以碲铜废料(主要成分是 )为原料提取碲,其工艺流程如下:
)为原料提取碲,其工艺流程如下: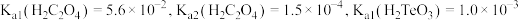 ,
,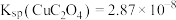 。
。
(1) 中碲元素的化合价为
中碲元素的化合价为_______ 。碲在元素周期表中的位置为_______ 。
(2)“氧化酸浸”得到 和
和 ,该反应的化学方程式为
,该反应的化学方程式为_______ 。
(3) 可溶于
可溶于 ,反应
,反应 的平衡常数为
的平衡常数为_______ 。(保留两位有效数字){已知:反应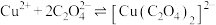 的平衡常数
的平衡常数 }
}
(4)“还原”在 50 ℃条件下进行: ,反应中还原产物和氧化产物的物质的量之比为
,反应中还原产物和氧化产物的物质的量之比为_______ 。
(5)“还原”时, 的实际投入量大于理论量,其可能原因有
的实际投入量大于理论量,其可能原因有_______ 。
(6)将一定质量的 置于
置于 气中热解,测得剩余固体的质量与原始固体的质量的比值约为
气中热解,测得剩余固体的质量与原始固体的质量的比值约为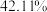 ,则剩余固体的化学式为
,则剩余固体的化学式为_______ 。
 )为原料提取碲,其工艺流程如下:
)为原料提取碲,其工艺流程如下:
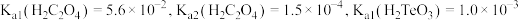 ,
,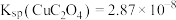 。
。(1)
 中碲元素的化合价为
中碲元素的化合价为(2)“氧化酸浸”得到
 和
和 ,该反应的化学方程式为
,该反应的化学方程式为(3)
 可溶于
可溶于 ,反应
,反应 的平衡常数为
的平衡常数为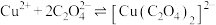 的平衡常数
的平衡常数 }
}(4)“还原”在 50 ℃条件下进行:
 ,反应中还原产物和氧化产物的物质的量之比为
,反应中还原产物和氧化产物的物质的量之比为(5)“还原”时,
 的实际投入量大于理论量,其可能原因有
的实际投入量大于理论量,其可能原因有(6)将一定质量的
 置于
置于 气中热解,测得剩余固体的质量与原始固体的质量的比值约为
气中热解,测得剩余固体的质量与原始固体的质量的比值约为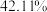 ,则剩余固体的化学式为
,则剩余固体的化学式为
您最近一年使用:0次
名校
3 . 尿素是一种重要化工生产原料。工业上以液氨和二氧化碳为原料,在高温高压条件下直接合成尿素,主要反应如下:
①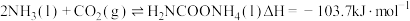
②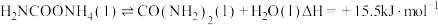
回答下列问题:
(1)
_______  。
。
(2)在 和
和 时
时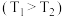 ,向恒容容器中投入等物质的量的两种反应物,发生反应:
,向恒容容器中投入等物质的量的两种反应物,发生反应: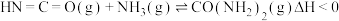 。
。
平衡时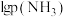 与
与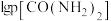 的关系如图所示,
的关系如图所示,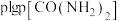 为物质的分压(单位为
为物质的分压(单位为 ),若
),若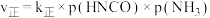 ,
,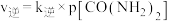 。
。 时,
时,
_______ 。 时此反应的标准平衡常数
时此反应的标准平衡常数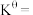
_______ 。{已知:分压 总压
总压 该组分物质的量分数,对于反应:
该组分物质的量分数,对于反应: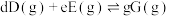 ,其中
,其中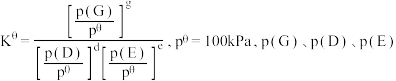 为各组分的平衡分压}
为各组分的平衡分压}_______ 。
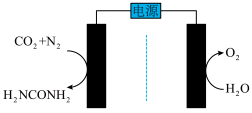
(4)电化学合成尿素为实现碳、氮中和与减轻环境污染提供了一种很有前景的解决方案。某碱性电化学合成系统如图所示,该系统中,合成尿素的一极与电源_______ 相连,其反应方程式为_______ 。
①
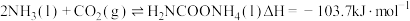
②
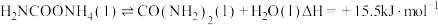
回答下列问题:
(1)

 。
。(2)在
 和
和 时
时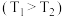 ,向恒容容器中投入等物质的量的两种反应物,发生反应:
,向恒容容器中投入等物质的量的两种反应物,发生反应: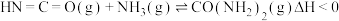 。
。平衡时
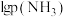 与
与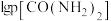 的关系如图所示,
的关系如图所示,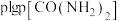 为物质的分压(单位为
为物质的分压(单位为 ),若
),若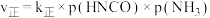 ,
,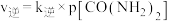 。
。 时,
时,
 时此反应的标准平衡常数
时此反应的标准平衡常数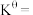
 总压
总压 该组分物质的量分数,对于反应:
该组分物质的量分数,对于反应: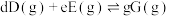 ,其中
,其中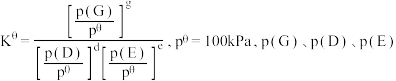 为各组分的平衡分压}
为各组分的平衡分压}
(4)电化学合成尿素为实现碳、氮中和与减轻环境污染提供了一种很有前景的解决方案。某碱性电化学合成系统如图所示,该系统中,合成尿素的一极与电源
您最近一年使用:0次
名校
4 . 氨硼烷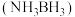 具有含氢量高,热稳定性好的特点,是一种具有潜力的固体储氢材料,回答下列问题。
具有含氢量高,热稳定性好的特点,是一种具有潜力的固体储氢材料,回答下列问题。
(1)基态N原子核外电子占据的最高能级的电子云轮廓图为___________ 形,基态N原子的轨道表示式为___________ 。
(2)已知 的第一电离能
的第一电离能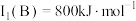 ,判断
,判断
___________ (填“>”或“<”) ,从核外电子排布的角度说明理由:
,从核外电子排布的角度说明理由:___________
(3) 分子中,与
分子中,与 原子相连的
原子相连的 原子对键合电子的吸引力小于
原子对键合电子的吸引力小于 原子,与
原子,与 原子相连的
原子相连的 原子对键合电子的吸引力大于
原子对键合电子的吸引力大于 原子。则在
原子。则在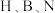 三种元素中:
三种元素中:
①电负性大小顺序是___________ (用元素符号表示,下同);
②原子半径大小顺序是___________ ;
③在元素周期表中的分区与其他两种元素不同的是___________ ;
(4)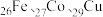 是目前氨硼烷水解产氢催化剂的研究热点。不同催化剂催化氨硼烷水解产氢的性能如图所示。
是目前氨硼烷水解产氢催化剂的研究热点。不同催化剂催化氨硼烷水解产氢的性能如图所示。___________ ,催化效果最差的金属的基态原子的价层电子排布式为___________ 。
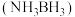 具有含氢量高,热稳定性好的特点,是一种具有潜力的固体储氢材料,回答下列问题。
具有含氢量高,热稳定性好的特点,是一种具有潜力的固体储氢材料,回答下列问题。(1)基态N原子核外电子占据的最高能级的电子云轮廓图为
(2)已知
 的第一电离能
的第一电离能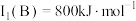 ,判断
,判断
 ,从核外电子排布的角度说明理由:
,从核外电子排布的角度说明理由:(3)
 分子中,与
分子中,与 原子相连的
原子相连的 原子对键合电子的吸引力小于
原子对键合电子的吸引力小于 原子,与
原子,与 原子相连的
原子相连的 原子对键合电子的吸引力大于
原子对键合电子的吸引力大于 原子。则在
原子。则在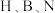 三种元素中:
三种元素中:①电负性大小顺序是
②原子半径大小顺序是
③在元素周期表中的分区与其他两种元素不同的是
(4)
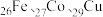 是目前氨硼烷水解产氢催化剂的研究热点。不同催化剂催化氨硼烷水解产氢的性能如图所示。
是目前氨硼烷水解产氢催化剂的研究热点。不同催化剂催化氨硼烷水解产氢的性能如图所示。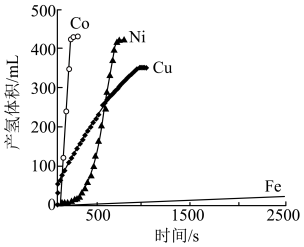
您最近一年使用:0次
名校
解题方法
5 . 苯及其同系物是一类重要的有机化工原料。
(1)B生成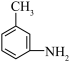 的反应类型为:
的反应类型为:________ ,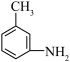 分子中最多有
分子中最多有________ 个原子共面。
(2)由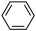 生成A温度控制在50~60℃,温度不宜过高或者过低,理由是
生成A温度控制在50~60℃,温度不宜过高或者过低,理由是________ 。
(3)已知: (R表示烃基),苯酚易被氧化。苯环上原有的取代基对新导入的取代基进入苯环的位置有显著的影响,根据上述转化关系,若以苯为原料有以下合成路线,则G的结构简式为
(R表示烃基),苯酚易被氧化。苯环上原有的取代基对新导入的取代基进入苯环的位置有显著的影响,根据上述转化关系,若以苯为原料有以下合成路线,则G的结构简式为________ 。
(4)反应②的副产物D与A互为同分异构体,写出生成D结构简式:________ 。
(5)反应④的条件为________ 。
(6)邻氨基苯甲酸在一定条件下可发生取代反应,生成酰胺类化合物,请写出由两个邻氨基苯甲酸分子生成的环状酰胺类化合物的结构简式________ 。
已知:①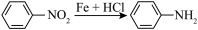 (苯胺,弱碱性,易被氧化)
(苯胺,弱碱性,易被氧化)
②苯的同系物能被酸性高锰酸钾氧化,如: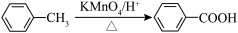
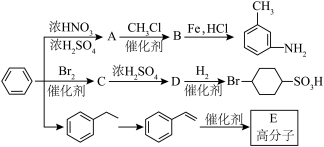
(1)B生成
 的反应类型为:
的反应类型为: 分子中最多有
分子中最多有(2)由
 生成A温度控制在50~60℃,温度不宜过高或者过低,理由是
生成A温度控制在50~60℃,温度不宜过高或者过低,理由是(3)已知:
 (R表示烃基),苯酚易被氧化。苯环上原有的取代基对新导入的取代基进入苯环的位置有显著的影响,根据上述转化关系,若以苯为原料有以下合成路线,则G的结构简式为
(R表示烃基),苯酚易被氧化。苯环上原有的取代基对新导入的取代基进入苯环的位置有显著的影响,根据上述转化关系,若以苯为原料有以下合成路线,则G的结构简式为 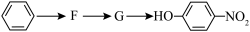
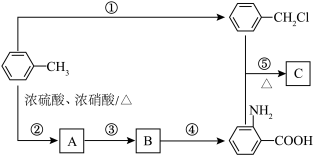
(4)反应②的副产物D与A互为同分异构体,写出生成D结构简式:
(5)反应④的条件为
(6)邻氨基苯甲酸在一定条件下可发生取代反应,生成酰胺类化合物,请写出由两个邻氨基苯甲酸分子生成的环状酰胺类化合物的结构简式
您最近一年使用:0次
名校
解题方法
6 . 金属资源都是不可再生资源,废旧金属回收利用,可以节约金属资源,还可以保护环境。一种电路板中回收铜元素的工艺如下:
(1)铜在周期表中的位置___________ 。
(2)将废电路板“粉碎”的目的是___________ ,“溶浸”时溶液温度不能太高的原因是___________ 。
某化学兴趣小组为探究“溶浸”过程中反应的实质,分别取50mL30%的双氧水溶液进行了如下对照实验:
(3)实验①中Cu与 发生微弱的反应,蓝色固体的成分为
发生微弱的反应,蓝色固体的成分为___________ 。
(4)经检测实验②中溶液变为深蓝色主要是因为生成了 ,则由铜生成该离子的离子方程式为
,则由铜生成该离子的离子方程式为___________ 。
(5)已知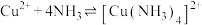 的平衡常数
的平衡常数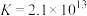 ,
,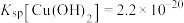 ,则反应
,则反应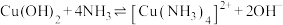 的平衡常数的数值为
的平衡常数的数值为___________ 。
(6)实验③中加入 的作用是
的作用是___________ 。
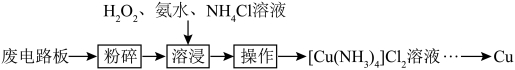
(1)铜在周期表中的位置
(2)将废电路板“粉碎”的目的是
某化学兴趣小组为探究“溶浸”过程中反应的实质,分别取50mL30%的双氧水溶液进行了如下对照实验:
| 序号 | 操作 | 现象描述 |
| ① | 加入一片光亮的铜片 | 开始无明显现象,10小时后,取出铜片晾干,表面附着一层蓝色固体 |
| ② | 加入一片光亮的铜片,并滴加少量氨水 | 立即产生大量的气泡,气体可以使带火星的木条复燃,溶液颜色变为深蓝色,取出铜片晾干,表面附着一层蓝色固体 |
| ③ | 加入一片光亮的铜片,并滴加少量氨水,同时加入少量 固体 固体 | 立即产生大量的气泡,溶液颜色变为深蓝色,取出铜片晾干,依然保持光亮 |
(3)实验①中Cu与
 发生微弱的反应,蓝色固体的成分为
发生微弱的反应,蓝色固体的成分为(4)经检测实验②中溶液变为深蓝色主要是因为生成了
 ,则由铜生成该离子的离子方程式为
,则由铜生成该离子的离子方程式为(5)已知
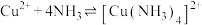 的平衡常数
的平衡常数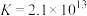 ,
,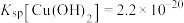 ,则反应
,则反应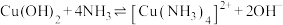 的平衡常数的数值为
的平衡常数的数值为(6)实验③中加入
 的作用是
的作用是
您最近一年使用:0次
名校
解题方法
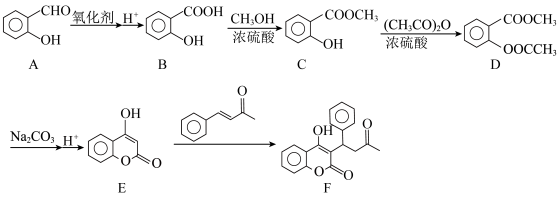
7 . 血栓栓塞类疾病漏诊、误诊、致残率高,是危害患者健康的重要疾病之一、华法林(物质F)可用于预防血栓栓塞类疾病,某种合成华法林的路线如图所示,请回答相关问题:________ ,物质E中的含氧官能团名称是________ 。
(2)A→B的氧化剂可以是________ (填序号)。
a.银氨溶液 b.氧气 c.新制 悬浊液 d.酸性
悬浊液 d.酸性 溶液
溶液
(3)C→D的化学方程式为________ 。
(4)E→F反应类型为________ 。
(5)物质C的同分异构体中符合下列条件的有________ 种。
①苯环上有三个取代基
②能够与 溶液反应显紫色
溶液反应显紫色
③能与碳酸氢钠溶液反应放出无色气体
(6)阿司匹林因被称为“销量最好的止痛药”被列入吉尼斯世界记录,其结构示意图为:_____ (所用试剂均从上述流程中选取)。
(2)A→B的氧化剂可以是
a.银氨溶液 b.氧气 c.新制
 悬浊液 d.酸性
悬浊液 d.酸性 溶液
溶液(3)C→D的化学方程式为
(4)E→F反应类型为
(5)物质C的同分异构体中符合下列条件的有
①苯环上有三个取代基
②能够与
 溶液反应显紫色
溶液反应显紫色③能与碳酸氢钠溶液反应放出无色气体
(6)阿司匹林因被称为“销量最好的止痛药”被列入吉尼斯世界记录,其结构示意图为:

您最近一年使用:0次
名校
8 . 钛(Ti)、铬(Cr)、锰(Mn)、钴(Co)、镉(Cd)等过渡金属及其化合物在生产生活中应用广泛,回答下列问题。
(1)基态Cr原子的价层电子轨道表示式为___________ 。
(2)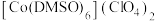 是一种紫色晶体,其中DMSO为二甲基亚砜,化学式为
是一种紫色晶体,其中DMSO为二甲基亚砜,化学式为 。
。 中Cl原子的杂化轨道类型是
中Cl原子的杂化轨道类型是___________ , 中键角<C-S-O
中键角<C-S-O___________  中键角<C-C-O(填“大于”“小于”或“等于”)。
中键角<C-C-O(填“大于”“小于”或“等于”)。
(3) 与
与 等配体可形成配离子。
等配体可形成配离子。 中2个
中2个 被2个
被2个 替代只得到1种结构,则
替代只得到1种结构,则 的空间构型是
的空间构型是___________ 。
(4)钛与卤素形成的化合物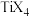 熔点如下表:
熔点如下表:
它们熔点差异的原因___________ 。
(5)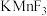 晶体有钙钛矿型的立方结构,晶胞结构如图1所示。在
晶体有钙钛矿型的立方结构,晶胞结构如图1所示。在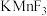 晶胞结构的另一种表示中,Mn处于各顶角位置,在该晶胞结构中,沿晶胞对角面取得的截图如图2所示。F在晶胞中的位置对应的序号为
晶胞结构的另一种表示中,Mn处于各顶角位置,在该晶胞结构中,沿晶胞对角面取得的截图如图2所示。F在晶胞中的位置对应的序号为___________ (填阿拉伯数字序号)。 占据
占据 形成的
形成的___________ (填“四面体空隙”或“八面体空隙”)。 为阿伏加德罗常数的值,钴蓝晶体的密度为
为阿伏加德罗常数的值,钴蓝晶体的密度为___________  (列计算式)。
(列计算式)。
(1)基态Cr原子的价层电子轨道表示式为
(2)
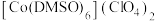 是一种紫色晶体,其中DMSO为二甲基亚砜,化学式为
是一种紫色晶体,其中DMSO为二甲基亚砜,化学式为 。
。 中Cl原子的杂化轨道类型是
中Cl原子的杂化轨道类型是 中键角<C-S-O
中键角<C-S-O 中键角<C-C-O(填“大于”“小于”或“等于”)。
中键角<C-C-O(填“大于”“小于”或“等于”)。(3)
 与
与 等配体可形成配离子。
等配体可形成配离子。 中2个
中2个 被2个
被2个 替代只得到1种结构,则
替代只得到1种结构,则 的空间构型是
的空间构型是(4)钛与卤素形成的化合物
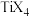 熔点如下表:
熔点如下表: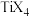 |  |  |  |  |
| 熔点℃ | 377 |  | 38.3 | 153 |
(5)
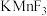 晶体有钙钛矿型的立方结构,晶胞结构如图1所示。在
晶体有钙钛矿型的立方结构,晶胞结构如图1所示。在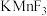 晶胞结构的另一种表示中,Mn处于各顶角位置,在该晶胞结构中,沿晶胞对角面取得的截图如图2所示。F在晶胞中的位置对应的序号为
晶胞结构的另一种表示中,Mn处于各顶角位置,在该晶胞结构中,沿晶胞对角面取得的截图如图2所示。F在晶胞中的位置对应的序号为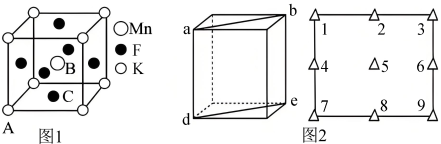
 占据
占据 形成的
形成的 为阿伏加德罗常数的值,钴蓝晶体的密度为
为阿伏加德罗常数的值,钴蓝晶体的密度为 (列计算式)。
(列计算式)。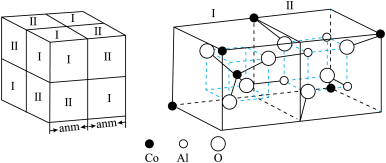
您最近一年使用:0次
名校
9 . A、B、C、D、E为短周期元素且它们的原子序数依次增大,A原子的核外电子总数与其周期数相同:D原子的L能层中,成对电子与未成对电子占据的轨道数相同,并且无空轨道;B原子的L能层中未成对电子数与D原子的相同,但有空轨道:D与E同族。回答下列问题。
(1)A与上述其他元素形成的二元共价化合物中,有一种化合物分子呈三角锥形,该分子的化学式为___________ ,其中心原子的杂化方式为___________ ,A分别与B、C、D形成的共价化合物中既含有极性共价键,又含有非极性共价键的化合物有___________ (填化学式,任意写出两种)。
(2)这些元素形成的含氧酸根离子中,其中心原子的价层电子对数为3的酸根离子是___________ (填化学式,下同);酸根离子呈三角锥形结构的是___________ 。
(3) 分子的空间结构为
分子的空间结构为___________ ;根据电子云重叠方式的不同,该分子中共价键的类型为___________ 。
(4)B的一种氢化物的相对分子质量是26,其分子中 键和
键和 键的数目之比为
键的数目之比为___________ 。
(1)A与上述其他元素形成的二元共价化合物中,有一种化合物分子呈三角锥形,该分子的化学式为
(2)这些元素形成的含氧酸根离子中,其中心原子的价层电子对数为3的酸根离子是
(3)
 分子的空间结构为
分子的空间结构为(4)B的一种氢化物的相对分子质量是26,其分子中
 键和
键和 键的数目之比为
键的数目之比为
您最近一年使用:0次
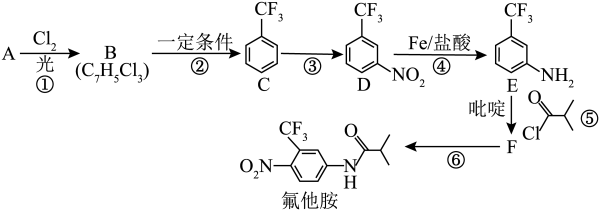
10 . I.氟他胺是一种抗肿瘤药,在实验室由芳香烃A制备氟他胺的合成路线如下所示:____________________ 。
(2)反应④的反应类型为____________________ 。
(3)请写出反应⑤的化学方程式____________________ 。
(4)吡啶是一种有机碱,请推测其在反应⑤中的作用____________________ 。
Ⅱ.取有机物A4.4g,完全燃烧后生成3.6gH2O和4.48LCO2(标准状况)。已知相同状况下,A蒸气的密度是氢气的44倍,其红外光谱图如下:__________ 。
(6)若A的核磁共振氢谱图有3组信号峰且A能与氢气加成,请写出A的结构简式____________________ 。
(2)反应④的反应类型为
(3)请写出反应⑤的化学方程式
(4)吡啶是一种有机碱,请推测其在反应⑤中的作用
Ⅱ.取有机物A4.4g,完全燃烧后生成3.6gH2O和4.48LCO2(标准状况)。已知相同状况下,A蒸气的密度是氢气的44倍,其红外光谱图如下:

(6)若A的核磁共振氢谱图有3组信号峰且A能与氢气加成,请写出A的结构简式
您最近一年使用:0次



