1 . 化学与生活息息相关,下列说法错误的是
| A.生活用品中加入银离子可有效防护细菌侵入 |
| B.铁粉可用作食品包装袋中的脱氧剂 |
| C.航天员手臂“延长器”中的碳纤维是无机非金属材料 |
| D.从石墨中剥离出的石墨烯薄片能导电,是一种电解质 |
您最近一年使用:0次
解题方法
2 . 丙烯是一种重要的化工原料,工业上丙烷制丙烯的相关反应如下:
ⅰ.
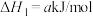
ⅱ.

ⅲ.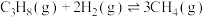
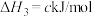
回答下列问题:
Ⅰ.单独投料(副反应抑制法)。
(1)反应: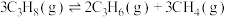

_________  。
。
(2) 时,单独加入
时,单独加入 至
至 后达到平衡,体系中部分组分(仅考虑表内转化)的体积分数
后达到平衡,体系中部分组分(仅考虑表内转化)的体积分数 见下表。
见下表。
①若只考虑体系中反应ⅱ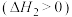 ,以下操作有利于减小
,以下操作有利于减小 平衡转化率的是
平衡转化率的是___________ (填字母)。
A.通入少量 B.使用高选择性催化剂 C.降温 D.减压
B.使用高选择性催化剂 C.降温 D.减压
② 内
内 消耗的平均速率:反应ⅰ
消耗的平均速率:反应ⅰ_________ 反应ⅱ(填“<”、“>”或“=”)。
(3)一定温度下,向 恒容密闭容器中通入
恒容密闭容器中通入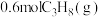 ,压强为
,压强为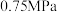 ,若只考虑反应ⅰ、ⅱ,反应后测得各组分的平衡压强(即组分的物质的量分数
,若只考虑反应ⅰ、ⅱ,反应后测得各组分的平衡压强(即组分的物质的量分数 总压)为
总压)为 、
、 ,则该温度下,用物质的量浓度表示反应Ⅰ的平衡常数
,则该温度下,用物质的量浓度表示反应Ⅰ的平衡常数
___________ 。
Ⅱ.共进料投料(耦合反应法)。
工业上也常采用 与
与 共进料投料,通过发生耦合反应制丙烯,反应如下:
共进料投料,通过发生耦合反应制丙烯,反应如下:
(4) 为用压强表示的反应平衡常数,一定温度下:
为用压强表示的反应平衡常数,一定温度下:
ⅰ.

ⅳ.
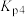
则体系中反应

___________ (用含 、
、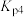 的式子表示)。
的式子表示)。
(5)实际工艺生产中按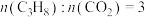 进料,平衡体系中部分组分的体积分数与温度的关系如图所示,综合反应分析:
进料,平衡体系中部分组分的体积分数与温度的关系如图所示,综合反应分析:________ (填“吸热”或“放热”)反应,在________ (填“高温”或“低温”)下进行自发反应。
②生产中温度须不低于 ,原因是
,原因是___________ 。
ⅰ.

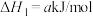
ⅱ.


ⅲ.
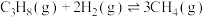
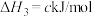
回答下列问题:
Ⅰ.单独投料(副反应抑制法)。
(1)反应:
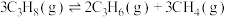

 。
。(2)
 时,单独加入
时,单独加入 至
至 后达到平衡,体系中部分组分(仅考虑表内转化)的体积分数
后达到平衡,体系中部分组分(仅考虑表内转化)的体积分数 见下表。
见下表。| 物质 |  |  |  |  |
体积分数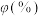 | 18 | 20 | 47 | 0 |
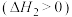 ,以下操作有利于减小
,以下操作有利于减小 平衡转化率的是
平衡转化率的是A.通入少量
 B.使用高选择性催化剂 C.降温 D.减压
B.使用高选择性催化剂 C.降温 D.减压②
 内
内 消耗的平均速率:反应ⅰ
消耗的平均速率:反应ⅰ(3)一定温度下,向
 恒容密闭容器中通入
恒容密闭容器中通入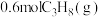 ,压强为
,压强为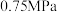 ,若只考虑反应ⅰ、ⅱ,反应后测得各组分的平衡压强(即组分的物质的量分数
,若只考虑反应ⅰ、ⅱ,反应后测得各组分的平衡压强(即组分的物质的量分数 总压)为
总压)为 、
、 ,则该温度下,用物质的量浓度表示反应Ⅰ的平衡常数
,则该温度下,用物质的量浓度表示反应Ⅰ的平衡常数
Ⅱ.共进料投料(耦合反应法)。
工业上也常采用
 与
与 共进料投料,通过发生耦合反应制丙烯,反应如下:
共进料投料,通过发生耦合反应制丙烯,反应如下:
(4)
 为用压强表示的反应平衡常数,一定温度下:
为用压强表示的反应平衡常数,一定温度下:ⅰ.


ⅳ.

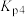
则体系中反应


 、
、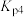 的式子表示)。
的式子表示)。(5)实际工艺生产中按
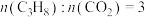 进料,平衡体系中部分组分的体积分数与温度的关系如图所示,综合反应分析:
进料,平衡体系中部分组分的体积分数与温度的关系如图所示,综合反应分析: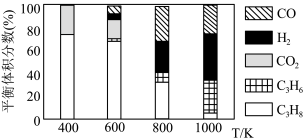
②生产中温度须不低于
 ,原因是
,原因是
您最近一年使用:0次
3 . 硅元素广泛应用于半导体、光伏、塑料工业。回答下列问题:
(1)同周期元素中,成对电子数比硅多的元素有___________ 种。
(2)晶体硅和碳化硅的熔点相比,较高的是___________ (填化学式),原因是___________ 。
(3)由于硅的价层有 轨道可以利用,而碳没有,因此化合物的结构具有较大差异:化合物
轨道可以利用,而碳没有,因此化合物的结构具有较大差异:化合物 (平面形)和
(平面形)和 (三角锥形)中,更易形成配合物的是
(三角锥形)中,更易形成配合物的是___________ (填化学式)。 中元素的电负性由大到小的顺序是
中元素的电负性由大到小的顺序是___________ 。下列划线原子与 中
中 原子杂化类型相同的是
原子杂化类型相同的是___________ (填字母)。
A.COCl2 B.NH3·BH3 C.CH3NH2
(4)一种钛硅碳新型材料可用作高铁车体与供电网的连接材料。该材料的晶胞属于六方晶系(x、y方向的夹角为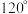 ,z方向垂直于x、y方向,底面棱长均为anm,侧面棱长为cnm),其晶胞结构如图甲所示,晶胞中碳原子的投影位置如图乙所示。
,z方向垂直于x、y方向,底面棱长均为anm,侧面棱长为cnm),其晶胞结构如图甲所示,晶胞中碳原子的投影位置如图乙所示。___________ ,已知该新型材料的摩尔质量为Mg/mol,阿伏加德罗常数的值用NA表示,则其密度为___________ g·cm-3(用含a、c、M、NA的代数式表示)。
(1)同周期元素中,成对电子数比硅多的元素有
(2)晶体硅和碳化硅的熔点相比,较高的是
(3)由于硅的价层有
 轨道可以利用,而碳没有,因此化合物的结构具有较大差异:化合物
轨道可以利用,而碳没有,因此化合物的结构具有较大差异:化合物 (平面形)和
(平面形)和 (三角锥形)中,更易形成配合物的是
(三角锥形)中,更易形成配合物的是 中元素的电负性由大到小的顺序是
中元素的电负性由大到小的顺序是 中
中 原子杂化类型相同的是
原子杂化类型相同的是A.COCl2 B.NH3·BH3 C.CH3NH2
(4)一种钛硅碳新型材料可用作高铁车体与供电网的连接材料。该材料的晶胞属于六方晶系(x、y方向的夹角为
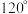 ,z方向垂直于x、y方向,底面棱长均为anm,侧面棱长为cnm),其晶胞结构如图甲所示,晶胞中碳原子的投影位置如图乙所示。
,z方向垂直于x、y方向,底面棱长均为anm,侧面棱长为cnm),其晶胞结构如图甲所示,晶胞中碳原子的投影位置如图乙所示。
您最近一年使用:0次
4 . 利用木质纤维素为起始原料结合(生产聚碳酸对二甲苯酯可以实现碳减排,缓解日益紧张的能源危机,路线如下:___________ 。
(2)Ⅰ分子中,手性碳(与四个各不相同的原子或基团相连的碳原子)的个数为___________ 。
(3)1mol化合物III与1mol乙烯反应得到1molIV,该反应原子利用率为100%,化合物IV的结构简式为___________ ,该反应的反应类型为___________ 。
(4)V分子的核磁共振氢谱的峰面积之比为___________ 。
(5)请写出VII生成VIII的化学反应方程式___________ 。
(6)化合物VII的芳香族同分异构体中符合下列条件的有___________ 种(不含立体异构)。
①最多能与相同物质的量的Na2CO3反应;②能与2倍物质的量的Na反应放出H2。
写出含有等效氢种类最少的同分异构体的结构简式___________ 。
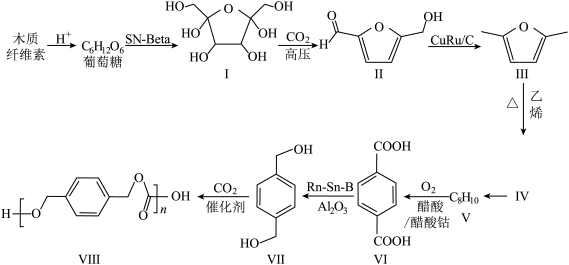
已知: 。回答下列问题:
。回答下列问题:
(2)Ⅰ分子中,手性碳(与四个各不相同的原子或基团相连的碳原子)的个数为
(3)1mol化合物III与1mol乙烯反应得到1molIV,该反应原子利用率为100%,化合物IV的结构简式为
(4)V分子的核磁共振氢谱的峰面积之比为
(5)请写出VII生成VIII的化学反应方程式
(6)化合物VII的芳香族同分异构体中符合下列条件的有
①最多能与相同物质的量的Na2CO3反应;②能与2倍物质的量的Na反应放出H2。
写出含有等效氢种类最少的同分异构体的结构简式
您最近一年使用:0次
解题方法
5 . X、Y、Z、W、M为原子序数依次增大的短周期主族元素。由这5种元素组成的某化合物是电池工业中的重要原料,该化合物的结构式如图所示。下列说法正确的是
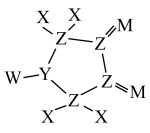
| A.原子半径:Y<Z<W |
| B.最高价含氧酸的酸性:Z>M |
| C.该化合物中除X外,其余原子均满足8电子稳定结构 |
| D.单质的熔点:W<M |
您最近一年使用:0次
6 . NA是阿伏加德罗常数的值,下列说法正确的是
| A.标准状况下,22.4L氩气含有的质子数为18NA |
| B.常温常压下,17gNH3中含有的非极性共价键数为3NA |
| C.2.4gMg在空气中燃烧生成MgO和Mg3N2,转移电子数目为0.1NA |
| D.1.0molCH4与Cl2在光照下反应生成的CH3Cl分子数为NA |
您最近一年使用:0次
7 . 某废水处理过程中始终保持 饱和,即
饱和,即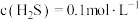 ,通过调节
,通过调节 使
使 和
和 形成硫化物而分离,体系中
形成硫化物而分离,体系中 与
与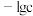 关系如图所示,c为
关系如图所示,c为 、
、 、
、 和
和 的浓度,单位为
的浓度,单位为 。已知
。已知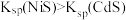 ,下列说法正确的是
,下列说法正确的是
 饱和,即
饱和,即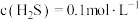 ,通过调节
,通过调节 使
使 和
和 形成硫化物而分离,体系中
形成硫化物而分离,体系中 与
与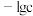 关系如图所示,c为
关系如图所示,c为 、
、 、
、 和
和 的浓度,单位为
的浓度,单位为 。已知
。已知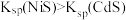 ,下列说法正确的是
,下列说法正确的是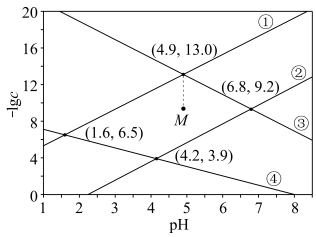
A.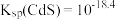 |
B.M点条件下能生成 沉淀,不能生成 沉淀,不能生成 沉淀 沉淀 |
C.③为 与 与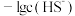 的关系曲线 的关系曲线 |
D.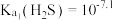 |
您最近一年使用:0次
解题方法
8 . 金属元素及其化合物在生活生产中应用十分广泛。
(1)磷酸亚铁锂( )和锰酸锂(
)和锰酸锂( )均可用作锂离子电池正极材料。在元素周期表中,与Li化学性质最相似的邻族元素是
)均可用作锂离子电池正极材料。在元素周期表中,与Li化学性质最相似的邻族元素是______ (填元素符号),基态Fe原子的价电子排布式为______ 。
(2)原子核外电子有两种相反的自旋状态,分别用 和
和 表示,称为电子的自旋磁量子数。基态Mn原子的价电子自旋磁量子数的代数和为
表示,称为电子的自旋磁量子数。基态Mn原子的价电子自旋磁量子数的代数和为_______ 。
(3)Mn、Fe均为第四周期过渡金属元素,两元素的部分电离能数据如表:
锰元素位于第_______ 周期_______ 族_______ 区;比较两元素的 、
、 可知,气态
可知,气态 再失去1个电子比气态
再失去1个电子比气态 再失去1个电子难,原因是
再失去1个电子难,原因是_______ 。
(4)铍由于重量轻、弹性模数高和热稳定性好,已成为引人注目的飞机和导弹结构材料。铍与相邻主族的铝元素性质相似。下列有关铍和铝的叙述正确的是_______(填字母)。
(5)写出氧化铍和NaOH溶液反应生成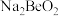 的离子方程式:
的离子方程式:_______ 。
(6)下列事实能说明氯与氧两元素非金属性相对强弱的有_______(填字母)。
(7)下列分子或离子:① 、②
、② 、③
、③ 、④
、④ 、⑤
、⑤ 中,键角由大到小的排列顺序是
中,键角由大到小的排列顺序是_______ (用序号表示)。
(1)磷酸亚铁锂(
 )和锰酸锂(
)和锰酸锂( )均可用作锂离子电池正极材料。在元素周期表中,与Li化学性质最相似的邻族元素是
)均可用作锂离子电池正极材料。在元素周期表中,与Li化学性质最相似的邻族元素是(2)原子核外电子有两种相反的自旋状态,分别用
 和
和 表示,称为电子的自旋磁量子数。基态Mn原子的价电子自旋磁量子数的代数和为
表示,称为电子的自旋磁量子数。基态Mn原子的价电子自旋磁量子数的代数和为(3)Mn、Fe均为第四周期过渡金属元素,两元素的部分电离能数据如表:
| 元素 | Mn | Fe | |
电离能 |  | 717 | 759 |
 | 1509 | 1561 | |
 | 3248 | 2957 | |
 、
、 可知,气态
可知,气态 再失去1个电子比气态
再失去1个电子比气态 再失去1个电子难,原因是
再失去1个电子难,原因是(4)铍由于重量轻、弹性模数高和热稳定性好,已成为引人注目的飞机和导弹结构材料。铍与相邻主族的铝元素性质相似。下列有关铍和铝的叙述正确的是_______(填字母)。
| A.都属于轻金属 | B.失电子的能力都比镁弱 |
| C.原子核外电子云形状都是2种 | D.氯化物的水溶液pH均小于7 |
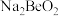 的离子方程式:
的离子方程式:(6)下列事实能说明氯与氧两元素非金属性相对强弱的有_______(填字母)。
| A.Cl原子最外层电子数比O多 | B.酸性: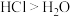 |
C. 中氯元素为+4价,氧元素为-2价 中氯元素为+4价,氧元素为-2价 | D.沸点: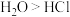 |
 、②
、② 、③
、③ 、④
、④ 、⑤
、⑤ 中,键角由大到小的排列顺序是
中,键角由大到小的排列顺序是
您最近一年使用:0次
解题方法
9 . 下列说法中不正确的是
A. 分子中的σ键和π键的比为2∶1 分子中的σ键和π键的比为2∶1 |
B. 、 、 、 、 的空间结构都是三角锥 的空间结构都是三角锥 |
C. 、 、 都是由极性键构成的非极性分子 都是由极性键构成的非极性分子 |
D. 、 、 、 、 的中心原子都是 的中心原子都是 杂化 杂化 |
您最近一年使用:0次
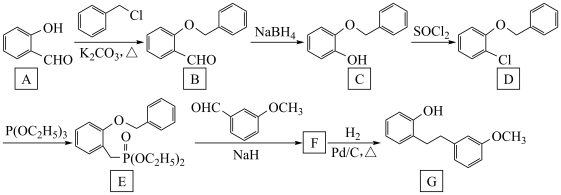
10 . 盐酸沙格雷酯片为抗血小板凝集药,能够抑制血小板聚集、抑制血管收缩,从而预防血栓的形成。化合物G是合成药物盐酸沙格雷酯的重要中间体,其合成路线如下:
① 的分子式为
的分子式为 。
。
(1)A的化学名称为_______ , 中所含官能团的名称是
中所含官能团的名称是_______ 。
(2) 的反应类型为
的反应类型为_______ , 的结构简式为
的结构简式为_______ 。
(3)B与银氨溶液反应的化学方程式为_______ 。
(4)分析整个合成路线,在合成化合物G路线中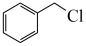 的作用为
的作用为_______ 。
(5) 是
是 的同分异构体,同时满足下列条件的
的同分异构体,同时满足下列条件的 有
有_______ 种(不考虑立体异构)。
①1 M可以与2
M可以与2 Na反应;
Na反应;
②每一个苯环上均有两个侧链; 的结构简式为
的结构简式为_______ 。
(6)参照上述合成路线,设计以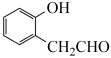 和
和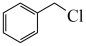 为原料制备
为原料制备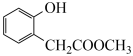 的合成路线
的合成路线_______ (其他试剂任选)。
①
 的分子式为
的分子式为 。
。②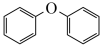
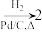
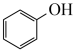 。
。
(1)A的化学名称为
 中所含官能团的名称是
中所含官能团的名称是(2)
 的反应类型为
的反应类型为 的结构简式为
的结构简式为(3)B与银氨溶液反应的化学方程式为
(4)分析整个合成路线,在合成化合物G路线中
 的作用为
的作用为(5)
 是
是 的同分异构体,同时满足下列条件的
的同分异构体,同时满足下列条件的 有
有①1
 M可以与2
M可以与2 Na反应;
Na反应;②每一个苯环上均有两个侧链;
③不存在甲基和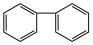 。
。
 的结构简式为
的结构简式为(6)参照上述合成路线,设计以
 和
和 为原料制备
为原料制备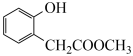 的合成路线
的合成路线
您最近一年使用:0次



