1 . 实验题
(一)实验室中有一瓶含有一定量杂质的烧碱样品,某学生用中和滴定法测定烧碱的纯度,若烧碱中所含杂质与酸不反应,请根据实验回答:
(1)将准确称取的5g烧碱样品配成100 mL待测液,需要的主要仪器除量筒、烧杯、玻璃棒、托盘天平外,还必须用到的玻璃仪器有:____________ 、_____________ 。
(2)取10.00 mL待测液,选择右图中_________ (填A或B)来移取。

(3)用0.5000mol/L标准盐酸滴定待测烧碱溶液,以酚酞为指示剂。滴定时左手旋转滴定管玻璃活塞,右手不停地摇动锥形瓶,两眼注视___________ ,直到滴定终点。滴定达到终点的标志是:_________ 。
(4)根据下列数据,烧碱的纯度为:_______________________ (纯度=纯物质的质量/样品的质量×100%)
(二)氧化还原滴定实验与酸碱中和滴定类似(用已知浓度的氧化剂溶液滴定未知浓度的还原剂溶液或反之)。测血钙的含量时,进行如下实验:
①可将2mL血液用蒸馏水稀释后,向其中加入足量草酸铵(NH4)2C2O4晶体,反应生成 CaC2O4沉淀,将沉淀用稀硫酸处理得H2C2O4溶液。
②将①得到的H2C2O4溶液,再用酸性KMnO4溶液滴定,氧化产物为CO2,还原产物为Mn2+。
③终点时用去20mL l.0×l0﹣4 mol/L的KMnO4溶液。
(1)写出用KMnO4滴定H2C2O4的离子方程式_____________________ 。
(2)滴定时,将KMnO4溶液装在________ (填“酸式”或“碱式”)滴定管中。
(3)计算:血液中含钙离子的浓度为_____ mol·L-1。
(一)实验室中有一瓶含有一定量杂质的烧碱样品,某学生用中和滴定法测定烧碱的纯度,若烧碱中所含杂质与酸不反应,请根据实验回答:
(1)将准确称取的5g烧碱样品配成100 mL待测液,需要的主要仪器除量筒、烧杯、玻璃棒、托盘天平外,还必须用到的玻璃仪器有:
(2)取10.00 mL待测液,选择右图中

(3)用0.5000mol/L标准盐酸滴定待测烧碱溶液,以酚酞为指示剂。滴定时左手旋转滴定管玻璃活塞,右手不停地摇动锥形瓶,两眼注视
(4)根据下列数据,烧碱的纯度为:
| 滴定次数 | 待测液体积(mL) | 标准盐酸体积(mL) | |
| 滴定前读数 | 滴定后读数 | ||
| 第一次 | 10.00 | 0.50 | 20.40 |
| 第二次 | 10.00 | 4.00 | 24.10 |
①可将2mL血液用蒸馏水稀释后,向其中加入足量草酸铵(NH4)2C2O4晶体,反应生成 CaC2O4沉淀,将沉淀用稀硫酸处理得H2C2O4溶液。
②将①得到的H2C2O4溶液,再用酸性KMnO4溶液滴定,氧化产物为CO2,还原产物为Mn2+。
③终点时用去20mL l.0×l0﹣4 mol/L的KMnO4溶液。
(1)写出用KMnO4滴定H2C2O4的离子方程式
(2)滴定时,将KMnO4溶液装在
(3)计算:血液中含钙离子的浓度为
您最近一年使用:0次
真题
名校
2 . K3[Fe(C2O4)3]·3H2O(三草酸合铁酸钾)为亮绿色晶体,可用于晒制蓝图。回答下列问题:
(1)晒制蓝图时,用K3[Fe(C2O4)3]·3H2O作感光剂,以K3[Fe(CN)6]溶液为显色剂。其光解反应的化学方程式为:2K3[Fe(C2O4)3]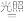 2FeC2O4+3K2C2O4+2CO2↑;显色反应的化学方程式为
2FeC2O4+3K2C2O4+2CO2↑;显色反应的化学方程式为______________ 。
(2)某小组为探究三草酸合铁酸钾的热分解产物,按下图所示装置进行实验。

①通入氮气的目的是________________________________________ 。
②实验中观察到装置B、F中澄清石灰水均变浑浊,装置E中固体变为红色,由此判断热分解产物中一定含有___________ 、___________ 。
③为防止倒吸,停止实验时应进行的操作是_____________________________ 。
④样品完全分解后,装置A中的残留物含有FeO和Fe2O3,检验Fe2O3存在的方法是:________________ 。
(3)测定三草酸合铁酸钾中铁的含量。
①称量m g样品于锥形瓶中,溶解后加稀H2SO4酸化,用c mol·L-1 KMnO4溶液滴定至终点。滴定终点的现象是___________________________ 。
②向上述溶液中加入过量锌粉至反应完全后,过滤、洗涤,将滤液及洗涤液全部收集到锥形瓶中。加稀H2SO4酸化,用c mol·L-1 KMnO4溶液滴定至终点,消耗KMnO4溶液V mL。该晶体中铁的质量分数的表达式为________________________________ 。
(1)晒制蓝图时,用K3[Fe(C2O4)3]·3H2O作感光剂,以K3[Fe(CN)6]溶液为显色剂。其光解反应的化学方程式为:2K3[Fe(C2O4)3]
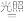 2FeC2O4+3K2C2O4+2CO2↑;显色反应的化学方程式为
2FeC2O4+3K2C2O4+2CO2↑;显色反应的化学方程式为(2)某小组为探究三草酸合铁酸钾的热分解产物,按下图所示装置进行实验。

①通入氮气的目的是
②实验中观察到装置B、F中澄清石灰水均变浑浊,装置E中固体变为红色,由此判断热分解产物中一定含有
③为防止倒吸,停止实验时应进行的操作是
④样品完全分解后,装置A中的残留物含有FeO和Fe2O3,检验Fe2O3存在的方法是:
(3)测定三草酸合铁酸钾中铁的含量。
①称量m g样品于锥形瓶中,溶解后加稀H2SO4酸化,用c mol·L-1 KMnO4溶液滴定至终点。滴定终点的现象是
②向上述溶液中加入过量锌粉至反应完全后,过滤、洗涤,将滤液及洗涤液全部收集到锥形瓶中。加稀H2SO4酸化,用c mol·L-1 KMnO4溶液滴定至终点,消耗KMnO4溶液V mL。该晶体中铁的质量分数的表达式为
您最近一年使用:0次
2018-06-09更新
|
13246次组卷
|
19卷引用:云南省马关县二中2020届高三上学期开学考试化学试题
云南省马关县二中2020届高三上学期开学考试化学试题云南省玉溪元江民中2020届高三开学考试化学试题云南省富宁县民族中学2020届高三上学期开学考试化学试题云南省大理白族自治州漾濞二中2019—2020学年9月份高三化学考试试题云南省富宁县第一中学2020届高三第一学期开学考试化学试题2018年全国普通高等学校招生统一考试化学(新课标II卷)(已下线)2018年高考题及模拟题汇编 专题16 化学实验综合题四川省攀枝花市第十二中学2019届高三上学期10月月考化学试题广东省惠州市第一中学2019届高三上学期理科综合测试(二)化学试题四川省自贡市田家炳中学2020届高三上学期期中考试化学试题(已下线)专题10.3 化学实验方案的设计与评价 (讲)-《2020年高考一轮复习讲练测》黑龙江省大庆市第四中学2020届高三下学期4月月考理综化学试题山东省潍坊市诸城一中2021届高三11月份模拟化学试题(已下线)考点32 化学实验方案设计与评价-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)考点35 化学实验方案的设计与评价-备战2022年高考化学一轮复习考点帮(浙江专用)重庆市开州中学高 2021-2022学年高三上学期10月月考化学试题(已下线)专题17化学实验综合题-五年(2018~2022)高考真题汇编(全国卷)西藏自治区拉萨中学2022届高三第六次月考理综化学试题西藏林芝市第二高级中学2022-2023学年高三上学期第二次月考化学试题
名校
解题方法
3 . 碱式碳酸铜是一种用途广泛的化工原料,实验室以废铜屑为原料制取碱式碳酸铜的步骤如下:
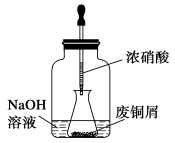
步骤一:废铜屑制硝酸铜
如图,用胶头滴管吸取浓硝酸缓慢加到锥形瓶内的废铜屑中(废铜屑过量),充分反应后过滤,得到硝酸铜溶液。
步骤二:碱式碳酸铜的制备
向大试管中加入碳酸钠溶液和硝酸铜溶液,水浴加热至70 ℃左右,用0.4 mol·L-1的NaOH溶液调节pH至8.5,振荡,静置,过滤,用热水洗涤,烘干,得到碱式碳酸铜产品。
完成下列填空:
(1)写出浓硝酸与铜反应的离子方程式___________________________________________ 。
(2)上图装置中NaOH溶液的作用是_________________________ 。
(3)步骤二中,水浴加热所需仪器有________ 、________ (加热、夹持仪器、石棉网除外),水浴加热的优点是_______________________ 。
(4) 已知:CuCO3、Cu(OH)2受热均易分解,产物中都有CuO生成。碱式碳酸铜可表示为xCuCO3·yCu(OH)2·zH2O(x、y、z取整数),测定碱式碳酸铜组成的方法有多种,现采用氢气还原法,请回答如下问题:(已知M(Cu)=63.5 g·mol-1)。
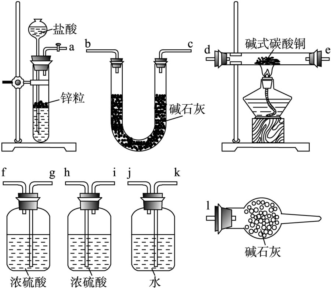
①写出xCuCO3·yCu(OH)2·zH2O与 氢气反应的化学方程式:
氢气反应的化学方程式:__________________ ;
②实验装置用上面所有仪器连接而成,按氢气流方向的连接顺序是(填入仪器接口字母编号):( a )→( )( )→( )( )→( )( )→( )( )→( )( )→( l )_____
③称取23.9 g某碱式碳酸铜样品,充分反应后得到12.7 g残留物,生成4.4 g二氧化碳和7.2 g水。该样品的结晶水质量为______ g,化学式为____________ 。
④某同学以氮气代替氢气,并用上述全部或部分仪器来测定碱式碳酸铜的组成,你认为是否可行?__________ (填“可行”或“不可行”)请说明理由________________________ 。

步骤一:废铜屑制硝酸铜
如图,用胶头滴管吸取浓硝酸缓慢加到锥形瓶内的废铜屑中(废铜屑过量),充分反应后过滤,得到硝酸铜溶液。
步骤二:碱式碳酸铜的制备
向大试管中加入碳酸钠溶液和硝酸铜溶液,水浴加热至70 ℃左右,用0.4 mol·L-1的NaOH溶液调节pH至8.5,振荡,静置,过滤,用热水洗涤,烘干,得到碱式碳酸铜产品。
完成下列填空:
(1)写出浓硝酸与铜反应的离子方程式
(2)上图装置中NaOH溶液的作用是
(3)步骤二中,水浴加热所需仪器有
(4) 已知:CuCO3、Cu(OH)2受热均易分解,产物中都有CuO生成。碱式碳酸铜可表示为xCuCO3·yCu(OH)2·zH2O(x、y、z取整数),测定碱式碳酸铜组成的方法有多种,现采用氢气还原法,请回答如下问题:(已知M(Cu)=63.5 g·mol-1)。

①写出xCuCO3·yCu(OH)2·zH2O与
 氢气反应的化学方程式:
氢气反应的化学方程式:②实验装置用上面所有仪器连接而成,按氢气流方向的连接顺序是(填入仪器接口字母编号):( a )→( )( )→( )( )→( )( )→( )( )→( )( )→( l )
③称取23.9 g某碱式碳酸铜样品,充分反应后得到12.7 g残留物,生成4.4 g二氧化碳和7.2 g水。该样品的结晶水质量为
④某同学以氮气代替氢气,并用上述全部或部分仪器来测定碱式碳酸铜的组成,你认为是否可行?
您最近一年使用:0次
2018-04-11更新
|
169次组卷
|
2卷引用:云南省玉溪第一中学2017-2018学年高一下学期4月月考化学试题
4 . 亚硝酸钠被称为工业盐,在漂白、电镀等方面应用广泛。某小组制备亚硝酸钠的实验装置如图所示(部分夹持装置已略去)。
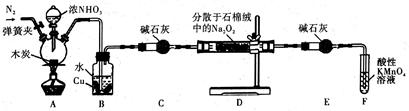
已知:
①2NO+Na2O2=2NaNO2、2NaNO2+O2=2NaNO3
②3NaNO2+3HCl=3NaCl+HNO3+2NO↑+H2O
③酸性条件下,NO或NO2都能与MnO4-反应生成NO3-和Mn2+
回答下列问题:
(1)反应前需先打开弹簧夹,通入氮气排尽装置中的空气,原因是__________________ 。
(2)装置A中反应的化学方程式为_________________ ;装置B中的实验现象为_____________ ,铜片逐渐溶解并有气泡产生。
(3)若省略装置C,则装置D中的固体产物除NaNO2、NaOH外,还有__________ 、___________ (填化学式)。检验产物中含有NaNO2的方法是:取少量样品于试管中,_____________________ ,则说明产物中含有NaNO2。
(4)装置E的作用是___________________________ 。
(5)NaNO2有像食盐一样的咸味,但能引起中毒。已知亚硝酸钠能发生如下反应:2NaNO2+4HI=2NO+I2+2NaI+2H2O。根据上述反应,可以用试剂和生活中常见的物质进行实验,以鉴别亚硝酸钠和食盐。进行实验时,除样品外必须选用的物质有_________ (填标号)。
a.白酒 b.碘化钾、淀粉溶液 c.白醋 d.白糖
(6)充分反应后,该小组设计实验检测产物中NaNO2的含量。称取装置D中固体2.3000g,完全溶解配制成溶液l00mL,取出25.00mL溶液用0.100 mol·L-1酸性KMnO4溶液进行滴定(杂质不与KMnO4反应),三次滴定平均消耗KMnO4溶液30.00mL,则样品中NaNO2的质量分数为_______________ 。(已知:NaNO2的摩尔质量为69g·mol-1)

已知:
①2NO+Na2O2=2NaNO2、2NaNO2+O2=2NaNO3
②3NaNO2+3HCl=3NaCl+HNO3+2NO↑+H2O
③酸性条件下,NO或NO2都能与MnO4-反应生成NO3-和Mn2+
回答下列问题:
(1)反应前需先打开弹簧夹,通入氮气排尽装置中的空气,原因是
(2)装置A中反应的化学方程式为
(3)若省略装置C,则装置D中的固体产物除NaNO2、NaOH外,还有
(4)装置E的作用是
(5)NaNO2有像食盐一样的咸味,但能引起中毒。已知亚硝酸钠能发生如下反应:2NaNO2+4HI=2NO+I2+2NaI+2H2O。根据上述反应,可以用试剂和生活中常见的物质进行实验,以鉴别亚硝酸钠和食盐。进行实验时,除样品外必须选用的物质有
a.白酒 b.碘化钾、淀粉溶液 c.白醋 d.白糖
(6)充分反应后,该小组设计实验检测产物中NaNO2的含量。称取装置D中固体2.3000g,完全溶解配制成溶液l00mL,取出25.00mL溶液用0.100 mol·L-1酸性KMnO4溶液进行滴定(杂质不与KMnO4反应),三次滴定平均消耗KMnO4溶液30.00mL,则样品中NaNO2的质量分数为
您最近一年使用:0次
名校
解题方法
5 . 镁、硼及其化合物在工农业生产中应用广泛。已知:硼、铝同主族;硼砂常指四硼酸钠的十水合物,化学式为Na2B4O7·10H2O。利用硼镁矿(主要成分为Mg2B2O5·H2O)制取金属镁及粗硼的工艺流程图如图所示:
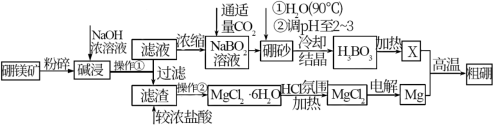
(1)Mg2B2O5·H2O 中B的化合价为______ 价。
(2)操作②的主要步骤是_______________ 和过滤,从而获得MgCl2•6H2O。
(3)MgCl2•6H2O在HCl氛围中加热才能制得无水氯化镁。其原因是____________________ ;若用情性电极电解MgCl2溶液,其阴极反应式为_____________________________ 。
(4)硼砂溶于90℃热水后,常用稀硫酸调pH至2~3制取H3BO3晶体,该反应的离子方程式为______ ;X为硼酸晶体加热完全脱水后的产物,其与Mg反应制取粗硼的化学方程式为_____________ 。
(5)镁-H2O2酸性燃料电池的反应机理为Mg+H2O2+2H+=Mg2++2H2O。常温下,若起始电解质溶液pH=1,则当pH =2时,溶液中Mg2+的浓度为___________ 。
(6)制得的粗硼在一定条件下可反位生成BI3,BI3加热分解即可得到纯净的单质硼。现将mg粗硼制成的BI3充全分解,生成的I2用c mol • L-1Na2S2O3溶液滴定至终点,三次消耗Na2S2O3溶液的体积平均值为 VmL。则该粗硼样品的纯度为___________ 。(提示:I2+2S2O32-=2I-+S4O62-)

(1)Mg2B2O5·H2O 中B的化合价为
(2)操作②的主要步骤是
(3)MgCl2•6H2O在HCl氛围中加热才能制得无水氯化镁。其原因是
(4)硼砂溶于90℃热水后,常用稀硫酸调pH至2~3制取H3BO3晶体,该反应的离子方程式为
(5)镁-H2O2酸性燃料电池的反应机理为Mg+H2O2+2H+=Mg2++2H2O。常温下,若起始电解质溶液pH=1,则当pH =2时,溶液中Mg2+的浓度为
(6)制得的粗硼在一定条件下可反位生成BI3,BI3加热分解即可得到纯净的单质硼。现将mg粗硼制成的BI3充全分解,生成的I2用c mol • L-1Na2S2O3溶液滴定至终点,三次消耗Na2S2O3溶液的体积平均值为 VmL。则该粗硼样品的纯度为
您最近一年使用:0次
6 . 某工厂的电镀污泥中含有铜、铁等金属化合物。为实现资源的回收利用并有效防止环境污染,设计如下工艺流程:
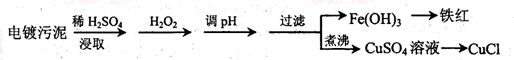
(1)酸浸后加入H2O2的目的是________________ ,调pH的最适宜范围为________________ 。
(2)调pH过程中加入的试剂最好是___________ 。
A. NaOH B. CuO C.NH3·H2O D.HCl
(3)煮沸CuSO4溶液的原因是_________ 。向CuSO4溶液中加入一定量的NaCl、Na2SO3,可以生成白色的CuCl沉淀,写出该反应的化学方程式_________ 。
(4)过滤后的沉淀表面通常附着有一些杂质离子,为得到纯净产物,需要进行洗涤,确定沉淀洗涤干净的操作及现象是_________ 。
(5)称取所制备的CuCl样品0.2500g置于一定量的0.5mol·L-1FeCl3溶液中,待样品完全溶解后,加水20mL,用0.1000 mol·L-1的Ce(SO4)2溶液滴定,到达终点时消耗Ce(SO4)2溶液25.00mL。有关的化学反应为Fe3++CuCl=Fe2++Cu2++Cl-,Ce4++Fe2+=Fe3++Ce3+。计算该CuCl样品的质量分数__________ 。

| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Cu(OH)2 |
| 开始沉淀的pH | 2.3 | 7.6 | 4.4 |
| 完全沉淀的pH | 3.2 | 9.7 | 6.4 |
(1)酸浸后加入H2O2的目的是
(2)调pH过程中加入的试剂最好是
A. NaOH B. CuO C.NH3·H2O D.HCl
(3)煮沸CuSO4溶液的原因是
(4)过滤后的沉淀表面通常附着有一些杂质离子,为得到纯净产物,需要进行洗涤,确定沉淀洗涤干净的操作及现象是
(5)称取所制备的CuCl样品0.2500g置于一定量的0.5mol·L-1FeCl3溶液中,待样品完全溶解后,加水20mL,用0.1000 mol·L-1的Ce(SO4)2溶液滴定,到达终点时消耗Ce(SO4)2溶液25.00mL。有关的化学反应为Fe3++CuCl=Fe2++Cu2++Cl-,Ce4++Fe2+=Fe3++Ce3+。计算该CuCl样品的质量分数
您最近一年使用:0次
2018-01-18更新
|
124次组卷
|
5卷引用:云南省昭通市大关县第一中学2019-2020学年高二上学期期末考试化学试题
7 . 某实验小组的同学为了探究CuSO4溶液与Na2CO3溶液的反应原理并验证产物,进行如下实验。
实验I:将CuSO4溶液与Na2CO3溶液混合,一定温度下充分反应至不产生气泡为止,
过滤、冷水洗涤、低温干燥,得到蓝绿色固体。该小组同学猜想此固体为xCuCO3·yCu(OH)2。
(1)为了验证猜想,先进行定性实验。
(2)为进一步确定蓝绿色固体的组成,使用如下装置再进行定量实验。

实验Ⅲ:称取5.190g样品,充分加热至不再产生气体为止,并使分解产生的气体全部进入装置C和D中。
①装置C中盛放的试剂是________________ ,装置E的作用是____________________ ,反应结束时要通入适量的空气,其作用是____________________________________ 。
②实验结束后,测得装置C增重0.270g,装置D增重1.320g。则该蓝绿色固体的化学式为____________ 。
(3)若x=y=1,写出CuSO4溶液与Na2CO3溶液混合时反应的化学方程式______________ 。
(4)已知20℃时溶解度数据:S[Ca(OH)2] =" 0.16" g,S[Ba(OH)2] =" 3.89" g。有同学据此提出可将装置D中的澄清石灰水换成等体积的饱和Ba(OH)2溶液,其可能的依据之一是_________________________ 。
(5)有同学为了降低实验误差,提出如下建议,其中合理的是______ (填字母序号)。
A.加热装置B前,先通空气一段时间后再称量C、D的初始质量
B.将D换为盛有碱石灰的U形管
C.将C、D颠倒并省去E装置
实验I:将CuSO4溶液与Na2CO3溶液混合,一定温度下充分反应至不产生气泡为止,
过滤、冷水洗涤、低温干燥,得到蓝绿色固体。该小组同学猜想此固体为xCuCO3·yCu(OH)2。
(1)为了验证猜想,先进行定性实验。
| 实验序号 | 实验步骤 | 实验现象 | 结论 |
| 实验Ⅱ | 取适量蓝绿色固体,加入足量稀硫酸 | 固体溶解,生成蓝色溶液, | 蓝绿色固体中含有CO32- |

实验Ⅲ:称取5.190g样品,充分加热至不再产生气体为止,并使分解产生的气体全部进入装置C和D中。
①装置C中盛放的试剂是
②实验结束后,测得装置C增重0.270g,装置D增重1.320g。则该蓝绿色固体的化学式为
(3)若x=y=1,写出CuSO4溶液与Na2CO3溶液混合时反应的化学方程式
(4)已知20℃时溶解度数据:S[Ca(OH)2] =" 0.16" g,S[Ba(OH)2] =" 3.89" g。有同学据此提出可将装置D中的澄清石灰水换成等体积的饱和Ba(OH)2溶液,其可能的依据之一是
(5)有同学为了降低实验误差,提出如下建议,其中合理的是
A.加热装置B前,先通空气一段时间后再称量C、D的初始质量
B.将D换为盛有碱石灰的U形管
C.将C、D颠倒并省去E装置
您最近一年使用:0次



