2014·上海崇明·二模
解题方法
1 . NA表示阿伏加 德罗常数,下列判断正确的是( )
| A.6.8g熔融的KHSO4中含有阳离子数0.05NA |
| B.1mol冰醋酸和lmol乙醇经催化加热反应可生成H2O分子数为NA |
| C.25℃时,pH=13的Ba(OH)2溶液中含有的OH-数为0.1NA |
| D.常温常压下,17g羟基中含有的电子数为9NA |
您最近一年使用:0次
2014·上海·零模
解题方法
2 . 苯分子等芳香烃化合物里的氢原子被硫酸分子里的磺酸基(—SO3H)所取代的反应,称为磺化反应。浓硫酸有时也用SO3代替浓硫酸,其优点是____________________ 、____________________________________ 。(至少写出两点),用浓硫酸吸收SO3可得发烟硫酸(H2SO4·SO3)。某化工厂用1.5m3 98.3%的浓硫酸(密度为1.84g/mL)吸收SO3形成发烟硫酸,再与水混合,可得到95%的硫酸(密度为1.79g/mL)_____________ m3(保留2位小数)。
您最近一年使用:0次
2014·上海奉贤·二模
3 . 硝酸工业尾气中氮氧化物(NO 和NO2)是主要的大气污染物之一,可用氨氧混合气体进行选择性还原处理。其主要反应原理如下:4NO+4NH3+O2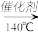 4N2+6H2O 6NO2+8NH3
4N2+6H2O 6NO2+8NH3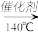 7N2+12H2O,某硝酸厂排放的尾气中氮氧化合物的含量为2490mg/m3(体积已换算成标准状况),其中NO NO2的物质的量比为4:1。设尾气中氮氧化物与氨氧混合气恰好完全反应。
7N2+12H2O,某硝酸厂排放的尾气中氮氧化合物的含量为2490mg/m3(体积已换算成标准状况),其中NO NO2的物质的量比为4:1。设尾气中氮氧化物与氨氧混合气恰好完全反应。
(1)尾气中氮氧化物的平均相对原子量为_____________ ;尾气中NO的含量为_____ mg/m3。
(2)要处理5m3的尾气,需要氨氧混合气的体积为_______ L。
另一种处理氮氧化物的方法是用烧碱进行吸收,产物为NaNO2、NaNO3和H2O。现有含0.5mol氮氧化物的尾气,恰好被一定体积25%NaOH溶液(密度1.28g/cm3)完全吸收。
(3)NaOH溶液的物质的量浓度为_____________ mol/L,体积为_____ mL。
(4)已知反应后溶液含有0.35molNaNO2。若将尾气NO 和NO2的平均组成用NOx表示,则x=______
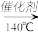 4N2+6H2O 6NO2+8NH3
4N2+6H2O 6NO2+8NH3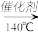 7N2+12H2O,某硝酸厂排放的尾气中氮氧化合物的含量为2490mg/m3(体积已换算成标准状况),其中NO NO2的物质的量比为4:1。设尾气中氮氧化物与氨氧混合气恰好完全反应。
7N2+12H2O,某硝酸厂排放的尾气中氮氧化合物的含量为2490mg/m3(体积已换算成标准状况),其中NO NO2的物质的量比为4:1。设尾气中氮氧化物与氨氧混合气恰好完全反应。(1)尾气中氮氧化物的平均相对原子量为
(2)要处理5m3的尾气,需要氨氧混合气的体积为
另一种处理氮氧化物的方法是用烧碱进行吸收,产物为NaNO2、NaNO3和H2O。现有含0.5mol氮氧化物的尾气,恰好被一定体积25%NaOH溶液(密度1.28g/cm3)完全吸收。
(3)NaOH溶液的物质的量浓度为
(4)已知反应后溶液含有0.35molNaNO2。若将尾气NO 和NO2的平均组成用NOx表示,则x=
您最近一年使用:0次
解题方法
4 . 将Cl2通入100mL NaOH溶液中充分反应,生成0.1mol的NaCl,下列说法正确的是( )
| A.反应后溶液中ClO﹣的个数为0.1NA |
| B.原NaOH浓度为1mol/L |
| C.参加反应的氯气分子为0.1NA |
| D.转移电子为0.2NA |
您最近一年使用:0次
5 . 磷及部分重要化合物的相互转化如图所示。
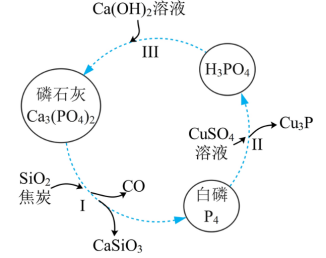
(1)不慎将白磷沾到皮肤上,可用0.2mol/L CuSO4溶液冲洗,根据步骤Ⅱ可判断,1mol CuSO4所能氧化的白磷的物质的量为______ 。
(2)步骤Ⅲ中,反应物的比例不同可获得不同的产物,除Ca3(PO4)2外可能的产物还有______ 。
磷灰石是生产磷肥的原料,它的组成可以看作是Ca3(PO4)2、CaF2、CaSO4、CaCO3、SiO2的混合物,部分元素的分析结果如下(各元素均以氧化物形式表示):
(3)磷灰石中,碳元素的质量分数为______ %(保留两位小数)。
(4)取100g磷灰石粉末,加入足量的浓硫酸,并加热,钙元素全部以CaSO4的形式存在,可以得到CaSO4______ g(保留两位小数)。
(5)取m g 磷灰石粉末,用50.00mL混酸溶液(磷酸为0.5mol/L、硫酸为0.1mol/L)与其反应,结果Ca、S、P元素全部以CaSO4和Ca(H2PO4)2的形式存在,求m的值______ 。

(1)不慎将白磷沾到皮肤上,可用0.2mol/L CuSO4溶液冲洗,根据步骤Ⅱ可判断,1mol CuSO4所能氧化的白磷的物质的量为
(2)步骤Ⅲ中,反应物的比例不同可获得不同的产物,除Ca3(PO4)2外可能的产物还有
磷灰石是生产磷肥的原料,它的组成可以看作是Ca3(PO4)2、CaF2、CaSO4、CaCO3、SiO2的混合物,部分元素的分析结果如下(各元素均以氧化物形式表示):
| 成分 | CaO | P2O5 | SO3 | CO2 |
| 质量分数(%) | 47.30 | 28.40 | 3.50 | 6.10 |
(3)磷灰石中,碳元素的质量分数为
(4)取100g磷灰石粉末,加入足量的浓硫酸,并加热,钙元素全部以CaSO4的形式存在,可以得到CaSO4
(5)取m g 磷灰石粉末,用50.00mL混酸溶液(磷酸为0.5mol/L、硫酸为0.1mol/L)与其反应,结果Ca、S、P元素全部以CaSO4和Ca(H2PO4)2的形式存在,求m的值
您最近一年使用:0次
6 . 现有1950g发烟硫酸(用a SO3•H2O 表示),SO3和H2SO4的质量分数分别为0.2和0.8,加b g水稀释成某浓度的硫酸(用H2SO4•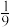 H2O 表示),则以下正确的是(允许最后一位数字不同)( )
H2O 表示),则以下正确的是(允许最后一位数字不同)( )
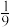 H2O 表示),则以下正确的是(允许最后一位数字不同)( )
H2O 表示),则以下正确的是(允许最后一位数字不同)( )| A.a=1.38 | B.a=1.31 | C.b=174 | D.b=129 |
您最近一年使用:0次
解题方法
7 . 取KClO3和MnO2的混合物16.60g加热至恒重,将反应后的固体加15g水充分溶解,剩余固体6.55g (25℃),再加5 g水充分溶解,仍剩余固体4.80g(25℃)。
(1)若剩余的4.80g固体全是MnO2,则原混合物中KClO3的质量为________________ g(保留2位小数)
(2)若剩余的4.80g固体是MnO2和KCl的混合物,则25℃时KCl的溶解度为_____ ;原混合物中KClO3的质量为________________ g(保留2位小数);所得KCl溶液的密度为1.72g/cm3,则溶液的物质的量浓度为______ mol/L(保留2位小数)。
(3)可用以下反应制备KIO3和K2H3IO6(高碘酸氢二钾):I2+2KClO3=2KIO3+Cl2① KIO3+Cl2+3KOH =K2H3IO6+2KCl ②最终制得的KIO3和K2H3IO6的物质的量之比x,若制得100molK2H3IO6, 共消耗ymolKClO3,试确定y与x的关系式________________ 。
(1)若剩余的4.80g固体全是MnO2,则原混合物中KClO3的质量为
(2)若剩余的4.80g固体是MnO2和KCl的混合物,则25℃时KCl的溶解度为
(3)可用以下反应制备KIO3和K2H3IO6(高碘酸氢二钾):I2+2KClO3=2KIO3+Cl2① KIO3+Cl2+3KOH =K2H3IO6+2KCl ②最终制得的KIO3和K2H3IO6的物质的量之比x,若制得100molK2H3IO6, 共消耗ymolKClO3,试确定y与x的关系式
您最近一年使用:0次
8 . 某稀土元素R的精矿样品中,R的氧化物的质量分数为0.85 10.1g该样品与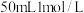 硫酸恰好完全反应
硫酸恰好完全反应 杂质不反应
杂质不反应 ,生成
,生成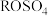 和
和 ,则R的相对原子质量约为
,则R的相对原子质量约为
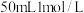 硫酸恰好完全反应
硫酸恰好完全反应 杂质不反应
杂质不反应 ,生成
,生成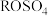 和
和 ,则R的相对原子质量约为
,则R的相对原子质量约为
| A.78 | B.140 | C.156 | D.172 |
您最近一年使用:0次
2019-12-26更新
|
152次组卷
|
3卷引用:【区级联考】上海市奉贤区2019届高三下学期高考二模化学试题
名校
9 . 有3.92 g铁的氧化物,用足量的CO在高温下将其还原,把生成的全部CO2通入到足量的澄清的石灰水中得到7.0 g固体沉淀物,这种铁的氧化物为
| A.Fe3O4 | B.FeO | C.Fe2O3 | D.Fe5O7 |
您最近一年使用:0次
2019-10-27更新
|
244次组卷
|
5卷引用:上海市松江区2017年高考化学二模试卷
上海市松江区2017年高考化学二模试卷上海市松江区2017届高三下学期期中教学质量监控(二模)化学试题上海市进才中学2022-2023学年高一上学期期末考试化学试题(已下线)第14讲 化学反应的计算-【暑假自学课】2023年新高一暑假精品课(苏教版2019)河南省博爱县第一中学2023-2024学年高二上学期9月月考化学试题
10 . KClO3是一种常见的氧化剂,常用于医药工业、印染工业和制造烟火。实验室用KClO3和MnO2混合加热制氧气,现取KClO3和MnO2的混合物16.60g加热至恒重,将反应后的固体加15g水充分溶解,剩余固体6.55g (25℃),再加5 g水充分溶解,仍剩余固体4.80g(25℃)。
(1)若剩余的4.80g固体全是MnO2,则原混合物中KClO3的质量为___ g。
(2)若剩余的4.80g固体是MnO2和KCl的混合物。
①求25℃时KCl的溶解度_____ ;
②求原混合物中KClO3的质量_____ ;
③所得KCl溶液的密度为1.72g/cm3,则溶液的物质的量浓度为多少_____ ?(保留2位小数)
(3)工业常利用3Cl2 + 6KOH KClO3 + 5KCl + 3H2O,制取KClO3(混有KClO)。实验室模拟KClO3制备,在热的KOH溶液中通入一定量氯气充分反应后,测定溶液中n(K+):n(Cl-) = 14:11,将所得溶液低温蒸干,那么在得到的固体中KClO3的质量分数的取值范围为多少
KClO3 + 5KCl + 3H2O,制取KClO3(混有KClO)。实验室模拟KClO3制备,在热的KOH溶液中通入一定量氯气充分反应后,测定溶液中n(K+):n(Cl-) = 14:11,将所得溶液低温蒸干,那么在得到的固体中KClO3的质量分数的取值范围为多少_____ ?(用小数表示,保留3位小数)
(1)若剩余的4.80g固体全是MnO2,则原混合物中KClO3的质量为
(2)若剩余的4.80g固体是MnO2和KCl的混合物。
①求25℃时KCl的溶解度
②求原混合物中KClO3的质量
③所得KCl溶液的密度为1.72g/cm3,则溶液的物质的量浓度为多少
(3)工业常利用3Cl2 + 6KOH
 KClO3 + 5KCl + 3H2O,制取KClO3(混有KClO)。实验室模拟KClO3制备,在热的KOH溶液中通入一定量氯气充分反应后,测定溶液中n(K+):n(Cl-) = 14:11,将所得溶液低温蒸干,那么在得到的固体中KClO3的质量分数的取值范围为多少
KClO3 + 5KCl + 3H2O,制取KClO3(混有KClO)。实验室模拟KClO3制备,在热的KOH溶液中通入一定量氯气充分反应后,测定溶液中n(K+):n(Cl-) = 14:11,将所得溶液低温蒸干,那么在得到的固体中KClO3的质量分数的取值范围为多少
您最近一年使用:0次



