名校
1 . 碲(Te)具有两性特征,铜阳极泥是提取碲的主要原料,碲在铜阳极泥中主要以MezTeCMe表 示金属Cu、Pb、Au、Ag等)的形式存在。
(1)利用“氯化浸出-还原法”制备Te的工艺流程如下所示。
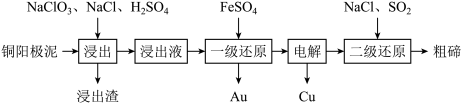
①浸出液的主要成分为CuSO4、HAuCu、H2TeO3,则浸出渣的主要成分 为____ (填化学式);“浸出”过程中有少量污染性气体生成,该气体是_______ (填物质名称)
②已知HAuCU是一种强酸,则“一级还原”过程中发生反应的离子方程式为_________ 。
③欲得到64g碲,则“二级还原”过程中至少需通入____ mol SO2。 “氧化碱浸-电解法”指的是在氧化剂的作用下,Cu2Te与NaOH溶液反应生成Na2TeO3和Cu(OH)2,经电解即可获得Te。
①以空气为氧化剂进行“氧化碱浸”的化学方程式为______ 。
②电解过程中,阴极的电极反应式为______ 。
③与“氯化浸出-还原法”相比“氧化碱浸-电解法”的优点是____ (任写一点)
(1)利用“氯化浸出-还原法”制备Te的工艺流程如下所示。

①浸出液的主要成分为CuSO4、HAuCu、H2TeO3,则浸出渣的主要成分 为
②已知HAuCU是一种强酸,则“一级还原”过程中发生反应的离子方程式为
③欲得到64g碲,则“二级还原”过程中至少需通入
①以空气为氧化剂进行“氧化碱浸”的化学方程式为
②电解过程中,阴极的电极反应式为
③与“氯化浸出-还原法”相比“氧化碱浸-电解法”的优点是
您最近一年使用:0次
名校
解题方法
2 . 有关 反应的叙述正确的为
反应的叙述正确的为
 反应的叙述正确的为
反应的叙述正确的为| A.还原剂与氧化剂物质的量之比为5:3 |
| B.生成lmolO2,反应共转移4mol电子 |
C.若有5mol水做还原剂时,被BrF3还原的BrF3为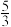 mol mol |
| D.若有5mol水参与反应时,被水还原的BrF3为2mol |
您最近一年使用:0次
2019-11-24更新
|
2665次组卷
|
7卷引用:重庆市育才中学2019-2020学年高一上学期期中考试化学试题
解题方法
3 . 无机化合物X与Y均由三种相同短周期的非金属元素组成(X比Y的相对分子质量大),常温下均为无色液体,易水解,均产生酸性白雾。取1.35gX与足量水完全反应,向反应后的溶液中滴加1.00 mol·L-1的NaOH溶液40.0mL恰好反应,溶液呈中性,继续滴加BaCl2溶液至过量,产生不溶于稀盐酸的2.33g白色沉淀。Y水解得到两种产物,其物质的量之比1:2,且产物之一能使品红溶液褪色。请回答:
(1)X的化学式______________ 。白色沉淀属于_____________ (填“强”、“弱”或“非”)电解质。
(2)Y与水反应的化学方程式_________________ 。
(3)二元化合物Z能与X化合生成Y。一定条件下,0.030 mol Z与足量氨反应生成0.92gA(原子个数之比1:1,其相对分子量为184)和淡黄色单质B及离子化合物M,且M的水溶液的pH<7。将0.92gA隔绝空气加强热可得到0.64gB和气体单质C。
①写出Z与足量氨反应的化学方程式____________ 。
②亚硝酸钠和M固体在加热条件下_____________ (填“可能”或“不能”)发生反应,判断理由是_________________ 。
③请设计检验离子化合物M中阳离子的实验方案:_________________ 。
(1)X的化学式
(2)Y与水反应的化学方程式
(3)二元化合物Z能与X化合生成Y。一定条件下,0.030 mol Z与足量氨反应生成0.92gA(原子个数之比1:1,其相对分子量为184)和淡黄色单质B及离子化合物M,且M的水溶液的pH<7。将0.92gA隔绝空气加强热可得到0.64gB和气体单质C。
①写出Z与足量氨反应的化学方程式
②亚硝酸钠和M固体在加热条件下
③请设计检验离子化合物M中阳离子的实验方案:
您最近一年使用:0次
4 . 碘及其化合物在合成杀菌剂、药物等方面具有广泛用途。回答下列问题:
(1)大量的碘富集在海藻中,用水浸取后浓缩,再向浓缩液中加MnO2和H2SO4,即可得到I2,该反应的还原产物为_______ 。
(2)上述浓缩液中含有I-、Cl-等离子,取一定量的浓缩液,向其中滴加AgNO3溶液,当AgCl开始沉淀时,溶液中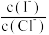 为:
为:_______ ,已知Ksp(AgCl)=1.8×10-10,Ksp(AgI)=8.5×10-17。
(3)已知反应2HI(g) =H2(g) + I2(g)的ΔH= +11kJ·mol-1,1mol H2(g)、1mol I2(g)分子中化学键断裂时分别需要吸收436kJ、151kJ的能量,则1molHI(g)分子中化学键断裂时需吸收的能量为_______ kJ。
(4)Bodensteins研究了下列反应:2HI(g)⇌H2(g) + I2(g)
在716K时,气体混合物中碘化氢的物质的量分数x(HI)与反应时间t的关系如下表:
①根据上述实验结果,该反应的平衡常数K的计算式为:_______ 。
②上述反应中,正反应速率为v正= k正·x2(HI),逆反应速率为v逆=k逆·x(H2)·x(I2),其中k正、k逆为速率常数,则k逆为_______ (以K和k正表示)。若k正 = 0.0027min-1,在t=40min时,v正=_______ min-1
③由上述实验数据计算得到v正~x(HI)和v逆~x(H2)的关系可用下图表示。当升高到某一温度时,反应重新达到平衡,相应的点分别为_______ (填字母)

(1)大量的碘富集在海藻中,用水浸取后浓缩,再向浓缩液中加MnO2和H2SO4,即可得到I2,该反应的还原产物为
(2)上述浓缩液中含有I-、Cl-等离子,取一定量的浓缩液,向其中滴加AgNO3溶液,当AgCl开始沉淀时,溶液中
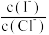 为:
为:(3)已知反应2HI(g) =H2(g) + I2(g)的ΔH= +11kJ·mol-1,1mol H2(g)、1mol I2(g)分子中化学键断裂时分别需要吸收436kJ、151kJ的能量,则1molHI(g)分子中化学键断裂时需吸收的能量为
(4)Bodensteins研究了下列反应:2HI(g)⇌H2(g) + I2(g)
在716K时,气体混合物中碘化氢的物质的量分数x(HI)与反应时间t的关系如下表:
| t/min | 0 | 20 | 40 | 60 | 80 | 120 |
| x(HI) | 1 | 0.91 | 0.85 | 0.815 | 0.795 | 0.784 |
| x(HI) | 0 | 0.60 | 0.73 | 0.773 | 0.780 | 0.784 |
①根据上述实验结果,该反应的平衡常数K的计算式为:
②上述反应中,正反应速率为v正= k正·x2(HI),逆反应速率为v逆=k逆·x(H2)·x(I2),其中k正、k逆为速率常数,则k逆为
③由上述实验数据计算得到v正~x(HI)和v逆~x(H2)的关系可用下图表示。当升高到某一温度时,反应重新达到平衡,相应的点分别为

您最近一年使用:0次
2019-01-30更新
|
7109次组卷
|
9卷引用:2015年全国普通高等学校招生统一考试化学(新课标I卷)
解题方法
5 . 含氮的化合物在化学反应中变化复杂。I.现用下图所示仪器(夹持装置已省略及药品,探究亚硝酸钠与硫酸反应及气体产物的成分。已知:①NO+NO2+2OH-=2NO2-+H2O;②气体液化的温度:NO2 21℃、NO -152℃。
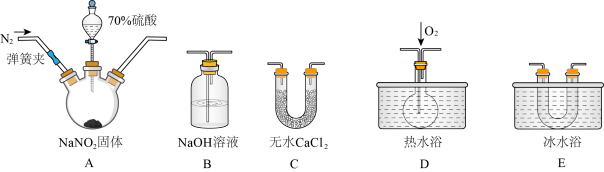
(1)为了检验装置A中生成的气体产物,上述仪器的连接顺序(按左→右连接)为__________ 。
(2)反应前应打开弹簧夹,先通入一段时间氮气,排除装置中的空气,目的是:____________ 。
(3)在关闭弹簧夹,滴入70%硫酸后,A中产生红棕色气体。
①盛装70%浓硫酸的仪器名称是___________ ;
②实验确认有NO的现象是______________________ 。
(4)通过上述实验探究过程,可得出装置A中反应的化学方程式是______________ 。
Ⅱ.NH3经一系列反应可以得到HNO3和NH4NO3,如图1所示。


图1 图2
【资料卡片】
a.NH4NO3是一种白色晶体,易溶于水,微溶于乙醇.
b.在230℃ 以上时,同时有弱光:2NH4NO3=2N2↑+ O2↑+ 4H2O
c.在400℃以上时,剧烈分解发生爆炸:4NH4NO3=3N2↑+ 2NO2↑+ 8H2O
(5)如图2 将水滴入盛有硝酸铵的试管中,观察到的A处液面上升,B处液面下降,产生该现象的原因_______________ 。
(6)实验室可以用氯化铵和熟石灰反应来制备氨气,该反应的化学方程式是____________ (填“能”或“不能”)_____ 用硝酸铵代替氯化铵。
(7)在汽车发生碰撞时,NaN3会产生________ (填化学式)气体充满安全气囊来减轻碰撞事故中乘员伤害程度。
(8)完成离子反应IV:______ NO+ _______ H2O=______ +______ +____ H+。

(1)为了检验装置A中生成的气体产物,上述仪器的连接顺序(按左→右连接)为
(2)反应前应打开弹簧夹,先通入一段时间氮气,排除装置中的空气,目的是:
(3)在关闭弹簧夹,滴入70%硫酸后,A中产生红棕色气体。
①盛装70%浓硫酸的仪器名称是
②实验确认有NO的现象是
(4)通过上述实验探究过程,可得出装置A中反应的化学方程式是
Ⅱ.NH3经一系列反应可以得到HNO3和NH4NO3,如图1所示。


图1 图2
【资料卡片】
a.NH4NO3是一种白色晶体,易溶于水,微溶于乙醇.
b.在230℃ 以上时,同时有弱光:2NH4NO3=2N2↑+ O2↑+ 4H2O
c.在400℃以上时,剧烈分解发生爆炸:4NH4NO3=3N2↑+ 2NO2↑+ 8H2O
(5)如图2 将水滴入盛有硝酸铵的试管中,观察到的A处液面上升,B处液面下降,产生该现象的原因
(6)实验室可以用氯化铵和熟石灰反应来制备氨气,该反应的化学方程式是
(7)在汽车发生碰撞时,NaN3会产生
(8)完成离子反应IV:
您最近一年使用:0次
2016-12-09更新
|
748次组卷
|
2卷引用:2015-2016学年重庆市巴蜀中学高一下3月月考化学试卷
解题方法
6 . 海带中含有丰富的碘,,为了从海带中提取碘,某研究性学习小组设计并进行了以下实验:
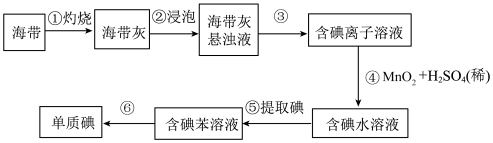
请填写下列空白:
(1)步骤①所需要的硅酸盐仪器是___________ ,步骤③的实验操作是___________ 。
(2)步骤⑤中,某学生选择用苯来提取碘水中的单质碘的理由是_____ 。(选填序号)
a.单质碘与苯不发生化学反应 b.碘在苯中溶解度小
c.碘在苯中溶解度大 d.苯与水互不相溶
(3)提取碘的过程中,不能使用的有机溶剂是_________ 。(选填序号)
a.酒精 b.汽油 c.四氯化碳
(4)步骤④中所发生的离子反应方程式______________ 。
(5)已知:2Fe3++2I-→2Fe2++I2氯气既可以氧化Fe2+,也可以氧化I-。 往FeI2溶液中通入一定量的 Cl2,反应完成后,溶液中有1/2Fe2+被氧化,请写出该反应的化学反应方程式:____________ 。

请填写下列空白:
(1)步骤①所需要的硅酸盐仪器是
(2)步骤⑤中,某学生选择用苯来提取碘水中的单质碘的理由是
a.单质碘与苯不发生化学反应 b.碘在苯中溶解度小
c.碘在苯中溶解度大 d.苯与水互不相溶
(3)提取碘的过程中,不能使用的有机溶剂是
a.酒精 b.汽油 c.四氯化碳
(4)步骤④中所发生的离子反应方程式
(5)已知:2Fe3++2I-→2Fe2++I2氯气既可以氧化Fe2+,也可以氧化I-。 往FeI2溶液中通入一定量的 Cl2,反应完成后,溶液中有1/2Fe2+被氧化,请写出该反应的化学反应方程式:
您最近一年使用:0次
名校
7 . 将一定量的镁和铜组成的混合物加入到稀硝酸中,金属完全溶解(假设反应中还原产物只有NO)。向反应后的溶液中加入3 mol·L−1NaOH溶液至沉淀完全,测得生成沉淀的质量比原合金的质量增加5.1 g。下列叙述不正确 的是
| A.当金属全部溶解时,参加反应的硝酸的物质的量一定是0.4mol |
| B.参加反应的金属的总质量3.6g<m<9.6g |
| C.当生成的沉淀量达到最大时,消耗NaOH溶液的体积一定为V=100mL |
| D.当金属全部溶解时收集到NO气体的体积在标准状况下为2.24L |
您最近一年使用:0次
2016-12-09更新
|
2466次组卷
|
11卷引用:2016届陕西省西藏民族学院附属中学高三上期末化学试卷
2016届陕西省西藏民族学院附属中学高三上期末化学试卷2017届湖南省长株潭岳益五市十校高三12月联考化学卷2017届福建省漳州市八校高三上学期期末联考化学试卷(已下线)2019年1月24日《每日一题》二轮复习—— 氮的氧化物、硝酸的性质及应用(已下线)2019年4月17日 《每日一题》三轮复习-其他金属及其化合物【全国百强校】云南省曲靖市第一中学2018-2019学年高一下学期期中考试化学试题安徽省安庆市怀宁县怀宁中学2021届高三年级第一次质量检测化学试题江西省南昌市莲塘一中2021届高三上学期11月月考化学试题江西省上高二中2022届高三第二次月考化学试卷河北省张家口市宣化第一中学2021-2022学年高三上学期12月月考化学试题辽宁省部分中学2019-2020高一下学期期末考试化学试题
名校
8 . 在一定浓度的浓硝酸中加入m克铜镁合金恰好完全溶解(假定硝酸的还原产物只有NO2),向反应后的混合溶液中滴加b mol/L NaOH溶液,当滴加到V mL时,恰好完全反应,得到沉淀质量为n克,则下列有关该实验的说法中正确的有
①沉淀中氢氧根的质量为(n−m)克 ②恰好溶解后溶液中 的物质的量为bV mol
的物质的量为bV mol
③反应过程中转移的电子数为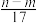 mol ④生成NO2气体的体积为
mol ④生成NO2气体的体积为 L
L
⑤与合金反应的硝酸的物质的量为 mol
mol
①沉淀中氢氧根的质量为(n−m)克 ②恰好溶解后溶液中
 的物质的量为bV mol
的物质的量为bV mol③反应过程中转移的电子数为
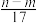 mol ④生成NO2气体的体积为
mol ④生成NO2气体的体积为 L
L⑤与合金反应的硝酸的物质的量为
 mol
mol| A.①②③④⑤ | B.①③④⑤ |
| C.①③⑤ | D.①②③⑤ |
您最近一年使用:0次
2016-12-09更新
|
2383次组卷
|
4卷引用:2016届山东省济宁市第一中学高三上学期期中考试化学试卷
2016届山东省济宁市第一中学高三上学期期中考试化学试卷(已下线)《2018,我的高考我的教师君》-【考前基础篇】高考化学必会知识大盘点江西师范大学附属中学2020-2021学年高一下学期4月月考化学试题辽宁省部分中学2019-2020高一下学期期末考试化学试题
名校
9 . 在100mL密度为1.2g/mL稀硝酸中,加入一定量的镁和铜组成的混合物,充分反应后金属完全溶解(假设还原产物只有NO),向反应后溶液中加入3mol/L NaOH溶液至沉淀完全,测得生成沉淀质量比原金属质量增加5.1g。则下列叙述不正确的是
| A.当金属全部溶解时收集到NO气体的体积为2.24L(标准状况) |
| B.当生成沉淀的量最多时,消耗NaOH溶液体积最小为100mL |
| C.原稀硝酸的物质的量浓度一定为4 mol/L |
| D.参加反应金属总质量(m)为9.6g>m>3.6g |
您最近一年使用:0次
2016-12-09更新
|
2961次组卷
|
11卷引用:2015届山西省临汾一中等四校高三第二次联考化学试卷
2015届山西省临汾一中等四校高三第二次联考化学试卷2015届陕西省西工大附中高三下学期三模考试化学试卷2016届湖南省长沙市明德中学高三上学期第三次月考化学试卷2016届湖南省益阳市箴言中学高三上学期第三次模拟化学试卷2016届河北省保定市高三上学期摸底考试化学试卷2015-2016学年浙江省宁波市北仑中学高二下学期期中考试化学试卷湖南省长沙市明德中学2016届高三上学期第三次月考化学试题湖南省长沙市一中2019-2020学年高一上学期期末考试化学试题黑龙江省大庆实验中学2019-2020学年高一下学期第一次阶段考试化学试题四川省乐山市第四中学2019-2020学年高一下学期期中考试化学试题陕西西北工业大学附属中学2022-2023学年高一下学期期中考试化学试题
10 . 向FeI2、FeBr2的混合溶液中通入适量氯气,溶液中某些离子的物质的量变化情况如图所示.则下列说法中不正确的是
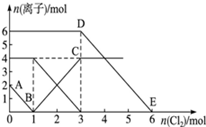

| A.还原性:I->Fe2+>Br- |
| B.原混合溶液中FeBr2的物质的量为3mol |
| C.线段AB表示Fe2+被氯气氧化 |
| D.原溶液中:n(Fe2+):n(I-):n(Br-)═2:1:3 |
您最近一年使用:0次
2016-12-09更新
|
2290次组卷
|
3卷引用:2016届山东省淄博实验中学高三上学期第一次诊断测试化学试卷



