名校
1 . 维生素C是一种水溶性维生素,有强还原性、水溶液显酸性。化学式为 。某小组同学测定了某新鲜水果中维生素C的含量,实验报告如下:
。某小组同学测定了某新鲜水果中维生素C的含量,实验报告如下:
【实验目的】测定某新鲜水果中维生素C的含量。
【实验原理】 ,
,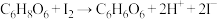 。
。
【实验用品】 标准溶液、指示剂、
标准溶液、指示剂、 溶液、
溶液、 溶液、蒸馏水等。
溶液、蒸馏水等。
【实验步骤】
(1)配制待测溶液:称取新鲜水果样品 ,加入适量蒸馏水进行粉碎、过滤,并将滤液转移至
,加入适量蒸馏水进行粉碎、过滤,并将滤液转移至 容量瓶中,定容,随后将待测溶液加到滴定管中。根据维生素C的性质,待测溶液应用
容量瓶中,定容,随后将待测溶液加到滴定管中。根据维生素C的性质,待测溶液应用___________ (填“酸式”或“碱式”)滴定管盛装。
(2)氧化还原滴定法:取(1)中配制好的待测溶液 于锥形瓶中,调节
于锥形瓶中,调节 至3,加入适量指示剂后,小心地滴入
至3,加入适量指示剂后,小心地滴入 标准溶液,直至滴定终点,记录相关数据。平行测定三次,计算新鲜水果中维生素
标准溶液,直至滴定终点,记录相关数据。平行测定三次,计算新鲜水果中维生素 的质量分数。
的质量分数。
①上述氧化还原滴定法应用___________ 作指示剂,滴定终点的现象为___________ 。
②除了样品的质量、待测溶液的体积外,计算新鲜水果中维生素C的质量分数还需要的数据有___________ 。
(3)库仑滴定法:取(1)中配制好的待测溶液 ,用库仑仪测定其中维生素C的含量。平行测定三次,计算新鲜水果中维生素C的质量分数。
,用库仑仪测定其中维生素C的含量。平行测定三次,计算新鲜水果中维生素C的质量分数。
已知:库仑仪中电解原理示意图如下。检测前,电解质溶液中 保持定值时,电解池不工作。将待测溶液加入电解池后,维生素C将
保持定值时,电解池不工作。将待测溶液加入电解池后,维生素C将 还原,库仑仪便立即自动进行电解到
还原,库仑仪便立即自动进行电解到 又回到原定值,测定结束,通过测定电解消托的电量可以求得维生素C的含量。
又回到原定值,测定结束,通过测定电解消托的电量可以求得维生素C的含量。

①库仑仪工作时电解池的阳极反应式为___________ 。
②若电解消耗的电量为Q库仑,维生素C的摩尔质量为 ,则新鲜水果中维生素C的质量分数为
,则新鲜水果中维生素C的质量分数为___________ 。(用含 的代数式表示)已知:电解中转移
的代数式表示)已知:电解中转移 电子所消耗的电量为96500库仑。
电子所消耗的电量为96500库仑。
③测定过程中,需控制电解质溶液 ,当
,当 时,部分
时,部分 易被空气中的
易被空气中的 直接氧化为
直接氧化为 ,该过程的离子方程式为
,该过程的离子方程式为___________ 。这部分非电解生成的 ;将导致测得的维生素C的含量
;将导致测得的维生素C的含量___________ 。(填“偏大”或“偏小”)。
 。某小组同学测定了某新鲜水果中维生素C的含量,实验报告如下:
。某小组同学测定了某新鲜水果中维生素C的含量,实验报告如下:【实验目的】测定某新鲜水果中维生素C的含量。
【实验原理】
 ,
,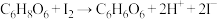 。
。【实验用品】
 标准溶液、指示剂、
标准溶液、指示剂、 溶液、
溶液、 溶液、蒸馏水等。
溶液、蒸馏水等。【实验步骤】
(1)配制待测溶液:称取新鲜水果样品
 ,加入适量蒸馏水进行粉碎、过滤,并将滤液转移至
,加入适量蒸馏水进行粉碎、过滤,并将滤液转移至 容量瓶中,定容,随后将待测溶液加到滴定管中。根据维生素C的性质,待测溶液应用
容量瓶中,定容,随后将待测溶液加到滴定管中。根据维生素C的性质,待测溶液应用(2)氧化还原滴定法:取(1)中配制好的待测溶液
 于锥形瓶中,调节
于锥形瓶中,调节 至3,加入适量指示剂后,小心地滴入
至3,加入适量指示剂后,小心地滴入 标准溶液,直至滴定终点,记录相关数据。平行测定三次,计算新鲜水果中维生素
标准溶液,直至滴定终点,记录相关数据。平行测定三次,计算新鲜水果中维生素 的质量分数。
的质量分数。①上述氧化还原滴定法应用
②除了样品的质量、待测溶液的体积外,计算新鲜水果中维生素C的质量分数还需要的数据有
(3)库仑滴定法:取(1)中配制好的待测溶液
 ,用库仑仪测定其中维生素C的含量。平行测定三次,计算新鲜水果中维生素C的质量分数。
,用库仑仪测定其中维生素C的含量。平行测定三次,计算新鲜水果中维生素C的质量分数。已知:库仑仪中电解原理示意图如下。检测前,电解质溶液中
 保持定值时,电解池不工作。将待测溶液加入电解池后,维生素C将
保持定值时,电解池不工作。将待测溶液加入电解池后,维生素C将 还原,库仑仪便立即自动进行电解到
还原,库仑仪便立即自动进行电解到 又回到原定值,测定结束,通过测定电解消托的电量可以求得维生素C的含量。
又回到原定值,测定结束,通过测定电解消托的电量可以求得维生素C的含量。
①库仑仪工作时电解池的阳极反应式为
②若电解消耗的电量为Q库仑,维生素C的摩尔质量为
 ,则新鲜水果中维生素C的质量分数为
,则新鲜水果中维生素C的质量分数为 的代数式表示)已知:电解中转移
的代数式表示)已知:电解中转移 电子所消耗的电量为96500库仑。
电子所消耗的电量为96500库仑。③测定过程中,需控制电解质溶液
 ,当
,当 时,部分
时,部分 易被空气中的
易被空气中的 直接氧化为
直接氧化为 ,该过程的离子方程式为
,该过程的离子方程式为 ;将导致测得的维生素C的含量
;将导致测得的维生素C的含量
您最近一年使用:0次
2023-12-11更新
|
105次组卷
|
3卷引用: 北京市第五中学2023-2024学年高二上学期12月月考化学试题
2 . 库仑滴定法是常用的快捷检测煤中全硫含量的方法。其方法为将煤中的硫元素在催化剂作用下转化为 ,再将
,再将 通入库仑测硫仪中,库仑测硫仪中电解原理示意图如图所示,检测前,电解质溶液中
通入库仑测硫仪中,库仑测硫仪中电解原理示意图如图所示,检测前,电解质溶液中 保持定值时,电解池不工作。待测气体进入电解池后,
保持定值时,电解池不工作。待测气体进入电解池后, 溶解并将
溶解并将 还原,测硫仪便立即自动进行电解到
还原,测硫仪便立即自动进行电解到 又回到原定值,测定结束,通过测定电解消耗的电量可以求得煤中含硫量,下列说法
又回到原定值,测定结束,通过测定电解消耗的电量可以求得煤中含硫量,下列说法不正确 的是
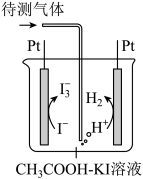
 ,再将
,再将 通入库仑测硫仪中,库仑测硫仪中电解原理示意图如图所示,检测前,电解质溶液中
通入库仑测硫仪中,库仑测硫仪中电解原理示意图如图所示,检测前,电解质溶液中 保持定值时,电解池不工作。待测气体进入电解池后,
保持定值时,电解池不工作。待测气体进入电解池后, 溶解并将
溶解并将 还原,测硫仪便立即自动进行电解到
还原,测硫仪便立即自动进行电解到 又回到原定值,测定结束,通过测定电解消耗的电量可以求得煤中含硫量,下列说法
又回到原定值,测定结束,通过测定电解消耗的电量可以求得煤中含硫量,下列说法
A. 在电解池中发生反应的离子方程式为 在电解池中发生反应的离子方程式为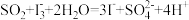 |
B.测硫仪工作时电解池的阳极反应式为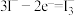 |
C.煤样为 ,电解消耗的电量为 ,电解消耗的电量为 库仑,煤样中硫的质量分数为 库仑,煤样中硫的质量分数为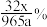 (已知:电解中转移 (已知:电解中转移 电子所消耗的电量为96500库仑) 电子所消耗的电量为96500库仑) |
D.煤中硫元素在催化剂作用下会有少量 产生,使测得的全硫含量偏小 产生,使测得的全硫含量偏小 |
您最近一年使用:0次
名校
解题方法
3 .  是制备某负载型活性铁催化剂 的主要原料,具有工业生产价值。某化学小组用如下方法制备
是制备某负载型活性铁催化剂 的主要原料,具有工业生产价值。某化学小组用如下方法制备 ,并测定产品中铁的含量。
,并测定产品中铁的含量。
I.制备晶体
i.称取 5 g 莫尔盐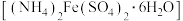 ,用 15 mL 水和几滴
,用 15 mL 水和几滴 溶液充分溶解,再加入25 mL饱和
溶液充分溶解,再加入25 mL饱和 溶液,加热至沸,生成黄色沉淀;
溶液,加热至沸,生成黄色沉淀;
ⅱ.将沉淀洗涤至中性,加入10 mL饱和 溶液,水浴加热至40℃,边搅拌边缓慢滴加
溶液,水浴加热至40℃,边搅拌边缓慢滴加 溶液,沉淀逐渐变为红褐色;
溶液,沉淀逐渐变为红褐色;
ⅲ.将混合物煮沸30 s,加入8 mL饱和 溶液,红褐色沉淀溶解,趁热过滤,滤液冷却后,析出翠绿色晶体,过滤、干燥。
溶液,红褐色沉淀溶解,趁热过滤,滤液冷却后,析出翠绿色晶体,过滤、干燥。
II.测定产品中铁的含量
ⅳ.称量 制得的样品,加水溶解,并加入稀
制得的样品,加水溶解,并加入稀 酸化,再滴入
酸化,再滴入 溶液使其恰好反应;
溶液使其恰好反应;
v.向ⅳ的溶液中加入过量Zn粉,反应完全后,弃去不溶物,向溶液中加入稀 酸化,用
酸化,用 溶液滴定至终点,消耗
溶液滴定至终点,消耗 溶液
溶液 。
。
已知: 为二元弱酸,具有较强的还原性
为二元弱酸,具有较强的还原性
(1)莫尔盐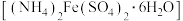 中铁元素的化合价是
中铁元素的化合价是_______ 。
(2)步骤ⅰ中黄色沉淀的化学式为 ,生成该沉淀的离子方程式是
,生成该沉淀的离子方程式是_______ 。
(3)步骤ⅱ中除了生成红褐色沉淀,另一部分铁元素转化为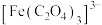 、将下述反应的离子方程式补充完整
、将下述反应的离子方程式补充完整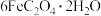 +____+____=
+____+____= ____
____ ,
,_____________ 。
(4)步骤ⅱ中水浴加热的温度不宜过高,原因是_______ 。
(5)步骤iv在铁的含量测定中所起的作用是_______ 。
(6)已知:ⅴ中Zn粉将铁元素全部还原为 ;反应中
;反应中 转化为
转化为 。则该样品中铁元素的质量分数是
。则该样品中铁元素的质量分数是_______ (用含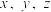 的代数式表示)。
的代数式表示)。
 是制备某负载型活性铁催化剂 的主要原料,具有工业生产价值。某化学小组用如下方法制备
是制备某负载型活性铁催化剂 的主要原料,具有工业生产价值。某化学小组用如下方法制备 ,并测定产品中铁的含量。
,并测定产品中铁的含量。I.制备晶体
i.称取 5 g 莫尔盐
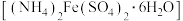 ,用 15 mL 水和几滴
,用 15 mL 水和几滴 溶液充分溶解,再加入25 mL饱和
溶液充分溶解,再加入25 mL饱和 溶液,加热至沸,生成黄色沉淀;
溶液,加热至沸,生成黄色沉淀;ⅱ.将沉淀洗涤至中性,加入10 mL饱和
 溶液,水浴加热至40℃,边搅拌边缓慢滴加
溶液,水浴加热至40℃,边搅拌边缓慢滴加 溶液,沉淀逐渐变为红褐色;
溶液,沉淀逐渐变为红褐色;ⅲ.将混合物煮沸30 s,加入8 mL饱和
 溶液,红褐色沉淀溶解,趁热过滤,滤液冷却后,析出翠绿色晶体,过滤、干燥。
溶液,红褐色沉淀溶解,趁热过滤,滤液冷却后,析出翠绿色晶体,过滤、干燥。II.测定产品中铁的含量
ⅳ.称量
 制得的样品,加水溶解,并加入稀
制得的样品,加水溶解,并加入稀 酸化,再滴入
酸化,再滴入 溶液使其恰好反应;
溶液使其恰好反应;v.向ⅳ的溶液中加入过量Zn粉,反应完全后,弃去不溶物,向溶液中加入稀
 酸化,用
酸化,用 溶液滴定至终点,消耗
溶液滴定至终点,消耗 溶液
溶液 。
。已知:
 为二元弱酸,具有较强的还原性
为二元弱酸,具有较强的还原性(1)莫尔盐
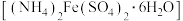 中铁元素的化合价是
中铁元素的化合价是(2)步骤ⅰ中黄色沉淀的化学式为
 ,生成该沉淀的离子方程式是
,生成该沉淀的离子方程式是(3)步骤ⅱ中除了生成红褐色沉淀,另一部分铁元素转化为
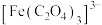 、将下述反应的离子方程式补充完整
、将下述反应的离子方程式补充完整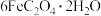 +____+____=
+____+____= ____
____ ,
,(4)步骤ⅱ中水浴加热的温度不宜过高,原因是
(5)步骤iv在铁的含量测定中所起的作用是
(6)已知:ⅴ中Zn粉将铁元素全部还原为
 ;反应中
;反应中 转化为
转化为 。则该样品中铁元素的质量分数是
。则该样品中铁元素的质量分数是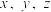 的代数式表示)。
的代数式表示)。
您最近一年使用:0次
2020-12-19更新
|
143次组卷
|
4卷引用:北京市海淀实验中学2022-2023学年高三上学期10月学科展示化学试题
解题方法
4 . 过硫酸(H2S2O8)为无色晶体,易溶于水,在热水中易水解。
(1)依据硫酸和过硫酸的结构式,下列说法正确的是______ (填序号)。
a.硫酸和过硫酸均为共价化合物
b. 过硫酸分子中含有与过氧化氢分子中相同的化学键
c. 过硫酸分子可看作2个硫酸分子脱去1个水分子
(2)工业上利用过硫酸铵制备过氧化氢的一种方法如下图。
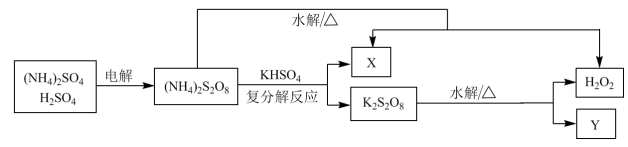
①电解法制(NH4)2S2O8过程中,得到S2 的电极反应式是
的电极反应式是______ 。
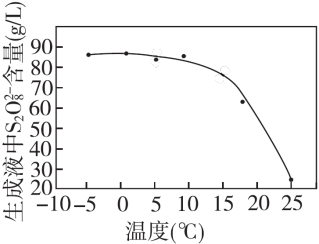
② 其他条件一定,电解相同时间后,测得生成液中S2 含量随温度变化如图。电解时通常控制15℃而不用更低温度的原因:
含量随温度变化如图。电解时通常控制15℃而不用更低温度的原因:______ 。
③X的化学式是______ 。
④过硫酸盐的水解反应______ (填“属于”或“不属于”)氧化还原反应。
⑤下图中a~e表示S2 中的部分化学键,则S2
中的部分化学键,则S2 发生水解反应时断裂的化学键是
发生水解反应时断裂的化学键是______ (选填字母)。

(3)过硫酸钾氧化法可用于分析锰钢中Mn元素的含量:取样品a g,加入过量浓硝酸,在加热条件下将Mn溶出,再用b L 过硫酸钾溶液将溶出的Mn2+全部转化为 ,检测
,检测 浓度,计算得出样品中Mn元素的质量分数为c。
浓度,计算得出样品中Mn元素的质量分数为c。
①该实验条件下氧化性:S2
______  (填“>”或“<”)。
(填“>”或“<”)。
②该过程中过硫酸钾溶液的浓度至少是______ mol/L(用含a、b、c的代数式表示)。
| 物质 | 硫酸 | 过硫酸 |
| 结构式 | 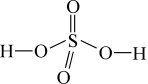 | 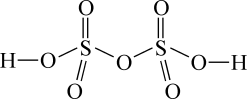 |
a.硫酸和过硫酸均为共价化合物
b. 过硫酸分子中含有与过氧化氢分子中相同的化学键
c. 过硫酸分子可看作2个硫酸分子脱去1个水分子
(2)工业上利用过硫酸铵制备过氧化氢的一种方法如下图。

①电解法制(NH4)2S2O8过程中,得到S2
 的电极反应式是
的电极反应式是② 其他条件一定,电解相同时间后,测得生成液中S2
 含量随温度变化如图。电解时通常控制15℃而不用更低温度的原因:
含量随温度变化如图。电解时通常控制15℃而不用更低温度的原因:
③X的化学式是
④过硫酸盐的水解反应
⑤下图中a~e表示S2
 中的部分化学键,则S2
中的部分化学键,则S2 发生水解反应时断裂的化学键是
发生水解反应时断裂的化学键是
(3)过硫酸钾氧化法可用于分析锰钢中Mn元素的含量:取样品a g,加入过量浓硝酸,在加热条件下将Mn溶出,再用b L 过硫酸钾溶液将溶出的Mn2+全部转化为
 ,检测
,检测 浓度,计算得出样品中Mn元素的质量分数为c。
浓度,计算得出样品中Mn元素的质量分数为c。①该实验条件下氧化性:S2

 (填“>”或“<”)。
(填“>”或“<”)。②该过程中过硫酸钾溶液的浓度至少是
您最近一年使用:0次
5 . Na2SO3应用广泛。利用工业废碱渣(主要成分Na2CO3)吸收硫酸厂尾气中的SO2制备无水Na2SO3的成本低,优势明显,其流程如下。
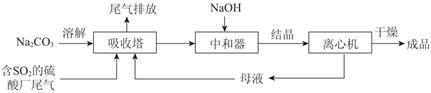
(1)举例说明向大气中排放SO2导致的环境问题:_________ 。
(2)下图为吸收塔中Na2CO3溶液与SO2反应过程中溶液组成变化。则初期反应(图中A点以前)的离子方程式是_________ 。

(3)中和器中发生的主要反应的化学方程式是_________ 。
(4)为了降低由中和器所得溶液中Na2SO3的溶解度,从而提高结晶产率,中和器中加入的NaOH是过量的。
①请结合Na2SO3的溶解平衡解释NaOH过量的原因_________ 。
②结晶时应选择的最佳操作是_________ (选填字母)。
a.95~100℃加热蒸发,直至蒸干
B.维持95~100℃蒸发浓缩至有大量晶体析出
C.95~100℃加热浓缩,冷却至室温结晶
(5)为检验Na2SO3成品中是否含少量Na2SO4,需选用的试剂是_________ 、_________ 。
(6)KIO3滴定法可测定成品中Na2SO3的含量:室温下将0.1260g 成品溶于水并加入淀粉做指示剂,再用酸性KIO3标准溶液(x mol/L)进行滴定至溶液恰好由无色变为蓝色,消耗KIO3标准溶液体积为y mL。
①滴定终点前反应的离子方程式是:____ IO3-+____ SO32- =___________ +___________ (将方程式补充完整)
②成品中Na2SO3(M =126 g/mol)的质量分数是_________ 。

(1)举例说明向大气中排放SO2导致的环境问题:
(2)下图为吸收塔中Na2CO3溶液与SO2反应过程中溶液组成变化。则初期反应(图中A点以前)的离子方程式是

(3)中和器中发生的主要反应的化学方程式是
| 资料显示: Ⅰ.Na2SO3在33℃时溶解度最大,将其饱和溶液加热至33℃以上时,由于溶解度降低会析出无水Na2SO3,冷却至33℃以下时析出Na2SO3·7H2O; Ⅱ.无水Na2SO3在空气中不易被氧化,Na2SO3·7H2O在空气中易被氧化。 |
(4)为了降低由中和器所得溶液中Na2SO3的溶解度,从而提高结晶产率,中和器中加入的NaOH是过量的。
①请结合Na2SO3的溶解平衡解释NaOH过量的原因
②结晶时应选择的最佳操作是
a.95~100℃加热蒸发,直至蒸干
B.维持95~100℃蒸发浓缩至有大量晶体析出
C.95~100℃加热浓缩,冷却至室温结晶
(5)为检验Na2SO3成品中是否含少量Na2SO4,需选用的试剂是
(6)KIO3滴定法可测定成品中Na2SO3的含量:室温下将0.1260g 成品溶于水并加入淀粉做指示剂,再用酸性KIO3标准溶液(x mol/L)进行滴定至溶液恰好由无色变为蓝色,消耗KIO3标准溶液体积为y mL。
①滴定终点前反应的离子方程式是:
②成品中Na2SO3(M =126 g/mol)的质量分数是
您最近一年使用:0次
2016-12-09更新
|
811次组卷
|
3卷引用:2016届北京市东城区高三一模理综化学试卷
名校
解题方法
6 .  是一种高效多功能的新型消毒剂。
是一种高效多功能的新型消毒剂。
已知: 微溶于水,在酸性或中性溶液中快速分解产生
微溶于水,在酸性或中性溶液中快速分解产生 ,在碱性溶液中较稳定。
,在碱性溶液中较稳定。
(1) 中铁元素的化合价为
中铁元素的化合价为_______ ,具有强氧化性。
(2)一种制备 的方法如下。
的方法如下。 的电极反应式:
的电极反应式:_______ 。
②阴极室 的浓度提高,结合电极反应式解释原因:
的浓度提高,结合电极反应式解释原因:_______ 。
(3)向含 的溶液中加入
的溶液中加入 固体,析出
固体,析出 固体,再用稀
固体,再用稀 溶液洗涤,得到
溶液洗涤,得到 产品。用化学方程式解释不能用水洗涤
产品。用化学方程式解释不能用水洗涤 的原因:
的原因:_______ 。
(4)称取 制得的
制得的 产品,加入足量
产品,加入足量 溶液,充分反应后,加入
溶液,充分反应后,加入 调节溶液
调节溶液 ,用
,用 溶液进行滴定,消耗
溶液进行滴定,消耗 溶液
溶液 。计算
。计算 样品的质量分数:
样品的质量分数:_______ 。[已知: ]
]
涉及的反应有:

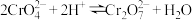
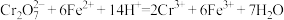
(5)电解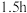 后,测得
后,测得 ,
, 。
。
已知: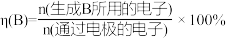

① ,说明除
,说明除 之外,还有其他含铁物质生成。经检验,阳极产物中含铁物质仅有
之外,还有其他含铁物质生成。经检验,阳极产物中含铁物质仅有 和
和 ,则
,则
_______ 。
②判断阳极有水(或 )放电,判断依据:
)放电,判断依据:
i.水(或 )有还原性;
)有还原性;
ii._______ 。
 是一种高效多功能的新型消毒剂。
是一种高效多功能的新型消毒剂。已知:
 微溶于水,在酸性或中性溶液中快速分解产生
微溶于水,在酸性或中性溶液中快速分解产生 ,在碱性溶液中较稳定。
,在碱性溶液中较稳定。(1)
 中铁元素的化合价为
中铁元素的化合价为(2)一种制备
 的方法如下。
的方法如下。
 的电极反应式:
的电极反应式:②阴极室
 的浓度提高,结合电极反应式解释原因:
的浓度提高,结合电极反应式解释原因:(3)向含
 的溶液中加入
的溶液中加入 固体,析出
固体,析出 固体,再用稀
固体,再用稀 溶液洗涤,得到
溶液洗涤,得到 产品。用化学方程式解释不能用水洗涤
产品。用化学方程式解释不能用水洗涤 的原因:
的原因:(4)称取
 制得的
制得的 产品,加入足量
产品,加入足量 溶液,充分反应后,加入
溶液,充分反应后,加入 调节溶液
调节溶液 ,用
,用 溶液进行滴定,消耗
溶液进行滴定,消耗 溶液
溶液 。计算
。计算 样品的质量分数:
样品的质量分数: ]
]涉及的反应有:

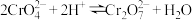
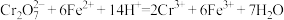
(5)电解
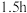 后,测得
后,测得 ,
, 。
。已知:
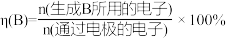

①
 ,说明除
,说明除 之外,还有其他含铁物质生成。经检验,阳极产物中含铁物质仅有
之外,还有其他含铁物质生成。经检验,阳极产物中含铁物质仅有 和
和 ,则
,则
②判断阳极有水(或
 )放电,判断依据:
)放电,判断依据:i.水(或
 )有还原性;
)有还原性;ii.
您最近一年使用:0次
2023-05-07更新
|
624次组卷
|
3卷引用:北京市朝阳区2022-2023年高三下学期第二次模拟考试化学试题
名校
7 . 为回收利用废钒催化剂(含有V2O5、VOSO4及不溶性残渣),科研人员研制了一种回收V2O5的新工艺,主要流程如下图。

已知:i.部分含钒物质常温下在水中的溶解性如下表所示:
ii.VO + 2 OH-
+ 2 OH-  VO
VO +H2O
+H2O
回答下列问题:
(1)用水浸泡废钒催化剂,为了提高单位时间内废钒的浸出率,可以采取的措施为_______ ; _______ (写两条)。
(2)滤液1和滤液2中含钒的主要物质成分相同。在滤渣1中加入Na2SO3和过量H2SO4溶液发生反应的化学方程式为_______ 。
(3)生成VO 的反应中消耗1mol KClO3时转移6mol电子,该反应的离子方程式为
的反应中消耗1mol KClO3时转移6mol电子,该反应的离子方程式为_______ 。
(4)结合化学用语,用平衡移动原理解释加入氨水的作用为_______ 。
(5)最后钒以NH4VO3的形式沉淀出来。以沉钒率(NH4VO3沉淀中V的质量和废催化剂中V的质量之比)表示该步反应钒的回收率。请解释下图温度超过80℃以后,沉钒率下降的可能原因是_______ ;_______ (写两条)。

(6)测定产品中V2O5的纯度,称取a g产品,先用硫酸溶解,得到 (VO2)2SO4溶液,再加入b1 mL c1 mol·L−1 H2C2O4溶液(2VO +H2C2O4+2H+= 2VO2++2CO2↑+2H2O),最后用c2 mol·L-1 KMnO4溶液滴定过量的H2C2O4至终点,消耗KMnO4溶液的体积为b2 mL。已知MnO
+H2C2O4+2H+= 2VO2++2CO2↑+2H2O),最后用c2 mol·L-1 KMnO4溶液滴定过量的H2C2O4至终点,消耗KMnO4溶液的体积为b2 mL。已知MnO 被还原为Mn2+,假设杂质不参与反应。则产品中V2O5(摩尔质量:182 g·mol−1)的质量分数是
被还原为Mn2+,假设杂质不参与反应。则产品中V2O5(摩尔质量:182 g·mol−1)的质量分数是_______ (列出计算式)。

已知:i.部分含钒物质常温下在水中的溶解性如下表所示:
| 物质 | VOSO4 | V2O5 | NH4VO3 | (VO2)2SO4 |
| 溶解性 | 可溶 | 难溶 | 难溶 | 易溶 |
 + 2 OH-
+ 2 OH-  VO
VO +H2O
+H2O回答下列问题:
(1)用水浸泡废钒催化剂,为了提高单位时间内废钒的浸出率,可以采取的措施为
(2)滤液1和滤液2中含钒的主要物质成分相同。在滤渣1中加入Na2SO3和过量H2SO4溶液发生反应的化学方程式为
(3)生成VO
 的反应中消耗1mol KClO3时转移6mol电子,该反应的离子方程式为
的反应中消耗1mol KClO3时转移6mol电子,该反应的离子方程式为(4)结合化学用语,用平衡移动原理解释加入氨水的作用为
(5)最后钒以NH4VO3的形式沉淀出来。以沉钒率(NH4VO3沉淀中V的质量和废催化剂中V的质量之比)表示该步反应钒的回收率。请解释下图温度超过80℃以后,沉钒率下降的可能原因是

(6)测定产品中V2O5的纯度,称取a g产品,先用硫酸溶解,得到 (VO2)2SO4溶液,再加入b1 mL c1 mol·L−1 H2C2O4溶液(2VO
 +H2C2O4+2H+= 2VO2++2CO2↑+2H2O),最后用c2 mol·L-1 KMnO4溶液滴定过量的H2C2O4至终点,消耗KMnO4溶液的体积为b2 mL。已知MnO
+H2C2O4+2H+= 2VO2++2CO2↑+2H2O),最后用c2 mol·L-1 KMnO4溶液滴定过量的H2C2O4至终点,消耗KMnO4溶液的体积为b2 mL。已知MnO 被还原为Mn2+,假设杂质不参与反应。则产品中V2O5(摩尔质量:182 g·mol−1)的质量分数是
被还原为Mn2+,假设杂质不参与反应。则产品中V2O5(摩尔质量:182 g·mol−1)的质量分数是
您最近一年使用:0次
2023-04-14更新
|
544次组卷
|
5卷引用:北京市门头沟区2023届高三下学期一模考试化学试题
名校
解题方法
8 . MnO2是重要化工原料,由软锰矿制备MnO2的一种工艺流程如下:
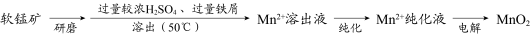
资料:
①软锰矿的主要成分为MnO2,主要杂质有Al2O3和SiO2。
②金属离子沉淀的pH
③该工艺条件下,MnO2与H2SO4不反应。
(1)溶出
①溶出前,软锰矿需研磨。目的是___________ 。
②溶出时,Fe的氧化过程及得到Mn2+的主要途径如图所示。
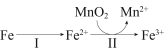
i、II是从软锰矿中溶出Mn2+的主要反应,反应的离子方程式是___________ 。
ii、若Fe2+全部来自于反应Fe+2H+=Fe2++H2↑,完全溶出Mn2+所需Fe与MnO2的物质的量比值为2。而实际比值(0.9)小于2,原因是___________ 。
(2)纯化
已知:MnO2的氧化性与溶液pH有关。纯化时先加入MnO2,后加入NH3·H2O,调溶液pH≈5。说明试剂加入顺序及调节pH的原因:___________ 。
(3)产品纯度测定
向ag产品中依次加入足量bgNa2C2O4和足量稀H2SO4,加热至充分反应,再用c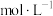 KMnO4溶液滴定剩余Na2C2O4至终点,消耗KMnO4溶液的体积为dL。(已知:MnO2及MnO
KMnO4溶液滴定剩余Na2C2O4至终点,消耗KMnO4溶液的体积为dL。(已知:MnO2及MnO 均被还原为Mn2+。相对分子质量:MnO286.94;Na2C2O4134.0)
均被还原为Mn2+。相对分子质量:MnO286.94;Na2C2O4134.0)
产品纯度为___________ (用质量分数表示)。
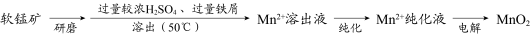
资料:
①软锰矿的主要成分为MnO2,主要杂质有Al2O3和SiO2。
②金属离子沉淀的pH
| Fe3+ | Al3+ | Mn2+ | Fe2+ | |
| 开始沉淀时 | 1.5 | 3.4 | 5.8 | 6.3 |
| 完全沉淀时 | 2.8 | 4.7 | 7.8 | 8.3 |
(1)溶出
①溶出前,软锰矿需研磨。目的是
②溶出时,Fe的氧化过程及得到Mn2+的主要途径如图所示。
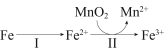
i、II是从软锰矿中溶出Mn2+的主要反应,反应的离子方程式是
ii、若Fe2+全部来自于反应Fe+2H+=Fe2++H2↑,完全溶出Mn2+所需Fe与MnO2的物质的量比值为2。而实际比值(0.9)小于2,原因是
(2)纯化
已知:MnO2的氧化性与溶液pH有关。纯化时先加入MnO2,后加入NH3·H2O,调溶液pH≈5。说明试剂加入顺序及调节pH的原因:
(3)产品纯度测定
向ag产品中依次加入足量bgNa2C2O4和足量稀H2SO4,加热至充分反应,再用c
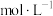 KMnO4溶液滴定剩余Na2C2O4至终点,消耗KMnO4溶液的体积为dL。(已知:MnO2及MnO
KMnO4溶液滴定剩余Na2C2O4至终点,消耗KMnO4溶液的体积为dL。(已知:MnO2及MnO 均被还原为Mn2+。相对分子质量:MnO286.94;Na2C2O4134.0)
均被还原为Mn2+。相对分子质量:MnO286.94;Na2C2O4134.0)产品纯度为
您最近一年使用:0次
名校
9 . Mn及其化合物在工业生产中具有重要的用途。
I.以含MnCO3的矿石为原料,经硫酸溶解得到含Mn2+的溶液,再经一系列处理后进行电解,获得金属Mn。
(1)Mn在_______ (填“阳极”或“阴极”)生成。
(2)阳极泥中含有MnO2,写出产生MnO2的电极反应式:_______ 。
II.阳极泥中除含锰元素外,还含有铅元素,采用如下方法可将它们分别转化为活性MnO2和PbO。
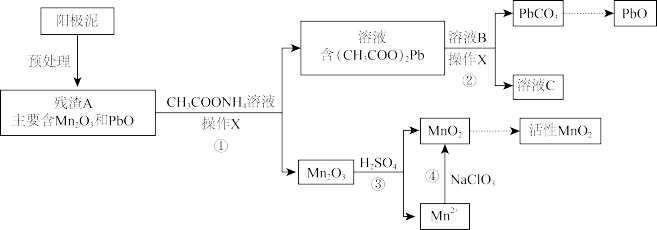
已知:(CH3COO)2Pb在水中难解离。
(3)操作X为_______ 。
(4)①中反应的离子方程式为_______ 。
(5)滤液C能循环使用,②中溶液B的溶质为_______ 。
(6)a.为了将③中Mn2O3完全转化为MnO2,理论上④中加入的NaClO3与Mn2O3的物质的量之比为_______ (已知NaClO3的还原产物为NaCl)。
b.加入NaClO3前,需将溶液pH调大至6左右。调节pH的目的是_______ 。
(7)活性MnO2纯度的测定
i.用V1mLc1mol∙L-1Na2C2O4溶液(H2SO4)酸化)溶解wg活性MnO2样。品。(MnO2+ +4H+=2CO2↑+Mn2++2H2O)
+4H+=2CO2↑+Mn2++2H2O)
ii.用c2mol∙L-1酸性KMnO4标准溶液滴定i中剩余的 消耗KMnO4标准溶液V2mL。(5
消耗KMnO4标准溶液V2mL。(5 +2
+2 +16H+=2Mn2++10CO2↑+8H2O)
+16H+=2Mn2++10CO2↑+8H2O)
样品中MnO2的质量分数=_______ [M(MnO2)=87g·mol-1]。
I.以含MnCO3的矿石为原料,经硫酸溶解得到含Mn2+的溶液,再经一系列处理后进行电解,获得金属Mn。
(1)Mn在
(2)阳极泥中含有MnO2,写出产生MnO2的电极反应式:
II.阳极泥中除含锰元素外,还含有铅元素,采用如下方法可将它们分别转化为活性MnO2和PbO。

已知:(CH3COO)2Pb在水中难解离。
(3)操作X为
(4)①中反应的离子方程式为
(5)滤液C能循环使用,②中溶液B的溶质为
(6)a.为了将③中Mn2O3完全转化为MnO2,理论上④中加入的NaClO3与Mn2O3的物质的量之比为
b.加入NaClO3前,需将溶液pH调大至6左右。调节pH的目的是
(7)活性MnO2纯度的测定
i.用V1mLc1mol∙L-1Na2C2O4溶液(H2SO4)酸化)溶解wg活性MnO2样。品。(MnO2+
 +4H+=2CO2↑+Mn2++2H2O)
+4H+=2CO2↑+Mn2++2H2O)ii.用c2mol∙L-1酸性KMnO4标准溶液滴定i中剩余的
 消耗KMnO4标准溶液V2mL。(5
消耗KMnO4标准溶液V2mL。(5 +2
+2 +16H+=2Mn2++10CO2↑+8H2O)
+16H+=2Mn2++10CO2↑+8H2O)样品中MnO2的质量分数=
您最近一年使用:0次
2022-05-08更新
|
494次组卷
|
4卷引用:北京市东城区2022届高三综合练习(二模)化学试题
名校
10 . 纳米Fe3O4在磁流体、催化剂、医学等领域具有广阔的应用前景。氧化共沉淀制备纳米Fe3O4的方法如下:
Ⅰ.Fe2+的氧化:将FeSO4溶液用NaOH溶液调节pH至a,再加入H2O2溶液,立即得到FeOOH红棕色悬浊液。
(1)①若用NaOH溶液调节pH过高会产生白色沉淀,该反应的离子方程式是___________ 。
②该白色沉淀置于空气中能观察的现象是___________ 。
③上述反应完成后,测得a值与FeOOH产率及其生成后溶液pH的关系,结果如下:
用离子方程式解释FeOOH生成后溶液pH下降的原因:___________ 。
(2)经检验:当a=7时,产物中存在大量Fe2O3。对Fe2O3的产生提出两种假设:
i.反应过程中溶液酸性增强,导致FeOOH向Fe2O3的转化;
ii.溶液中存在少量Fe2+,导致FeOOH向Fe2O3的转化。
①经分析,假设i不成立的实验依据是___________ 。
②其他条件相同时,向FeOOH浊液中加入不同浓度Fe2+,30min后测定物质的组成,结果如下:
以上结果表明:___________ 。
③a=7和a=9时,FeOOH产率差异很大的原因是___________ 。
Ⅱ.Fe2+和Fe3+共沉淀:向FeOOH红棕色悬浊液中同时加入FeSO4溶液和NaOH浓溶液进行共沉淀,再将此混合液加热回流、冷却、过滤、洗涤、干燥,得到纳米Fe3O4。
(3)共沉淀时的反应条件对产物纯度和产率的影响极大。
①共沉淀pH过高时,会导致FeSO4溶液被快速氧化;共沉淀pH过低时,得到的纳米Fe3O4中会混有的物质是___________ 。
②已知N=n(FeOOH)/n(Fe2+),其他条件一定时,测得纳米Fe3O4的产率随N的变化曲线如下图所示:
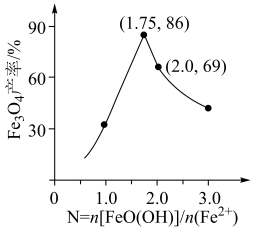
经理论分析,N=2共沉淀时纳米Fe3O4产率应最高,事实并非如此的可能原因是___________ 。
(4)测量制得的纳米Fe3O4中n(Fe3+)/n(Fe2+):取ag样品,加入足量盐酸使之完全溶解,加入SnCl2将Fe3+还原为Fe2+;除去过量SnCl2后,用c1mol/LK2Cr2O7标准溶液滴定(还原产物为Cr3+),消耗K2Cr2O7溶液的体积为v1mL,另取ag样品,加入足量稀硫酸使之完全溶解,用c2mol/LKMnO4标准溶液滴定至终点,消耗KMnO4溶液的体积为v2mL,则样品中n(Fe3+)/n(Fe2+)为___________ 。
Ⅰ.Fe2+的氧化:将FeSO4溶液用NaOH溶液调节pH至a,再加入H2O2溶液,立即得到FeOOH红棕色悬浊液。
(1)①若用NaOH溶液调节pH过高会产生白色沉淀,该反应的离子方程式是
②该白色沉淀置于空气中能观察的现象是
③上述反应完成后,测得a值与FeOOH产率及其生成后溶液pH的关系,结果如下:
| a | 7.0 | 8.0 | 9.0 |
| FeO(OH)的产率 | <50% | 95% | >95% |
| FeO(OH)生成后的pH | 接近4 | 接近4 | 接近4 |
(2)经检验:当a=7时,产物中存在大量Fe2O3。对Fe2O3的产生提出两种假设:
i.反应过程中溶液酸性增强,导致FeOOH向Fe2O3的转化;
ii.溶液中存在少量Fe2+,导致FeOOH向Fe2O3的转化。
①经分析,假设i不成立的实验依据是
②其他条件相同时,向FeOOH浊液中加入不同浓度Fe2+,30min后测定物质的组成,结果如下:
| c(Fe2+)/mol/L | FeO(OH)百分含量/% | Fe2O3百分含量/% |
| 0.00 | 100 | 0 |
| 0.01 | 40 | 60 |
| 0.02 | 0 | 100 |
③a=7和a=9时,FeOOH产率差异很大的原因是
Ⅱ.Fe2+和Fe3+共沉淀:向FeOOH红棕色悬浊液中同时加入FeSO4溶液和NaOH浓溶液进行共沉淀,再将此混合液加热回流、冷却、过滤、洗涤、干燥,得到纳米Fe3O4。
(3)共沉淀时的反应条件对产物纯度和产率的影响极大。
①共沉淀pH过高时,会导致FeSO4溶液被快速氧化;共沉淀pH过低时,得到的纳米Fe3O4中会混有的物质是
②已知N=n(FeOOH)/n(Fe2+),其他条件一定时,测得纳米Fe3O4的产率随N的变化曲线如下图所示:

经理论分析,N=2共沉淀时纳米Fe3O4产率应最高,事实并非如此的可能原因是
(4)测量制得的纳米Fe3O4中n(Fe3+)/n(Fe2+):取ag样品,加入足量盐酸使之完全溶解,加入SnCl2将Fe3+还原为Fe2+;除去过量SnCl2后,用c1mol/LK2Cr2O7标准溶液滴定(还原产物为Cr3+),消耗K2Cr2O7溶液的体积为v1mL,另取ag样品,加入足量稀硫酸使之完全溶解,用c2mol/LKMnO4标准溶液滴定至终点,消耗KMnO4溶液的体积为v2mL,则样品中n(Fe3+)/n(Fe2+)为
您最近一年使用:0次



