名校
1 . 已知下列变化过程中,2个 参加反应时,共转移4个电子。
参加反应时,共转移4个电子。
 则x的值为
则x的值为
 参加反应时,共转移4个电子。
参加反应时,共转移4个电子。
 则x的值为
则x的值为| A.1 | B.2 | C.3 | D.4 |
您最近一年使用:0次
名校
2 . 制取氯酸钾的化学方程式是: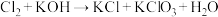 (方程式未配平),该反应的氧化剂与还原剂物质的量之比为
(方程式未配平),该反应的氧化剂与还原剂物质的量之比为
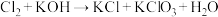 (方程式未配平),该反应的氧化剂与还原剂物质的量之比为
(方程式未配平),该反应的氧化剂与还原剂物质的量之比为| A.1∶1 | B.1∶2 | C.5∶1 | D.6∶1 |
您最近一年使用:0次
名校
解题方法
3 . 铜和三氧化二铁在工农业生产中用途广泛,用黄铜矿(主要成分为CuFeS2,其中Cu为+2价、Fe为+2价)制取铜和三氧化二铁的工艺流程如图所示

(1)将黄铜矿粉碎的目的是___________ 。
(2)高温焙烧时发生的反应是CuFeS2+O2 SO2+FeS+Cu,该反应中,还原产物是
SO2+FeS+Cu,该反应中,还原产物是___________ ;1molO2参加反应时,反应中转移电子___________ mol。
(3)滤液A中含有FeCl2,向滤液A通入Cl2的离子方程式为___________ 。
(4)向溶液B中通入NH3后发生反应的离子方程式为___________ 。
(5)操作b后检验滤渣已经洗涤干净的实验操作为___________ 。
(6)工业上用生物法处理H2S的原理为(硫杆菌有较强的活性作催化剂):H2S+Fe2(SO4)3=S↓+2FeSO4+H2SO4;4FeSO4+O2+2H2SO4=2Fe2(SO4)3+2H2O,由图甲和图乙判断使用硫杆菌的最佳条件为___________ ,若反应温度过高,反应速率下降,其原因是___________ 。


(1)将黄铜矿粉碎的目的是
(2)高温焙烧时发生的反应是CuFeS2+O2
 SO2+FeS+Cu,该反应中,还原产物是
SO2+FeS+Cu,该反应中,还原产物是(3)滤液A中含有FeCl2,向滤液A通入Cl2的离子方程式为
(4)向溶液B中通入NH3后发生反应的离子方程式为
(5)操作b后检验滤渣已经洗涤干净的实验操作为
(6)工业上用生物法处理H2S的原理为(硫杆菌有较强的活性作催化剂):H2S+Fe2(SO4)3=S↓+2FeSO4+H2SO4;4FeSO4+O2+2H2SO4=2Fe2(SO4)3+2H2O,由图甲和图乙判断使用硫杆菌的最佳条件为

您最近一年使用:0次
4 . 回答下列问题
(1)氨分解反应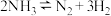 在容积为
在容积为 的密闭容器内进行。已知起始时氨气的物质的量为
的密闭容器内进行。已知起始时氨气的物质的量为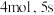 末为
末为 ,则用氨气表示该反应的速率为
,则用氨气表示该反应的速率为______ 氨分解反应的逆反应为合成氨,当消耗 时,放出
时,放出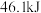 的热量,写出该反应的热化学方程式
的热量,写出该反应的热化学方程式______ 。
(2)如图所示,将锌、铜通过导线连接,置于稀硫酸中。
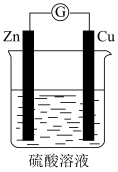
①负极电极反应式为______ 。
②正极电极反应式为______ 。
③溶液中 由
由______ (填“锌”或者“铜”下同)向_______ 移动。
④若反应过程中有 电子发生转移,则生成的氢气在标准状况下的体积为
电子发生转移,则生成的氢气在标准状况下的体积为______ 。
(1)氨分解反应
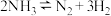 在容积为
在容积为 的密闭容器内进行。已知起始时氨气的物质的量为
的密闭容器内进行。已知起始时氨气的物质的量为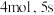 末为
末为 ,则用氨气表示该反应的速率为
,则用氨气表示该反应的速率为 时,放出
时,放出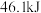 的热量,写出该反应的热化学方程式
的热量,写出该反应的热化学方程式(2)如图所示,将锌、铜通过导线连接,置于稀硫酸中。

①负极电极反应式为
②正极电极反应式为
③溶液中
 由
由④若反应过程中有
 电子发生转移,则生成的氢气在标准状况下的体积为
电子发生转移,则生成的氢气在标准状况下的体积为
您最近一年使用:0次
名校
5 . 亚氯酸钠 主要用于棉纺,造纸业的漂白,也用于食品消毒、水处理等。以氯酸钠等为原料制备亚氯酸钠的工艺流程如下
主要用于棉纺,造纸业的漂白,也用于食品消毒、水处理等。以氯酸钠等为原料制备亚氯酸钠的工艺流程如下
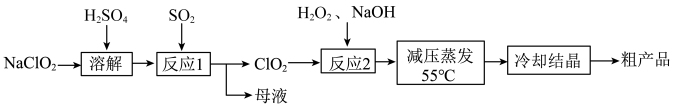
已知:①亚氯酸钠 受热易分解;②高浓度的
受热易分解;②高浓度的 易爆炸。
易爆炸。
(1) 与
与 因有强氧化性而用作常用消毒剂,消毒时均被还原为
因有强氧化性而用作常用消毒剂,消毒时均被还原为 ,则
,则 的消毒能力(转移电子的物质的量)是等质量的
的消毒能力(转移电子的物质的量)是等质量的 的
的______ 倍(保留小数点后一位)。“反应1”需要鼓入空气,空气的作用是______ 。
(2)“反应2”发生反应的化学方程式:______ 。“反应2”需要控制反应温度不能过高,温度过高可能导致______ 。
(3)从“母液”中可回收的主要物质是______ 。
(4)为探究 的氧化性,可以选择下列试剂
的氧化性,可以选择下列试剂______ 。根据选择的试剂,描述能体现 氧化性的实验现象是
氧化性的实验现象是______
A.淀粉-KI溶液 B.酸性高锰酸钾溶液 C.氯水 D. 溶液
溶液
 主要用于棉纺,造纸业的漂白,也用于食品消毒、水处理等。以氯酸钠等为原料制备亚氯酸钠的工艺流程如下
主要用于棉纺,造纸业的漂白,也用于食品消毒、水处理等。以氯酸钠等为原料制备亚氯酸钠的工艺流程如下
已知:①亚氯酸钠
 受热易分解;②高浓度的
受热易分解;②高浓度的 易爆炸。
易爆炸。(1)
 与
与 因有强氧化性而用作常用消毒剂,消毒时均被还原为
因有强氧化性而用作常用消毒剂,消毒时均被还原为 ,则
,则 的消毒能力(转移电子的物质的量)是等质量的
的消毒能力(转移电子的物质的量)是等质量的 的
的(2)“反应2”发生反应的化学方程式:
(3)从“母液”中可回收的主要物质是
(4)为探究
 的氧化性,可以选择下列试剂
的氧化性,可以选择下列试剂 氧化性的实验现象是
氧化性的实验现象是A.淀粉-KI溶液 B.酸性高锰酸钾溶液 C.氯水 D.
 溶液
溶液
您最近一年使用:0次
名校
6 . 我国古代四大发明之一的黑火药是由硫黄粉、硝酸钾和木炭粉按一定比例混合而成的,爆炸时的反应为:S+2KNO3+3C=K2S+N2↑+3CO2↑。下列说法错误的是
| A.氧化剂是KNO3和S |
| B.木炭被氧化 |
| C.每生成1mol的CO2转移8NA个电子 |
| D.KNO3的氧化性强于CO2 |
您最近一年使用:0次
2024-03-12更新
|
86次组卷
|
2卷引用:青海省西宁市海湖中学2023-2024学年高一下学期开学考试化学试卷
名校
解题方法
7 .  常作为漂白布匹后的“脱氯剂”,
常作为漂白布匹后的“脱氯剂”, 和
和 反应的产物之一为
反应的产物之一为 ,下列说法错误的是
,下列说法错误的是
 常作为漂白布匹后的“脱氯剂”,
常作为漂白布匹后的“脱氯剂”, 和
和 反应的产物之一为
反应的产物之一为 ,下列说法错误的是
,下列说法错误的是A.该反应中还原剂是 | B. 参与该反应,且作氧化剂 参与该反应,且作氧化剂 |
C.根据该反应可判断氧化性: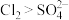 | D.该反应中每消耗1mol ,可脱去4mol ,可脱去4mol |
您最近一年使用:0次
名校
解题方法
8 . 常温下,实验室可用 和浓盐酸反应制取
和浓盐酸反应制取 ,下列说法正确的是
,下列说法正确的是
 和浓盐酸反应制取
和浓盐酸反应制取 ,下列说法正确的是
,下列说法正确的是A.该制备反应中 被氧化 被氧化 |
B.该制备反应中氧化剂与还原剂的物质的量之比为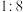 |
C.该制备反应说明氧化性: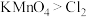 |
D.该制备反应中,若浓盐酸足量,则每消耗 ,生成 ,生成 |
您最近一年使用:0次
名校
9 . 水体中氨氮含量超标会造成水体富营养化,用次氯酸钙除去氨氮的原理如图所示。下列说法错误的是

| A.标准状况下,4.48LHCl气体溶于100mL水中形成的溶液浓度为2mol/L |
B.反应②每生成 ,转移6mol电子 ,转移6mol电子 |
C.标准状况下,22.4L二氧化碳所含的共用电子对数目为 |
D. 在该反应中能够循环利用 在该反应中能够循环利用 |
您最近一年使用:0次
2024-03-11更新
|
57次组卷
|
2卷引用:黑龙江省哈尔滨市第九中学校2023-2024学年高一下学期开学学业阶段性评价考试化学试卷
名校
10 . 常温下,关于反应 ,下列说法正确的是
,下列说法正确的是
 ,下列说法正确的是
,下列说法正确的是A.该反应的还原产物是 |
B.每生成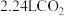 ,反应共转移 ,反应共转移 电子 电子 |
C.氧化剂与还原剂的物质的量之比为 |
D.该反应体现了 单质的氧化性 单质的氧化性 |
您最近一年使用:0次



