名校
1 . 为消除燃煤烟气中含有的 、
、 ,研究者提出若干烟气“脱硫”“脱硝”的方法。
,研究者提出若干烟气“脱硫”“脱硝”的方法。
【方法一】以NaClO作为吸收剂进行一体化“脱硫”“脱硝”,将烟气中的 、NO转化为
、NO转化为 、
、 。
。
(1)

 溶液理论上最多能吸收标准状况下NO的体积为
溶液理论上最多能吸收标准状况下NO的体积为_______ L。
(2)实验室利用模拟烟气(模拟烟气中 和NO的物质的量之比为
和NO的物质的量之比为 )探究该方法“脱硫”“脱硝”的效果,一定时间内,温度对硫、硝脱除率的影响曲线如图所示。
)探究该方法“脱硫”“脱硝”的效果,一定时间内,温度对硫、硝脱除率的影响曲线如图所示。

①此方法“脱硫”“脱硝”探究实验的最佳温度为_______ ; 的脱除率高于
的脱除率高于 ,其原因除
,其原因除 的还原性比
的还原性比 强外,还可能是
强外,还可能是_______ 。
② 时,吸收液中烟气转化生成的
时,吸收液中烟气转化生成的 和
和 的物质的量之比为
的物质的量之比为_______ 。
【方法二】 技术(选择性催化还原氮氧化物)
技术(选择性催化还原氮氧化物)
研究表明,铁基催化剂在260~300℃范围内实现 技术的过程如图所示。
技术的过程如图所示。
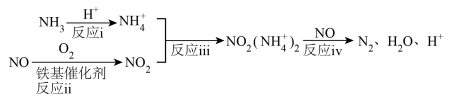
(3)根据上述机理, 在反应过程中的作用为
在反应过程中的作用为_______ ;等物质的量的 、
、 在有氧条件下转化为
在有氧条件下转化为 的总反应化学方程式为
的总反应化学方程式为_______ ;
(4)若使用锰基催化剂(活性物质为 )代替铁基催化剂,烟气中含有的
)代替铁基催化剂,烟气中含有的 会使催化剂失效而降低
会使催化剂失效而降低 脱除率,用化学方程式表示催化剂失效的原因:
脱除率,用化学方程式表示催化剂失效的原因:_______ 。
(5)向反应体系中添加 可显著提高
可显著提高 脱除率,原因是
脱除率,原因是 与
与 反应生成
反应生成 和阴离子M;阴离子M再与
和阴离子M;阴离子M再与 发生反应转化为
发生反应转化为 ,则阴离子M为
,则阴离子M为_______ 。
 、
、 ,研究者提出若干烟气“脱硫”“脱硝”的方法。
,研究者提出若干烟气“脱硫”“脱硝”的方法。【方法一】以NaClO作为吸收剂进行一体化“脱硫”“脱硝”,将烟气中的
 、NO转化为
、NO转化为 、
、 。
。(1)


 溶液理论上最多能吸收标准状况下NO的体积为
溶液理论上最多能吸收标准状况下NO的体积为(2)实验室利用模拟烟气(模拟烟气中
 和NO的物质的量之比为
和NO的物质的量之比为 )探究该方法“脱硫”“脱硝”的效果,一定时间内,温度对硫、硝脱除率的影响曲线如图所示。
)探究该方法“脱硫”“脱硝”的效果,一定时间内,温度对硫、硝脱除率的影响曲线如图所示。
①此方法“脱硫”“脱硝”探究实验的最佳温度为
 的脱除率高于
的脱除率高于 ,其原因除
,其原因除 的还原性比
的还原性比 强外,还可能是
强外,还可能是②
 时,吸收液中烟气转化生成的
时,吸收液中烟气转化生成的 和
和 的物质的量之比为
的物质的量之比为【方法二】
 技术(选择性催化还原氮氧化物)
技术(选择性催化还原氮氧化物)研究表明,铁基催化剂在260~300℃范围内实现
 技术的过程如图所示。
技术的过程如图所示。
(3)根据上述机理,
 在反应过程中的作用为
在反应过程中的作用为 、
、 在有氧条件下转化为
在有氧条件下转化为 的总反应化学方程式为
的总反应化学方程式为(4)若使用锰基催化剂(活性物质为
 )代替铁基催化剂,烟气中含有的
)代替铁基催化剂,烟气中含有的 会使催化剂失效而降低
会使催化剂失效而降低 脱除率,用化学方程式表示催化剂失效的原因:
脱除率,用化学方程式表示催化剂失效的原因:(5)向反应体系中添加
 可显著提高
可显著提高 脱除率,原因是
脱除率,原因是 与
与 反应生成
反应生成 和阴离子M;阴离子M再与
和阴离子M;阴离子M再与 发生反应转化为
发生反应转化为 ,则阴离子M为
,则阴离子M为
您最近一年使用:0次
2022-11-19更新
|
208次组卷
|
2卷引用:甘肃省永昌县第一高级中学2023-2024学年高三上学期期中考试化学试题
名校
解题方法
2 . 碱式硫酸铁[Fe(OH)SO4]是一种絮疑剂,常用于污水处理。工业上利用废铁屑(含少量Al2O3、Fe2O3等)生产碱式硫酸铁的工艺流程如图所示。
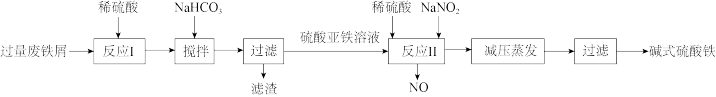
下列说法错误的是

下列说法错误的是
| A.“反应I”后的溶液中主要存在的阳离子有H+、Fe2+、Al3+ |
| B.“反应II”中加入稀硫酸可抑制Fe3+的水解 |
C.“反应II”对应的离子方程式为Fe2++NO +2H+=Fe3++NO↑+H2O +2H+=Fe3++NO↑+H2O |
| D.若用O2代替NaNO2,则每消耗112mL(标准状况)O2相当于节约了2.76gNaNO2 |
您最近一年使用:0次
2022-08-23更新
|
827次组卷
|
3卷引用:甘肃省兰州市西北师范大学附属中学2022-2023学年高三上学期期中考试化学试题
3 . 合理利用工业烟尘,变废为宝,对保护环境具有重要意义。一种铜冶炼烟尘(主要成分是CuO、ZnO、PbO、SiO2、As2O3)为原料回收铜和锌的流程如图。回答下列问题:
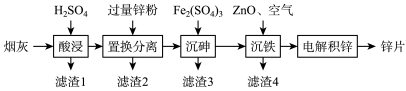
(1)写出能提高“酸浸”浸出率的两个措施____ 。
(2)“滤渣1”的主要成分是____ 。
(3)已知As2O3是一种两性氧化物,“滤渣3”的成分为FeAsO4,则“沉砷”过程中发生的离子反应方程式为____ 。
(4)“沉铁”通入过量空气的目的是____ 。
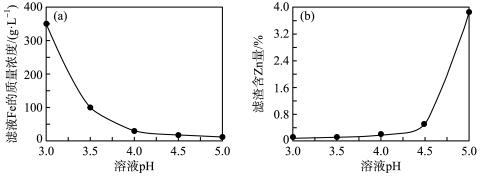
(5)加入ZnO的目的是调节溶液的pH,如图所示是溶液pH与滤液中Fe元素及滤渣中Zn元素的含量关系,则“沉铁”过程中溶液最合适的pH为____ 。
(6)“电解积锌”后的电解液可返回____ 工序继续使用。
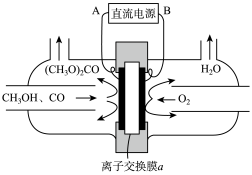
(7)合成碳酸二甲酯的工作原理如图所示。阳极的电极反应式为____ 。

(1)写出能提高“酸浸”浸出率的两个措施
(2)“滤渣1”的主要成分是
(3)已知As2O3是一种两性氧化物,“滤渣3”的成分为FeAsO4,则“沉砷”过程中发生的离子反应方程式为
(4)“沉铁”通入过量空气的目的是
(5)加入ZnO的目的是调节溶液的pH,如图所示是溶液pH与滤液中Fe元素及滤渣中Zn元素的含量关系,则“沉铁”过程中溶液最合适的pH为

(6)“电解积锌”后的电解液可返回
(7)合成碳酸二甲酯的工作原理如图所示。阳极的电极反应式为

您最近一年使用:0次
名校
解题方法
4 . 回答下列问题
(1)金属与硝酸反应通常不能生成H2,用3mol/L HNO3与过量铁粉反应,HNO3的还原产物主要是NO,请写出反应的离子方程式:___________ 。
有同学在查阅文献时发现文献有记载:HNO3与铁反应能产生H2。于是其小组进行了金属铁与硝酸反应能否产生H2及其有利条件的探究。
实验I:20℃,将过量铁粉溶于0.5mol·L-1 HNO3中,立即有无色气体生成,充分反应后,溶液几乎无色。
(2)检验气体:方法如图所示。
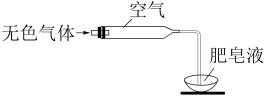
确认气体是H2,不含NO。实验证据是___________ 。
(3)检验溶液:取上层清液,等分两份
①向一份滴加K3[Fe(CN)6]溶液,___________ (填现象),说明含有Fe2+。
②向另一份加入NaOH溶液,产生灰绿色沉淀;加热至沸,有刺激性气味气体逸出,用湿润红色石蕊试纸检验,试纸变蓝。综合①、②,说明实验I中发生的反应有Fe+2H+=Fe2++H2↑,另外还有___________ (写出离子方程式)。
对H2产生的原因提出假设:在稀的酸性溶液中,HNO3中H+的氧化性大于NO ,验证如下:
,验证如下:
(4)实验II:将铜粉溶于0.5mol/L HNO3中。经检测,发现没有___________ 生成,初步证实假设不成立。
(5)再次查阅文献发现:在酸性介质中,尽管电极电势数据显示NO 离子是个颇强的氧化剂,然而动力学原因导致它在稀酸中的反应一般都很慢。于是小组改变条件重复实验I,向2mL 0.5mol·L-1 HNO3中加入过量铁粉,结果如下:
离子是个颇强的氧化剂,然而动力学原因导致它在稀酸中的反应一般都很慢。于是小组改变条件重复实验I,向2mL 0.5mol·L-1 HNO3中加入过量铁粉,结果如下:
经检验,实验III、IV、V中,NO 的还原产物与实验I相同。
的还原产物与实验I相同。
从反应速率的角度解释温度升高H2体积减少的原因___________ 。
(6)综上所述,有利于金属与硝酸反应生成氢气的条件是___________ 。
(1)金属与硝酸反应通常不能生成H2,用3mol/L HNO3与过量铁粉反应,HNO3的还原产物主要是NO,请写出反应的离子方程式:
有同学在查阅文献时发现文献有记载:HNO3与铁反应能产生H2。于是其小组进行了金属铁与硝酸反应能否产生H2及其有利条件的探究。
实验I:20℃,将过量铁粉溶于0.5mol·L-1 HNO3中,立即有无色气体生成,充分反应后,溶液几乎无色。
(2)检验气体:方法如图所示。

确认气体是H2,不含NO。实验证据是
(3)检验溶液:取上层清液,等分两份
①向一份滴加K3[Fe(CN)6]溶液,
②向另一份加入NaOH溶液,产生灰绿色沉淀;加热至沸,有刺激性气味气体逸出,用湿润红色石蕊试纸检验,试纸变蓝。综合①、②,说明实验I中发生的反应有Fe+2H+=Fe2++H2↑,另外还有
对H2产生的原因提出假设:在稀的酸性溶液中,HNO3中H+的氧化性大于NO
 ,验证如下:
,验证如下:(4)实验II:将铜粉溶于0.5mol/L HNO3中。经检测,发现没有
(5)再次查阅文献发现:在酸性介质中,尽管电极电势数据显示NO
 离子是个颇强的氧化剂,然而动力学原因导致它在稀酸中的反应一般都很慢。于是小组改变条件重复实验I,向2mL 0.5mol·L-1 HNO3中加入过量铁粉,结果如下:
离子是个颇强的氧化剂,然而动力学原因导致它在稀酸中的反应一般都很慢。于是小组改变条件重复实验I,向2mL 0.5mol·L-1 HNO3中加入过量铁粉,结果如下:| 实验序号 | Ⅲ | Ⅳ | Ⅴ |
| 温度 | 20℃ | 40℃ | 60℃ |
| 生成H2体积 | 6.0mL | 3.4mL | 2.6mL |
经检验,实验III、IV、V中,NO
 的还原产物与实验I相同。
的还原产物与实验I相同。从反应速率的角度解释温度升高H2体积减少的原因
(6)综上所述,有利于金属与硝酸反应生成氢气的条件是
您最近一年使用:0次
2022-01-19更新
|
1006次组卷
|
6卷引用:甘肃省兰州市西北师范大学附属中学2022-2023学年高三上学期期中考试化学试题
甘肃省兰州市西北师范大学附属中学2022-2023学年高三上学期期中考试化学试题湖北省宜城市第三高级中学2021-2022学年高三上学期期中考试化学试题(已下线)第18周 晚练题-备战2022年高考化学周测与晚练(新高考专用)广东省韶关市北江中等职业学校等九校 2021-2022学年高三上学期11月联考化学试题(已下线)化学(云南,安徽,黑龙江,山西,吉林五省通用B卷)-学易金卷:2023年高考第一次模拟考试卷(已下线)模拟卷03-2023年高三化学对接新高考全真模拟试卷(云南,安徽,黑龙江,山西,吉林五省通用)
名校
5 . 以铬矿石(主要成分为Cr2O3,还有Al2O3、SiO2等杂质)为原料制取红矾钠 (Na2Cr2O7·2H2O)的流程如图所示。

已知:I.Cr2O3在碱性条件下易被氧化;
II.高温条件下,Al2O3与Na2CO3发生的反应为:Al2O3 +Na2CO3=2NaAlO2 +CO2↑;
III.2CrO42-+2H+ Cr2O72- +H2O K=1.0×1012
Cr2O72- +H2O K=1.0×1012
(1)“煅烧”时,Cr2O3参加反应的化学方程式为_____ 。若“煅烧”操作最适宜的温度是800~900℃,则在实验室中进行此项操作时,应选择_____ 坩埚(填字母)。
a.陶瓷 b.玻璃 c.石英 d.铁
(2)流程中可循环利用的物质除CO2外还有_____ (填化学式)。
(3)“过滤II”所得沉淀主要有______ (填化学式)。
(4)由Na2Cr2O7溶液制备红矾钠的具体实验操作有_____ ,经洗涤、干燥得到红矾钠样品。
(5)“电解”时,利用以下装置将Na2CrO4溶液转化为Na2Cr2O7溶液,当a、b均为石墨电极时,a电极的电极反应式为____ 。若初始加入电解池中的c (Na2CrO4)=1.0mol·L-l,随着“电解”的进行,当溶液pH=6时,Na2CrO4的转化率为______ (忽略电解过程中溶液体积变化)。


已知:I.Cr2O3在碱性条件下易被氧化;
II.高温条件下,Al2O3与Na2CO3发生的反应为:Al2O3 +Na2CO3=2NaAlO2 +CO2↑;
III.2CrO42-+2H+
 Cr2O72- +H2O K=1.0×1012
Cr2O72- +H2O K=1.0×1012(1)“煅烧”时,Cr2O3参加反应的化学方程式为
a.陶瓷 b.玻璃 c.石英 d.铁
(2)流程中可循环利用的物质除CO2外还有
(3)“过滤II”所得沉淀主要有
(4)由Na2Cr2O7溶液制备红矾钠的具体实验操作有
(5)“电解”时,利用以下装置将Na2CrO4溶液转化为Na2Cr2O7溶液,当a、b均为石墨电极时,a电极的电极反应式为

您最近一年使用:0次
2019-10-13更新
|
479次组卷
|
4卷引用:甘肃省临夏回族自治州临夏中学2020届高三上学期期中考试化学试题
6 . 亚硝酸钠易溶于水,水溶液显碱性,有氧化性,也有还原性。由于NaNO2有毒性,将含该物质的废水直接排放会引起水体严重污染,所以这种废水必须处理后才能排放。处理方法之一如下:
NaNO2+KI+ →NO↑+I2+K2SO4+Na2SO4+____
(1)请完成该化学方程式并配平。
(2)将上述反应方程式改写为离子反应方程式:_____
(3)用上述反应来处理NaNO2并不是最佳方法,其原因是__ 。从环保角度来讲,要处理NaNO2,所用的物质的___ (填“氧化性”或“还原性”)应该比KI更__ (填“强”或“弱”)。
(4)简便鉴别亚硝酸钠和氯化钠的方法是____ 。
(5)已知亚硝酸钠可以与氯化铵反应生成氮气和氯化钠,写出该反应的化学反应方程式并用单线桥表示其电子转移的方向和数目。___
NaNO2+KI+ →NO↑+I2+K2SO4+Na2SO4+
(1)请完成该化学方程式并配平。
(2)将上述反应方程式改写为离子反应方程式:
(3)用上述反应来处理NaNO2并不是最佳方法,其原因是
(4)简便鉴别亚硝酸钠和氯化钠的方法是
(5)已知亚硝酸钠可以与氯化铵反应生成氮气和氯化钠,写出该反应的化学反应方程式并用单线桥表示其电子转移的方向和数目。
您最近一年使用:0次
2019-09-17更新
|
2975次组卷
|
7卷引用:甘肃省庆阳市华池县第一中学2022-2023学年高一上学期期中考试化学试题
名校
7 . 某离子反应涉及到 H2O、ClO-、NH4+、OH-、N2、Cl-等微粒,其中N2、ClO-的物质的量随时间变化的曲线如图所示,下列说法不正确 的是
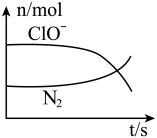

| A.该反应中Cl-为还原产物 |
| B.氧化剂与还原剂物质的量比为3:2 |
| C.消耗1 mol还原剂,转移6 mol电子 |
| D.氧化性:ClO-比 N2强 |
您最近一年使用:0次
2019-07-02更新
|
970次组卷
|
11卷引用:甘肃省兰州第一中学2019-2020学年高一上学期期中考试化学试题
甘肃省兰州第一中学2019-2020学年高一上学期期中考试化学试题福建省莆田第六中学2018-2019学年高一(实验班)下学期期中考试化学试题福建省莆田第六中学2018-2019学年高一下学期期中考试化学试题甘肃省嘉峪关市第一中学2021届高三上学期一模考试化学试卷(已下线)2019年10月6日《每日一题》必修1 —— 每周一测上海市格致中学2020届高三上学期开学考试化学试题鲁科版(2019)高一必修第一册第二章B 素养拓展区 过素养 学科素养拓展训练高一必修第一册(苏教2019版)专题3 B 素养拓展区 过素养 学科素养拓展训练辽宁省沈阳市东北育才学校2020届高三上学期第一次模拟考试化学试题湖北省十堰市第二中学2021-2022学年高一上学期12月考试化学试题福建省宁德博雅培文学校2022-2023学年高一上学期线上期末考试化学试题
解题方法
8 . FeCl3具有净水作用,但腐蚀设备,而聚合氯化铁是一种新型的絮凝剂,处理污水比FeCl3高效,且腐蚀性小。请回答下列问题:
(1)FeCl3净水的原理是____________ 。FeCl3溶液腐蚀钢铁设备,除H+作用外,另一主要原因是(用离子方程式表示)_______________ 。
(2)为节约成本,工业上用NaClO3氧化酸性FeCl2废液得到FeCl3。
①若酸性FeCl2废液中c(Fe2+)=2.0×10-2mol·L-1,c(Fe3+)=1.0×10-3mol·L-1,c(Cl-)=5.3×10-2mol·L-1,则该溶液的pH约为_________________ 。
②完成NaClO3氧化FeCl2的离子方程式:_____ _____ +______Fe2++______=_____Cl-+_____Fe3++______ 。
+______Fe2++______=_____Cl-+_____Fe3++______ 。
(3)FeCl3在溶液中分三步水解:Fe3++H2O Fe(OH)2++H+ K1
Fe(OH)2++H+ K1
Fe(OH)2++H2O
 +H+ K2
+H+ K2  +H2O
+H2O Fe(OH)3+H+ K3
Fe(OH)3+H+ K3
通过控制条件,以上水解产物聚合,生成聚合氧化铁,离子方程式为:
xFe3++yH2O
 +yH+,欲使平衡正向移动可采用的方法是(填序号)___________。
+yH+,欲使平衡正向移动可采用的方法是(填序号)___________。
(1)FeCl3净水的原理是
(2)为节约成本,工业上用NaClO3氧化酸性FeCl2废液得到FeCl3。
①若酸性FeCl2废液中c(Fe2+)=2.0×10-2mol·L-1,c(Fe3+)=1.0×10-3mol·L-1,c(Cl-)=5.3×10-2mol·L-1,则该溶液的pH约为
②完成NaClO3氧化FeCl2的离子方程式:
 +______Fe2++______=_____Cl-+_____Fe3++______ 。
+______Fe2++______=_____Cl-+_____Fe3++______ 。(3)FeCl3在溶液中分三步水解:Fe3++H2O
 Fe(OH)2++H+ K1
Fe(OH)2++H+ K1Fe(OH)2++H2O

 +H+ K2
+H+ K2  +H2O
+H2O Fe(OH)3+H+ K3
Fe(OH)3+H+ K3通过控制条件,以上水解产物聚合,生成聚合氧化铁,离子方程式为:
xFe3++yH2O

 +yH+,欲使平衡正向移动可采用的方法是(填序号)___________。
+yH+,欲使平衡正向移动可采用的方法是(填序号)___________。| A.降温 | B.加水稀释 | C.加入NH4Cl | D.加入NaHCO3 |
您最近一年使用:0次
名校
解题方法
9 . NH3、N2H4在工业生产和国防建设中都有广泛应用。回答下列问题:
(1)①N2H4 (g) ⇌ N2(g)+2H2(g) △H1
②N2(g)+3H2(g) ⇌ 2NH3(g) △H2
③7N2H4(g) ⇌ 8NH3(g)+3N2(g)+2H2(g) △H3
△H3=___________ (用含△H1和△H2的代数式表示),反应③的平衡行数表达式为K=___________ 。
(2)纳米钴的催化作用下,N2H4可分解生成两种气体,其中一种能使湿润的红色石蕊试纸变蓝。当反应在不同温度下达到平衡时,混合气体中各组分的体积分数如图所示。
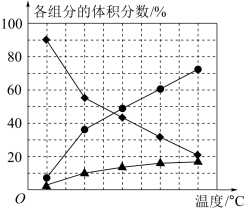
该反应的△H_____________ (填“>”或“<”)0,N2H4发生分解反应的化学方程式为________ 。
(1)①N2H4 (g) ⇌ N2(g)+2H2(g) △H1
②N2(g)+3H2(g) ⇌ 2NH3(g) △H2
③7N2H4(g) ⇌ 8NH3(g)+3N2(g)+2H2(g) △H3
△H3=
(2)纳米钴的催化作用下,N2H4可分解生成两种气体,其中一种能使湿润的红色石蕊试纸变蓝。当反应在不同温度下达到平衡时,混合气体中各组分的体积分数如图所示。

该反应的△H
您最近一年使用:0次
2017-09-02更新
|
340次组卷
|
3卷引用:2017-2018学年甘肃省白银一中期中考试高三化学试卷



