名校
1 . 氯酸是一种强酸,浓度超过 40%时会发生分解,反应可表示为 aHClO3=bO2↑+ cCl2↑+ dHClO4 + eH2O,用湿润的淀粉碘化钾试纸检验气体产物时,试纸先变蓝后褪色。下列说法正确的是
| A.若化学计量数 a = 8,b = 3,则该反应转移电子为 20e- |
| B.变蓝的淀粉碘化钾试纸褪色是因为可能发生了:4Cl2+I2 + 6H2O=12H++8Cl-+2IO3- |
| C.氧化产物是高氯酸和氯气 |
| D.由反应可确定:氧化性:HClO4>HClO3 |
您最近一年使用:0次
2019-11-05更新
|
212次组卷
|
4卷引用:宁夏石嘴山市第三中学2022-2023学年高三上学期期中考试化学试题
宁夏石嘴山市第三中学2022-2023学年高三上学期期中考试化学试题山西省吕梁市2020届高三10月模拟化学试题2020届高三化学二轮冲刺新题专练——氯及其化合物(已下线)专题39 氯的氧化物、含氧酸及含氧酸盐-2022年高考化学毕业班二轮热点题型归纳与变式演练(全国通用)
名校
2 . 二氧化氯是一种黄绿色的气体,被国际上公认为安全、低毒的绿色消毒剂,近几年我国用ClO2代替氯气对饮用水进行消毒。
(1)在进行饮用水消毒时,ClO2可将水中的Fe2+、Mn2+等转化成Fe(OH)3和MnO2等难溶物除去,据此说明ClO2具有________ 性。
(2)液氯也常用作自来水消毒。已知ClO2、Cl2的还原产物均为Cl-,则相同物质的量的ClO2的消毒效率是Cl2的_____ 倍。(消毒效率指单位物质的量的物质的得电子数)
(3)自来水厂用ClO2处理后的水中,要求ClO2的浓度在0.1~0.8 mg·L-1之间。碘量法可以检测水中ClO2的浓度,步骤如下:
操作Ⅰ:取一定体积的水样,加入一定量的碘化钾,使碘游离出来。已知:8HCl + 2ClO2 + 10KI === 5I2 + 10KCl + 4H2O。
操作Ⅱ: 加入一定量的Na2S2O3溶液。(已知:2Na2S2O3+I2===Na2S4O6+2NaI)
请回答:
①操作Ⅰ中反应的离子方程式是___________________________________________ 。
②若水样的体积为1.0 L,在操作Ⅱ时消耗了1.0×10-3 mol·L-1的Na2S2O3溶液10 mL,则水样中ClO2的浓度是_______ mg·L-1。
(1)在进行饮用水消毒时,ClO2可将水中的Fe2+、Mn2+等转化成Fe(OH)3和MnO2等难溶物除去,据此说明ClO2具有
(2)液氯也常用作自来水消毒。已知ClO2、Cl2的还原产物均为Cl-,则相同物质的量的ClO2的消毒效率是Cl2的
(3)自来水厂用ClO2处理后的水中,要求ClO2的浓度在0.1~0.8 mg·L-1之间。碘量法可以检测水中ClO2的浓度,步骤如下:
操作Ⅰ:取一定体积的水样,加入一定量的碘化钾,使碘游离出来。已知:8HCl + 2ClO2 + 10KI === 5I2 + 10KCl + 4H2O。
操作Ⅱ: 加入一定量的Na2S2O3溶液。(已知:2Na2S2O3+I2===Na2S4O6+2NaI)
请回答:
①操作Ⅰ中反应的离子方程式是
②若水样的体积为1.0 L,在操作Ⅱ时消耗了1.0×10-3 mol·L-1的Na2S2O3溶液10 mL,则水样中ClO2的浓度是
您最近一年使用:0次
名校
3 . 已知M2On2-离子可与R2-离子反应,R2- 被氧化为R单质,M2On2-的还原产物中M为+3价;又已知100mL c(M2On2- )=0.2 mol·L-1的溶液可与100mL c(R2- )=0.6 mol·L-1的溶液恰好完全反应,则n值为( )
| A.4 | B.5 | C.6 | D.7 |
您最近一年使用:0次
名校
4 . 已知Na2O2(过氧化钠)与H2O反应的方程式是: 2Na2O2+2H2O =4NaOH+O2↑,将一定质量的Na2O2固体加入足量水中充分反应可生成O2 3.36L标准状况,试计算:
(1)参加反应的Na2O2固体质量为_____________ 克?
(2)反应后所得溶液加入2 mol/L硫酸溶液_____________ 毫升恰好被中和?(要求两步均写出计算过程)
(1)参加反应的Na2O2固体质量为
(2)反应后所得溶液加入2 mol/L硫酸溶液
您最近一年使用:0次
名校
解题方法
5 . 氯化铬晶体(CrCl3·6H2O)是一种重要的工业原料,工业上常用铬酸钠(Na2CrO4)来制备。实验室以红矾钠(Na2Cr2O7)为原料制备CrCl3·6H2O的流程如下:

已知:① Cr2O72-+H2O 2CrO42-+2H+;
2CrO42-+2H+;
② CrCl3·6H2O不溶于乙醚,易溶于水、乙醇,易水解。
(1)写出碱溶发生反应的化学方程式____________________________________ ,所加40%NaOH不宜过量太多的原因是______________________________ 。
(2)还原时先加入过量CH3OH再加入10%HCl,生成CO2,写出该反应的离子方程式_________________ ,反应后从剩余溶液中分离出CH3OH的实验方法是_____________ 。
(3)使用下列用品来测定溶液的pH,合理的是_________ (填字母)。
A.酚酞溶液 B.石蕊试纸 C.pH计
(4)请补充完整由过滤后得到的固体Cr(OH)3制备CrCl3·6H2O的实验方案:将过滤后所得的洁净固体_______________________ ,蒸发浓缩,__________ ,过滤, ______________ ,低温干燥,得到CrCl3·6H2O(实验中可供选择的试剂:盐酸、硫酸、蒸馏水、乙醇、乙醚)。
(5)若取原料红矾钠26.2g,实验最终得到氯化铬晶体42.64g,则该实验的产率为_________ 。

已知:① Cr2O72-+H2O
 2CrO42-+2H+;
2CrO42-+2H+;② CrCl3·6H2O不溶于乙醚,易溶于水、乙醇,易水解。
(1)写出碱溶发生反应的化学方程式
(2)还原时先加入过量CH3OH再加入10%HCl,生成CO2,写出该反应的离子方程式
(3)使用下列用品来测定溶液的pH,合理的是
A.酚酞溶液 B.石蕊试纸 C.pH计
(4)请补充完整由过滤后得到的固体Cr(OH)3制备CrCl3·6H2O的实验方案:将过滤后所得的洁净固体
(5)若取原料红矾钠26.2g,实验最终得到氯化铬晶体42.64g,则该实验的产率为
您最近一年使用:0次
2017-11-19更新
|
372次组卷
|
3卷引用:【全国百强校】宁夏回族自治区石嘴山市第三中学2019届高三上学期期中考试化学试题
名校
解题方法
6 . 根据所学知识,回答下列问题:
(1)现有下列物质;①熔融的NaCl ②液态HCl ③蔗糖 ④汞 ⑤NaOH溶液 ⑥稀硫酸 ⑦CO2 ⑧KCl晶体
其中属于电解质的是_______ ;属于非电解质的是_______ ;能导电的有_______ 。
(2)按要求填空。
①NaHSO4溶液(写出电离方程式)_______ 。
②氯水与KI溶液反应(写出离子方程式)_______ 。
③苏打和澄清石灰水反应(写出离子方程式)_______ 。
(3)配平下列氧化还原方程式:
①_______ Fe+_______ HNO3 = _______ Fe(NO3)3+_______ NO↑+_______ H2O
②_______ CO+_______ Fe2O3 
_______ Fe+_______ CO2
(1)现有下列物质;①熔融的NaCl ②液态HCl ③蔗糖 ④汞 ⑤NaOH溶液 ⑥稀硫酸 ⑦CO2 ⑧KCl晶体
其中属于电解质的是
(2)按要求填空。
①NaHSO4溶液(写出电离方程式)
②氯水与KI溶液反应(写出离子方程式)
③苏打和澄清石灰水反应(写出离子方程式)
(3)配平下列氧化还原方程式:
①
②

您最近一年使用:0次
2017-11-14更新
|
579次组卷
|
2卷引用:宁夏育才中学2017-2018学年高一上学期期中化学试题
名校
7 . 锌与100mL 18.5mol·L-1的浓硫酸充分反应后,锌完全溶解,同时生成气体甲33.6L(标准状况)。将反应后的溶液稀释至1L,测得溶液的pH=1。下列叙述不正确的是( )
| A.气体甲中SO2与H2的体积比为4∶1 | B.反应中共消耗1.8mol H2SO4 |
| C.反应中共消耗97.5g Zn | D.反应中共转移3mol电子 |
您最近一年使用:0次
2017-10-28更新
|
357次组卷
|
2卷引用:宁夏青铜峡市高级中学2021-2022学年高三上学期期中考试化学试题
名校
8 . 铝是一种重要的金属,在生产、生活中具有许多重要的用途,如图是从铝土矿中制备铝的工艺流程:
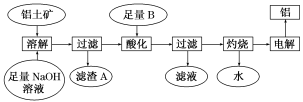
已知:(1)铝土矿的主要成分是Al2O3,此外还含有少量SiO2、Fe2O3等杂质;
(2)溶液中的硅酸钠与偏铝酸钠反应,能生成硅铝酸盐沉淀,化学反应方程式为2Na2SiO3+2NaAlO2+2H2O===Na2Al2Si2O8↓+4NaOH。
请回答下列问题:
(1)铝土矿中Al2O3与氢氧化钠溶液反应的离子方程式为
________________________________________________________________________ 。
(2)在工艺流程中“酸化”时,加入的最佳物质B是______ ,理由是________________________________________________________________________ ,
写出酸化过程发生反应的化学方程式________________________________________________________________________ 。
(3)工业上用Al2O3与C、Cl2在高温条件下反应制取AlCl3,理论上每消耗6.0 g碳单质,转移1 mol电子,则反应的化学方程式为______________________________ 。
(4)某同学推测铝与氧化铁发生铝热反应得到的熔融物中还含有Fe2O3,设计了如下方案来验证:取一块该熔融物投入少量稀硫酸中,反应一段时间后,向反应后的混合液中滴加物质甲的溶液,观察溶液颜色的变化,即可证明熔融物中是否含有Fe2O3。
则物质甲是________ (填化学式),请判断该同学设计的实验方案的合理性________ (填“合理”或“不合理”)。原因是_____________________________ (若合理,则不用填写)。

已知:(1)铝土矿的主要成分是Al2O3,此外还含有少量SiO2、Fe2O3等杂质;
(2)溶液中的硅酸钠与偏铝酸钠反应,能生成硅铝酸盐沉淀,化学反应方程式为2Na2SiO3+2NaAlO2+2H2O===Na2Al2Si2O8↓+4NaOH。
请回答下列问题:
(1)铝土矿中Al2O3与氢氧化钠溶液反应的离子方程式为
(2)在工艺流程中“酸化”时,加入的最佳物质B是
写出酸化过程发生反应的化学方程式
(3)工业上用Al2O3与C、Cl2在高温条件下反应制取AlCl3,理论上每消耗6.0 g碳单质,转移1 mol电子,则反应的化学方程式为
(4)某同学推测铝与氧化铁发生铝热反应得到的熔融物中还含有Fe2O3,设计了如下方案来验证:取一块该熔融物投入少量稀硫酸中,反应一段时间后,向反应后的混合液中滴加物质甲的溶液,观察溶液颜色的变化,即可证明熔融物中是否含有Fe2O3。
则物质甲是
您最近一年使用:0次
2017-05-24更新
|
1024次组卷
|
8卷引用:宁夏银川市景博中学2022-2023学年高二上学期期中考试化学试题
宁夏银川市景博中学2022-2023学年高二上学期期中考试化学试题内蒙古巴彦淖尔市第一中学2018届高三上学期期中考试理科综合化学试题河北省邢台市第一中学2016-2017学年高二下学期第三次月考化学试题黑龙江省大庆实验中学2016-2017学年高一6月月考化学试题【全国百强校】广西陆川县中学2017-2018学年高一下学期6月考化学试题(已下线)2019高考备考一轮复习精品资料 第三章 金属及其化合物 第2讲 镁、铝及其重要化合物【押题专练】江苏省启东中学2020-2021学年高一上学期第二次月考化学试题(已下线)考点11 镁、铝及其重要化合物(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(新高考专用)
13-14高三·海南海口·阶段练习
9 . 已知A为常见的金属单质,根据如图所示的转化关系回答下列问题。
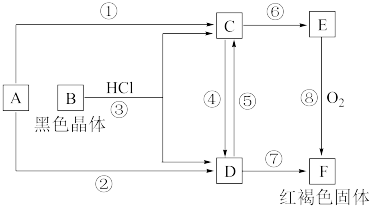
(1)确定A、B、C、D、E、F的化学式:
A为________ ,B为________ ,C为________ 。
D为________ ,E为________ ,F为________ 。
(2)写出⑧的化学方程式及④、⑤的离子方程式:___________________________ 。

(1)确定A、B、C、D、E、F的化学式:
A为
D为
(2)写出⑧的化学方程式及④、⑤的离子方程式:
您最近一年使用:0次
2016-12-09更新
|
1001次组卷
|
4卷引用:宁夏石嘴山市第三中学2018届高三上学期期中考试化学试题
宁夏石嘴山市第三中学2018届高三上学期期中考试化学试题(已下线)2015届海南省海口市琼山区海政学校高三第四次月考化学试卷2015-2016学年辽宁省实验中学高一上12月月考化学试卷【全国百强校】江苏省苏州市第九高级中学2018-2019学年高一上学期十一月份月考化学试题
10-11高一上·宁夏银川·期中
10 . 某反应中反应物与生成物有:AsH3、H2SO4、HBrO3、K2SO4、H3AsO4、Br2和水。
(1)配平上述化学反应方程式并标出电子转移的方向和数目:
AsH3+ H2SO4+ KBrO3→K2SO4+ H3AsO4+ H2O+ Br2________________ 。
(2)反应中,被还原的元素是___________ ,还原剂是________________ 。
(3)根据上述反应可推知_________ 。
a.氧化性:KBrO3>H3AsO4 b.氧化性:H3AsO4>KBrO3
c.还原性:AsH3>Br2 d.还原性:Br2>AsH3
(1)配平上述化学反应方程式并标出电子转移的方向和数目:
AsH3+ H2SO4+ KBrO3→K2SO4+ H3AsO4+ H2O+ Br2
(2)反应中,被还原的元素是
(3)根据上述反应可推知
a.氧化性:KBrO3>H3AsO4 b.氧化性:H3AsO4>KBrO3
c.还原性:AsH3>Br2 d.还原性:Br2>AsH3
您最近一年使用:0次



