1 . 高铁酸钾(K2FeO4)是一种绿色氧化剂,具有高效的杀菌消毒作用,常用于饮水处理,在许多领域展现出广阔的应用前景。制备高铁酸钾有下列两种方法:
方法一:Fe2O3+3KNO3+4KOH=2K2FeO4+3KNO2+2H2O
方法二:Fe(OH)3+KClO+KOH—K2FeO4+KCl+H2O(未配平)
(1)方法一中的氧化产物为_______ (写化学式),将方法一的化学方程式改写为离子方程式_______ ,根据该反应方程式可以判断氧化性强弱:KNO3_______ K2FeO4(填“>”“<”或“=”);
(2)写出方法二配平后的化学方程式_______ ;
(3)利用方法二制备K2FeO4,若有0.2molK2FeO4生成,转移的电子数为_______ mol。
方法一:Fe2O3+3KNO3+4KOH=2K2FeO4+3KNO2+2H2O
方法二:Fe(OH)3+KClO+KOH—K2FeO4+KCl+H2O(未配平)
(1)方法一中的氧化产物为
(2)写出方法二配平后的化学方程式
(3)利用方法二制备K2FeO4,若有0.2molK2FeO4生成,转移的电子数为
您最近一年使用:0次
2 . 化学与人类生活、生产密切相关。请根据题意填空:
(1)我国5G通信技术处于世界领先地位,高速通信离不开光导纤维。用于制造光导纤维的基本原料是_______ (填“SiO2”或“Si”);
(2)一定条件下,将1 mol N2和3 mol H2置于l L密闭容器中合成 NH3,10 min 后测得H2为 l.2 mol,则用H2 表示该反应的速率为_______ mol •L-1• min-1。
(3)在汽车排气管上安装催化转化装置,可使尾气中的NO和CO反应转化为无污染的物质。请完成一定条件该反应的化学方程式: 2CO + 2NO 2CO2 +
2CO2 + _______ 。
(1)我国5G通信技术处于世界领先地位,高速通信离不开光导纤维。用于制造光导纤维的基本原料是
(2)一定条件下,将1 mol N2和3 mol H2置于l L密闭容器中合成 NH3,10 min 后测得H2为 l.2 mol,则用H2 表示该反应的速率为
(3)在汽车排气管上安装催化转化装置,可使尾气中的NO和CO反应转化为无污染的物质。请完成一定条件该反应的化学方程式: 2CO + 2NO
 2CO2 +
2CO2 +
您最近一年使用:0次
解题方法
3 . 在工业上次磷酸(H3PO2)常用于化学镀银,发生的反应如下:____Ag++____H3PO2____H2O→____Ag↓+____H3PO4+____H+。
(1)H3PO2中,P元素的化合价为______ ,该反应中的氧化剂为_____ 。
(2)次磷酸H3PO2能与足量的NaOH反应生成NaH2PO2,则从酸的元数分类来看,次磷酸属于____ 酸。(填“一元”、“二元”或“三元”)
(3)配平并书写该离子方程式:____ 。
(4)用双线桥法标出(3)中氧化还原反应的电子转移情况____ 。
(5)该条件下,氧化性强弱Ag+____ H3PO4(填“>”或“<”)。
(6)一定浓度的CuSO4溶液也能将次磷酸氧化为H3PO4,自身被还原为单质,试写出该反应的离子方程式_____ 。
(1)H3PO2中,P元素的化合价为
(2)次磷酸H3PO2能与足量的NaOH反应生成NaH2PO2,则从酸的元数分类来看,次磷酸属于
(3)配平并书写该离子方程式:
(4)用双线桥法标出(3)中氧化还原反应的电子转移情况
(5)该条件下,氧化性强弱Ag+
(6)一定浓度的CuSO4溶液也能将次磷酸氧化为H3PO4,自身被还原为单质,试写出该反应的离子方程式
您最近一年使用:0次
4 . 高铁酸钠( )是经常使用的一种新型净水剂,它的氧化性很强。工业上制取高铁酸钠的化学方程式是(未配平):
)是经常使用的一种新型净水剂,它的氧化性很强。工业上制取高铁酸钠的化学方程式是(未配平):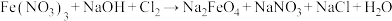
(1)高铁酸钠中,铁元素的化合价是___________
(2)上述反应中的还原产物为___________ ,配平并书写出上述方程式___________ 。
(3)高铁酸钠溶解于水,立即与水发生反应,放出氧气,正是这些在水中新产生出的氧原子发挥其极强的氧化能力可以用来给水杀菌消毒。根据氧化还原反应的基本规律判断其与水反应的过程中还会生成另外一种具有净水作用的胶体,该胶体是___________ 。
(4)次磷酸( )是一种化工产品,具有弱酸性,
)是一种化工产品,具有弱酸性, 的工业制法是:将白磷(P4)与
的工业制法是:将白磷(P4)与 溶液反应生成
溶液反应生成 气体和
气体和 ,后者再与
,后者再与 反应。配平白磷与
反应。配平白磷与 溶液反应的化学方程式(
溶液反应的化学方程式( )依次写出各物质的系数
)依次写出各物质的系数___________
(5)少量的次磷酸与足量的NaOH溶液反应能生成 ,根据上述信息写出次磷酸(
,根据上述信息写出次磷酸( )在水中的电离方程式
)在水中的电离方程式___________ ,从分类来看, 属于
属于___________ (书写弱酸电离方程式时需要用 连接弱酸与电离出来的离子)
连接弱酸与电离出来的离子)
a.酸式盐 B.碱 C.正盐 D.钠盐
 )是经常使用的一种新型净水剂,它的氧化性很强。工业上制取高铁酸钠的化学方程式是(未配平):
)是经常使用的一种新型净水剂,它的氧化性很强。工业上制取高铁酸钠的化学方程式是(未配平):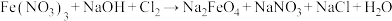
(1)高铁酸钠中,铁元素的化合价是
(2)上述反应中的还原产物为
(3)高铁酸钠溶解于水,立即与水发生反应,放出氧气,正是这些在水中新产生出的氧原子发挥其极强的氧化能力可以用来给水杀菌消毒。根据氧化还原反应的基本规律判断其与水反应的过程中还会生成另外一种具有净水作用的胶体,该胶体是
(4)次磷酸(
 )是一种化工产品,具有弱酸性,
)是一种化工产品,具有弱酸性, 的工业制法是:将白磷(P4)与
的工业制法是:将白磷(P4)与 溶液反应生成
溶液反应生成 气体和
气体和 ,后者再与
,后者再与 反应。配平白磷与
反应。配平白磷与 溶液反应的化学方程式(
溶液反应的化学方程式( )依次写出各物质的系数
)依次写出各物质的系数(5)少量的次磷酸与足量的NaOH溶液反应能生成
 ,根据上述信息写出次磷酸(
,根据上述信息写出次磷酸( )在水中的电离方程式
)在水中的电离方程式 属于
属于 连接弱酸与电离出来的离子)
连接弱酸与电离出来的离子)a.酸式盐 B.碱 C.正盐 D.钠盐
您最近一年使用:0次
名校
解题方法
5 . 汽车尾气(含CO2、N2、CO、SO2、NOx等)是城市空气的污染源之一;
(1)汽车尾气对环境的危害主要有温室效应、雾霾、___________ 、___________ 等。
(2)在汽车的排气管上安装一个“催化转化器”,可将尾气中的CO和NO转化为参与大气循环的气体和无毒的气体,该反应的化学方程式为___________ ;但使用“催化转化器”的缺点是一定程度提高了空气的酸度,其原因是___________ 。
(3)在一定条件下,NH3可将NOx转化为无污染的物质。写出NH3与NO2在一定条件下反应的化学方程式:___________ 。
(4)NOx储存还原技术可有效降低柴油发动机在空气过量条件下NOx的排放。如图所示NOx的储存和还原在不同时段交替进行。

通过BaO和Ba(NO3)2的相互转化实现NOx的储存和还原。储存时,部分NO发生反应的化学方程式为___________ ;储存NOx的物质是___________ 。 还原性尾气CO与Ba(NO3)2反应生成N2的化学方程式是___________ 。
(1)汽车尾气对环境的危害主要有温室效应、雾霾、
(2)在汽车的排气管上安装一个“催化转化器”,可将尾气中的CO和NO转化为参与大气循环的气体和无毒的气体,该反应的化学方程式为
(3)在一定条件下,NH3可将NOx转化为无污染的物质。写出NH3与NO2在一定条件下反应的化学方程式:
(4)NOx储存还原技术可有效降低柴油发动机在空气过量条件下NOx的排放。如图所示NOx的储存和还原在不同时段交替进行。

通过BaO和Ba(NO3)2的相互转化实现NOx的储存和还原。储存时,部分NO发生反应的化学方程式为
您最近一年使用:0次
2021-01-29更新
|
1219次组卷
|
4卷引用:湖南省益阳市箴言中学2020-2021学年高一下学期3月月考化学(选考)试题
湖南省益阳市箴言中学2020-2021学年高一下学期3月月考化学(选考)试题山东省烟台市2020-2021学年高一上学期期末考试化学试题(已下线)专题04 氧化还原反应-备战2021届高考化学二轮复习题型专练(已下线)第04讲 氮与氮的氧化物(word讲义)-【帮课堂】2021-2022学年高一化学同步精品讲义(人教版2019必修第二册)
名校
6 . 要准确掌握化学基本概念和研究方法。按要求回答下列问题:
(1)下列是某同学对有关物质进行分类的列表
每组分类均有错误,其错误的物质分别是第一组__ 、第二组__ (填化学式)。
(2)一个密闭容器中放入M、N、Q、P四种物质,在一定条件下发生化学反应,一段时间后,测得有关数据如下表,按要求回答下列问题:
①该变化的基本反应类型是___ 反应;
②物质Q在反应中可能起的作用是___ 。
(3)向NaHSO4溶液中逐滴加入Ba(OH)2溶液至中性,请写出发生反应的离子方程式:__ 。
(4)已知反应:2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O
①用双线桥 表示上述反应中电子转移的方向和数目__ 。
②浓盐酸在该反应中表现的性质是__ (填序号)。
A.只有还原性 B.还原性和酸性
C.只有氧化性 D.氧化性和酸性
(1)下列是某同学对有关物质进行分类的列表
| 碱 | 酸 | 盐 | 碱性氧化物 | 酸性氧化物 | |
| 第一组 | Na2CO3 | H2SO4 | NaHCO3 | CaO | CO2 |
| 第二组 | NaOH | HCl | NaCl | Na2O | CO |
每组分类均有错误,其错误的物质分别是第一组
(2)一个密闭容器中放入M、N、Q、P四种物质,在一定条件下发生化学反应,一段时间后,测得有关数据如下表,按要求回答下列问题:
| 物质 | M | N | Q | P |
| 反应前质量/g | 50 | 1 | 3 | 12 |
| 反应后质量/g | x | 26 | 3 | 30 |
①该变化的基本反应类型是
②物质Q在反应中可能起的作用是
(3)向NaHSO4溶液中逐滴加入Ba(OH)2溶液至中性,请写出发生反应的离子方程式:
(4)已知反应:2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O
①用
②浓盐酸在该反应中表现的性质是
A.只有还原性 B.还原性和酸性
C.只有氧化性 D.氧化性和酸性
您最近一年使用:0次
名校
解题方法
7 . (1)在一个绝热、容积不变的密闭容器中发生可逆反应:N2(g)+3H2(g) 2NH3(g)△H<0。下列各项能说明该反应已经达到平衡状态的是
2NH3(g)△H<0。下列各项能说明该反应已经达到平衡状态的是
B、容器内温度不再变化
C、断裂1mol N≡N键的同时,生成6mol N﹣H键
D、反应消耗N2、H2与产生NH3的速率之比1:3:2
(2)已知:①Zn(s)+1/2O2(g) = ZnO(s) △H =-348.3 kJ/mol
②2Ag(s)+1/2O2(g) = Ag2O(s) △H =-31.0 kJ/mol
则Zn(s)+Ag2O(s) = ZnO(s)+2Ag(s)的△H=
(3)已知两个热化学方程式:
C(s)+O2(g)==CO2(g) △H = -393.5kJ/mol
2H2(g)+O2(g)==2H2O(g)△H = -483.6kJ/mol
现有0.2mol炭粉和H2组成悬浮气,使其在O2中完全燃烧,共放出63.53kJ的热量,则炭粉与H2的物质的量之比是
(4)在水溶液中,YO3n-和S2-发生反应的离子方程式如下:YO3n- + 3S2- + 6H+ = Y-+ 3S↓+ 3H2O
①YO3n-中Y的化合价是
②Y元素原子的最外层电子数是
您最近一年使用:0次
2017-07-15更新
|
440次组卷
|
3卷引用:湖南省益阳市箴言中学2016-2017学年高一下学期期末化学试题



