名校
解题方法
1 . 科研小组以硫酸、五氧化二钒、三氧化二钒为原料,在:85℃下发生反应,制备可溶于水的VOSO4。所用实验装置如图所示。
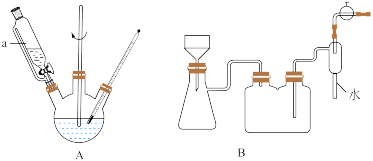
(1)仪器a的名称为___________ ,加热装置A的最佳方式为___________ 。
(2)A中搅拌的作用为___________ ,A中发生反应的化学方程式为___________ 。
(3)A中充分反应后的固液混合物转入B中的布氏漏斗中进行分离,该分离操作的名称为___________ ,B中自来水的作用为___________ 。
(4)若在A中加入50mL6.0mol⋅L-1H2SO4,4.55gV2O₅固体,3.00gV2O3固体,充分反应后,经过B装置的固液分离后,将所得滤液经___________ 、___________ 、过滤,可得VOSO4⋅3H2O固体。
(5)将(4)中所得固体溶于水,再向该溶液中加入硫酸酸化的10mL0.8mol⋅L-1KMnO4溶液,VOSO4与KMnO4恰好完全反应生成 ,则VOSO4⋅3H2O的产率为
,则VOSO4⋅3H2O的产率为___________ 。
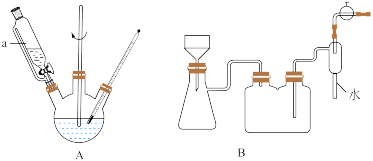
(1)仪器a的名称为
(2)A中搅拌的作用为
(3)A中充分反应后的固液混合物转入B中的布氏漏斗中进行分离,该分离操作的名称为
(4)若在A中加入50mL6.0mol⋅L-1H2SO4,4.55gV2O₅固体,3.00gV2O3固体,充分反应后,经过B装置的固液分离后,将所得滤液经
(5)将(4)中所得固体溶于水,再向该溶液中加入硫酸酸化的10mL0.8mol⋅L-1KMnO4溶液,VOSO4与KMnO4恰好完全反应生成
 ,则VOSO4⋅3H2O的产率为
,则VOSO4⋅3H2O的产率为
您最近一年使用:0次
2 . 工业上以菱锰矿(主要成分为MnCO3,含杂质CaCO3、FeCO3、NiCO3)为原料制取金属锰的工艺流程如下:
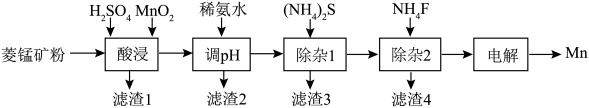
已知常温下,溶度积常数(Ksp)如下表:
(1)基态Mn2+的价层电子轨道表示式为___________ , 的空间结构为
的空间结构为___________ 。
(2)“酸浸”时,为了加快反应速率,可采取的措施有___________ (答两条),该过程一般选择硫酸而不用盐酸的原因是___________ 。
(3)“酸浸”过程中,MnO2发生的主要反应的离子方程式为___________ 。
(4)常温下,加稀氨水时调pH约为4,则滤渣2的主要成分是___________ 。
(5)“除杂1”时加入适量的(NH4)2S,除去的主要离子为___________ ,过滤后得到的滤液中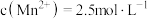 ,则其
,则其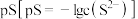 的范围是
的范围是___________ 。

已知常温下,溶度积常数(Ksp)如下表:
 |  |  |  |  |  |
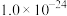 | 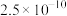 | 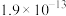 |  | 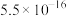 | 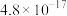 |
(1)基态Mn2+的价层电子轨道表示式为
 的空间结构为
的空间结构为(2)“酸浸”时,为了加快反应速率,可采取的措施有
(3)“酸浸”过程中,MnO2发生的主要反应的离子方程式为
(4)常温下,加稀氨水时调pH约为4,则滤渣2的主要成分是
(5)“除杂1”时加入适量的(NH4)2S,除去的主要离子为
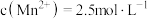 ,则其
,则其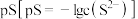 的范围是
的范围是
您最近一年使用:0次
解题方法
3 . 微颗粒的氧化锌作为一种纳米材料开始在相关领域发挥作用,利用锌焙砂 主要成分为
主要成分为 ,含
,含 及铅、铜、镉的氧化物
及铅、铜、镉的氧化物 生产高纯氧化锌的工业流程如图所示,回答下列问题:
生产高纯氧化锌的工业流程如图所示,回答下列问题:

已知: 微溶于水而生成亚砷酸
微溶于水而生成亚砷酸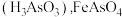 和
和 难溶于水。
难溶于水。
(1)基态 原子核外价层电子轨道表达式为
原子核外价层电子轨道表达式为______ , 中
中 的化合价为
的化合价为______ 。
(2)“浸出”过程中 足量,则生成的主要配离子的化学式为
足量,则生成的主要配离子的化学式为______ ;增大浸出率可采取的措施是______  写出两条
写出两条 。
。
(3)“除砷”过程中, 作氧化剂
作氧化剂 溶液呈酸性
溶液呈酸性 ,发生反应的离子方程式为
,发生反应的离子方程式为______ 。
(4)“除重金属”过程中加入 后
后 在溶液中的残留浓度为
在溶液中的残留浓度为 ,此时
,此时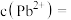
______ 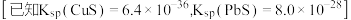 。
。
(5)“沉锌”前锌元素以 存在,写出“沉锌”的化学方程式
存在,写出“沉锌”的化学方程式______ 。
(6)流程中可循环利用的物质有 、
、______ 、______  填化学式
填化学式 。
。
 主要成分为
主要成分为 ,含
,含 及铅、铜、镉的氧化物
及铅、铜、镉的氧化物 生产高纯氧化锌的工业流程如图所示,回答下列问题:
生产高纯氧化锌的工业流程如图所示,回答下列问题:
已知:
 微溶于水而生成亚砷酸
微溶于水而生成亚砷酸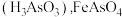 和
和 难溶于水。
难溶于水。(1)基态
 原子核外价层电子轨道表达式为
原子核外价层电子轨道表达式为 中
中 的化合价为
的化合价为(2)“浸出”过程中
 足量,则生成的主要配离子的化学式为
足量,则生成的主要配离子的化学式为 写出两条
写出两条 。
。(3)“除砷”过程中,
 作氧化剂
作氧化剂 溶液呈酸性
溶液呈酸性 ,发生反应的离子方程式为
,发生反应的离子方程式为(4)“除重金属”过程中加入
 后
后 在溶液中的残留浓度为
在溶液中的残留浓度为 ,此时
,此时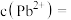
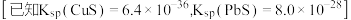 。
。(5)“沉锌”前锌元素以
 存在,写出“沉锌”的化学方程式
存在,写出“沉锌”的化学方程式(6)流程中可循环利用的物质有
 、
、 填化学式
填化学式 。
。
您最近一年使用:0次
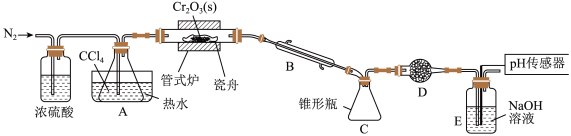
4 . 三氯化铬是有机金属化学中的重要原料,为紫色晶体,熔点为83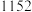 ℃,易潮解,高温下易被氧气氧化。实验室用
℃,易潮解,高温下易被氧气氧化。实验室用 和
和 加热到
加热到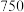 ℃时可制取
℃时可制取 ,同时还生成
,同时还生成 ,其装置图如下
,其装置图如下 加热及夹持装置略去
加热及夹持装置略去 ,请回答下列问题:
,请回答下列问题:
已知: 沸点
沸点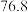 ℃;
℃; 有毒,沸点
有毒,沸点 ℃,遇水剧烈水解生成刺激性气味的气体。
℃,遇水剧烈水解生成刺激性气味的气体。
Ⅰ.制备 :
:
(1)仪器 的名称是
的名称是______ 。
(2)装置 、
、 的作用分别是
的作用分别是______ 、______ 。
(3)实验前先通入一段时间 的目的是
的目的是______ 。
(4)制备 的化学方程式为
的化学方程式为______ 。
(5)判断反应结束的依据是______ 。
Ⅱ.测定 纯度:
纯度:
称取 产品,在强碱性条件下,加入过量
产品,在强碱性条件下,加入过量 溶液,并小火加热,使
溶液,并小火加热,使 元素完全转化为
元素完全转化为 ;继续加热一段时间,冷却后配制成
;继续加热一段时间,冷却后配制成 溶液;取出
溶液;取出 ,滴加适量硫酸酸化后,用新配制的
,滴加适量硫酸酸化后,用新配制的 标准液滴定至终点,消耗标准液
标准液滴定至终点,消耗标准液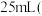 已知
已知 被
被 还原为
还原为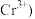 。
。
(6) 被
被 氧化成
氧化成 的离子方程式为
的离子方程式为______ 。
(7)产品中 的纯度为
的纯度为______  杂质不参与反应
杂质不参与反应 。
。
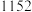 ℃,易潮解,高温下易被氧气氧化。实验室用
℃,易潮解,高温下易被氧气氧化。实验室用 和
和 加热到
加热到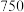 ℃时可制取
℃时可制取 ,同时还生成
,同时还生成 ,其装置图如下
,其装置图如下 加热及夹持装置略去
加热及夹持装置略去 ,请回答下列问题:
,请回答下列问题:
已知:
 沸点
沸点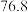 ℃;
℃; 有毒,沸点
有毒,沸点 ℃,遇水剧烈水解生成刺激性气味的气体。
℃,遇水剧烈水解生成刺激性气味的气体。Ⅰ.制备
 :
:(1)仪器
 的名称是
的名称是(2)装置
 、
、 的作用分别是
的作用分别是(3)实验前先通入一段时间
 的目的是
的目的是(4)制备
 的化学方程式为
的化学方程式为(5)判断反应结束的依据是
Ⅱ.测定
 纯度:
纯度:称取
 产品,在强碱性条件下,加入过量
产品,在强碱性条件下,加入过量 溶液,并小火加热,使
溶液,并小火加热,使 元素完全转化为
元素完全转化为 ;继续加热一段时间,冷却后配制成
;继续加热一段时间,冷却后配制成 溶液;取出
溶液;取出 ,滴加适量硫酸酸化后,用新配制的
,滴加适量硫酸酸化后,用新配制的 标准液滴定至终点,消耗标准液
标准液滴定至终点,消耗标准液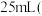 已知
已知 被
被 还原为
还原为 。
。(6)
 被
被 氧化成
氧化成 的离子方程式为
的离子方程式为(7)产品中
 的纯度为
的纯度为 杂质不参与反应
杂质不参与反应 。
。
您最近一年使用:0次
5 . 亚硝酸钙 广泛应用于钢筋混凝土工程中,主要用作水泥硬化促进剂和防冻阻锈剂,其为白色粉末,易潮解、易溶于水。实验室采用下列装置,用干燥的
广泛应用于钢筋混凝土工程中,主要用作水泥硬化促进剂和防冻阻锈剂,其为白色粉末,易潮解、易溶于水。实验室采用下列装置,用干燥的 与过氧化钙反应制取
与过氧化钙反应制取 。
。
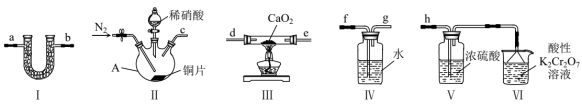
(1)仪器A的名称是
(2)装置的连接顺序是:c→
(3)滴入稀硝酸前需要通入一段时间
 ,待反应结束后还需继续通一会
,待反应结束后还需继续通一会 ,继续通
,继续通 的目的是
的目的是(4)装置Ⅱ中滴入稀硝酸后,A中观察到的现象是
(5)装置Ⅴ的作用是
(6)装置Ⅵ中氮元素被氧化成
 价,则反应的离子方程式为
价,则反应的离子方程式为(7)测定所得亚硝酸钙产品中硝酸钙的含量,实验步骤如下:

①除去 时,需要煮沸
时,需要煮沸 ,其反应的化学方程式为
,其反应的化学方程式为
②滴定时消耗标准液的体积为 ,则所得产品中硝酸钙的质量分数为
,则所得产品中硝酸钙的质量分数为
您最近一年使用:0次
名校
解题方法
6 . 某小组在实验室用NaClO溶液和NH3反应制备N2H4,并进行相关的性质探究实验。
I.制备N2H4
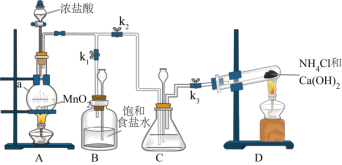
(1)装置A中盛放的浓盐酸的装置名称是_____ 。
(2)装置C中试剂是_____ ,作用是_____ (用离子方程式表示)。
(3)装置D发生反应的离子方程式为_____ 。
(4)制备N2H4的离子方程式为_____ 。
Ⅱ.N2H4的性质与NH3类似。为探究N2H4的性质,将制得的肼分离提纯后,进行如图实验。
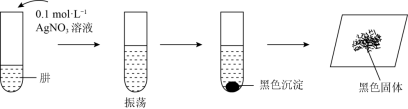
【查阅资料】AgOH在溶液中不稳定,易分解生成黑色的Ag2O,Ag2O可溶于氨水。
【提出假设】黑色固体可能是Ag、Ag2O中的一种或两种。
【实验验证】设计如表方案,进行实验。
(5)请完成表中的空白部分
(6)实验表明,黑色固体主要成分是Ag,还有少量氧化银。请解释原因:_____ 。
I.制备N2H4

(1)装置A中盛放的浓盐酸的装置名称是
(2)装置C中试剂是
(3)装置D发生反应的离子方程式为
(4)制备N2H4的离子方程式为
Ⅱ.N2H4的性质与NH3类似。为探究N2H4的性质,将制得的肼分离提纯后,进行如图实验。

【查阅资料】AgOH在溶液中不稳定,易分解生成黑色的Ag2O,Ag2O可溶于氨水。
【提出假设】黑色固体可能是Ag、Ag2O中的一种或两种。
【实验验证】设计如表方案,进行实验。
(5)请完成表中的空白部分
| 操作 | 现象 | 实验结论 |
| 取少量黑色固体于试管中,加入适量 | 黑色固体部分溶解 | 黑色固体有Ag2O |
| 取少量黑色固体于试管中加入足量稀硝酸,振荡。 | 黑色固体是Ag和Ag2O |
(6)实验表明,黑色固体主要成分是Ag,还有少量氧化银。请解释原因:
您最近一年使用:0次
名校
解题方法
7 . 砷化镓是一种半导体化合物,可用于太阳能电池。一种砷化镓废料(主要成分为GaAs,含 、
、 、
、 等杂质)中回收单质镓和砷的化合物的工艺流程如图所示。
等杂质)中回收单质镓和砷的化合物的工艺流程如图所示。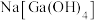 的形式进入溶液。
的形式进入溶液。
②离子完全沉淀时的pH: 为8,
为8, 为5.6。
为5.6。
(1)第一电离能比较:As________ Ga(填“<”“>”或“=”,下同),原子半径比较:As________ Ga。
(2)下图为砷化镓晶胞,白球所代表原子的配位数是________ 。已知:晶胞参数为apm,密度为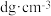 ,则阿伏加德罗常数
,则阿伏加德罗常数 可表示为
可表示为________ (用含a、d的式子表示)。________ 。
(4)“调pH①”时,pH=________ 最合适;滤液②的溶质成分为________ (写化学式)。
(5)写出用惰性电极电解制备镓单质的电极反应方程式:________ 。
 、
、 、
、 等杂质)中回收单质镓和砷的化合物的工艺流程如图所示。
等杂质)中回收单质镓和砷的化合物的工艺流程如图所示。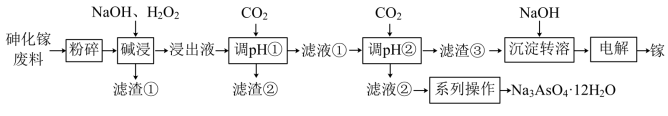
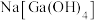 的形式进入溶液。
的形式进入溶液。②离子完全沉淀时的pH:
 为8,
为8, 为5.6。
为5.6。(1)第一电离能比较:As
(2)下图为砷化镓晶胞,白球所代表原子的配位数是
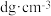 ,则阿伏加德罗常数
,则阿伏加德罗常数 可表示为
可表示为
(4)“调pH①”时,pH=
(5)写出用惰性电极电解制备镓单质的电极反应方程式:
您最近一年使用:0次
2024-03-25更新
|
112次组卷
|
2卷引用:重庆市渝西中学2023-2024学年高二下学期4月月考化学试题
名校
解题方法
8 . 某化学实验小组在实验室中模拟制取 的实验装置如图所示(略去夹持仪器):
的实验装置如图所示(略去夹持仪器):

实验原理如下:
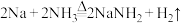


已知: 易潮解和易氧化。
易潮解和易氧化。
请回答下列问题:
(1)仪器D的名称是______ ,F中盛放浓硫酸的作用是______ 。
(2)制备 时,打开
时,打开 、
、 ,首先加热的是
,首先加热的是______ (填“C”或“E”),按图示方法制备 的化学方程式为
的化学方程式为______ 。
(3)实验时G中生成沉淀 ,反应的化学方程式为
,反应的化学方程式为______ 。
(4)将制取的 冷却,先加
冷却,先加 溶解,再加入乙醇,经过滤,洗涤,干燥得产品。用乙醇洗涤的原因是
溶解,再加入乙醇,经过滤,洗涤,干燥得产品。用乙醇洗涤的原因是______ 。
(5)称取2.0g产品,配制成100mL溶液,取10.00mL溶液于锥形瓶中,加入0.1mol/L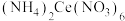 溶液40.00mL,充分反应后,再用0.1mol/L
溶液40.00mL,充分反应后,再用0.1mol/L 标准溶液滴定过量的
标准溶液滴定过量的 ,终点时消耗标准溶液10.00mL。相关反应如下(假设杂质不参与反应):
,终点时消耗标准溶液10.00mL。相关反应如下(假设杂质不参与反应):
第一步: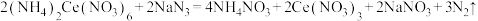
第二步:
①若滴加 标准溶液至终点时,滴定管玻璃尖嘴部分有气泡,则产品纯度
标准溶液至终点时,滴定管玻璃尖嘴部分有气泡,则产品纯度______ (填“偏大”或“偏小”)
②若2.0g该产品完全发生第一步反应时,转移的电子的物质的量为______ 。
 的实验装置如图所示(略去夹持仪器):
的实验装置如图所示(略去夹持仪器):
实验原理如下:
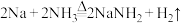


已知:
 易潮解和易氧化。
易潮解和易氧化。请回答下列问题:
(1)仪器D的名称是
(2)制备
 时,打开
时,打开 、
、 ,首先加热的是
,首先加热的是 的化学方程式为
的化学方程式为(3)实验时G中生成沉淀
 ,反应的化学方程式为
,反应的化学方程式为(4)将制取的
 冷却,先加
冷却,先加 溶解,再加入乙醇,经过滤,洗涤,干燥得产品。用乙醇洗涤的原因是
溶解,再加入乙醇,经过滤,洗涤,干燥得产品。用乙醇洗涤的原因是(5)称取2.0g产品,配制成100mL溶液,取10.00mL溶液于锥形瓶中,加入0.1mol/L
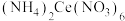 溶液40.00mL,充分反应后,再用0.1mol/L
溶液40.00mL,充分反应后,再用0.1mol/L 标准溶液滴定过量的
标准溶液滴定过量的 ,终点时消耗标准溶液10.00mL。相关反应如下(假设杂质不参与反应):
,终点时消耗标准溶液10.00mL。相关反应如下(假设杂质不参与反应):第一步:
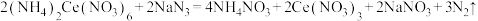
第二步:

①若滴加
 标准溶液至终点时,滴定管玻璃尖嘴部分有气泡,则产品纯度
标准溶液至终点时,滴定管玻璃尖嘴部分有气泡,则产品纯度②若2.0g该产品完全发生第一步反应时,转移的电子的物质的量为
您最近一年使用:0次
名校
解题方法
9 . 在生活中亚硝酸钠 应用十分广泛,它是一种白色固体,外观与
应用十分广泛,它是一种白色固体,外观与 极其相似;少量可做食品的护色剂,可防止肉毒杆菌在肉类食品中生长。某化学兴趣小组查阅资料得知
极其相似;少量可做食品的护色剂,可防止肉毒杆菌在肉类食品中生长。某化学兴趣小组查阅资料得知 ,该学习小组利用下列装置制备干燥的亚硝酸钠(夹持及加热装置略去,部分仪器可重复使用)。
,该学习小组利用下列装置制备干燥的亚硝酸钠(夹持及加热装置略去,部分仪器可重复使用)。

已知:① 能被高锰酸钾氧化,但不能被浓硫酸氧化。
能被高锰酸钾氧化,但不能被浓硫酸氧化。
②酸性高锰酸钾溶液可将 氧化成
氧化成 。
。
回答下列问题:
I. 的制备:
的制备:
(1)装置A中的仪器名称分别是___________ ,仪器按气流方向连接顺序为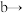
___________
(2)反应开始前打开止水夹a,通入过量氮气的目的是___________ ;反应结束后打开止水夹a,再通入过量氮气的目的是___________ 。
(3)装置D的作用是___________ 。
(4)判断Na2O2已被NO反应完全的现象是___________ 。
(5)写出装置E中发生反应的离子反应方程式______________________ 。
Ⅱ.测定的纯度(假设杂质不与反应):
(6)准确称取反应后的固体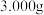 于烧杯中,加入蒸馏水溶解,配成
于烧杯中,加入蒸馏水溶解,配成 的溶液;取出
的溶液;取出 的溶液于锥形瓶中,滴入
的溶液于锥形瓶中,滴入 的酸性
的酸性 溶液至恰好完全反应,用去
溶液至恰好完全反应,用去 的酸性
的酸性 溶液。固体中
溶液。固体中 的纯度为
的纯度为___________  。
。
 应用十分广泛,它是一种白色固体,外观与
应用十分广泛,它是一种白色固体,外观与 极其相似;少量可做食品的护色剂,可防止肉毒杆菌在肉类食品中生长。某化学兴趣小组查阅资料得知
极其相似;少量可做食品的护色剂,可防止肉毒杆菌在肉类食品中生长。某化学兴趣小组查阅资料得知 ,该学习小组利用下列装置制备干燥的亚硝酸钠(夹持及加热装置略去,部分仪器可重复使用)。
,该学习小组利用下列装置制备干燥的亚硝酸钠(夹持及加热装置略去,部分仪器可重复使用)。
已知:①
 能被高锰酸钾氧化,但不能被浓硫酸氧化。
能被高锰酸钾氧化,但不能被浓硫酸氧化。②酸性高锰酸钾溶液可将
 氧化成
氧化成 。
。回答下列问题:
I.
 的制备:
的制备:(1)装置A中的仪器名称分别是
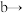
(2)反应开始前打开止水夹a,通入过量氮气的目的是
(3)装置D的作用是
(4)判断Na2O2已被NO反应完全的现象是
(5)写出装置E中发生反应的离子反应方程式
Ⅱ.测定的纯度(假设杂质不与反应):
(6)准确称取反应后的固体
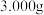 于烧杯中,加入蒸馏水溶解,配成
于烧杯中,加入蒸馏水溶解,配成 的溶液;取出
的溶液;取出 的溶液于锥形瓶中,滴入
的溶液于锥形瓶中,滴入 的酸性
的酸性 溶液至恰好完全反应,用去
溶液至恰好完全反应,用去 的酸性
的酸性 溶液。固体中
溶液。固体中 的纯度为
的纯度为 。
。
您最近一年使用:0次
名校
10 . 一种湿法回收 技术如下图所示,已知正极废料中主要含有铝箔,碳黑,磷酸铁锂(
技术如下图所示,已知正极废料中主要含有铝箔,碳黑,磷酸铁锂( )。
)。
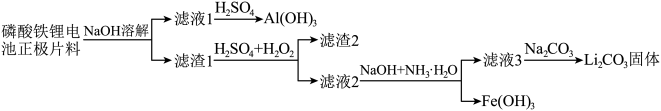
(1)①磷酸铁锂电池的内部结构如图a所示,充电时总反应是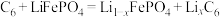 放电时,电池的正极反应为
放电时,电池的正极反应为______ 。
②下列分析合理的是______ (填序号)。
A.拆分前对废旧电池进行预放电,有利于释放残余能量,消除安全隐患
B.预放电时电池中的锂离子移向负极,有利于提高正极片中锂元素的回收率
C.对废旧锂离子电池进行热处理可以除去其中的难溶有机物、碳粉等
D.锂离子电池不含汞、镉、铅等有毒重金属,可直接深埋处理
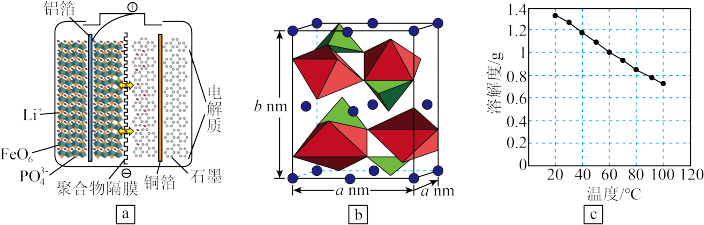
③磷酸铁锂( )的晶胞结构如图b所示,其中“○”代表
)的晶胞结构如图b所示,其中“○”代表 。则磷酸铁锂晶体的摩尔体积
。则磷酸铁锂晶体的摩尔体积
______  (已知阿伏加德罗常数为
(已知阿伏加德罗常数为 )。
)。
(2)正极材料经过一系列预处理后粉碎,然后使用氢氧化钠溶液浸泡,请写出该过程发生的主要离子方程式:______ 。
(3)已知磷酸铁易溶于硫酸,请写出用硫酸和 ,与滤渣1作用的离子反应方程式:
,与滤渣1作用的离子反应方程式:______ 。
(4)碳酸锂的溶解度随温度变化如图c所示。向滤液3中加入 溶液,将温度升至90℃的目的是
溶液,将温度升至90℃的目的是______ ;得到碳酸锂沉淀的最佳操作为______ (填序号)。
a.静置,过滤 b.加热,趁热过滤 c.蒸发浓缩、冷却结晶 d.蒸发结晶
(5)取100mL滤液3,其中 ,为使锂元素的回收率不低于80%,则至少应加入
,为使锂元素的回收率不低于80%,则至少应加入 固体的物质的量为
固体的物质的量为______ mol。[已知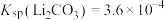 ]。
]。
 技术如下图所示,已知正极废料中主要含有铝箔,碳黑,磷酸铁锂(
技术如下图所示,已知正极废料中主要含有铝箔,碳黑,磷酸铁锂( )。
)。
(1)①磷酸铁锂电池的内部结构如图a所示,充电时总反应是
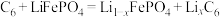 放电时,电池的正极反应为
放电时,电池的正极反应为
②下列分析合理的是
A.拆分前对废旧电池进行预放电,有利于释放残余能量,消除安全隐患
B.预放电时电池中的锂离子移向负极,有利于提高正极片中锂元素的回收率
C.对废旧锂离子电池进行热处理可以除去其中的难溶有机物、碳粉等
D.锂离子电池不含汞、镉、铅等有毒重金属,可直接深埋处理
③磷酸铁锂(
 )的晶胞结构如图b所示,其中“○”代表
)的晶胞结构如图b所示,其中“○”代表 。则磷酸铁锂晶体的摩尔体积
。则磷酸铁锂晶体的摩尔体积
 (已知阿伏加德罗常数为
(已知阿伏加德罗常数为 )。
)。(2)正极材料经过一系列预处理后粉碎,然后使用氢氧化钠溶液浸泡,请写出该过程发生的主要离子方程式:
(3)已知磷酸铁易溶于硫酸,请写出用硫酸和
 ,与滤渣1作用的离子反应方程式:
,与滤渣1作用的离子反应方程式:(4)碳酸锂的溶解度随温度变化如图c所示。向滤液3中加入
 溶液,将温度升至90℃的目的是
溶液,将温度升至90℃的目的是a.静置,过滤 b.加热,趁热过滤 c.蒸发浓缩、冷却结晶 d.蒸发结晶
(5)取100mL滤液3,其中
 ,为使锂元素的回收率不低于80%,则至少应加入
,为使锂元素的回收率不低于80%,则至少应加入 固体的物质的量为
固体的物质的量为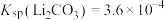 ]。
]。
您最近一年使用:0次



