1 . 某化学兴趣小组,利用NaHSO3溶液和酸性KMnO4溶液(使用稀H2SO4酸化)反应探究外界因素对化学反应速率的影响。
Ⅰ.原理分析:
(1)反应过程中 被氧化为
被氧化为 ,
, 被还原为Mn2+,请写出实验过程中的离子方程式
被还原为Mn2+,请写出实验过程中的离子方程式_______________ 。
(2)实验过程中,NaHSO3的用量要保证足量,通过比较________ (填“实验现象”)所需时间的长短来判断反应的快慢。
Ⅱ.实验过程
该化学兴趣小组设计如下实验方案:
(3)对比实验①②,使用探究________ 对化学反应速率的影响;若实验②③是用来探究温度对化学反应速率的影响,则V1=________ mL。
(4)若t1=25s,则用HSO 表示实验①的化学反应速率v(
表示实验①的化学反应速率v( )=
)= ________ 。
Ⅲ.实验分析和探究
该化学兴趣小组通过反复实验发现,该反应的化学反应速率总是先增大后减小,该化学兴趣小组猜想可能有两个原因,并作出了猜想:
猜想1:该反应放热,使溶液温度升高,化学反应速率加快
猜想2:新生成的微粒Mn2+对该反应有催化的作用
该化学兴趣小组,通过监测实验①反应过程的温度变化情况,数据显示反应过程中混合溶液的温度基本保持不变,排除猜想1的可能性。并设计第④组实验验证猜想2。设计如下:
(5)为了实验结论的可靠性,试剂X应该选择________。
(6)实验后,若t4_____ t1(填“大于”、“小于”或 “等于”),说明猜想2成立。
Ⅰ.原理分析:
(1)反应过程中
 被氧化为
被氧化为 ,
, 被还原为Mn2+,请写出实验过程中的离子方程式
被还原为Mn2+,请写出实验过程中的离子方程式(2)实验过程中,NaHSO3的用量要保证足量,通过比较
Ⅱ.实验过程
该化学兴趣小组设计如下实验方案:
| 编号 | 实验温度/℃ | 所用试剂的体积/mL | 达到(2)中现象所需时间/min | ||
| 0.6mol/L NaHSO3溶液 | 0.2mol/L酸性KMnO4溶液 | 水 | |||
| ① | 25 | 20 | 20 | 10 | t1 |
| ② | 25 | 25 | 20 | 5 | t2 |
| ③ | 50 | V1 | 20 | 5 | t3 |
(3)对比实验①②,使用探究
(4)若t1=25s,则用HSO
 表示实验①的化学反应速率v(
表示实验①的化学反应速率v( )=
)= Ⅲ.实验分析和探究
该化学兴趣小组通过反复实验发现,该反应的化学反应速率总是先增大后减小,该化学兴趣小组猜想可能有两个原因,并作出了猜想:
猜想1:该反应放热,使溶液温度升高,化学反应速率加快
猜想2:新生成的微粒Mn2+对该反应有催化的作用
该化学兴趣小组,通过监测实验①反应过程的温度变化情况,数据显示反应过程中混合溶液的温度基本保持不变,排除猜想1的可能性。并设计第④组实验验证猜想2。设计如下:
| 编号 | 实验温度/℃ | 所用试剂的体积/mL | 达到(2)中现象所需时间/min | ||
| 0.5mol/L NaHSO3溶液 | 0.2mol/L 酸性KMnO4溶液 | 试剂X | |||
| ④ | 25 | 20 | 20 | 10 | t4 |
(5)为了实验结论的可靠性,试剂X应该选择________。
| A.MnCl2溶液 | B.MnSO4溶液 |
| C.Mn(NO3)2溶液 | D.Mn(HSO3)2溶液 |
(6)实验后,若t4
您最近一年使用:0次
解题方法
2 . 铬和钒具有广泛用途。铬钒渣中铬和钒以低价态含氧酸盐形式存在,主要杂质为铁、铝、硅、磷等的化合物,从铬钒渣中分离提取铬和钒的一种流程如下图所示:
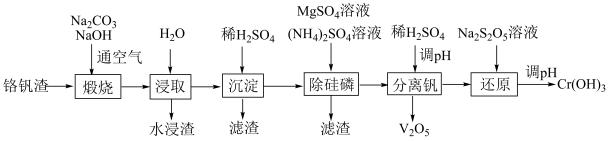
已知:最高价铬酸根在酸性介质中以Cr2O 存在,在碱性介质中以CrO
存在,在碱性介质中以CrO 存在。回答下列问题:
存在。回答下列问题:
(1)煅烧过程中,钒和铬被氧化为相应的最高价含氧酸盐,其中含铬化合物主要为___________ (填化学式)。
(2)水浸渣中主要有SiO2和___________ 。
(3)“分离钒”步骤中,将溶液pH调到1.8左右得到V2O5沉淀,V2O5在pH<1时,溶解为VO 或VO3+;在碱性条件下,溶解为VO
或VO3+;在碱性条件下,溶解为VO 或VO
或VO ,上述性质说明V2O5具有
,上述性质说明V2O5具有___________ (填标号)。
A.酸性 B.碱性 C.两性
(4)“还原”步骤中加入焦亚硫酸钠(Na2S2O5)溶液,反应的离子方程式为___________ 。

已知:最高价铬酸根在酸性介质中以Cr2O
 存在,在碱性介质中以CrO
存在,在碱性介质中以CrO 存在。回答下列问题:
存在。回答下列问题:(1)煅烧过程中,钒和铬被氧化为相应的最高价含氧酸盐,其中含铬化合物主要为
(2)水浸渣中主要有SiO2和
(3)“分离钒”步骤中,将溶液pH调到1.8左右得到V2O5沉淀,V2O5在pH<1时,溶解为VO
 或VO3+;在碱性条件下,溶解为VO
或VO3+;在碱性条件下,溶解为VO 或VO
或VO ,上述性质说明V2O5具有
,上述性质说明V2O5具有A.酸性 B.碱性 C.两性
(4)“还原”步骤中加入焦亚硫酸钠(Na2S2O5)溶液,反应的离子方程式为
您最近一年使用:0次
名校
解题方法
3 . 采用废铁屑还原软锰矿(软锰矿主要成分是 ,还含少量
,还含少量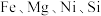 等元素的氧化物杂质)来制备
等元素的氧化物杂质)来制备 的工艺流程如图所示:
的工艺流程如图所示: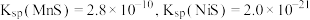 ;
;
②假设溶液中某离子浓度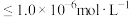 时,该离子沉淀完全;
时,该离子沉淀完全;
③室温时生成氢氧化物的 见下表。
见下表。
回答下列问题:
(1)“酸浸”时,为提高浸取效率,可采取的措施有_____ (任写一点)。
(2)在“浸出液”中加入 时发生反应的离子方程式为
时发生反应的离子方程式为_____ 。
(3)“除杂”过程中有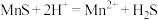 反应发生,其平衡常数
反应发生,其平衡常数 与
与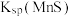 、
、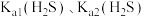 的代数关系式为
的代数关系式为
_____ 。加入 “除杂”后的滤渣为
“除杂”后的滤渣为_____ (填化学式),“除杂”后的滤液中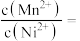
_____ 。
(4)“沉锰”过程中温度和 对
对 和
和 沉淀率的影响如图所示。则“沉锰”的合适条件是
沉淀率的影响如图所示。则“沉锰”的合适条件是_____ 。“沉锰”时发生反应的离子方程式为_____ 。
 ,还含少量
,还含少量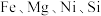 等元素的氧化物杂质)来制备
等元素的氧化物杂质)来制备 的工艺流程如图所示:
的工艺流程如图所示: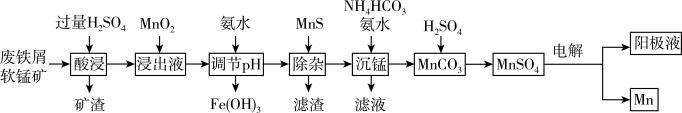
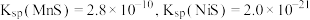 ;
;②假设溶液中某离子浓度
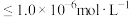 时,该离子沉淀完全;
时,该离子沉淀完全;③室温时生成氢氧化物的
 见下表。
见下表。| 离子 |  |  |  |  |  |
开始沉淀的 | 7.5 | 1.8 | 8.1 | 7.7 | 8.3 |
完全沉淀的 | 9.7 | 3 | 9.4 | 8.4 | 9.8 |
(1)“酸浸”时,为提高浸取效率,可采取的措施有
(2)在“浸出液”中加入
 时发生反应的离子方程式为
时发生反应的离子方程式为(3)“除杂”过程中有
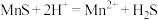 反应发生,其平衡常数
反应发生,其平衡常数 与
与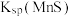 、
、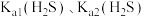 的代数关系式为
的代数关系式为
 “除杂”后的滤渣为
“除杂”后的滤渣为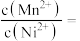
(4)“沉锰”过程中温度和
 对
对 和
和 沉淀率的影响如图所示。则“沉锰”的合适条件是
沉淀率的影响如图所示。则“沉锰”的合适条件是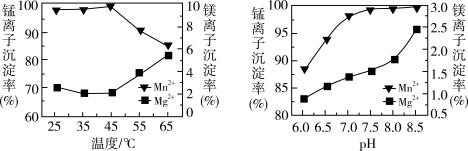
您最近一年使用:0次
2024-03-11更新
|
149次组卷
|
3卷引用:广东省佛山市顺德区勒流中学、均安中学、龙江中学等十五校2023-2024学年高二上学期12月联考化学试题
4 . 回答下列问题:
(1)已知H2A在水中发生电离:H2A=H++HA-,HA-⇌H++A2-。
①向H2A稀溶液中加入少量NaHA固体,溶液的pH_______ (填“增大”“减小”或“不变”)。
②常温下H2A的钙盐(CaA)饱和溶液中存在以下平衡:CaA(s)⇌Ca2+(aq)+A2-(aq)。加入少量Na2A固体,c(Ca2+)_______ (填“增大”“减小”或“不变”),原因是_______ 。
(2)含有Cr2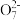 的废水毒性较大。经化学分析,某工厂废水中Cr2
的废水毒性较大。经化学分析,某工厂废水中Cr2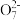 的浓度为4.00×10-3mol·L-1。为使废水能达标排放,作如下处理:Cr2
的浓度为4.00×10-3mol·L-1。为使废水能达标排放,作如下处理:Cr2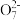
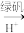 Cr3+、Fe3+
Cr3+、Fe3+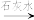 Cr(OH)3、Fe(OH)3。
Cr(OH)3、Fe(OH)3。
①在废水中加入FeSO4·7H2O和稀硫酸,发生反应的离子方程式为_______ 。
②已知:Ksp[Fe(OH)3]=2.8×10-39,Ksp[Cr(OH)3]=7.0×10-31。若处理后的废水中残留的c(Fe3+)=2.0×10-14mol·L-1,则残留的Cr3+的浓度为_______ 。
(1)已知H2A在水中发生电离:H2A=H++HA-,HA-⇌H++A2-。
①向H2A稀溶液中加入少量NaHA固体,溶液的pH
②常温下H2A的钙盐(CaA)饱和溶液中存在以下平衡:CaA(s)⇌Ca2+(aq)+A2-(aq)。加入少量Na2A固体,c(Ca2+)
(2)含有Cr2
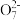 的废水毒性较大。经化学分析,某工厂废水中Cr2
的废水毒性较大。经化学分析,某工厂废水中Cr2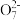 的浓度为4.00×10-3mol·L-1。为使废水能达标排放,作如下处理:Cr2
的浓度为4.00×10-3mol·L-1。为使废水能达标排放,作如下处理:Cr2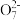
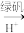 Cr3+、Fe3+
Cr3+、Fe3+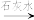 Cr(OH)3、Fe(OH)3。
Cr(OH)3、Fe(OH)3。①在废水中加入FeSO4·7H2O和稀硫酸,发生反应的离子方程式为
②已知:Ksp[Fe(OH)3]=2.8×10-39,Ksp[Cr(OH)3]=7.0×10-31。若处理后的废水中残留的c(Fe3+)=2.0×10-14mol·L-1,则残留的Cr3+的浓度为
您最近一年使用:0次
解题方法
5 . 尿素[CO(NH2)2]合成的发展体现了化学科学与技术的不断进步。
(1)十九世纪初,用氰酸银(AgOCN)与NH4Cl在一定条件下反应制得CO(NH2)2,实现了由无机物到有机物的合成。该反应的化学方程式是___________ 。
(2)二十世纪初,工业上以CO2和NH3为原料在一定温度和压强下合成尿素。反应分两步(反应过程中能量变化如图1所示):
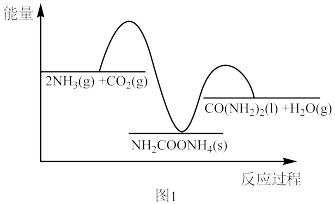
已知:Ⅰ.CO2和NH3生成NH2COONH4
Ⅱ.NH2COONH4分解生成尿素
①为防止反应Ⅰ中NH2COONH4分解为CO2和NH3,应采取的措施___________ 。
A.升温 B.降温 C.增大压强 D.减少压强
②密闭体系中除发生Ⅰ和Ⅱ外,尿素会发生水解、尿素缩合生成缩二脲[(NH2CO)2NH]和尿素转化为氰酸铵等副反应。尿素生产中实际投入NH3和CO2物质的量之比为4:1,其实际投料比值远大于理论值的原因是___________ 。
(3)尿素[CO(NH)2]溶液可吸收含SO2、NO烟气中SO2,其反应为:SO2+CO(NH2)2+2H2O=(NH4)2SO3+CO2,若吸收烟气时同时通入少量C1O2,可同时实现脱硫、脱硝。脱硝的反应分为两步。第一步:5NO+2ClO2+H2O=5NO2+2HCl;第二步:6NO2+4CO(NH2)2=7N2+4CO2+8H2O。将含SO2、NO烟气以一定的流速通过10%的CO(NH2)2溶液,其他条件相同,不通ClO2和通少量ClO2时SO2的去除率如图2所示。

①通少量ClO2时SO2的去除率较低的原因是___________ 。
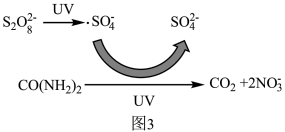
②处理后的废水含有尿素,可用过硫酸钠结合紫外线(UV)辐照去除废水中尿素,其过程机理如图3所示,尿素和过硫酸钠溶液发生的离子反应方程式为___________ 。
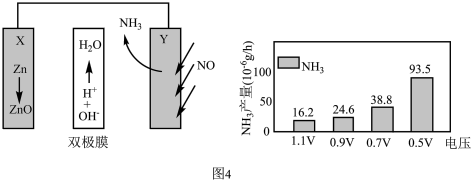
(4)电催化NO合成技术凭借其低能耗、绿色环保等优势成为化工行业关注的热点。某科研团队设计的Zn-NO电池装置及在不同电压下NH3的单位时间产量如图4所示,
已知:a.双极膜中H2O电离出的H+和OH−在电场作用下可以向两极迁移;
b.法拉第效率= ×100%
×100%
①写出正极的电极反应式___________ 。
②0.7V电压下连续放电10小时,外电路通过1.8×10-4mole-,则法拉第效率为___________ 。(保留两位小数)
(1)十九世纪初,用氰酸银(AgOCN)与NH4Cl在一定条件下反应制得CO(NH2)2,实现了由无机物到有机物的合成。该反应的化学方程式是
(2)二十世纪初,工业上以CO2和NH3为原料在一定温度和压强下合成尿素。反应分两步(反应过程中能量变化如图1所示):

已知:Ⅰ.CO2和NH3生成NH2COONH4
Ⅱ.NH2COONH4分解生成尿素
①为防止反应Ⅰ中NH2COONH4分解为CO2和NH3,应采取的措施
A.升温 B.降温 C.增大压强 D.减少压强
②密闭体系中除发生Ⅰ和Ⅱ外,尿素会发生水解、尿素缩合生成缩二脲[(NH2CO)2NH]和尿素转化为氰酸铵等副反应。尿素生产中实际投入NH3和CO2物质的量之比为4:1,其实际投料比值远大于理论值的原因是
(3)尿素[CO(NH)2]溶液可吸收含SO2、NO烟气中SO2,其反应为:SO2+CO(NH2)2+2H2O=(NH4)2SO3+CO2,若吸收烟气时同时通入少量C1O2,可同时实现脱硫、脱硝。脱硝的反应分为两步。第一步:5NO+2ClO2+H2O=5NO2+2HCl;第二步:6NO2+4CO(NH2)2=7N2+4CO2+8H2O。将含SO2、NO烟气以一定的流速通过10%的CO(NH2)2溶液,其他条件相同,不通ClO2和通少量ClO2时SO2的去除率如图2所示。

①通少量ClO2时SO2的去除率较低的原因是
②处理后的废水含有尿素,可用过硫酸钠结合紫外线(UV)辐照去除废水中尿素,其过程机理如图3所示,尿素和过硫酸钠溶液发生的离子反应方程式为

(4)电催化NO合成技术凭借其低能耗、绿色环保等优势成为化工行业关注的热点。某科研团队设计的Zn-NO电池装置及在不同电压下NH3的单位时间产量如图4所示,

已知:a.双极膜中H2O电离出的H+和OH−在电场作用下可以向两极迁移;
b.法拉第效率=
 ×100%
×100%①写出正极的电极反应式
②0.7V电压下连续放电10小时,外电路通过1.8×10-4mole-,则法拉第效率为
您最近一年使用:0次
6 . 连二亚硫酸钠(Na2S2O4)广泛应用于造纸等行业。Na2S2O4易被氧化,129℃时分解,在碱性条件下较稳定,易溶于水,不溶于乙醇。
实验室用NaBH4碱性溶液和NaHSO3酸性溶液制取Na2S2O4,实验室制备装置如图1所示。

(1)实验前需打开K通入一段时间氮气,其目的是___________ 。
(2)在10℃~35℃下,向盛有一定浓度的NaHSO3溶液容器中滴加NaBH4溶液,生成Na2S2O4和NaBO2,制备Na2S2O4的化学方程式为___________ 。
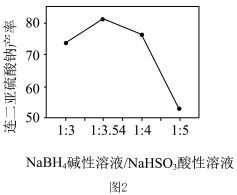
(3)Na2S2O4产率与加入NaBH4溶液与NaHSO3溶液质量比的关系如图2所示,NaBH4碱性溶液与NaHSO3酸性溶液加料质量比增大时,Na2S2O4产率下降的原因是___________ 。
(4)称量5.0g含Na2S2O4•2H2O晶体粗品溶于水配制成250mL溶液,准确量取25.00mL配制溶液于锥形瓶中,加入足量甲醛溶液,充分反应后,再滴加几滴淀粉溶液,用0.2000mol•L-1标准碘溶液滴定至反应终点,重复实验三次后,平均消耗标准碘溶液20.00mL。有关反应如下:Na2S2O4+2CH2O+H2O=NaHSO3•CH2O+NaHSO2•CH2O,NaHSO2•CH2O+2I2+2H2O=NaHSO4+4HI+CH2O,计算该粗品中Na2S2O4•2H2O晶体质量分数为___________ 。(写出计算过程)
实验室用NaBH4碱性溶液和NaHSO3酸性溶液制取Na2S2O4,实验室制备装置如图1所示。

(1)实验前需打开K通入一段时间氮气,其目的是
(2)在10℃~35℃下,向盛有一定浓度的NaHSO3溶液容器中滴加NaBH4溶液,生成Na2S2O4和NaBO2,制备Na2S2O4的化学方程式为
(3)Na2S2O4产率与加入NaBH4溶液与NaHSO3溶液质量比的关系如图2所示,NaBH4碱性溶液与NaHSO3酸性溶液加料质量比增大时,Na2S2O4产率下降的原因是

(4)称量5.0g含Na2S2O4•2H2O晶体粗品溶于水配制成250mL溶液,准确量取25.00mL配制溶液于锥形瓶中,加入足量甲醛溶液,充分反应后,再滴加几滴淀粉溶液,用0.2000mol•L-1标准碘溶液滴定至反应终点,重复实验三次后,平均消耗标准碘溶液20.00mL。有关反应如下:Na2S2O4+2CH2O+H2O=NaHSO3•CH2O+NaHSO2•CH2O,NaHSO2•CH2O+2I2+2H2O=NaHSO4+4HI+CH2O,计算该粗品中Na2S2O4•2H2O晶体质量分数为
您最近一年使用:0次
解题方法
7 . KIO3是常见的食盐加碘剂,某小组制备KIO3晶体的流程如下,请回答下列问题:

已知:①碘易溶于乙醚;乙醚微溶于水,沸点:34.5℃,密度:0.714g∙cm-3,易燃。
②KIO3在水中的溶解度:20℃为8.1g,80℃为21.8g;KIO3难溶于乙醇。
(1)步骤①“氧化”的离子方程式为___________ 。
(2)步骤②进行萃取操作时,需要放气,下图中正确的放气图示是___________ (填字母)。
a. b.
b.  c.
c.
(3)步骤④用带磁力搅拌的电热套控温85℃加热约1h,判断氧化反应已完全的方法是___________ 。
(4)步骤⑧后,往滤液中加入一定量___________ ,再次抽滤,可提高产品收率。
(5)为了测定KIO3产品的纯度,可采用碘量法滴定。准确称取1.000g产品,配制成250.00mL溶液,用移液管移取25.00mL溶液于锥形瓶中,加稀硫酸酸化,再加入足量KI溶液充分反应,加淀粉指示剂,用0.1000mol·L−1的Na2S2O3标准溶液滴定,平行测定3次,平均消耗标准溶液28.80mL。已知:I2+2S2O =2I-+S4O
=2I-+S4O
①滴定管需要用标准溶液润洗,润洗滴定管的具体操作为___________ 。
②KIO3在酸性条件下氧化KI的离子方程式为___________ 。
③产品的质量分数为___________ (保留4位有效数字)。
④在确认滴定操作无误的情况下,质量分数异常的原因可能是___________ 。

已知:①碘易溶于乙醚;乙醚微溶于水,沸点:34.5℃,密度:0.714g∙cm-3,易燃。
②KIO3在水中的溶解度:20℃为8.1g,80℃为21.8g;KIO3难溶于乙醇。
(1)步骤①“氧化”的离子方程式为
(2)步骤②进行萃取操作时,需要放气,下图中正确的放气图示是
a.
 b.
b.  c.
c.
(3)步骤④用带磁力搅拌的电热套控温85℃加热约1h,判断氧化反应已完全的方法是
(4)步骤⑧后,往滤液中加入一定量
(5)为了测定KIO3产品的纯度,可采用碘量法滴定。准确称取1.000g产品,配制成250.00mL溶液,用移液管移取25.00mL溶液于锥形瓶中,加稀硫酸酸化,再加入足量KI溶液充分反应,加淀粉指示剂,用0.1000mol·L−1的Na2S2O3标准溶液滴定,平行测定3次,平均消耗标准溶液28.80mL。已知:I2+2S2O
 =2I-+S4O
=2I-+S4O
①滴定管需要用标准溶液润洗,润洗滴定管的具体操作为
②KIO3在酸性条件下氧化KI的离子方程式为
③产品的质量分数为
④在确认滴定操作无误的情况下,质量分数异常的原因可能是
您最近一年使用:0次
解题方法
8 . 锰是冶金工业中不可缺少的添加剂,它的作用是增加合金金属材料的硬度、韧性、耐磨性和耐腐性,应用最广泛的有不锈钢、高锰钢、锰铝合金等。位于遵义市红花岗区坪桥工业园区的遵义天磁锰业集团有限公司就是一家电解锰公司;以碳酸锰为主要原料,其中含有少量铁、铝、钙、硅的氧化物或硫化物等杂质,以下是电解锰的简化工艺流程图:

(1)粉碎的目的___________ 。
(2)写出浸出时主要的离子反应___________ ,同时会产生的有毒气体是___________ 。
(3)加双氧水的作用方程式表示出来___________ 。
(4)加入氨水的作用是___________ ,除铁的离子反应___________ 。
(5)电解制锰的电极反应___________ ,当外电路转移2mol电子时,生成的气体是___________ ,在标准状况下的体积为___________ L,阳极液中产生的___________ 可循环使用。

(1)粉碎的目的
(2)写出浸出时主要的离子反应
(3)加双氧水的作用方程式表示出来
(4)加入氨水的作用是
(5)电解制锰的电极反应
您最近一年使用:0次
解题方法
9 . 无论是在环境保护领域还是在工农业生产领域,氮及其化合物一直是我国科研重点。回答下列问题:
(1)下列过程属于氮的固定过程的是______ (填选项字母)。
(2)消除汽车尾气中的氮氧化合物的原理之一为2NO(g)+2CO(g)⇌N2(g)+2CO2(g)。一定温度下,向体积为5L的刚性密闭容器中充入0.5molNO和0.5molCO,发生上述反应,测得部分气体的物质的量随时间变化关系如图所示:_______ (填“N2”或“CO2”)物质的量的变化曲线。
②该温度下,反应开始至5min时该反应的平均反应速率v(NO)=_______ 。
③3min时,反应_______ (填“达到”或“未达到”)化学平衡,6min时,正反应速率______ (填“>”“<”或“=”)逆反应速率。
④下列情况能说明该反应达到平衡状态的是______ (填选项字母)。
A.化学反应速率 正(NO)=
正(NO)= 逆(N2)
逆(N2)
B.CO与CO2的物质的量之和不再发生变化
C.容器内气体压强不再发生变化
D.容器内混合气体密度不再发生变化
(3)实验室用NaOH溶液对氮氧化合物进行尾气吸收,例如NaOH溶液可将NO2转化为NaNO3和NaNO2。该吸收过程中发生反应的离子方程式为______ 。
(1)下列过程属于氮的固定过程的是
| A.工业合成氨 |
| B.工业利用氨气合成硝酸 |
| C.雷雨天中氮气与氧气生成氮氧化合物 |
| D.通过碱性试剂将气态的氮氧化合物转化为固态含氮化合物 |

②该温度下,反应开始至5min时该反应的平均反应速率v(NO)=
③3min时,反应
④下列情况能说明该反应达到平衡状态的是
A.化学反应速率
 正(NO)=
正(NO)= 逆(N2)
逆(N2)B.CO与CO2的物质的量之和不再发生变化
C.容器内气体压强不再发生变化
D.容器内混合气体密度不再发生变化
(3)实验室用NaOH溶液对氮氧化合物进行尾气吸收,例如NaOH溶液可将NO2转化为NaNO3和NaNO2。该吸收过程中发生反应的离子方程式为
您最近一年使用:0次
23-24高二上·广东深圳·期末
名校
解题方法
10 . 镍及其化合物在工业上有广泛用途,以某地红土镍矿(主要成分NiO、MgO、Al2O3、SiO2和FeO)为原料,采用酸溶法制取 和MgSO4·7H2O,工业流程如图所示:
和MgSO4·7H2O,工业流程如图所示:
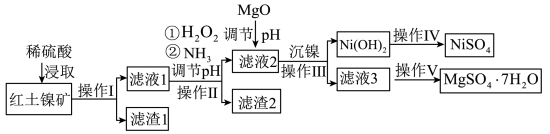
已知:①常温下,NiSO4易溶于水,Ni(OH)2和NiOOH不溶于水。
②在上述流程中,某些金属离子开始沉淀和沉淀完全时的pH如下:
回答下列问题:
(1)“滤液1”中加入H2O2的作用是___________ (用离子反应方程式表示)。
(2)操作II为达到实验目的,由表中的数据判断通入NH3调节溶液pH的范围是___________ 。
(3)Ksp[Ni(OH)2]=1.0×10-15,“沉镍”中pH调为8.5,则滤液中 的浓度为
的浓度为___________ mol/L。
(4)工业上使用Ni(OH)2在碱性溶液中电解,在电解池的阳极可制得电极材料NiOOH,该电极反应方程式为___________ 。
(5)用滴定法测定NiSO4产品中镍元素含量。取5.90g样品,酸溶后配成100mL溶液,取20.00mL于锥形瓶中进行滴定,滴入几滴紫脲酸胺指示剂,用浓度为0.100mol∙L-1的Na2H2Y标准液滴定,重复操作2~3次,消耗Na2H2Y标准液平均值为12.00mL。
已知:i.Ni2++H2Y2-=[NiY]2-+2H+;
ii.紫脲酸胺:紫色试剂,遇Ni2+显橙黄色。
①滴定终点的颜色变化为___________ ;
②样品中镍元素的质量分数为___________ %(保留3位有效数字);
③以下操作,会使测定结果偏低的有___________ 。
A.滴定终点读数时,俯视滴定管刻度
B.盛装Na2H2Y标准液的滴定管未润洗
C.滴定前,发现装有滴定管尖嘴处有一个气泡,滴定后,气泡消失
D.滴定终点读数后,发现尖嘴处悬挂了一滴溶液
 和MgSO4·7H2O,工业流程如图所示:
和MgSO4·7H2O,工业流程如图所示:
已知:①常温下,NiSO4易溶于水,Ni(OH)2和NiOOH不溶于水。
②在上述流程中,某些金属离子开始沉淀和沉淀完全时的pH如下:
| 沉淀物 | Ni(OH)2 | Fe(OH)2 | Fe(OH)3 | Al(OH)3 | Mg(OH)2 |
| 开始沉淀时的pH | 7.1 | 7.6 | 2.7 | 3.4 | 9.2 |
| 沉淀完全(c<10-5mol/L)时的pH | 9.0 | 9.6 | 3.2 | 4.7 | 11.1 |
(1)“滤液1”中加入H2O2的作用是
(2)操作II为达到实验目的,由表中的数据判断通入NH3调节溶液pH的范围是
(3)Ksp[Ni(OH)2]=1.0×10-15,“沉镍”中pH调为8.5,则滤液中
 的浓度为
的浓度为(4)工业上使用Ni(OH)2在碱性溶液中电解,在电解池的阳极可制得电极材料NiOOH,该电极反应方程式为
(5)用滴定法测定NiSO4产品中镍元素含量。取5.90g样品,酸溶后配成100mL溶液,取20.00mL于锥形瓶中进行滴定,滴入几滴紫脲酸胺指示剂,用浓度为0.100mol∙L-1的Na2H2Y标准液滴定,重复操作2~3次,消耗Na2H2Y标准液平均值为12.00mL。
已知:i.Ni2++H2Y2-=[NiY]2-+2H+;
ii.紫脲酸胺:紫色试剂,遇Ni2+显橙黄色。
①滴定终点的颜色变化为
②样品中镍元素的质量分数为
③以下操作,会使测定结果偏低的有
A.滴定终点读数时,俯视滴定管刻度
B.盛装Na2H2Y标准液的滴定管未润洗
C.滴定前,发现装有滴定管尖嘴处有一个气泡,滴定后,气泡消失
D.滴定终点读数后,发现尖嘴处悬挂了一滴溶液
您最近一年使用:0次



