解题方法
1 . 下列说法不正确的是
A. 俗称铁红,可用作油漆、涂料的红色颜料 俗称铁红,可用作油漆、涂料的红色颜料 |
| B.还原铁粉具有强还原性,可用作食品脱氧剂 |
| C.碳酸钠溶液显碱性,可用作食用碱或工业用碱 |
D. 有毒,且有刺激性气味,不可用于食品加工 有毒,且有刺激性气味,不可用于食品加工 |
您最近一年使用:0次
解题方法
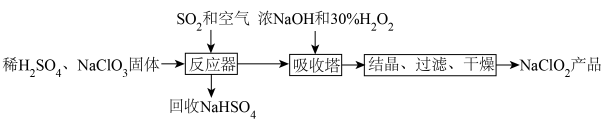
2 . ClO2是新一代高效安全的杀菌剂,可用于自来水消毒。由于其浓度过高时易分解,常将其转化成NaClO2晶体以便储运。亚氯酸钠(NaClO2)是一种高效氧化剂和漂白剂,主要用于棉纺、纸张漂白、食品消毒、水处理等,消毒时本身被还原成Cl-。亚氯酸钠晶体的一种生产工艺如图:
②H2O受热易分解。
(1)向“反应器”中鼓入空气的作用是______ 。
(2)“吸收塔”的作用是将产生的ClO2转化为NaClO2,在此过程中加入的H2O2的作用是_____ (填“氧化剂”或“还原剂”),当有1molH2O2参与该反应时,反应转移的电子数为______ 。
(3)“吸收塔”中需要控制温度不超过20℃,其原因是______ 。
(4)写出“反应器”步骤中生成ClO2的离子方程式______ 。
②H2O受热易分解。
(1)向“反应器”中鼓入空气的作用是
(2)“吸收塔”的作用是将产生的ClO2转化为NaClO2,在此过程中加入的H2O2的作用是
(3)“吸收塔”中需要控制温度不超过20℃,其原因是
(4)写出“反应器”步骤中生成ClO2的离子方程式
您最近一年使用:0次
解题方法
3 . 下列有关实验的操作、现象和实验结论错误的是
选项 | 操作 | 现象 | 实验结论 |
A | 将浓硫酸滴入胆矾晶体中 | 蓝色晶体变白 | 浓硫酸具有吸水性,发生化学变化 |
B | 将 SO2通入H2S溶液 | 产生淡黄色沉淀 | SO2具有氧化性 |
C | 向蔗糖中加入浓硫酸,将产生的气体通入溴水 | 蔗糖膨胀变黑,溴水褪色 | 浓硫酸具有脱水性和氧化性 |
D | 将SO2通入酸性 KMnO4溶液 | 溶液褪色 | SO2具有漂白性 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
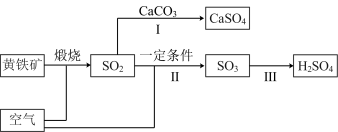
4 . 工业上煅烧含硫矿物产生的SO2可以按如下流程脱除或利用。
(1)下列说法正确的是_______。
(2)在足量空气中煅烧燃煤,产生的低浓度SO2可以在炉内添加CaCO3通过途径Ⅰ脱除,并产生一种无毒的气体,写出该反应的化学方程式_______ 。
(3)几位同学围绕浓硫酸的化学性质进行了如下探究实验:将适量的蔗糖放入烧杯中,加入几滴水,搅拌均匀;然后再加入适量浓硫酸,迅速搅拌,观察到蔗糖逐渐变黑,体积膨胀,并产生有刺激性气味的气体;
①写出产生刺激性气味气体的反应的化学方程式_______ 。
②上述实验现象表明浓硫酸具有_______ (填字母)。
a.酸性 b.脱水性 c.强氧化性 d.挥发性
③某同学将收集到的刺激性气味气体通入品红溶液,品红溶液褪色。然后在该试管口套上气球,将无色溶液加热恢复至红色,冷却后,发现溶液颜色再次变浅。解释“无色→红色→颜色变浅”变化的原因_______ 。

(1)下列说法正确的是_______。
| A.工业上还可以用硫黄代替黄铁矿制备SO2 |
| B.步骤I,如果通入过量空气,可以实现SO2的完全转化 |
| C.SO2是无色、无臭、有毒的气体,易溶于水 |
| D.步骤Ⅲ用浓硫酸吸收SO3 |
(2)在足量空气中煅烧燃煤,产生的低浓度SO2可以在炉内添加CaCO3通过途径Ⅰ脱除,并产生一种无毒的气体,写出该反应的化学方程式
(3)几位同学围绕浓硫酸的化学性质进行了如下探究实验:将适量的蔗糖放入烧杯中,加入几滴水,搅拌均匀;然后再加入适量浓硫酸,迅速搅拌,观察到蔗糖逐渐变黑,体积膨胀,并产生有刺激性气味的气体;
①写出产生刺激性气味气体的反应的化学方程式
②上述实验现象表明浓硫酸具有
a.酸性 b.脱水性 c.强氧化性 d.挥发性
③某同学将收集到的刺激性气味气体通入品红溶液,品红溶液褪色。然后在该试管口套上气球,将无色溶液加热恢复至红色,冷却后,发现溶液颜色再次变浅。解释“无色→红色→颜色变浅”变化的原因
您最近一年使用:0次
解题方法
5 . 下列离子反应方程式书写正确的是
A.向酸性高锰酸钾溶液中滴加过氧化氢: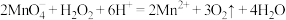 |
B.在氨水中加入少量 溶液: 溶液: |
C.向 溶液中加入 溶液中加入 溶液至 溶液至 沉淀完全 沉淀完全 |
D.苯酚钠溶液中通入少量二氧化碳: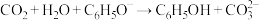 |
您最近一年使用:0次
2024-03-16更新
|
147次组卷
|
2卷引用:浙江省杭州学军中学海创园学校2023-2024学年高二上学期期末考试化学试题
解题方法
6 . 在探究 水溶液成分和性质的实验中,下列实验现象或实验结论
水溶液成分和性质的实验中,下列实验现象或实验结论不正确 的是
 水溶液成分和性质的实验中,下列实验现象或实验结论
水溶液成分和性质的实验中,下列实验现象或实验结论| 选项 | 实验操作 | 实验现象 | 实验结论 |
| A | 向 水溶液中加入 水溶液中加入 粉末 粉末 | 有气泡产生 |  水溶液呈酸性 水溶液呈酸性 |
| B | 向 水溶液中滴加2滴石蕊溶液,振荡 水溶液中滴加2滴石蕊溶液,振荡 | 溶液先变红后褪色 |  有漂白作用 有漂白作用 |
| C | 向 水溶液中加入 水溶液中加入 溶液 溶液 | 有淡黄色沉淀产生 |  具有氧化性 具有氧化性 |
| D | 向 溶液中加入足量 溶液中加入足量 水溶液 水溶液 | 溶液紫色褪去 |  具有还原性 具有还原性 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2024-03-14更新
|
125次组卷
|
2卷引用:浙江省宁波市鄞州高级中学2023-2024学年高二上学期12月月考化学试题
名校
7 . 下列离子方程式书写正确的是
A.大理石与稀硝酸反应: |
B.碳酸氢钠溶液和过量的澄清石灰水混合: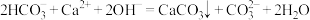 |
C.少量 通入 通入 溶液中: 溶液中: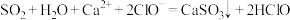 |
D.过量铁粉投入稀硝酸中: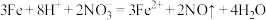 |
您最近一年使用:0次
2024-03-08更新
|
278次组卷
|
2卷引用:浙江省杭州市长河高级中学2023-2024学年高一上学期期末考试化学试题
8 . 下列说法不正确的是
| A.储氢合金要求储氢量大,金属氢化物既容易形成,受热又不容易分解 |
| B.二氧化硫可用于杀菌消毒,还是一种食品添加剂 |
| C.中国华为集团自主研发的“麒麟”芯片生产时需要用到硅 |
| D.硬铝是一种铝合金,是制造飞机和宇宙飞船的理想材料 |
您最近一年使用:0次
2024-03-08更新
|
123次组卷
|
3卷引用:浙江省杭州市长河高级中学2023-2024学年高一上学期期末考试化学试题
9 . 物质的性质决定用途,下列两者对应关系不正确 的是
A. 溶液呈碱性,其热溶液可用于去除厨房油渍 溶液呈碱性,其热溶液可用于去除厨房油渍 |
B. 难溶于水和酸且不能被X射线穿透,可用作人体造影剂 难溶于水和酸且不能被X射线穿透,可用作人体造影剂 |
C. 具有强氧化性,可用作自来水消毒剂 具有强氧化性,可用作自来水消毒剂 |
| D.钠、钾具有很强还原性,钠钾合金可用作核反应堆的传热介质 |
您最近一年使用:0次
解题方法
10 . Ⅰ.下面是某校化学研究性学习小组探究足量锌与浓硫酸反应的实验:甲同学设计如图实验验证该反应产生的混合气体中含有SO2、H2、H2O,已知装置C中试剂过量。
A. B.
B. C.
C. D.
D. E.
E.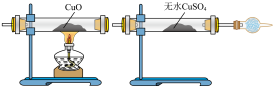 F.
F.
(1)按气体从左到右的流向,气体流经的各装置连接顺序是:________ 。
___________→___________→___________→___________→___________→___________
(2)证明混合气体中含有H2的实验现象为___________ 。
乙同学设计如下实验步骤测定44.8L(标准状况下)混合气体中SO2的体积分数。

(3)W溶液可以是___________(填序号)。
(4)该混合气体中二氧化硫的体积分数为___________ (用含m的代数式表示)。
Ⅱ.电子工业中,常用FeCl3溶液“腐蚀”覆铜板制作印刷电路板。某兴趣小组设计了印刷电路板腐蚀液再生和铜回收的新方法,具体步骤如下图所示

(5)写出生成印刷电路板“腐蚀废液”的离子方程式___________ 。
(6)下列说法错误的是___________ 。
A.滤渣③的成分是Cu
B.④可以是稀盐酸,不能用稀硫酸
C.通入⑥时发生反应的离子方程式是:2Fe2++Cl2=2Fe3++2Cl-
A.
 B.
B. C.
C. D.
D. E.
E. F.
F.
(1)按气体从左到右的流向,气体流经的各装置连接顺序是:
___________→___________→___________→___________→___________→___________
(2)证明混合气体中含有H2的实验现象为
乙同学设计如下实验步骤测定44.8L(标准状况下)混合气体中SO2的体积分数。

(3)W溶液可以是___________(填序号)。
| A.H2O2溶液 | B.酸性KMnO4溶液 | C.溴水 | D.稀硫酸 |
(4)该混合气体中二氧化硫的体积分数为
Ⅱ.电子工业中,常用FeCl3溶液“腐蚀”覆铜板制作印刷电路板。某兴趣小组设计了印刷电路板腐蚀液再生和铜回收的新方法,具体步骤如下图所示

(5)写出生成印刷电路板“腐蚀废液”的离子方程式
(6)下列说法错误的是
A.滤渣③的成分是Cu
B.④可以是稀盐酸,不能用稀硫酸
C.通入⑥时发生反应的离子方程式是:2Fe2++Cl2=2Fe3++2Cl-
您最近一年使用:0次



