名校
解题方法
1 . 高铁酸钾 为暗紫色固体,是一种高效多功能的新型非氯绿色消毒剂,易溶于水,在KOH浓溶液中溶解度较低,在酸性或中性溶液中不稳定,在碱性溶液中较稳定且碱性越强越稳定。某实验小组设计如图装置制备
为暗紫色固体,是一种高效多功能的新型非氯绿色消毒剂,易溶于水,在KOH浓溶液中溶解度较低,在酸性或中性溶液中不稳定,在碱性溶液中较稳定且碱性越强越稳定。某实验小组设计如图装置制备 ,根据所学知识回答下列问题:
,根据所学知识回答下列问题:
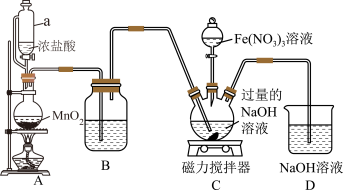
(1)装置A为 的发生装置,写出发生反应的离子方程式:
的发生装置,写出发生反应的离子方程式:________ 。
(2)装置B中盛装的液体是________ ,其作用为________ 。
(3)先向装置C的三颈烧瓶中通入一段时间的 制备NaClO,再滴加
制备NaClO,再滴加 溶液时发生反应的离子方程式为
溶液时发生反应的离子方程式为________ 。
(4)向装置C中通入的 不能过量,原因是
不能过量,原因是________ 。
(5)写出D中发生反应的离子方程式:________ 。
(6)高铁酸钾 是一种新型综合型的水处理剂。高铁酸钾具有强氧化性,在净水过程中可生成
是一种新型综合型的水处理剂。高铁酸钾具有强氧化性,在净水过程中可生成 胶体,高铁酸钾用作水处理剂的理由是
胶体,高铁酸钾用作水处理剂的理由是________ 。
 为暗紫色固体,是一种高效多功能的新型非氯绿色消毒剂,易溶于水,在KOH浓溶液中溶解度较低,在酸性或中性溶液中不稳定,在碱性溶液中较稳定且碱性越强越稳定。某实验小组设计如图装置制备
为暗紫色固体,是一种高效多功能的新型非氯绿色消毒剂,易溶于水,在KOH浓溶液中溶解度较低,在酸性或中性溶液中不稳定,在碱性溶液中较稳定且碱性越强越稳定。某实验小组设计如图装置制备 ,根据所学知识回答下列问题:
,根据所学知识回答下列问题:
(1)装置A为
 的发生装置,写出发生反应的离子方程式:
的发生装置,写出发生反应的离子方程式:(2)装置B中盛装的液体是
(3)先向装置C的三颈烧瓶中通入一段时间的
 制备NaClO,再滴加
制备NaClO,再滴加 溶液时发生反应的离子方程式为
溶液时发生反应的离子方程式为(4)向装置C中通入的
 不能过量,原因是
不能过量,原因是(5)写出D中发生反应的离子方程式:
(6)高铁酸钾
 是一种新型综合型的水处理剂。高铁酸钾具有强氧化性,在净水过程中可生成
是一种新型综合型的水处理剂。高铁酸钾具有强氧化性,在净水过程中可生成 胶体,高铁酸钾用作水处理剂的理由是
胶体,高铁酸钾用作水处理剂的理由是
您最近一年使用:0次
名校
解题方法
2 . 双氧水和含氯消毒剂是生活中常用的消毒剂,了解物质的性质是科学合理使用化学品的基础和前提。请回答下列问题:
(1)某同学设计如下实验研究H2O2的性质:
①从理论上看H2O2既有氧化性又有还原性,具有还原性的原因是_______ 。
②能证明H2O2具有还原性的实验是_______ (填序号),写出该过程的离子方程式_______ 。
(2)“84”消毒液的有效成分为NaClO。
①将Cl2通入NaOH溶液中可制得“84”消毒液,反应的化学方程式_______ 。
②“84”消毒液不能与洁厕灵(主要成分为盐酸)混用的原因_______ (用化学用语解释其原理)。
(3)二氧化氯(ClO2)是广谱性具有强氧化性的高效低毒的消毒剂。
①用NaClO3氧化浓盐酸来制取ClO2,同时有Cl2生成,该过程的化学方程式为_______ 。
②若上述反应产生0.1 mol Cl2,转移电子的物质的量为_______ mol。
③ClO2消毒的效率(以单位质量得到电子数表示)是Cl2的_______ 倍。
(1)某同学设计如下实验研究H2O2的性质:
| 序号 | 实验 | 实验现象 |
| i | 向5%H2O2溶液中滴加酸性KMnO4溶液 | a.溶液紫色褪去 b.有大量气泡产生 |
| ii | 向5%H2O2溶液中滴加淀粉碘化钾溶液 | c.溶液变蓝 |
②能证明H2O2具有还原性的实验是
(2)“84”消毒液的有效成分为NaClO。
①将Cl2通入NaOH溶液中可制得“84”消毒液,反应的化学方程式
②“84”消毒液不能与洁厕灵(主要成分为盐酸)混用的原因
(3)二氧化氯(ClO2)是广谱性具有强氧化性的高效低毒的消毒剂。
①用NaClO3氧化浓盐酸来制取ClO2,同时有Cl2生成,该过程的化学方程式为
②若上述反应产生0.1 mol Cl2,转移电子的物质的量为
③ClO2消毒的效率(以单位质量得到电子数表示)是Cl2的
您最近一年使用:0次
名校
解题方法
3 . 氯气在工业生产中有重要的用途。某课外活动小组利用下列装置在实验室中制备氯气,并进行有关氯气性质的研究。

(1)该小组同学欲用图1所示仪器及试剂(不一定全用)制备并收集干燥纯净的氯气。
①写出实验室制氯气的化学方程式:____ ;浓盐酸在反应中体现了____ (填编号)的性质。
A.酸性 B.氧化性 C.还原性 D.不稳定性
②选择装置,将各仪器按先后顺序连接起来,应该是a接_____,_____接_____,_____接_____,_____接h(用导管口处的字母表示)。____
(2)该小组同学设计并分别利用图2和图3所示装置探究氯气的氧化性,已知碘单质遇淀粉会变蓝。

①G中的现象是_____ ,原因是_____ (用化学方程式表示)。
②H中的现象是____ ,I中发生的离子反应方程式为____ 。

(1)该小组同学欲用图1所示仪器及试剂(不一定全用)制备并收集干燥纯净的氯气。
①写出实验室制氯气的化学方程式:
A.酸性 B.氧化性 C.还原性 D.不稳定性
②选择装置,将各仪器按先后顺序连接起来,应该是a接_____,_____接_____,_____接_____,_____接h(用导管口处的字母表示)。
(2)该小组同学设计并分别利用图2和图3所示装置探究氯气的氧化性,已知碘单质遇淀粉会变蓝。

①G中的现象是
②H中的现象是
您最近一年使用:0次
解题方法
4 .  溶液和84消毒液是生活中常用的两种消毒剂。请回答下列问题:
溶液和84消毒液是生活中常用的两种消毒剂。请回答下列问题:
(1)某同学设计如下实验研究 的性质:
的性质:
①理论上 既有氧化性又有还原性,具有还原性的原因是
既有氧化性又有还原性,具有还原性的原因是_______ 。
②能证明 具有还原性的是实验
具有还原性的是实验_______ (填序号)。
(2)84消毒液的有效成分为 。
。
①NaClO中Cl元素的化合价是_______ 。
②84消毒液不能用于钢制器具的消毒,原因是 具有
具有_______ 性。
③84消毒液吸收空气中的 ,其消毒杀菌能力增强,该过程中发生反应的化学方程式为
,其消毒杀菌能力增强,该过程中发生反应的化学方程式为_______ 。
(3)漂白粉在社会生活、工业生产中用途广泛。漂白粉除了具有漂白作用外,还能杀菌、消毒。
已知漂白粉溶于水后加入少量的酸能增强漂白效果。某同学据此将少量漂白粉溶于水后,再加入浓盐酸,观察到有黄绿色气体生成。回答下列问题:
①生成黄绿色气体的化学方程式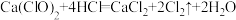 ,用双线桥表示反应电子转移方向和数目:
,用双线桥表示反应电子转移方向和数目:_______ 。
②家庭生活中常使用“84”消毒液进行消毒。这种消毒液和某品牌洁厕净(主要成分为盐酸)_______ (填“能”或“不能”)同时使用,其原因是_______ 。
 溶液和84消毒液是生活中常用的两种消毒剂。请回答下列问题:
溶液和84消毒液是生活中常用的两种消毒剂。请回答下列问题:(1)某同学设计如下实验研究
 的性质:
的性质:| 实验 | 操作 | 现象 |
| i | 向5% 溶液中滴加酸性 溶液中滴加酸性 溶液 溶液 | a.溶液紫色褪去 b.有大量气泡产生 |
| ii | 向5% 溶液中滴加淀粉碘化钾溶液 溶液中滴加淀粉碘化钾溶液 | c.溶液变蓝 |
 既有氧化性又有还原性,具有还原性的原因是
既有氧化性又有还原性,具有还原性的原因是②能证明
 具有还原性的是实验
具有还原性的是实验(2)84消毒液的有效成分为
 。
。①NaClO中Cl元素的化合价是
②84消毒液不能用于钢制器具的消毒,原因是
 具有
具有③84消毒液吸收空气中的
 ,其消毒杀菌能力增强,该过程中发生反应的化学方程式为
,其消毒杀菌能力增强,该过程中发生反应的化学方程式为(3)漂白粉在社会生活、工业生产中用途广泛。漂白粉除了具有漂白作用外,还能杀菌、消毒。
已知漂白粉溶于水后加入少量的酸能增强漂白效果。某同学据此将少量漂白粉溶于水后,再加入浓盐酸,观察到有黄绿色气体生成。回答下列问题:
①生成黄绿色气体的化学方程式
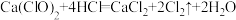 ,用双线桥表示反应电子转移方向和数目:
,用双线桥表示反应电子转移方向和数目:②家庭生活中常使用“84”消毒液进行消毒。这种消毒液和某品牌洁厕净(主要成分为盐酸)
您最近一年使用:0次
名校
5 . 某小组在实验室用NaClO溶液和NH3反应制备N2H4,并进行相关的性质探究实验。
I.制备N2H4
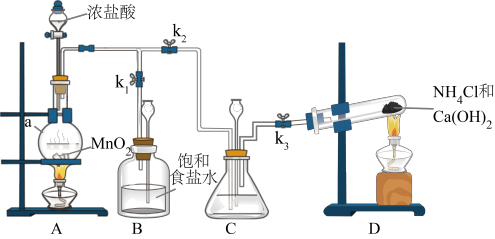
(1)装置C中盛放的试剂是___________ ,其作用是___________ 。(用离子方程式表示)
(2)装置D发生的反应的方程式为___________ 。
(3)制备N2H4的离子方程式为___________ 。
II.探究N2H4的还原性与碱性。将制得的肼分离提纯后,进行如图实验。
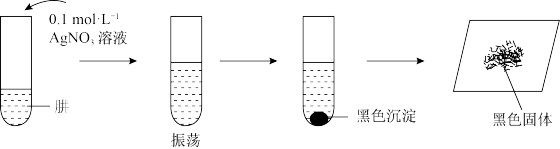
【查阅资料】AgOH在溶液中不稳定,易分解生成黑色的Ag2O,Ag2O可溶于氨水。
【提出假设】黑色固体可能是Ag、Ag2O中的一种或两种。
【实验验证】设计如表方案,进行实验。
(4)请完成表中的空白部分
(5)实验表明,黑色固体主要成分是Ag,还有少量氧化银。请解释原因:___________ 。
I.制备N2H4

(1)装置C中盛放的试剂是
(2)装置D发生的反应的方程式为
(3)制备N2H4的离子方程式为
II.探究N2H4的还原性与碱性。将制得的肼分离提纯后,进行如图实验。

【查阅资料】AgOH在溶液中不稳定,易分解生成黑色的Ag2O,Ag2O可溶于氨水。
【提出假设】黑色固体可能是Ag、Ag2O中的一种或两种。
【实验验证】设计如表方案,进行实验。
(4)请完成表中的空白部分
| 操作 | 现象 | 实验结论 |
| i. 取少量黑色固体于试管中,加入适量 | 黑色固体部分溶解 | 黑色固体有Ag2O |
| ii. 取少量黑色固体于试管中加入足量稀硝酸,振荡。 | 黑色固体是Ag和Ag2O |
您最近一年使用:0次
名校
解题方法
6 . 氯气在生产生活中应用广泛。
(1)实验室可用 与浓盐酸反应制取,反应原理如下:
与浓盐酸反应制取,反应原理如下: ,若制得标准状况下
,若制得标准状况下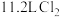 ,则被氧化的
,则被氧化的 为
为_______  。
。
(2)多余的氯气可用 溶液吸收,反应的离子方程式为
溶液吸收,反应的离子方程式为_______ 。工业上也可用 溶液吸收氯气获得
溶液吸收氯气获得 ,
, 广泛应用于电子工业、印染工业等领域。请写出该化学反应的离子方程式
广泛应用于电子工业、印染工业等领域。请写出该化学反应的离子方程式_______ 。
(3)海底蕴藏着丰富的锰结核矿,其主要成分是 。1991年由Allen等人研究,用硫酸淋洗后使用不同的方法可制备纯净的
。1991年由Allen等人研究,用硫酸淋洗后使用不同的方法可制备纯净的 ,其制备过程如图所示:
,其制备过程如图所示:

①步骤1中,试剂甲必须具有的性质是_______ (填序号)。
A. 氧化性 B. 还原性 C. 酸性
②步骤Ⅲ中,以 为氧化剂,当生成
为氧化剂,当生成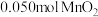 时,消耗
时,消耗 的
的 溶液
溶液 ,该反应的离子方程式为
,该反应的离子方程式为_______ 。
(4)已知:① 常温下与浓盐酸反应可制得
常温下与浓盐酸反应可制得 。②
。② 不溶于水。根据如图所示装置回答以下问题。
不溶于水。根据如图所示装置回答以下问题。
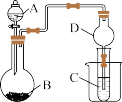
①利用如图装置可以验证元素非金属性的变化规律。图中 装置的名称是
装置的名称是_______ 。干燥管 的作用是
的作用是_______ 。
②实验室中现有药品 、
、 、浓盐酸、
、浓盐酸、 ,请选择合适药品设计实验验证氯的非金属性强于硫:烧瓶中发生反应的离子方程式为
,请选择合适药品设计实验验证氯的非金属性强于硫:烧瓶中发生反应的离子方程式为_______ 。装置 中的实验现象为有淡黄色沉淀生成,离子方程式为
中的实验现象为有淡黄色沉淀生成,离子方程式为_______ 。
(1)实验室可用
 与浓盐酸反应制取,反应原理如下:
与浓盐酸反应制取,反应原理如下: ,若制得标准状况下
,若制得标准状况下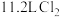 ,则被氧化的
,则被氧化的 为
为 。
。(2)多余的氯气可用
 溶液吸收,反应的离子方程式为
溶液吸收,反应的离子方程式为 溶液吸收氯气获得
溶液吸收氯气获得 ,
, 广泛应用于电子工业、印染工业等领域。请写出该化学反应的离子方程式
广泛应用于电子工业、印染工业等领域。请写出该化学反应的离子方程式(3)海底蕴藏着丰富的锰结核矿,其主要成分是
 。1991年由Allen等人研究,用硫酸淋洗后使用不同的方法可制备纯净的
。1991年由Allen等人研究,用硫酸淋洗后使用不同的方法可制备纯净的 ,其制备过程如图所示:
,其制备过程如图所示:
①步骤1中,试剂甲必须具有的性质是
A. 氧化性 B. 还原性 C. 酸性
②步骤Ⅲ中,以
 为氧化剂,当生成
为氧化剂,当生成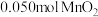 时,消耗
时,消耗 的
的 溶液
溶液 ,该反应的离子方程式为
,该反应的离子方程式为(4)已知:①
 常温下与浓盐酸反应可制得
常温下与浓盐酸反应可制得 。②
。② 不溶于水。根据如图所示装置回答以下问题。
不溶于水。根据如图所示装置回答以下问题。
①利用如图装置可以验证元素非金属性的变化规律。图中
 装置的名称是
装置的名称是 的作用是
的作用是②实验室中现有药品
 、
、 、浓盐酸、
、浓盐酸、 ,请选择合适药品设计实验验证氯的非金属性强于硫:烧瓶中发生反应的离子方程式为
,请选择合适药品设计实验验证氯的非金属性强于硫:烧瓶中发生反应的离子方程式为 中的实验现象为有淡黄色沉淀生成,离子方程式为
中的实验现象为有淡黄色沉淀生成,离子方程式为
您最近一年使用:0次
名校
7 . 某小组在实验室先制备NaClO溶液,再通入 反应制备
反应制备 (肼),并进行相关的性质探究实验。
(肼),并进行相关的性质探究实验。
I.制备
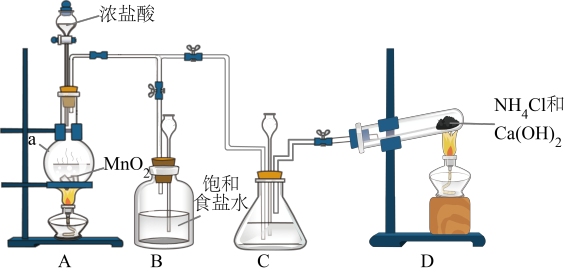
(1)仪器a的名称是___________ 。
(2)装置C中盛放的试剂是___________ 。
(3)装置D发生的化学反应方程式为___________ 。
(4)制备 的离子方程式为
的离子方程式为___________ 。
II.探究 (肼)的还原性与碱性。将制得的肼分离提纯后,进行如图实验。
(肼)的还原性与碱性。将制得的肼分离提纯后,进行如图实验。
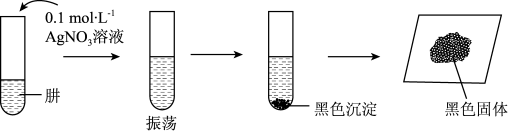
【查阅资料】AgOH在溶液中不稳定,易分解生成黑色的 ,
, 可溶于氨水。
可溶于氨水。
【提出假设】黑色固体可能是Ag、 中的一种或两种。
中的一种或两种。
【实验验证】设计如下方案,进行实验。
(5)请完成表中的空白部分
(6)实验表明,黑色固体主要成分是Ag,还有少量氧化银,请解释原因: ___________ 。
 反应制备
反应制备 (肼),并进行相关的性质探究实验。
(肼),并进行相关的性质探究实验。I.制备


(1)仪器a的名称是
(2)装置C中盛放的试剂是
(3)装置D发生的化学反应方程式为
(4)制备
 的离子方程式为
的离子方程式为II.探究
 (肼)的还原性与碱性。将制得的肼分离提纯后,进行如图实验。
(肼)的还原性与碱性。将制得的肼分离提纯后,进行如图实验。
【查阅资料】AgOH在溶液中不稳定,易分解生成黑色的
 ,
, 可溶于氨水。
可溶于氨水。【提出假设】黑色固体可能是Ag、
 中的一种或两种。
中的一种或两种。【实验验证】设计如下方案,进行实验。
(5)请完成表中的空白部分
| 操作 | 现象 | 实验结论 |
| i.取少量黑色固体于试管中,加入适量① | 黑色固体部分溶解 | 黑色固体有 |
| ii.取少量黑色固体于试管中加入足量稀硝酸,振荡 | ② | 黑色固体是Ag和 |
您最近一年使用:0次
8 . 利用下图,可以从不同角度研究含氯物质的性质及其转化关系,图中甲~辛均含氯元素。回答下列问题:

(1)丙的化学式为_______ ;从组成和性质上分析,丁属于_______ (填“酸性”或“碱性”)氧化物。
(2)图中甲、乙、丁、戊中,属于电解质的是__________ (填化学式);根据氯元素的化合价判断,乙物质__________ 。
a 只有氧化性 b 既有氧化性又有还原性
c 只有还原性 d 既能做氧化剂也能做还原剂
(3)电解甲溶液制备己的化学反应为:甲+ H2O→己+H2↑,反应中甲与H2O的物质的量之比是______ 。
(4)庚是漂白粉的有效成分,用乙制取庚的化学反应方程式为_________ 。
(5)辛在MnO2催化下受热分解可用于制备一种常见气体,这种气体的化学式是____ 。

(1)丙的化学式为
(2)图中甲、乙、丁、戊中,属于电解质的是
a 只有氧化性 b 既有氧化性又有还原性
c 只有还原性 d 既能做氧化剂也能做还原剂
(3)电解甲溶液制备己的化学反应为:甲+ H2O→己+H2↑,反应中甲与H2O的物质的量之比是
(4)庚是漂白粉的有效成分,用乙制取庚的化学反应方程式为
(5)辛在MnO2催化下受热分解可用于制备一种常见气体,这种气体的化学式是
您最近一年使用:0次
2020-03-15更新
|
265次组卷
|
4卷引用:山东省淄博市2019-2020学年高一上学期期末质量检测化学试题
山东省淄博市2019-2020学年高一上学期期末质量检测化学试题(已下线)【浙江新东方】【2020】【高一上】【期中】【HD-LP409】【化学】(已下线)【浙江新东方】72云南省大理州祥云县2019-2020学年高一下学期期末统测化学试题
名校
9 . 某小组同学探究不同条件下氯气与二价锰化合物的反应
资料:
ⅰ. 在一定条件下被
在一定条件下被  或
或 氧化成
氧化成  (棕黑色)、
(棕黑色)、 (绿色)、
(绿色)、 (紫色)。
(紫色)。
ⅱ.浓碱条件下, 可被
可被  还原为
还原为  。
。
ⅲ. 的氧化性与溶液的酸碱性无关,
的氧化性与溶液的酸碱性无关, 的氧化性随碱性增强而减弱。
的氧化性随碱性增强而减弱。
实验装置如图(夹持装置略)
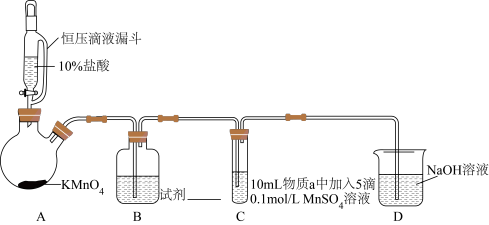
(1) 装置中制备
装置中制备  的化学反应方程式是
的化学反应方程式是__________ 。
(2) 中试剂是
中试剂是__________ 。
(3)通入 前,Ⅱ、Ⅲ中沉淀由白色变为黑色的化学方程式为
前,Ⅱ、Ⅲ中沉淀由白色变为黑色的化学方程式为__________ 。
(4)根据资料ⅱ,Ⅲ中应得到绿色溶液,实验中得到紫色溶液,分析现象与资料不符原因:
原因一:可能是通入 导致溶液的碱性减弱。
导致溶液的碱性减弱。
原因二:可能是氧化剂过量,氧化剂将 氧化为
氧化为  。
。
①化学方程式表示可能导致溶液碱性减弱的原因__________ ,但通过实验测定溶液的碱性变化很小。
②取Ⅲ中放置后的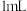 悬浊液,加入
悬浊液,加入 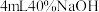 溶液,溶液紫色迅速变为绿色,且绿色缓慢加深。溶液紫色变为绿色的离子方程式为
溶液,溶液紫色迅速变为绿色,且绿色缓慢加深。溶液紫色变为绿色的离子方程式为__________ ,溶液绿色缓慢加深,原因是  被
被__________ (填化学式)氧化,可证明Ⅲ的悬浊液中氧化剂过量;
③取Ⅱ中放置后的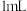 悬浊液,加入
悬浊液,加入  水,溶液紫色缓慢加深,发生的反应是
水,溶液紫色缓慢加深,发生的反应是__________ 。
资料:
ⅰ.
 在一定条件下被
在一定条件下被  或
或 氧化成
氧化成  (棕黑色)、
(棕黑色)、 (绿色)、
(绿色)、 (紫色)。
(紫色)。ⅱ.浓碱条件下,
 可被
可被  还原为
还原为  。
。ⅲ.
 的氧化性与溶液的酸碱性无关,
的氧化性与溶液的酸碱性无关, 的氧化性随碱性增强而减弱。
的氧化性随碱性增强而减弱。实验装置如图(夹持装置略)

序号 | 物质 | C中实验现象 | |
通入 | 通入 | ||
Ⅰ | 水 | 得到无色溶液 | 产生棕黑色沉淀,且放置后不发生变化 |
Ⅱ |
| 产生白色沉淀,在空气中缓慢变成棕黑色沉淀 | 棕黑色沉淀增多,放置后溶液变为紫色,仍有沉淀 |
Ⅲ |
| 产生白色沉淀,在空气中缓慢变成棕黑色沉淀 | 棕黑色沉淀增多,放置后溶液变为紫色,仍有沉淀 |
(1)
 装置中制备
装置中制备  的化学反应方程式是
的化学反应方程式是(2)
 中试剂是
中试剂是(3)通入
 前,Ⅱ、Ⅲ中沉淀由白色变为黑色的化学方程式为
前,Ⅱ、Ⅲ中沉淀由白色变为黑色的化学方程式为(4)根据资料ⅱ,Ⅲ中应得到绿色溶液,实验中得到紫色溶液,分析现象与资料不符原因:
原因一:可能是通入
 导致溶液的碱性减弱。
导致溶液的碱性减弱。原因二:可能是氧化剂过量,氧化剂将
 氧化为
氧化为  。
。①化学方程式表示可能导致溶液碱性减弱的原因
②取Ⅲ中放置后的
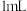 悬浊液,加入
悬浊液,加入 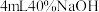 溶液,溶液紫色迅速变为绿色,且绿色缓慢加深。溶液紫色变为绿色的离子方程式为
溶液,溶液紫色迅速变为绿色,且绿色缓慢加深。溶液紫色变为绿色的离子方程式为 被
被③取Ⅱ中放置后的
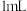 悬浊液,加入
悬浊液,加入  水,溶液紫色缓慢加深,发生的反应是
水,溶液紫色缓慢加深,发生的反应是
您最近一年使用:0次
名校
解题方法
10 . 下图是实验室制备 的实验装置图,其中甲为制氯气的装置。(资料:
的实验装置图,其中甲为制氯气的装置。(资料: 为紫色固体,微溶于KOH,具有强氧化性)
为紫色固体,微溶于KOH,具有强氧化性)
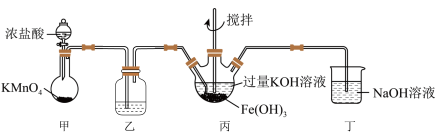
下列说法不正确 的是
 的实验装置图,其中甲为制氯气的装置。(资料:
的实验装置图,其中甲为制氯气的装置。(资料: 为紫色固体,微溶于KOH,具有强氧化性)
为紫色固体,微溶于KOH,具有强氧化性)
下列说法
A.甲装置不需要加热即可以产生氯气,说明氧化性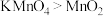 |
B.丙和丁中均会发生反应: |
C.丙中产生紫色固体,说明碱性条件下, 氧化性强于 氧化性强于 |
D.若取反应后丙中紫色溶液加入稀硫酸产生 ,可以证明 ,可以证明 具有氧化性 具有氧化性 |
您最近一年使用:0次


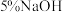 溶液
溶液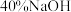 溶液
溶液

