解题方法
1 . 妈妈教小鲁蒸馒头:先用酵头发面,面团发酵至两倍大后,再加纯碱调节酸性,然后将面团揉切后上锅蒸即可。小鲁查阅资料得知,酵头可使面团在微生物作用下产生 气体,从而使面团疏松,但同时也会产生乳酸、醋酸等有机酸。
气体,从而使面团疏松,但同时也会产生乳酸、醋酸等有机酸。
(1)下列关于纯碱的认识正确的是_______。
(2)小鲁探究用 调节面团酸度,而不用
调节面团酸度,而不用 的原因。质量均为1g的
的原因。质量均为1g的 与
与 分别与足量酸反应生成
分别与足量酸反应生成 时,消耗
时,消耗 的物质的量更多的是
的物质的量更多的是_______ 。
(3)小鲁实际操作时,发现面团发得不好,面团内的气孔少。妈妈指导小鲁将 改用
改用 ,继续揉面,上锅蒸后果然蒸出了松软的馒头。该过程中
,继续揉面,上锅蒸后果然蒸出了松软的馒头。该过程中 的作用为
的作用为_______ 。
(4)Na保存在_______ 或石蜡油中,Na着火了,应用_______ 灭火。
 气体,从而使面团疏松,但同时也会产生乳酸、醋酸等有机酸。
气体,从而使面团疏松,但同时也会产生乳酸、醋酸等有机酸。(1)下列关于纯碱的认识正确的是_______。
| A.受热易分解 | B.水溶液显碱性 | C.属于碱 | D.可与酸反应 |
 调节面团酸度,而不用
调节面团酸度,而不用 的原因。质量均为1g的
的原因。质量均为1g的 与
与 分别与足量酸反应生成
分别与足量酸反应生成 时,消耗
时,消耗 的物质的量更多的是
的物质的量更多的是(3)小鲁实际操作时,发现面团发得不好,面团内的气孔少。妈妈指导小鲁将
 改用
改用 ,继续揉面,上锅蒸后果然蒸出了松软的馒头。该过程中
,继续揉面,上锅蒸后果然蒸出了松软的馒头。该过程中 的作用为
的作用为(4)Na保存在
您最近一年使用:0次
名校
2 . I.完成下列问题。
(1)明胶溶于水形成胶体,与溶液相比,胶体最本质的特征是________ 。
A.丁达尔效应 B.分散质直径在1-100nm之间 C.加入电解质会发生沉降
(2)下列方法不能用于鉴别碳酸钠固体和碳酸氢钠固体的是___________。
II.某研究性学习小组查阅资料发现,Na2O2与干燥的HCl气体能发生反应生成Cl2.;Na2O2+4HCl= 2NaCl+Cl2+2H2O。
(3)用双线桥标出该反应电子转移的方向和数目:Na2O2 + 4HCl = 2NaCl + Cl2 + 2H2O________ 。
(4)该反应中氧化剂是___________ (化学式,下同),氧化产物是___________ ,两者氧化性强弱相比,___________ 氧化性更强。
(1)明胶溶于水形成胶体,与溶液相比,胶体最本质的特征是
A.丁达尔效应 B.分散质直径在1-100nm之间 C.加入电解质会发生沉降
(2)下列方法不能用于鉴别碳酸钠固体和碳酸氢钠固体的是___________。
| A.滴加盐酸 | B.溶于水,滴加氯化钙 |
| C.滴加水,测温度变化 | D.溶于水,滴加澄清石灰水 |
II.某研究性学习小组查阅资料发现,Na2O2与干燥的HCl气体能发生反应生成Cl2.;Na2O2+4HCl= 2NaCl+Cl2+2H2O。
(3)用双线桥标出该反应电子转移的方向和数目:Na2O2 + 4HCl = 2NaCl + Cl2 + 2H2O
(4)该反应中氧化剂是
您最近一年使用:0次
2023-11-11更新
|
30次组卷
|
2卷引用:浙江省嘉兴市海盐高级中学2023-2024学年高一上学期10月阶段测化学试题
名校
解题方法
3 . 元素的价一类二维图是我们学习元素及其化合物相关知识的重要模型和工具,图为钠的价一类二维图。请回答以下问题:

(1)NaH中H元素的化合价是___________ 。
(2)钠单质通常保存在___________ 中。
(3)请写出①中某种淡黄色固体的用途:___________ 。
(4)把钠放到装有水的烧杯中,钠会浮在水面上,原因是___________ ;金属钠与水反应的离子方程式是___________ 。
(5)利用如图实验比较碳酸钠和碳酸氢钠的热稳定性,则物质甲的化学式为___________ ,写出实验过程中试管内发生反应的化学方程式:___________ 。


(1)NaH中H元素的化合价是
(2)钠单质通常保存在
(3)请写出①中某种淡黄色固体的用途:
(4)把钠放到装有水的烧杯中,钠会浮在水面上,原因是
(5)利用如图实验比较碳酸钠和碳酸氢钠的热稳定性,则物质甲的化学式为

您最近一年使用:0次
4 . 钠及其化合物在认识物质转化规律以及生产生活中均有重要应用。
Ⅰ.钠与水的反应
(1)将钠投入足量含有酚酞的水中,作了如下记录,将实验现象与匹配的实验结论连线:_______ 。
(2)写出钠与水反应的化学方程式_______ 。
(3)若反应中生成H2的体积为1.12L(标准状况下),则参与反应的金属Na的质量是_______ 。
(4)同物质类别的金属Mg也能与水发生反应,试着调用反应规律分析Na和Mg分别与水反应的剧烈程度:Na_______ Mg(填“>”“<”或“=”)。
Ⅱ.钠与氧气的反应
(5)钠与氧气反应的产物有多种可能,造成产物多样的原因是_______ 。
(6)其中产物_______ (填化学式)可用作潜水艇和呼吸面具中的供氧剂,写出其与CO2反应的化学方程式_______ 。
Ⅲ.碳酸钠、碳酸氢钠在食品加工方面有着广泛的用途
(7)下列关于Na2CO3的认识正确的是_______ 。
a.受热易分解 b.俗称纯碱、苏打 c.属于碱 d.可与酸反应
(8)传统蒸馒头常采用酵头发面,酵头可使面团在微生物作用下产生CO2气体,从而使面团疏松,但同时也会产生乳酸、醋酸等有机酸,需要额外添加“碱面”将酸去除。等质量的Na2CO3和NaHCO3,因_______ (填“Na2CO3”或“NaHCO3”)消耗酸更多,更适合作为中和发酵带来的酸味的“碱面”。
(9)若面团发得不好,面团内的气孔少,不够膨松。需添加_______ (填“Na2CO3”或“NaHCO3”),继续揉面,上锅蒸后也能蒸出松软的馒头。用化学方程式表示其产气原理_______ 。
Ⅰ.钠与水的反应
(1)将钠投入足量含有酚酞的水中,作了如下记录,将实验现象与匹配的实验结论连线:
实验现象 实验结论 A.钠浮在水面上 a.有碱生成B.钠四处游动 b.有气体产生 C.溶液变红 c.反应放热,钠熔点低 D.钠熔成光亮的小球 d.钠的密度比水小 |
(3)若反应中生成H2的体积为1.12L(标准状况下),则参与反应的金属Na的质量是
(4)同物质类别的金属Mg也能与水发生反应,试着调用反应规律分析Na和Mg分别与水反应的剧烈程度:Na
Ⅱ.钠与氧气的反应
(5)钠与氧气反应的产物有多种可能,造成产物多样的原因是
(6)其中产物
Ⅲ.碳酸钠、碳酸氢钠在食品加工方面有着广泛的用途
(7)下列关于Na2CO3的认识正确的是
a.受热易分解 b.俗称纯碱、苏打 c.属于碱 d.可与酸反应
(8)传统蒸馒头常采用酵头发面,酵头可使面团在微生物作用下产生CO2气体,从而使面团疏松,但同时也会产生乳酸、醋酸等有机酸,需要额外添加“碱面”将酸去除。等质量的Na2CO3和NaHCO3,因
(9)若面团发得不好,面团内的气孔少,不够膨松。需添加
您最近一年使用:0次
名校
5 . 据已经学过的化学知识,回答下列问题。金属及其化合物在生产生活中有着广泛的应用。
(1)胃舒平(主要成分为氢氧化铝)可用于治疗胃酸过多,氢氧化铝体现_______ 性;_______ (填“能”或“不能”)用氢氧化钠溶液代替。
(2)NaHSO4是一种酸式盐,写出NaHSO4在水中的电离方程式:_______ 。
(3)将Cu与稀硫酸混合,二者不能反应,滴入H2O2后,溶液很快变成蓝色,该反应的化学方程式为_______ 。
(4)Na2CO3和NaHCO3是厨房中常见的两种盐,可用化学性质的差异进行鉴别。回答下列问题:
①与酸反应的差异。甲组进行了如图4组实验。

其中实验_______ 和_______ (填实验序号)可以鉴别Na2CO3和NaHCO3。
②热稳定性差异。乙组设计如图装置进行实验(加热及夹持装置省略)。

将分别装有Na2CO3和NaHCO3的试管同时放入甘油浴加热(甘油沸点为290℃)。该实验用饱和碳酸钠溶液检验反应的产物,b试管中的实验现象分别为:_______ ,试管b中发生反应的化学方程式为_______ 。
(1)胃舒平(主要成分为氢氧化铝)可用于治疗胃酸过多,氢氧化铝体现
(2)NaHSO4是一种酸式盐,写出NaHSO4在水中的电离方程式:
(3)将Cu与稀硫酸混合,二者不能反应,滴入H2O2后,溶液很快变成蓝色,该反应的化学方程式为
(4)Na2CO3和NaHCO3是厨房中常见的两种盐,可用化学性质的差异进行鉴别。回答下列问题:
①与酸反应的差异。甲组进行了如图4组实验。

其中实验
②热稳定性差异。乙组设计如图装置进行实验(加热及夹持装置省略)。

将分别装有Na2CO3和NaHCO3的试管同时放入甘油浴加热(甘油沸点为290℃)。该实验用饱和碳酸钠溶液检验反应的产物,b试管中的实验现象分别为:
您最近一年使用:0次
名校
6 . 通过学习小鲁知道膨松剂的主要成分是碳酸氢钠,但妈妈教小鲁蒸馒头时是先用酵头发面,面团发酵至两倍大后,再加纯碱调节酸性,然后将面团揉切后上锅蒸即可。小鲁查阅资料得知,酵头可使面团在微生物作用下产生 气体,从而使面团疏松,但同时也会产生乳酸、醋酸等有机酸。
气体,从而使面团疏松,但同时也会产生乳酸、醋酸等有机酸。
(1)下列关于纯碱的认识正确的是___________(填字母)。
(2)小鲁探究用 调节面团酸度,而不用
调节面团酸度,而不用 的原因。等质量的
的原因。等质量的 与
与 与酸反应时,消耗酸的物质的量更多的是
与酸反应时,消耗酸的物质的量更多的是___________ 。(填化学式)
(3)小鲁实际操作时,发现面团发得不好,面团内的气孔少,略有酸味。妈妈指导小鲁将 改用
改用 ,继续揉面,上锅蒸后果然蒸出了松软的馒头。解释
,继续揉面,上锅蒸后果然蒸出了松软的馒头。解释 的作用
的作用___________ (用化学方程式表示),若膨松剂中含有 完全分解产生的
完全分解产生的 在标况下的体积为
在标况下的体积为___________ L。
 气体,从而使面团疏松,但同时也会产生乳酸、醋酸等有机酸。
气体,从而使面团疏松,但同时也会产生乳酸、醋酸等有机酸。(1)下列关于纯碱的认识正确的是___________(填字母)。
| A.受热易分解 | B.水溶液显碱性 | C.属于醎 | D.可与酸反应 |
 调节面团酸度,而不用
调节面团酸度,而不用 的原因。等质量的
的原因。等质量的 与
与 与酸反应时,消耗酸的物质的量更多的是
与酸反应时,消耗酸的物质的量更多的是(3)小鲁实际操作时,发现面团发得不好,面团内的气孔少,略有酸味。妈妈指导小鲁将
 改用
改用 ,继续揉面,上锅蒸后果然蒸出了松软的馒头。解释
,继续揉面,上锅蒸后果然蒸出了松软的馒头。解释 的作用
的作用 完全分解产生的
完全分解产生的 在标况下的体积为
在标况下的体积为
您最近一年使用:0次
23-24高一上·全国·课时练习
解题方法
7 . 相同质量的Na2CO3和NaHCO3分别与足量盐酸反应时,哪个放出CO2的速度快且量多?______
您最近一年使用:0次
8 . NaCl是一种化工原料,可以制备一系列物质,如图所示。

(1)下列说法不正确的是___________(填字母)。
(2)Cl2与Ca(OH)2反应的化学方程式为___________ 。
(3)84消毒液(含次氯酸钠)不能与洁厕剂(含盐酸)混合使用,否则可能产生使人中毒的气体,请解释其原因___________ (用化学反应方程式表示)。
(4)纯净的氢气在氯气中燃烧的现象是___________ 。
(5)实验室常用浓盐酸和MnO2加热制备氯气,请写出该反应的离子方程式___________ 。

(1)下列说法不正确的是___________(填字母)。
| A.Na2CO3的热稳定性比NaHCO3强 |
| B.侯氏制碱法可以制得Na2CO3 |
| C.图示转化反应都是氧化还原反应 |
| D.焰色试验中需用硫酸洗净铁丝,并灼烧至与原来的火焰颜色相同为止 |
(2)Cl2与Ca(OH)2反应的化学方程式为
(3)84消毒液(含次氯酸钠)不能与洁厕剂(含盐酸)混合使用,否则可能产生使人中毒的气体,请解释其原因
(4)纯净的氢气在氯气中燃烧的现象是
(5)实验室常用浓盐酸和MnO2加热制备氯气,请写出该反应的离子方程式
您最近一年使用:0次
解题方法
9 . 碳酸钠和碳酸氢钠是厨房常见物质,某小组为探究碳酸钠和碳酸氢钠的性质,进行如下实验。
(1)取少量Na2CO3粉末配成溶液,向其中滴加几滴酚酞试液,现象是
_____ 。
(2)利用如图所示装置进行NaHCO3的受热分解实验。

①安装好仪器后首先应该进行的操作是_____ ;
②试管a中盛放的试剂是_____ ;
③NaHCO3受热分解的化学方程式是_____ ;
(3)可用来鉴别NaHCO3溶液和Na2CO3溶液的试剂为
_____ 。
①CO2②澄清石灰水③CaCl2溶液④NaHSO4溶液⑤稀盐酸⑥NaOH溶液
(4)写出澄清石灰水与过量NaHCO3溶液反应的离子方程式
_____ ;
(1)取少量Na2CO3粉末配成溶液,向其中滴加几滴酚酞试液,现象是
(2)利用如图所示装置进行NaHCO3的受热分解实验。

①安装好仪器后首先应该进行的操作是
②试管a中盛放的试剂是
③NaHCO3受热分解的化学方程式是
(3)可用来鉴别NaHCO3溶液和Na2CO3溶液的试剂为
①CO2②澄清石灰水③CaCl2溶液④NaHSO4溶液⑤稀盐酸⑥NaOH溶液
(4)写出澄清石灰水与过量NaHCO3溶液反应的离子方程式
您最近一年使用:0次
名校
解题方法
10 . 分类是研究物质性质的重要方法,如图对某些物质进行分类。
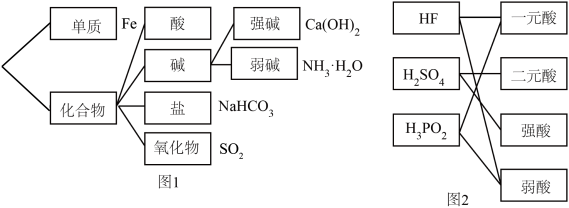
回答下列问题:
(1) 在水溶液中的电离方程式是
在水溶液中的电离方程式是_______ 。
(2)写出 与足量
与足量 反应的离子方程式是
反应的离子方程式是_______ 。
(3) 可以与
可以与 反应生成
反应生成 沉淀,反应的离子方程式是
沉淀,反应的离子方程式是_______ 。
(4)食品工业经常把 和
和 用作膨松剂,室温下向含
用作膨松剂,室温下向含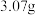 某膨松剂试样
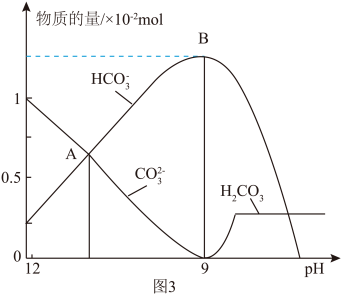
某膨松剂试样 溶液中逐滴加入稀盐酸,反应过程中含碳元素微粒的物质的量随
溶液中逐滴加入稀盐酸,反应过程中含碳元素微粒的物质的量随 变化的图象如图(
变化的图象如图( 因有逸出未画出)。已知:
因有逸出未画出)。已知: 与少量盐酸发生下列反应
与少量盐酸发生下列反应 。
。
①图3中 点溶液溶质的主要成分为
点溶液溶质的主要成分为_______ (填化学式),B点后发生反应的离子反应方程式为_______ 。
②如图3所示,试计算该试样中水的含量为_______  ,某同学用酒精灯对该试样固体充分加热至恒重,残留在试管中的固体是
,某同学用酒精灯对该试样固体充分加热至恒重,残留在试管中的固体是_______ (填化学式)。

回答下列问题:
(1)
 在水溶液中的电离方程式是
在水溶液中的电离方程式是(2)写出
 与足量
与足量 反应的离子方程式是
反应的离子方程式是(3)
 可以与
可以与 反应生成
反应生成 沉淀,反应的离子方程式是
沉淀,反应的离子方程式是(4)食品工业经常把
 和
和 用作膨松剂,室温下向含
用作膨松剂,室温下向含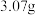 某膨松剂试样
某膨松剂试样 溶液中逐滴加入稀盐酸,反应过程中含碳元素微粒的物质的量随
溶液中逐滴加入稀盐酸,反应过程中含碳元素微粒的物质的量随 变化的图象如图(
变化的图象如图( 因有逸出未画出)。已知:
因有逸出未画出)。已知: 与少量盐酸发生下列反应
与少量盐酸发生下列反应 。
。①图3中
 点溶液溶质的主要成分为
点溶液溶质的主要成分为②如图3所示,试计算该试样中水的含量为
 ,某同学用酒精灯对该试样固体充分加热至恒重,残留在试管中的固体是
,某同学用酒精灯对该试样固体充分加热至恒重,残留在试管中的固体是
您最近一年使用:0次



