名校
解题方法
1 . 黔江中学某研究小组对工业废水所含离子成分进行了探究。已知该废水中仅含H+、Na+、Fe3+、Ag+、Cl-、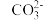 、NO
、NO 、SO
、SO 中的几种离子,且每种离子数目相等。
中的几种离子,且每种离子数目相等。
实验步骤如下:
①取废水少许,加入紫色石蕊溶液显红色;另取废水少许,加入硫氰化钾溶液显红色。
②取废水少许,加入BaCl2溶液产生白色沉淀,再加入足量盐酸白色沉淀不溶解。
③取②中上层清液,加入AgNO3溶液,产生白色沉淀。
下列说法正确的是
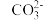 、NO
、NO 、SO
、SO 中的几种离子,且每种离子数目相等。
中的几种离子,且每种离子数目相等。实验步骤如下:
①取废水少许,加入紫色石蕊溶液显红色;另取废水少许,加入硫氰化钾溶液显红色。
②取废水少许,加入BaCl2溶液产生白色沉淀,再加入足量盐酸白色沉淀不溶解。
③取②中上层清液,加入AgNO3溶液,产生白色沉淀。
下列说法正确的是
A.该废水中一定含有H+、Fe3+、SO 、Cl-、NO 、Cl-、NO |
B.该废水中一定不含Cl-、CO |
C.无法确定是否含有NO 、Ag+ 、Ag+ |
D.实验①加入硫氰化钾溶液显红色的离子方程式为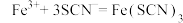 |
您最近一年使用:0次
名校
解题方法
2 . 下列各组离子在选项条件下一定能大量共存的是
A.无色溶液:Na+、Cu2+、Cl−、 |
B.酸性溶液: 、Fe3+、S2−、 、Fe3+、S2−、 |
C.遇酚酞变红的溶液:Na+、K+、 、 、 |
D.碱性溶液:K+、Al3+、 、 、 |
您最近一年使用:0次
名校
解题方法
3 . 根据下列操作和现象所得到的结论正确的是( )
| 选项 | 实验操作和现象 | 实验结论 |
| A | 向某黄色溶液中加入苯,振荡,静置,溶液分层,上层为橙红色 | 溶液中含Br2 |
| B | 用氢氧化铁胶体做电泳实验,通电一段时间后,与电源负极相连的一极颜色变深 | 氢氧化铁胶体带正电荷 |
| C | 将少量铜粉加入1.0 mol • L-1 Fe2(SO4)3溶液中,铜粉溶解 | 金属铁比铜活泼 |
| D | 向饱和Na2CO3溶液中加入少量甲酸溶液,无气泡冒出 | 酸性:碳酸>甲酸 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
4 . 二氧化铈(CeO2)是一种重要的稀土氧化物,平板电视显示屏生产过程中产生大量的废玻璃粉末(含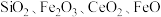 等物质)。某课题组以此粉末为原料,设计如下工艺流程对资源进行回收,得到纯净的CeO2和硫酸铁铵晶体。已知:CeO2不溶于稀硫酸,也不溶于NaOH溶液。
等物质)。某课题组以此粉末为原料,设计如下工艺流程对资源进行回收,得到纯净的CeO2和硫酸铁铵晶体。已知:CeO2不溶于稀硫酸,也不溶于NaOH溶液。
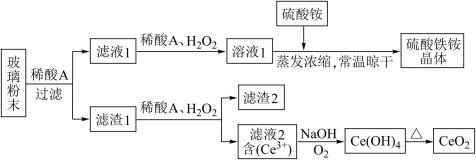
(1)稀酸A的分子式是___________ 。
(2)滤液1中加入H2O2溶液的目的是___________ 。
(3)设计实验证明滤液1中含有Fe2+____________ 。
(4)在酸性溶液中,已知Fe2+溶液可以和难溶于水的FeO(OH)反应生成Fe3O4,书写该反应的离子方程式________________ 。
(5)由滤液2生成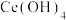 的离子方程式
的离子方程式______________ 。
(6)硫酸铁铵晶体 广泛用于水的净化处理,但其在去除酸性废水中的悬浮物时效率降低,其原因是
广泛用于水的净化处理,但其在去除酸性废水中的悬浮物时效率降低,其原因是_________ 。
(7)取上述流程中得到的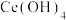 产品0.832g,加硫酸溶解后,用浓度为0.1000
产品0.832g,加硫酸溶解后,用浓度为0.1000 的
的 标准溶液滴定至终点时(铈被还原为
标准溶液滴定至终点时(铈被还原为 ),消耗20.00mL标准溶液。该产品中
),消耗20.00mL标准溶液。该产品中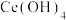 的质量分数为
的质量分数为___________ 。
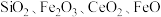 等物质)。某课题组以此粉末为原料,设计如下工艺流程对资源进行回收,得到纯净的CeO2和硫酸铁铵晶体。已知:CeO2不溶于稀硫酸,也不溶于NaOH溶液。
等物质)。某课题组以此粉末为原料,设计如下工艺流程对资源进行回收,得到纯净的CeO2和硫酸铁铵晶体。已知:CeO2不溶于稀硫酸,也不溶于NaOH溶液。
(1)稀酸A的分子式是
(2)滤液1中加入H2O2溶液的目的是
(3)设计实验证明滤液1中含有Fe2+
(4)在酸性溶液中,已知Fe2+溶液可以和难溶于水的FeO(OH)反应生成Fe3O4,书写该反应的离子方程式
(5)由滤液2生成
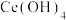 的离子方程式
的离子方程式(6)硫酸铁铵晶体
 广泛用于水的净化处理,但其在去除酸性废水中的悬浮物时效率降低,其原因是
广泛用于水的净化处理,但其在去除酸性废水中的悬浮物时效率降低,其原因是(7)取上述流程中得到的
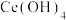 产品0.832g,加硫酸溶解后,用浓度为0.1000
产品0.832g,加硫酸溶解后,用浓度为0.1000 的
的 标准溶液滴定至终点时(铈被还原为
标准溶液滴定至终点时(铈被还原为 ),消耗20.00mL标准溶液。该产品中
),消耗20.00mL标准溶液。该产品中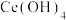 的质量分数为
的质量分数为
您最近一年使用:0次
2020-07-03更新
|
234次组卷
|
2卷引用:重庆市黔江新华中学校2021届高三上学期9月月考化学试题



