名校
1 . 将 和
和 的混合气体通入
的混合气体通入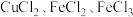 的混合溶液中,转化关系如图所示,下列说法正确的是
的混合溶液中,转化关系如图所示,下列说法正确的是
 和
和 的混合气体通入
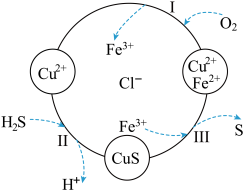
的混合气体通入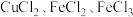 的混合溶液中,转化关系如图所示,下列说法正确的是
的混合溶液中,转化关系如图所示,下列说法正确的是
A.整个过程可以循环利用的离子只有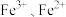 |
B.过程Ⅱ反应的离子方程式为 |
| C.在图示转化关系中化合价发生改变的元素只有O和S |
D.从上述转化过程可以得出氧化性强弱顺序为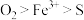 |
您最近一年使用:0次
2023-07-05更新
|
320次组卷
|
2卷引用:重庆市西南大学附属中学2022-2023学年高一上学期期中考试化学试题
名校
2 . 下列指定反应的离子方程式正确的是
A.氯化铁溶液腐蚀铜箔: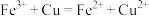 |
B.氯气通入KI溶液中: |
C.氯化铝溶液与浓氨水混合: |
D.氢氧化镁固体溶解于氯化铵溶液: |
您最近一年使用:0次
3 . 硼酸( )是一种重要的化工原料,广泛应用于玻璃、医药、肥料等工艺。一种以硼镁矿(含
)是一种重要的化工原料,广泛应用于玻璃、医药、肥料等工艺。一种以硼镁矿(含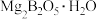 、
、 及少量
及少量 、
、 )为原料生产硼酸及轻质氧化镁的工艺流程如下:
)为原料生产硼酸及轻质氧化镁的工艺流程如下:
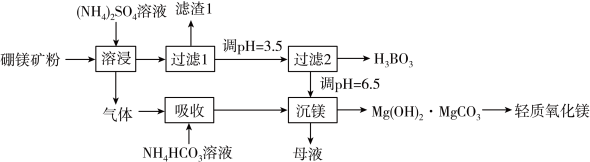
已知:
回答下列问题:
(1)在95℃“溶浸”硼镁矿粉,产生的气体在“吸收”中反应的化学方程式___________ 。
(2)“滤渣1”的主要成分有___________ (填化学式)。为检验“过滤1”后的滤液中是否含有 离子,可选用的化学试剂是
离子,可选用的化学试剂是___________ (填化学式)。
(3)已知 的电离方程式为
的电离方程式为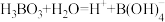 ,可知
,可知 为
为___________ 元弱酸,请写出 与足量
与足量 溶液反应的离子方程式
溶液反应的离子方程式___________ ;“过滤2”前,将溶液pH调节至3.5的目的是___________ 。
(4)“沉镁”后分离生成的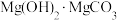 沉淀的操作为
沉淀的操作为___________ ,母液经加热后可返回___________ (填“溶浸”“吸收”或“沉镁”)工序循环使用。高温焙烧碱式碳酸镁可制备轻质氧化镁,写出化学方程式___________ 。
 )是一种重要的化工原料,广泛应用于玻璃、医药、肥料等工艺。一种以硼镁矿(含
)是一种重要的化工原料,广泛应用于玻璃、医药、肥料等工艺。一种以硼镁矿(含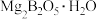 、
、 及少量
及少量 、
、 )为原料生产硼酸及轻质氧化镁的工艺流程如下:
)为原料生产硼酸及轻质氧化镁的工艺流程如下:
已知:

回答下列问题:
(1)在95℃“溶浸”硼镁矿粉,产生的气体在“吸收”中反应的化学方程式
(2)“滤渣1”的主要成分有
 离子,可选用的化学试剂是
离子,可选用的化学试剂是(3)已知
 的电离方程式为
的电离方程式为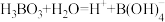 ,可知
,可知 为
为 与足量
与足量 溶液反应的离子方程式
溶液反应的离子方程式(4)“沉镁”后分离生成的
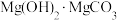 沉淀的操作为
沉淀的操作为
您最近一年使用:0次
名校
解题方法
4 . 下列除杂试剂选用正确且除杂过程涉及氧化还原的是
| 括号内为杂质 | 除杂试剂 | |
| A |  溶液 溶液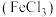 | 铜粉 |
| B |  溶液 溶液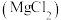 |  溶液、稀盐酸 溶液、稀盐酸 |
| C |  | 饱和 溶液、浓硫酸 溶液、浓硫酸 |
| D |  | 酸性高锰酸钾溶液、浓硫酸 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-03-22更新
|
247次组卷
|
2卷引用:重庆西南大学附属中学2022-2023学年高一下学期第一次月考化学试题
名校
解题方法
5 . 铁是人类使用最早的金属之一。运用所学知识,回答下列问题:
(1)电子工业用 溶液腐蚀覆在绝缘板上的铜,制造印刷电路板,请写出
溶液腐蚀覆在绝缘板上的铜,制造印刷电路板,请写出 溶液与铜反应的化学方程式为
溶液与铜反应的化学方程式为_______ 。
(2)某研究性学习小组为测定 溶液腐蚀铜后所得溶液的组成,进行了如下实验:
溶液腐蚀铜后所得溶液的组成,进行了如下实验:
①取少量待测溶液,滴入KSCN溶液呈红色,则待测液中含有的金属阳离子有_______ 。
②溶液组成测定:取50.0mL待测溶液,加入足量的 溶液,得到14.35g白色沉淀,则溶液中
溶液,得到14.35g白色沉淀,则溶液中
_______  。
。
③验证该溶液中是否含有 ,正确的实验方法是
,正确的实验方法是_______ (填序号)。
A.观察溶液是否呈浅绿色
B.取适量溶液,滴入酸性高锰酸钾溶液,若褪色,证明含有
C.取适量溶液先滴入双氧水再滴入KSCN溶液,若溶液显红色,证明原溶液中含有
D.取适量溶液,滴入 溶液,若产生蓝色沉淀,证明含有
溶液,若产生蓝色沉淀,证明含有
(3)工程师欲从制造印刷电路板的废液中回收铜,并获得 溶液,设计如下方案:
溶液,设计如下方案:
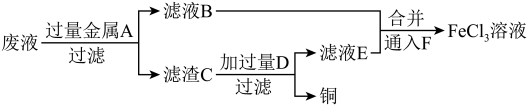
①滤渣C中物质的化学式为_______ 。
②加入过量D发生反应的离子方程式为_______ 。
③向滤液B和滤液E中通入F的目的是_______ ,该反应的离子方程式为_______ 。
④向盛有氯化铁、氯化亚铁、氯化铜混合溶液的烧杯中加入铁粉和铜粉,反应结束后,下列结果不可能出现的是_______ (填序号)。
A.有铜单质剩余但无铁单质剩余 B.有铁单质剩余但无铜单质剩余
C.铁、铜单质都有剩余 D.铁、铜单质都无剩余
(1)电子工业用
 溶液腐蚀覆在绝缘板上的铜,制造印刷电路板,请写出
溶液腐蚀覆在绝缘板上的铜,制造印刷电路板,请写出 溶液与铜反应的化学方程式为
溶液与铜反应的化学方程式为(2)某研究性学习小组为测定
 溶液腐蚀铜后所得溶液的组成,进行了如下实验:
溶液腐蚀铜后所得溶液的组成,进行了如下实验:①取少量待测溶液,滴入KSCN溶液呈红色,则待测液中含有的金属阳离子有
②溶液组成测定:取50.0mL待测溶液,加入足量的
 溶液,得到14.35g白色沉淀,则溶液中
溶液,得到14.35g白色沉淀,则溶液中
 。
。③验证该溶液中是否含有
 ,正确的实验方法是
,正确的实验方法是A.观察溶液是否呈浅绿色
B.取适量溶液,滴入酸性高锰酸钾溶液,若褪色,证明含有

C.取适量溶液先滴入双氧水再滴入KSCN溶液,若溶液显红色,证明原溶液中含有

D.取适量溶液,滴入
 溶液,若产生蓝色沉淀,证明含有
溶液,若产生蓝色沉淀,证明含有
(3)工程师欲从制造印刷电路板的废液中回收铜,并获得
 溶液,设计如下方案:
溶液,设计如下方案:
①滤渣C中物质的化学式为
②加入过量D发生反应的离子方程式为
③向滤液B和滤液E中通入F的目的是
④向盛有氯化铁、氯化亚铁、氯化铜混合溶液的烧杯中加入铁粉和铜粉,反应结束后,下列结果不可能出现的是
A.有铜单质剩余但无铁单质剩余 B.有铁单质剩余但无铜单质剩余
C.铁、铜单质都有剩余 D.铁、铜单质都无剩余
您最近一年使用:0次
名校
解题方法
6 . 下列反应的离子方程式正确的是
A. 沉淀溶于 沉淀溶于 溶液: 溶液: |
B.向 溶液中加入过量的氨水: 溶液中加入过量的氨水: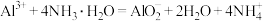 |
C.向 溶液中通入少量 溶液中通入少量 : :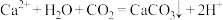 |
D.碳酸氢钠溶液与 溶液反应: 溶液反应: |
您最近一年使用:0次
名校
解题方法
7 . 根据下列实验和现象,所得实验结论正确的是
| 实验 | 现象 | 实验结论 | |
| A |  | 左边棉球变橙色,右边棉球变蓝色 | 氧化性: |
| B |  | 加入KSCN溶液后,试管中溶液颜色变红 | 加入 溶液前试管内的溶液中有 溶液前试管内的溶液中有 |
| C |  | 左边试管产生白色沉淀,加入KI溶液后产生黄色沉淀 |  |
| D |  | 以甲基橙做指示剂,达滴定终点时锥形瓶中溶液由红色变为橙色 | 测得的醋酸浓度偏大 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2022-11-28更新
|
198次组卷
|
3卷引用:重庆市西南大学附属中学校2022-2023学年高三上学期11月拔尖强基联合定时检测化学试题
名校
解题方法
8 . 下列实验方案的设计、现象和结论不正确的是
| 选项 | 实验操作 | 实验现象 | 解释与结论 |
| A | 将红棕色气体X通入淀粉-KI溶液中 | 溶液变成蓝色 | X为溴蒸气 |
| B | 用pH计测量同温同浓度的 和 和 溶液的pH 溶液的pH | 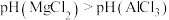 | 金属性:Mg>Al |
| C | 向足量含有KSCN的 溶液中滴加2滴氯水 溶液中滴加2滴氯水 | 溶液变成血红色 | 还原性: |
| D | 向等浓度的NaCl和NaI混合溶液中滴加几滴银氨溶液 | 立即产生黄色沉淀 |  : : |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
9 . 在硫酸铁溶液中,加入铜粉至完全溶解后,又加入一定量的铁粉,充分反应后有残余固体,则下列判断正确的是
| A.最后得到的溶液中只含Cu2+ | B.残余固体一定全部是铜 |
| C.残余固体可能为铁、铜混合物 | D.最后得到的溶液中含有Fe3+ |
您最近一年使用:0次
2021-09-13更新
|
322次组卷
|
17卷引用:重庆市北碚区2019-2020学年高一11月联合性测试化学试题
重庆市北碚区2019-2020学年高一11月联合性测试化学试题广西陆川中学2017-2018学年高一上学期期末考试化学试题甘肃省天水市一中2017-2018学年高一上学期第三次(期末)考试化学试题福建师大附中2017-2018学年高一上学期期末考试化学试题江西省南昌市第十中学2017-2018学年高一上学期期末考试化学试题【校级联考】天津市六校(静海一中、宝坻一中、杨村一中等)2018-2019学年高一上学期期末考试化学试题福建省莆田第六中学2018-2019学年高一(实验班)下学期期中考试化学试题福建省莆田第六中学2018-2019学年高一下学期期中考试化学试题宁夏银川市第二中学2019-2020学年高一上学期期末考试化学试题高一必修第一册(鲁科2019)第3章 第1节 铁的多样性江西省贵溪市实验中学高中部2020-2021学年高一下学期第二次月考化学试题河北省石家庄精英中学2018-2019学年高一上学期期末考试化学试题河南省范县第一中学等学校2021-2022学年高一上学期联考检测化学(B卷)试题河南省洛阳市伊川县第一高中2021-2022学年高一上学期第二次月考化学试题云南省玉溪市江川区第二中学2021-2022学年高一上学期12月考试化学试题(已下线)河北省石家庄精英中学2022-2023学年高一上学期第四次考试化学试题山东省菏泽市第一中学2023-2024学年高一上学期第三次月考化学试题
名校
10 . 某废催化剂含58.2% SiO2、21.0% ZnO、4.50% ZnS和12.8% CuS及少量的Fe3O4。某同学用15.0 g该废催化剂为原料,回收锌和铜。设计实验流程如图:
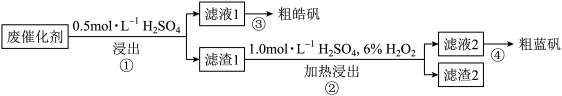
下列说法正确的是

下列说法正确的是
| A.某同学在实验完成之后,得到1.50 g CuSO4∙5H2O,则铜的回收率为30% |
| B.检验滤液1中是否含有Fe2+,可以选用KSCN和新制的氯水 |
| C.步骤②操作中,应先加6% H2O2,再在加热搅拌下缓慢加入1.0 mol∙L−1 H2SO4 |
| D.步骤①④都需要用到蒸发皿、酒精灯、漏斗、烧杯等玻璃仪器 |
您最近一年使用:0次



