名校
解题方法
1 . 氢能是一种极具发展潜力的清洁能源,目前有以下制取氢气的方法:
(1)水煤气变换制氢: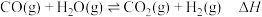
已知: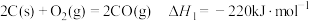
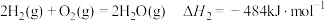
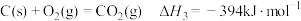
水煤气变换制氢体系中,一定时间内, 的添加情况与
的添加情况与 的体积分数关系如图。
的体积分数关系如图。
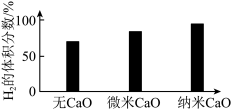
①水煤气变换制氢反应的
___________  。
。
②添加 后
后 的体积分数增大的原因是
的体积分数增大的原因是___________ (用化学方程式表达)。
③对比纳米 和微
和微 ,前者
,前者 的体积分数更大的原因是
的体积分数更大的原因是___________ 。
(2)甲醇水蒸气重整制氢: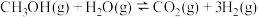 。控制原料气
。控制原料气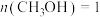 ,体系中甲醇的平衡转化率与温度和压强的关系如图。
,体系中甲醇的平衡转化率与温度和压强的关系如图。
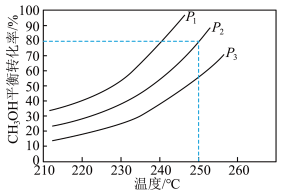
①甲醇水蒸气重整制氢反应在___________ 条件(填“高温”“低温”或“任意温度”)下能自发进行。
②图中的压强由小到大的顺序是___________ ,理由是___________ 。
③温度为250℃、压强为P2时,该反应的压力平衡常数Kp=___________ (列出算式)。
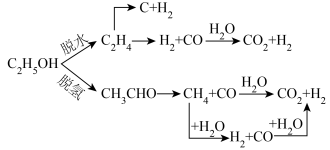
(3)乙醇重整制氢两条途径的机理如下图,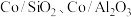 和
和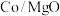 催化剂(酸性
催化剂(酸性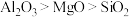 )在反应中表现出良好的催化活性和氢气选择性,但经长期反应后,催化剂表面均发现了积碳,积碳量
)在反应中表现出良好的催化活性和氢气选择性,但经长期反应后,催化剂表面均发现了积碳,积碳量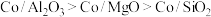 ,试分析
,试分析 表面的积碳量最大的原因
表面的积碳量最大的原因___________ 。
(1)水煤气变换制氢:
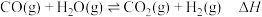
已知:
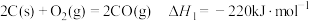
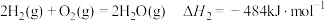
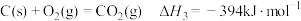
水煤气变换制氢体系中,一定时间内,
 的添加情况与
的添加情况与 的体积分数关系如图。
的体积分数关系如图。
①水煤气变换制氢反应的

 。
。②添加
 后
后 的体积分数增大的原因是
的体积分数增大的原因是③对比纳米
 和微
和微 ,前者
,前者 的体积分数更大的原因是
的体积分数更大的原因是(2)甲醇水蒸气重整制氢:
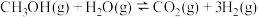 。控制原料气
。控制原料气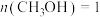 ,体系中甲醇的平衡转化率与温度和压强的关系如图。
,体系中甲醇的平衡转化率与温度和压强的关系如图。
①甲醇水蒸气重整制氢反应在
②图中的压强由小到大的顺序是
③温度为250℃、压强为P2时,该反应的压力平衡常数Kp=
(3)乙醇重整制氢两条途径的机理如下图,
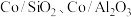 和
和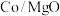 催化剂(酸性
催化剂(酸性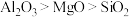 )在反应中表现出良好的催化活性和氢气选择性,但经长期反应后,催化剂表面均发现了积碳,积碳量
)在反应中表现出良好的催化活性和氢气选择性,但经长期反应后,催化剂表面均发现了积碳,积碳量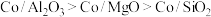 ,试分析
,试分析 表面的积碳量最大的原因
表面的积碳量最大的原因
您最近一年使用:0次
2024-01-13更新
|
336次组卷
|
2卷引用:江西省宜春市宜丰中学2023-2024学年高三上学期1月月考化学试题
名校
解题方法
2 . 室温下,下列实验操作、现象和结论均正确的是
| 选项 | 实验操作 | 现象 | 结论 |
| A | 将1mL0.1mol/L 溶液滴入5mL 0.1mol/L NaOH溶液有沉淀产生,再滴加0.1mol/L 溶液滴入5mL 0.1mol/L NaOH溶液有沉淀产生,再滴加0.1mol/L 溶液 溶液 | 先有白色沉淀生成,后变为浅蓝色沉淀 | 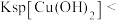 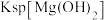 |
| B | 向浓度均为0.1mol/L的 和 和 混合溶液中滴加0.1mol/L 混合溶液中滴加0.1mol/L 溶液 溶液 | 先出现黄色沉淀 |  还原性强于 还原性强于 |
| C | 室温时,在pH试纸上滴2~3滴 溶液 溶液 | 测得, |  溶液中 溶液中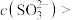  |
| D | 用pH计测量相同浓度NaClO溶液和 溶液的pH值 溶液的pH值 | NaClO溶液的pH值大于 溶液 溶液 |  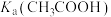 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-12-29更新
|
429次组卷
|
2卷引用:江西省上饶市第一中学2023-2024学年高二下学期开学考试化学试题
解题方法
3 . I.如图为工业合成氨的流程图:_______ (填序号)。
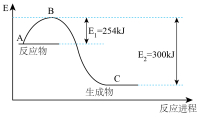
(2)如图是未用催化剂N2(g)和H2(g)反应生成1molNH3(g)过程中能量的变化示意图,请在图中绘制同条件下加入铁触媒后相应的能量变化曲线:_______ ,并写出该条件下2molNH3(g)分解对应的热化学方程式:_______ 。
(3)则:α1_______ α2、α1_______ α3(填“>”、“=”或“<”)
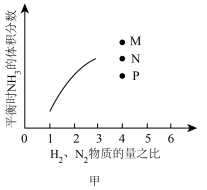
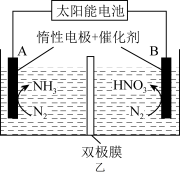
(4)如图甲表示500℃、60.0MPa条件下,平衡时NH3的体积分数与原料气投料比的关系。若投料比为4时,氨气的体积分数为40%,NH3的体积分数可能为图中的_______ 点,平衡时N2的体积分数为_______ 。_______ 。
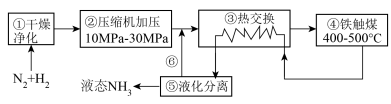
(2)如图是未用催化剂N2(g)和H2(g)反应生成1molNH3(g)过程中能量的变化示意图,请在图中绘制同条件下加入铁触媒后相应的能量变化曲线:
| 序号 | 起始投入量 | 平衡转化率 | ||
| N2 | H2 | NH3 | ||
| ①恒温恒容 | 1mol | 3mol | 0 | α1 |
| ②绝热恒容 | 1mol | 3mol | 0 | α2 |
| ③恒温恒压 | 2mol | 6mol | 0 | α3 |
(4)如图甲表示500℃、60.0MPa条件下,平衡时NH3的体积分数与原料气投料比的关系。若投料比为4时,氨气的体积分数为40%,NH3的体积分数可能为图中的
您最近一年使用:0次
解题方法
4 . 研究CO2资源的综合利用,对实现“碳达峰”和“碳中和”有重要意义。
(1)已知:
Ⅰ.
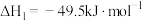
Ⅱ.
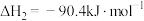
Ⅲ.

①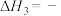
_______ 
②一定条件下,向体积为2L的恒容密闭容器中通入1molCO2和3molH2,发生上述反应,达到平衡时,容器中CH3OH(g)的物质的量为0.5mol;CO的物质的量为0.3mol;此时H2O(g)的浓度为_______ mol·L-1。
(2)CO2在Cu—ZnO催化下,同时发生反应Ⅰ、Ⅲ;此方法是解决温室效应和能源短缺问题的重要手段。保持温度T时,在容积不变的密闭容器中,充入一定量的CO2及H2;起始及达到平衡时(t min时恰好达到平衡);容器内各气体物质的量及总压强如下表:
若反应Ⅰ、Ⅲ均达到平衡时,p0=1.4p;则表中n=_______ ;0~t min内,CO2的分压变化率为_______ kPa·min⁻¹;反应Ⅰ的平衡常数Kp=_______ (kPa)-2(用含p的式子表示)。
(3)CO2催化加氢制甲烷涉及的反应主要有:
主反应:
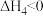
副反应:

若将CO2和H2按体积比为1∶4混合(n总=5mol);匀速通入装有催化剂的反应容器中,发生反应(包括主反应和副反应)。反应相同时间,CO2转化率、CH4和CO选择性随温度变化的曲线分别如图所示。
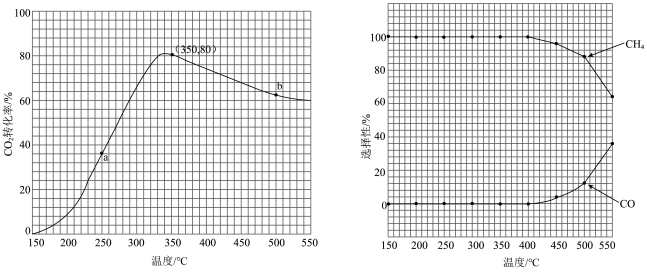
①a点的正反应速率和逆反应速率的大小关系为v正(a)_______ (填“>”、“=”或“<”)v逆(a)。
②催化剂在较低温度时主要选择_______ (填“主反应”或“副反应”)。
③350~400℃;CO2转化率呈现减小的变化趋势,其原因是_______ 。
(1)已知:
Ⅰ.

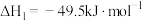
Ⅱ.

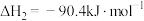
Ⅲ.


①
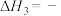

②一定条件下,向体积为2L的恒容密闭容器中通入1molCO2和3molH2,发生上述反应,达到平衡时,容器中CH3OH(g)的物质的量为0.5mol;CO的物质的量为0.3mol;此时H2O(g)的浓度为
(2)CO2在Cu—ZnO催化下,同时发生反应Ⅰ、Ⅲ;此方法是解决温室效应和能源短缺问题的重要手段。保持温度T时,在容积不变的密闭容器中,充入一定量的CO2及H2;起始及达到平衡时(t min时恰好达到平衡);容器内各气体物质的量及总压强如下表:
| 物质的量/mol | 总压强/kPa | |||||
| CO2 | H2 | CH3OH(g) | CO | H2O(g) | ||
| 起始 | 0.5 | 0.9 | 0 | 0 | 0 | p0 |
| 平衡 | n | 0.3 | p | |||
(3)CO2催化加氢制甲烷涉及的反应主要有:
主反应:

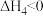
副反应:


若将CO2和H2按体积比为1∶4混合(n总=5mol);匀速通入装有催化剂的反应容器中,发生反应(包括主反应和副反应)。反应相同时间,CO2转化率、CH4和CO选择性随温度变化的曲线分别如图所示。

①a点的正反应速率和逆反应速率的大小关系为v正(a)
②催化剂在较低温度时主要选择
③350~400℃;CO2转化率呈现减小的变化趋势,其原因是
您最近一年使用:0次
2023-09-09更新
|
264次组卷
|
4卷引用:江西省部分高中学校2024届高三上学期9月第一次联考化学试题
名校
5 . 据文献报道,钒催化某反应的反应机理如图所示。下列叙述正确的是
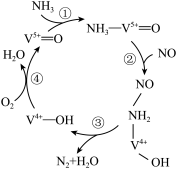

| A.H2O参与了该催化循环 |
| B.该反应利用了NH3的还原性除去NO,减少了空气污染 |
| C.过量的O2有利于V5+=O催化该反应 |
| D.该催化循环过程中V的价态变化为+5→+4 |
您最近一年使用:0次
解题方法
6 . 尿素 是一种重要的化工产品和常用氮肥。回答下列问题:
是一种重要的化工产品和常用氮肥。回答下列问题:
(1)尿素中C、N、O三种元素的电负性由小到大的顺序是_______ (用元素符号表示)。
(2)工业上,用 和
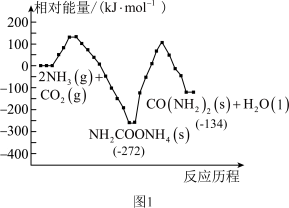
和 制备尿素,总反应分两个基元反应(反应历程与相对能量关系如图1):
制备尿素,总反应分两个基元反应(反应历程与相对能量关系如图1):
①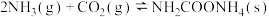
②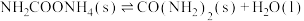
写出总反应的热化学方程式:_______ 。该历程中决速步骤的反应是_______ (填“①”或“②”)。
(3)有人设想直接利用反应 进行人工固氮制备尿素,从热力学角度判断该反应
进行人工固氮制备尿素,从热力学角度判断该反应_______ (填“可行”或“不可行”'),理由为_______ 。
(4)碳酸丙烯酯(PC)是锂离子电池的常用溶剂。工业上常用尿素合成碳酸丙烯酯。已知:碳酸丙烯酯的结构简式为 ,沸点为238.14℃;1,2-丙二醇(PG)的沸点为162℃。1,2-丙二醇和尿素(160℃以上会分解)合成PC的反应如下:
,沸点为238.14℃;1,2-丙二醇(PG)的沸点为162℃。1,2-丙二醇和尿素(160℃以上会分解)合成PC的反应如下:

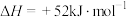
在烧瓶中加入物质的量之比为2:1的PG和尿素,加入催化剂充分反应,测定不同温度下PC的平衡收率变化如图2所示。PC的收率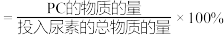 。
。

①160℃以上,PC的收率下降的主要原因可能是_______ 。
②150℃时,PG的平衡转化率为_______ 。以液相中各物质的量分数代替浓度表示平衡常数
_______ (保留2位小数)。
 是一种重要的化工产品和常用氮肥。回答下列问题:
是一种重要的化工产品和常用氮肥。回答下列问题:(1)尿素中C、N、O三种元素的电负性由小到大的顺序是
(2)工业上,用
 和
和 制备尿素,总反应分两个基元反应(反应历程与相对能量关系如图1):
制备尿素,总反应分两个基元反应(反应历程与相对能量关系如图1):
①
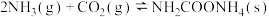
②
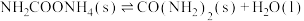
写出总反应的热化学方程式:
(3)有人设想直接利用反应
 进行人工固氮制备尿素,从热力学角度判断该反应
进行人工固氮制备尿素,从热力学角度判断该反应(4)碳酸丙烯酯(PC)是锂离子电池的常用溶剂。工业上常用尿素合成碳酸丙烯酯。已知:碳酸丙烯酯的结构简式为
 ,沸点为238.14℃;1,2-丙二醇(PG)的沸点为162℃。1,2-丙二醇和尿素(160℃以上会分解)合成PC的反应如下:
,沸点为238.14℃;1,2-丙二醇(PG)的沸点为162℃。1,2-丙二醇和尿素(160℃以上会分解)合成PC的反应如下:
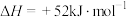
在烧瓶中加入物质的量之比为2:1的PG和尿素,加入催化剂充分反应,测定不同温度下PC的平衡收率变化如图2所示。PC的收率
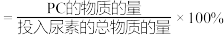 。
。
①160℃以上,PC的收率下降的主要原因可能是
②150℃时,PG的平衡转化率为

您最近一年使用:0次
名校
解题方法
7 . 含氮化合物在现代工业、环境治理中有重要地位。请回答下列有关问题:
(1)用 催化还原氮氧化物可以消除氮氧化物的污染。
催化还原氮氧化物可以消除氮氧化物的污染。
已知:①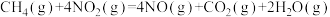
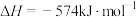
②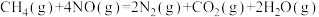
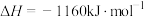
③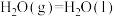
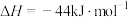
写出 与
与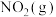 反应生成
反应生成 、
、 和
和 的热化学方程式
的热化学方程式_______ 。
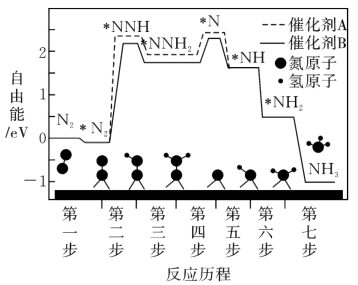
(2)不同催化剂下合成氨反应的历程如下图,吸附在催化剂表面的物种用“*”表示。由图可知,使用催化剂A时,决定总反应速率的步骤的产物是_______ 。
(3)氨气的催化氧化是工业制取硝酸的重要步骤,假设只会发生以下两个竞争反应I、II。
反应I:

反应II:
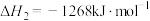
为分析某催化剂对该反应的选择性,将1mol 和2mol
和2mol  充入2L密闭容器中,在不同温度,相同时间下,测得有关物质的量关系如下图所示。
充入2L密闭容器中,在不同温度,相同时间下,测得有关物质的量关系如下图所示。
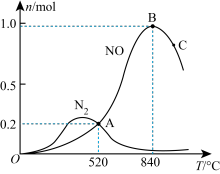
①该催化剂在低温时对反应_______ (填“I”或“II”)的选择性更好。
②520℃时,反应II: 的平衡常数K=
的平衡常数K=_______ (只需列出有具体数字的计算式,不要求计算出结果)。
③高于840℃时,NO的产率降低的可能原因是_______ 。
A. 溶于水 B.反应活化能增大 C.反应I的平衡常数变小 D.催化剂活性降低
溶于水 B.反应活化能增大 C.反应I的平衡常数变小 D.催化剂活性降低
(4) 也是造成水体富营养化的重要原因之一,用NaClO溶液氧化可除去氨。为了提高氨的去除率,在实际工艺过程中温度控制在15℃~30℃时,其可能的原因是
也是造成水体富营养化的重要原因之一,用NaClO溶液氧化可除去氨。为了提高氨的去除率,在实际工艺过程中温度控制在15℃~30℃时,其可能的原因是_______ 。
(1)用
 催化还原氮氧化物可以消除氮氧化物的污染。
催化还原氮氧化物可以消除氮氧化物的污染。已知:①
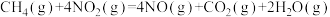
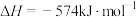
②
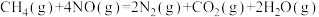
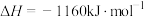
③
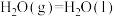
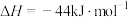
写出
 与
与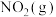 反应生成
反应生成 、
、 和
和 的热化学方程式
的热化学方程式(2)不同催化剂下合成氨反应的历程如下图,吸附在催化剂表面的物种用“*”表示。由图可知,使用催化剂A时,决定总反应速率的步骤的产物是

(3)氨气的催化氧化是工业制取硝酸的重要步骤,假设只会发生以下两个竞争反应I、II。
反应I:


反应II:

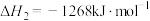
为分析某催化剂对该反应的选择性,将1mol
 和2mol
和2mol  充入2L密闭容器中,在不同温度,相同时间下,测得有关物质的量关系如下图所示。
充入2L密闭容器中,在不同温度,相同时间下,测得有关物质的量关系如下图所示。
①该催化剂在低温时对反应
②520℃时,反应II:
 的平衡常数K=
的平衡常数K=③高于840℃时,NO的产率降低的可能原因是
A.
 溶于水 B.反应活化能增大 C.反应I的平衡常数变小 D.催化剂活性降低
溶于水 B.反应活化能增大 C.反应I的平衡常数变小 D.催化剂活性降低(4)
 也是造成水体富营养化的重要原因之一,用NaClO溶液氧化可除去氨。为了提高氨的去除率,在实际工艺过程中温度控制在15℃~30℃时,其可能的原因是
也是造成水体富营养化的重要原因之一,用NaClO溶液氧化可除去氨。为了提高氨的去除率,在实际工艺过程中温度控制在15℃~30℃时,其可能的原因是
您最近一年使用:0次
名校
8 . 已知某反应的一种反应机理如图所示,下列说法错误 的是


A. 参与了该催化循环 参与了该催化循环 |
B.该反应可消耗温室气体 |
C.该催化循环中 的成键数目发生变化 的成键数目发生变化 |
D. 降低了该反应的活化能,提高了化学反应速率 降低了该反应的活化能,提高了化学反应速率 |
您最近一年使用:0次
2022-12-02更新
|
340次组卷
|
5卷引用:江西省宜春市上高二中2023-2024学年高二上学期第二次月考化学试题
名校
解题方法
9 . Ⅰ.醋酸是一种重要的基本有机化工原料,主要制取醋酸乙烯单体、VCM、醋酸纤维、聚乙烯醇等。
(1)据文献报道:铑阳离子配合物催化甲醇羰基化反应过程如下图所示。

①甲醇羰基化总反应方程式为_______ 。
②化合物Ⅰ转化为Ⅱ,存在二步机理反应,在不同催化剂a和b催化下各驻点相对能量(kJ·mol-1)如下:
可知化合物I转化为II的∆H_______ 0(填“大于”“等于”或“小于”),该历程中最大能垒(活化能)E正=_______ kJ·mol-1,该条件下更好的催化剂是_______ (填“催化剂a”或“催化剂b”)
Ⅱ.氢的热值高、无污染使其成为理想的能源。工业制取氢气的主要方法有煤转化、天然气转化等方法。煤制取氢的主要原理可简化为如下反应:
反应①:C(s) + H2O(g) CO(g) + H2(g) ΔH1= -131.5 kJ·mol-1
CO(g) + H2(g) ΔH1= -131.5 kJ·mol-1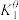
反应②:CO(g) + H2O(g) CO2(g) + H2(g) ΔH2= -41.2 kJ·mol-1
CO2(g) + H2(g) ΔH2= -41.2 kJ·mol-1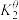
反应③:CaO(s) + CO2(g) CaCO3(s) ΔH3=-179.2 kJ·mol-1
CaCO3(s) ΔH3=-179.2 kJ·mol-1
对于反应:aA(g) +bB(g) cC(g) + dD(g) 其标准平衡常数:
cC(g) + dD(g) 其标准平衡常数: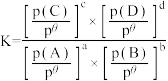 。在温度恒定为1120K,压强恒定为16p⊝的反应炉内加入2molC(s) 、2molH2O(g) 、2molCaO(s),发生上述3个反应,平衡时 CO的分压p(CO)=5
。在温度恒定为1120K,压强恒定为16p⊝的反应炉内加入2molC(s) 、2molH2O(g) 、2molCaO(s),发生上述3个反应,平衡时 CO的分压p(CO)=5 。已知:p⊝= 105 Pa,该温度下
。已知:p⊝= 105 Pa,该温度下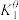 =20,
=20, 1。
1。
(2)写出反应③的标准平衡常数表达式: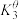 =
=_______ 。
(3)反应④:C(s) +CO2(g) 2CO(g) ΔH4=
2CO(g) ΔH4=_______ 。
(4)求该温度下反应②的标准平衡常数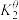 =
=_______ 。
(5)平衡时H2的分压p(H2)=_______ Pa,平衡时剩余C(s)的质量=_______ g。
(6)简述CaO(s)的作用_______ 。
(7)平衡后再加入2molCaO(s)对最终氢气的产率有何影响_______。
(1)据文献报道:铑阳离子配合物催化甲醇羰基化反应过程如下图所示。

①甲醇羰基化总反应方程式为
②化合物Ⅰ转化为Ⅱ,存在二步机理反应,在不同催化剂a和b催化下各驻点相对能量(kJ·mol-1)如下:
| 反应物 | 过渡态1 | 1步生成物 | 过渡态2 | 2步生成物 | |
| 催化剂a | 0.00 | 27.53 | 27.35 | 195.09 | 92.63 |
| 催化剂b | 0.00 | 63.93 | 61.86 | 191.88 | 101.04 |
Ⅱ.氢的热值高、无污染使其成为理想的能源。工业制取氢气的主要方法有煤转化、天然气转化等方法。煤制取氢的主要原理可简化为如下反应:
反应①:C(s) + H2O(g)
 CO(g) + H2(g) ΔH1= -131.5 kJ·mol-1
CO(g) + H2(g) ΔH1= -131.5 kJ·mol-1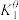
反应②:CO(g) + H2O(g)
 CO2(g) + H2(g) ΔH2= -41.2 kJ·mol-1
CO2(g) + H2(g) ΔH2= -41.2 kJ·mol-1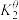
反应③:CaO(s) + CO2(g)
 CaCO3(s) ΔH3=-179.2 kJ·mol-1
CaCO3(s) ΔH3=-179.2 kJ·mol-1对于反应:aA(g) +bB(g)
 cC(g) + dD(g) 其标准平衡常数:
cC(g) + dD(g) 其标准平衡常数: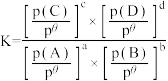 。在温度恒定为1120K,压强恒定为16p⊝的反应炉内加入2molC(s) 、2molH2O(g) 、2molCaO(s),发生上述3个反应,平衡时 CO的分压p(CO)=5
。在温度恒定为1120K,压强恒定为16p⊝的反应炉内加入2molC(s) 、2molH2O(g) 、2molCaO(s),发生上述3个反应,平衡时 CO的分压p(CO)=5 。已知:p⊝= 105 Pa,该温度下
。已知:p⊝= 105 Pa,该温度下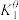 =20,
=20, 1。
1。(2)写出反应③的标准平衡常数表达式:
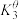 =
=(3)反应④:C(s) +CO2(g)
 2CO(g) ΔH4=
2CO(g) ΔH4=(4)求该温度下反应②的标准平衡常数
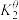 =
=(5)平衡时H2的分压p(H2)=
(6)简述CaO(s)的作用
(7)平衡后再加入2molCaO(s)对最终氢气的产率有何影响_______。
| A.增大 | B.减小 | C.无影响 | D.无法判断 |
您最近一年使用:0次
10 . 研发二氧化碳利用技术,降低空气中远氧化碳含量是现在的研究热点。
Ⅰ.二氧化碳催化加氢制甲醇,有利于减少温室气体二氧化碳。已知:
①

②

③

回答下列问题:
(1)
_________ 。
(2)在200℃恒容密闭容器中,加入2mol 和6mol
和6mol ,发生上述反应,初始压强10kPa.反应达平衡时,
,发生上述反应,初始压强10kPa.反应达平衡时, 的转化率为75%,容器压强为7.5kPa,则
的转化率为75%,容器压强为7.5kPa,则 的物质的量为
的物质的量为_________ mol,CO的物质的量为_________ mol。反应①的平衡常数
_________ 。
(3)一定条件下,向1L恒容密闭容器充入0.23mol 和0.19mol
和0.19mol ,选择合适催化剂使之只发生反应③,相同时间内
,选择合适催化剂使之只发生反应③,相同时间内 的转化率随温度变化如图所示:
的转化率随温度变化如图所示:
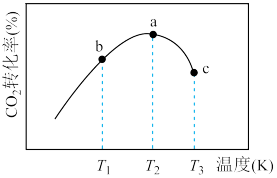
①b点
_________  ,c点
,c点
_________  (填“>”“<”或“=”,下同)。
(填“>”“<”或“=”,下同)。
②不同温度下的平衡常数,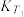
_________ 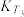 。
。
③a点为图像中最高点,a点的转化率比c点高的原因是_________ 。
④平衡时测得生成甲醇0.03mol,保持温度不变再通入0.1mol 和0.1mol水蒸气,此时平衡将
和0.1mol水蒸气,此时平衡将_________ (填“正向移动”“逆向移动”或“不移动”)。
Ⅰ.二氧化碳催化加氢制甲醇,有利于减少温室气体二氧化碳。已知:
①


②


③


回答下列问题:
(1)

(2)在200℃恒容密闭容器中,加入2mol
 和6mol
和6mol ,发生上述反应,初始压强10kPa.反应达平衡时,
,发生上述反应,初始压强10kPa.反应达平衡时, 的转化率为75%,容器压强为7.5kPa,则
的转化率为75%,容器压强为7.5kPa,则 的物质的量为
的物质的量为
(3)一定条件下,向1L恒容密闭容器充入0.23mol
 和0.19mol
和0.19mol ,选择合适催化剂使之只发生反应③,相同时间内
,选择合适催化剂使之只发生反应③,相同时间内 的转化率随温度变化如图所示:
的转化率随温度变化如图所示:
①b点

 ,c点
,c点
 (填“>”“<”或“=”,下同)。
(填“>”“<”或“=”,下同)。②不同温度下的平衡常数,
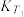
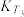 。
。③a点为图像中最高点,a点的转化率比c点高的原因是
④平衡时测得生成甲醇0.03mol,保持温度不变再通入0.1mol
 和0.1mol水蒸气,此时平衡将
和0.1mol水蒸气,此时平衡将
您最近一年使用:0次



