1 . 依据事实,写出下列反应的热化学方程式。
(1)在25℃、101kPa下,1g液态甲醇(CH3OH)燃烧生成CO2和液态水时放热22.68kJ。则表示甲醇燃烧热的热化学方程式为:___________ ;
(2)若适量的N2和O2完全反应,每生成15g气态NO需要吸收16.95kJ热量___________ 。
(1)在25℃、101kPa下,1g液态甲醇(CH3OH)燃烧生成CO2和液态水时放热22.68kJ。则表示甲醇燃烧热的热化学方程式为:
(2)若适量的N2和O2完全反应,每生成15g气态NO需要吸收16.95kJ热量
您最近一年使用:0次
2 . 25℃、101kPa下充分燃烧一定量丁烷(C4H10)气体放出的热量为QkJ,用5mol/L的KOH溶液400mL完全吸收生成的CO2,并恰好全部转化生成正盐(K2CO3),则丁烷的燃烧热的数值是
| A.16Q | B.8Q | C.4Q | D.2Q |
您最近一年使用:0次
解题方法
3 . 如图1是反应A(g)+3B(g) 2C(g) ΔH=-akJ•mol-1在反应过程中的能量变化关系图,回答下列问题。
2C(g) ΔH=-akJ•mol-1在反应过程中的能量变化关系图,回答下列问题。

(1)由示意图知,反应物的总能量____ (填“>”、“<”或“=”)生成物的总能量,此反应中反应物的总键能____ (填“>”、“<”或“=”)生成物的总键能。
(2)a=____ (用Ec和Ec′表示)。
(3)加入催化剂对该反应的ΔH____ 影响(填“有”或“无”)。
(4)已知:
2CH3OH(l)+2O2(g)=2CO(g)+4H2O(g) ΔH1=-akJ•mol-1;
2CO(g)+O2(g)=2CO2(g) ΔH2=-bkJ•mol-1;
H2O(g)=H2O(l) ΔH3=-ckJ•mol-1。
则表示CH3OH(l)燃烧热的热化学方程式为:_____ 。
(5)工业上用H2(g)和Cl2(g)反应制HCl(g),各键能为H-H:436kJ/mol,Cl-Cl:243kJ/mol,H-Cl:431kJ/mol。该反应的热化学方程式是_____ 。
(6)298K时,0.5molC2H4(g)完全燃烧生成二氧化碳和液态水,放出705.5kJ的热量。请写出表示C2H4(g)燃烧热的热化学方程式:_____ 。
 2C(g) ΔH=-akJ•mol-1在反应过程中的能量变化关系图,回答下列问题。
2C(g) ΔH=-akJ•mol-1在反应过程中的能量变化关系图,回答下列问题。
(1)由示意图知,反应物的总能量
(2)a=
(3)加入催化剂对该反应的ΔH
(4)已知:
2CH3OH(l)+2O2(g)=2CO(g)+4H2O(g) ΔH1=-akJ•mol-1;
2CO(g)+O2(g)=2CO2(g) ΔH2=-bkJ•mol-1;
H2O(g)=H2O(l) ΔH3=-ckJ•mol-1。
则表示CH3OH(l)燃烧热的热化学方程式为:
(5)工业上用H2(g)和Cl2(g)反应制HCl(g),各键能为H-H:436kJ/mol,Cl-Cl:243kJ/mol,H-Cl:431kJ/mol。该反应的热化学方程式是
(6)298K时,0.5molC2H4(g)完全燃烧生成二氧化碳和液态水,放出705.5kJ的热量。请写出表示C2H4(g)燃烧热的热化学方程式:
您最近一年使用:0次
2022-09-17更新
|
274次组卷
|
2卷引用:新疆呼图壁县第一中学2021-2022学年高二上学期期中考试化学试题
名校
解题方法
4 . 下列叙述正确的是
| A.HCl(aq)和NaOH(aq)反应的中和热为ΔH=–57.3kJ/mol,则H2SO4(aq)和Ba(OH)2(aq)反应的中和热为ΔH=2×(–57.3)kJ/mol |
| B.用等体积的0.50mol·L-1盐酸、0.55mol·L-1NaOH溶液进行中和热测定的实验,会使测得值偏小 |
| C.CO(g)燃烧热ΔH=–283.0kJ/mol,则2CO2(g)=2CO(g)+O2(g)反应的ΔH=+2×283.0kJ/mol |
| D.1mol甲烷燃烧生成气态水和二氧化碳所放出的热量是甲烷的燃烧热 |
您最近一年使用:0次
2022-09-05更新
|
305次组卷
|
2卷引用:新疆昌吉州行知学校2022-2023学年高二上学期第一次线上月考化学试题
名校
解题方法
5 . 下列热化学方程式中,正确的是
| A.甲烷燃烧热为890.3 kJ•mol-1,热化学方程式为:CH4(g)+2O2(g)=CO2(g)+2H2O(g) △H=+890.3 kJ•molˉ1 |
| B.稀盐酸和稀氢氧化钠溶液混合,其热化学方程式为:H++OH-=H2O △H=-57.3 kJ•molˉ1 |
| C.C(石墨,s)=C(金刚石,s) ΔH>0,说明石墨比金刚石稳定 |
D.500℃、30 MPa下,将0.5 mol N2和1.5 mol H2置于密闭的容器中充分反应生成NH3(g),放热19.3 kJ,其热化学方程式为:N2(g)+3H2(g) 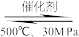 2NH3(g) △H=-38.6 kJ·mol-1 2NH3(g) △H=-38.6 kJ·mol-1 |
您最近一年使用:0次
2022-08-20更新
|
446次组卷
|
3卷引用:新疆生产建设兵团第三师图木舒克市第一中学2022-2023学年高二上学期11月阶段性检测化学试题
6 . 燃烧热与反应热的关系是
| A.燃烧热是反应热的一种类型 |
| B.当一个反应是燃烧反应时,该燃烧反应的反应热就是燃烧热 |
| C.燃烧热不属于反应热 |
| D.反应热有正负之分,燃烧反应的焓变全部是正值 |
您最近一年使用:0次
名校
7 . 下列热化学方程正确的是( 的绝对值均正确)
的绝对值均正确)
 的绝对值均正确)
的绝对值均正确)A.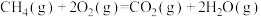 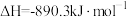 (燃烧热) (燃烧热) |
B. 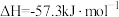 (中和热) (中和热) |
C. 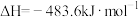 (反应热) (反应热) |
D.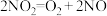 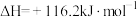 (反应热) (反应热) |
您最近一年使用:0次
2022-07-01更新
|
327次组卷
|
6卷引用:新疆石河子第二中学2021-2022学年高二上学期第二次月考化学试题
名校
解题方法
8 . 下列判断及叙述,正确的是
| A.CH4(g)+2O2(g)=CO2(g)+2H2O(g) △H= - 801.3 kJ/mol,则CH4的燃烧热为801.3 kJ/mol |
| B.C(s,石墨)+O2(g)=CO2(g) △H=-393.5kJ/mol,C(s,金刚石)+O2(g)=CO2(g) △H=-395kJ/mol,则石墨转化为金刚石的过程中会放出热量 |
| C.稀盐酸与稀氢氧化钠溶液反应的中和热为57.3kJ/mol,则稀硫酸与稀氢氧化钡溶液反应生成1 mol H2O(l), 放出热量57.3 kJ |
D.Sn(s,灰) 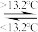 Sn(s,白)△H=+2.1 kJ/mol,则锡制品在寒冷的冬天易转化为灰锡(粉末状)而损坏 Sn(s,白)△H=+2.1 kJ/mol,则锡制品在寒冷的冬天易转化为灰锡(粉末状)而损坏 |
您最近一年使用:0次
2022-06-12更新
|
81次组卷
|
2卷引用:新疆和田地区民丰县2022-2023学年高二上学期11月期中考试化学试题
名校
解题方法
9 . 下列热化学方程式中,正确的是
| A.甲烷的燃烧热为890.3kJ·mol-1,则甲烷燃烧的热化学方程式可表示为CH4(g)+2O2(g)=CO2(g)+2H2O(g) △H=-890.3kJ·mol-1 |
B.500℃、30MPa下,将0.5molN2(g)和1.5molH2(g)置于密闭容器中充分反应生成NH3(g)放热19.3kJ,其热化学方程式为:N2(g)+3H2(g) 2NH3(g) △H=-38.6kJ·mol-1 2NH3(g) △H=-38.6kJ·mol-1 |
| C.HCl和NaOH反应的中和热△H=-57.3kJ·mol-1,则H2SO4和Ca(OH)2反应的中和热△H=2×(-57.3)kJ·mol-1 |
| D.在101kPa时,2gH2完全燃烧生成液态水,放出285.8kJ热量,氢气燃烧的热化学方程式表示为2H2(g)+O2(g)=2H2O(l) △H=-571.6kJ·mol-1 |
您最近一年使用:0次
2022-05-14更新
|
370次组卷
|
17卷引用:新疆巴音郭楞蒙古自治州第一中学2022-2023学年高二上学期期末考试化学试题
新疆巴音郭楞蒙古自治州第一中学2022-2023学年高二上学期期末考试化学试题辽宁省营口市第二高级中学2020届高三上学期第一次月考化学试题安徽省安庆市怀宁县第二中学2019-2020学年高二下学期期中线上检测化学试题(已下线)专题07 化学反应中的能量变化-2020年高考真题和模拟题化学分项汇编黑龙江省大庆市第四中学2019-2020学年高二上学期第一次检测化学试题(已下线)1.1.2 反应热的测量和计算(重点练)——2020-2021学年高二化学上学期十分钟同步课堂专练(苏教版选修4)黑龙江省哈尔滨市第一中学校2019-2020学年高一下学期期末考试化学试题西藏自治区拉萨市拉萨中学2020-2021学年高二第一次月考理综化学试题甘肃省武威第八中学2020-2021学年高二上学期月考化学试题黑龙江省伊春市伊美区第二中学2020-2021学年高二上学期开学考试化学试题(已下线)专题05 化学反应与能量——备战2021年高考化学纠错笔记福建省南安市柳城中学2020-2021学年高一下学期期中考试化学试题四川省成都市蒲江县蒲江中学2019-2020学年高二上学期10月月考化学试题江苏省海安市南莫中学2021-2022学年高二上学期第一次月考备考金卷B卷化学试题湖南省益阳市箴言中学2021-2022学年高二上学期10月月考化学试题(已下线)第04讲 燃料燃烧释放的能量与氢燃料的发展前景-【寒假自学课】2022年高一化学寒假精品课(苏教版必修第二册)辽宁省沈阳市第一二〇中学2020-2021学年高一下学期期中化学试题
名校
解题方法
10 . 下列说法中正确的选项是
①已知25℃时H2(g)的燃烧热是285.8 kJ·mol-1,则323.15K、101kPa时,2H2O(l) =2H2(g)+O2(g) ΔH=+571.6 kJ·mol-1
②中和热测定实验中为减少热量散失,NaOH溶液应分多次到入量热计中。
③同温同压下,反应H2(g)+Cl2(g)=2HCl(g)在光照和点燃条件下反应的ΔH不同
④由N2O4(g) 2NO2(g) ΔH=-56.9 kJ·mol-1,可知将1 mol N2O4(g)置于密闭容器中充分反应后放出热量为56.9 kJ
2NO2(g) ΔH=-56.9 kJ·mol-1,可知将1 mol N2O4(g)置于密闭容器中充分反应后放出热量为56.9 kJ
⑤在稀溶液中:H+(aq)+OH-(aq)=H2O(l) ΔH=-57.3 kJ·mol-1,若将含0.5 mol H2SO4的浓硫酸与含1 mol NaOH的溶液混合,放出的热量为57.3 kJ
⑥煤、石油、天然气均为化石能源,是非再生能源
⑦已知相同条件下2SO2(g)+O2(g) 2SO3(g) ΔH1,反应2SO2(g)+O2(g)
2SO3(g) ΔH1,反应2SO2(g)+O2(g)  2SO3(s) ΔH2,则ΔH1>ΔH2
2SO3(s) ΔH2,则ΔH1>ΔH2
⑧C(石墨,s)=C(金刚石,s) ΔH >0,说明石墨比金刚石稳定
①已知25℃时H2(g)的燃烧热是285.8 kJ·mol-1,则323.15K、101kPa时,2H2O(l) =2H2(g)+O2(g) ΔH=+571.6 kJ·mol-1
②中和热测定实验中为减少热量散失,NaOH溶液应分多次到入量热计中。
③同温同压下,反应H2(g)+Cl2(g)=2HCl(g)在光照和点燃条件下反应的ΔH不同
④由N2O4(g)
 2NO2(g) ΔH=-56.9 kJ·mol-1,可知将1 mol N2O4(g)置于密闭容器中充分反应后放出热量为56.9 kJ
2NO2(g) ΔH=-56.9 kJ·mol-1,可知将1 mol N2O4(g)置于密闭容器中充分反应后放出热量为56.9 kJ⑤在稀溶液中:H+(aq)+OH-(aq)=H2O(l) ΔH=-57.3 kJ·mol-1,若将含0.5 mol H2SO4的浓硫酸与含1 mol NaOH的溶液混合,放出的热量为57.3 kJ
⑥煤、石油、天然气均为化石能源,是非再生能源
⑦已知相同条件下2SO2(g)+O2(g)
 2SO3(g) ΔH1,反应2SO2(g)+O2(g)
2SO3(g) ΔH1,反应2SO2(g)+O2(g)  2SO3(s) ΔH2,则ΔH1>ΔH2
2SO3(s) ΔH2,则ΔH1>ΔH2⑧C(石墨,s)=C(金刚石,s) ΔH >0,说明石墨比金刚石稳定
| A.0项 | B.1项 | C.3项 | D.4项 |
您最近一年使用:0次



