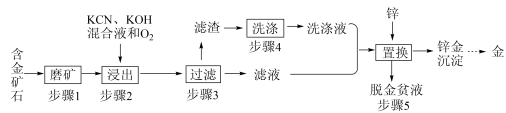
1 . 金是一种用途广泛的贵重金属。某化工厂利用氰化法从一种含金矿石中提取金的工艺流程如下:
资料:
① Zn + O2 + H2O = Zn(OH)2
O2 + H2O = Zn(OH)2
② Zn2+(aq) Zn(CN)2(s)
Zn(CN)2(s)  Zn(CN)42-(aq)
Zn(CN)42-(aq)
(1)步骤2中发生的反应有:
① 2Au(s) + 4CN-(aq) + 2H2O(l) + O2(g) = 2Au(CN)2-(aq) + 2OH-(aq) + H2O2(aq) ∆H = -197.61 kJ·mol-1
② 2Au(s) + 4CN-(aq)+ H2O2(aq) = 2Au(CN)2-(aq) + 2OH-(aq) ∆H = -386.93 kJ·mol-1
则2Au(s)+ 4CN-(aq)+ H2O(l) + 1/2O2(g) = 2Au(CN)2-(aq) + 2OH-(aq)的∆H =_______ 。
(2)下图是步骤2中金的溶解速率与温度的关系。80℃以后溶解速率降低的原因是___________ 。

(3)步骤4的目的是_________________ 。
(4)步骤5置换的总反应是:
2Au(CN)2- + 3Zn + 4CN- + 2H2O = 2Au + 2Zn(CN)42- + ZnO22- + 2H2↑
则以下说法正确的是________ (填字母序号)。
A 步骤5进行时要先脱氧,否则会增加锌的用量
B 若溶液中c(CN-)过小,会生成Zn(CN)2,减缓置换速率
C 实际生产中加入适量Pb(NO3)2的目的是形成原电池加快置换速率
(5)脱金贫液(主要含有CN-)会破坏环境,影响人类健康,可通过化学方法转化为无毒废水净化排放。碱性条件下,用Cl2将贫液中的CN-氧化成无毒的CO2和N2,该反应的离子方程式为_______________ 。

资料:
① Zn +
 O2 + H2O = Zn(OH)2
O2 + H2O = Zn(OH)2② Zn2+(aq)
 Zn(CN)2(s)
Zn(CN)2(s)  Zn(CN)42-(aq)
Zn(CN)42-(aq)(1)步骤2中发生的反应有:
① 2Au(s) + 4CN-(aq) + 2H2O(l) + O2(g) = 2Au(CN)2-(aq) + 2OH-(aq) + H2O2(aq) ∆H = -197.61 kJ·mol-1
② 2Au(s) + 4CN-(aq)+ H2O2(aq) = 2Au(CN)2-(aq) + 2OH-(aq) ∆H = -386.93 kJ·mol-1
则2Au(s)+ 4CN-(aq)+ H2O(l) + 1/2O2(g) = 2Au(CN)2-(aq) + 2OH-(aq)的∆H =
(2)下图是步骤2中金的溶解速率与温度的关系。80℃以后溶解速率降低的原因是

(3)步骤4的目的是
(4)步骤5置换的总反应是:
2Au(CN)2- + 3Zn + 4CN- + 2H2O = 2Au + 2Zn(CN)42- + ZnO22- + 2H2↑
则以下说法正确的是
A 步骤5进行时要先脱氧,否则会增加锌的用量
B 若溶液中c(CN-)过小,会生成Zn(CN)2,减缓置换速率
C 实际生产中加入适量Pb(NO3)2的目的是形成原电池加快置换速率
(5)脱金贫液(主要含有CN-)会破坏环境,影响人类健康,可通过化学方法转化为无毒废水净化排放。碱性条件下,用Cl2将贫液中的CN-氧化成无毒的CO2和N2,该反应的离子方程式为
您最近一年使用:0次
名校
解题方法
2 . 煤的洁净技术(包括固硫技术和脱硫技术两类)可有效降低燃煤废气中SO2的含量,已成为我国解决环境问题的主导技术之一。
I.固硫技术:通过加入固硫剂,将硫元素以固体形式留在煤燃烧的残渣中。石灰石是常用的固硫剂,固硫过程中涉及的部分反应如下:
①CaCO3(s) CaO(s)+CO2(g) △H1=+178.30kJ/mol
CaO(s)+CO2(g) △H1=+178.30kJ/mol
②CaO(s)+SO2(g)+0.5O2(g) CaSO4(s) △H2=-501.92kJ/mol
CaSO4(s) △H2=-501.92kJ/mol
③CO(g)+0.5O2(g) CO2(g) △H3
CO2(g) △H3
④CaSO4(s)+CO(g) CaO(s)+SO2(g)+CO2(g) △H4=+218.92kJ/mol
CaO(s)+SO2(g)+CO2(g) △H4=+218.92kJ/mol
(1)温度升高,反应①的化学平衡常数____ (填“增大”“减小”或“不变”)。
(2)△H3=____ kJ/mol。
(3)在煤燃烧过程中常鼓入稍过量的空气以提高固硫率(燃烧残渣中硫元素的质量占燃煤中硫元素总质量的百分比),结合反应②、③、④分析其原因:____ 。
II.电化学脱硫技术是一种温和的净化技术,其基本原理为利用阳极反应产生的羟基自由基(·OH,氧元素为-1价)将燃煤中的含硫物质氧化除去。
(4)将煤打成煤浆加入电解槽的目的是____ 。
(5)补全用羟基自由基除去煤中二硫化亚铁(FeS2)的反应的离子方程式:____ 。
FeS2+·OH=Fe3++SO +H2O+_____。
+H2O+_____。
(6)对某含FeS2的煤样品进行电解脱硫,测得一定时间内随溶液起始pH的改变脱硫率(溶于水中的硫元素质量占煤样中硫元素总质量的百分比)的变化如图所示。

pH大于1.5后脱硫率下降的可能原因有:随着pH的升高,反应物的氧化性或还原性降低;____ 。
I.固硫技术:通过加入固硫剂,将硫元素以固体形式留在煤燃烧的残渣中。石灰石是常用的固硫剂,固硫过程中涉及的部分反应如下:
①CaCO3(s)
 CaO(s)+CO2(g) △H1=+178.30kJ/mol
CaO(s)+CO2(g) △H1=+178.30kJ/mol②CaO(s)+SO2(g)+0.5O2(g)
 CaSO4(s) △H2=-501.92kJ/mol
CaSO4(s) △H2=-501.92kJ/mol③CO(g)+0.5O2(g)
 CO2(g) △H3
CO2(g) △H3④CaSO4(s)+CO(g)
 CaO(s)+SO2(g)+CO2(g) △H4=+218.92kJ/mol
CaO(s)+SO2(g)+CO2(g) △H4=+218.92kJ/mol(1)温度升高,反应①的化学平衡常数
(2)△H3=
(3)在煤燃烧过程中常鼓入稍过量的空气以提高固硫率(燃烧残渣中硫元素的质量占燃煤中硫元素总质量的百分比),结合反应②、③、④分析其原因:
II.电化学脱硫技术是一种温和的净化技术,其基本原理为利用阳极反应产生的羟基自由基(·OH,氧元素为-1价)将燃煤中的含硫物质氧化除去。
(4)将煤打成煤浆加入电解槽的目的是
(5)补全用羟基自由基除去煤中二硫化亚铁(FeS2)的反应的离子方程式:
FeS2+·OH=Fe3++SO
 +H2O+_____。
+H2O+_____。(6)对某含FeS2的煤样品进行电解脱硫,测得一定时间内随溶液起始pH的改变脱硫率(溶于水中的硫元素质量占煤样中硫元素总质量的百分比)的变化如图所示。

pH大于1.5后脱硫率下降的可能原因有:随着pH的升高,反应物的氧化性或还原性降低;
您最近一年使用:0次
21-22高三上·辽宁沈阳·阶段练习
3 . 双氧水(过氧化氢的水溶液)在工业生产和日常生活中应用广泛。
(1)双氧水的强氧化性使其对大多数病菌和病毒具有消杀功能。用3%医用双氧水对不传染病房喷洒消毒时,地板上有气泡冒出,该气体是__ 。
(2)火箭推进器中盛有强还原剂液态肼(N2H4)和强氧化剂液态过氧化氢。知0.4mol液态肼与足量的液态过氧化氢反应,生成氮气和水蒸气,并放出256.652kJ的热量。该反应的热化学方程式为__ 。
(3)双氧水能将碱性废水中的CN-转化成碳酸盐和一种对环境无污染的气体,CN-的电子式为__ ,写出该反应的离子方程式__ 。
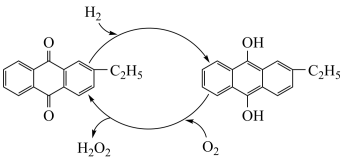
(4)如图是工业上制备过氧化氢最常见的方法,写出实际发生反应的总方程式___ 。
(5)如图是一种用电解原理来制备H2O2,并用产生的H2O2处理废氨水的装置。

①Ir—Ru惰性电极吸附O2生成H2O2,其电极反应式是__ 。
②处理废氨水中溶质(以NH3计)的质量是34g,理论上电路中转移电子数为__ mol。
(1)双氧水的强氧化性使其对大多数病菌和病毒具有消杀功能。用3%医用双氧水对不传染病房喷洒消毒时,地板上有气泡冒出,该气体是
(2)火箭推进器中盛有强还原剂液态肼(N2H4)和强氧化剂液态过氧化氢。知0.4mol液态肼与足量的液态过氧化氢反应,生成氮气和水蒸气,并放出256.652kJ的热量。该反应的热化学方程式为
(3)双氧水能将碱性废水中的CN-转化成碳酸盐和一种对环境无污染的气体,CN-的电子式为
(4)如图是工业上制备过氧化氢最常见的方法,写出实际发生反应的总方程式

(5)如图是一种用电解原理来制备H2O2,并用产生的H2O2处理废氨水的装置。

①Ir—Ru惰性电极吸附O2生成H2O2,其电极反应式是
②处理废氨水中溶质(以NH3计)的质量是34g,理论上电路中转移电子数为
您最近一年使用:0次
名校
4 . 将天然气(主要成分为CH4)中的CO2、H2S资源化转化在能源利用、环境保护等方面意义重大。
(1)CO2转化为CO、H2S转化为S的反应如下:
i.2CO2(g)=2CO(g)+O2(g) △H1=+566kJ/mol
ii.2H2S(g)+O2(g)=2H2O(l)+2S(s) △H2=-530kJ/mol
iii.CO2、H2S转化生成CO、S等物质的热化学方程式是___________
(2)CO2性质稳定,是一种“惰性”分子。对于反应iii,通过设计合适的催化剂可以降低___________ ,提高反应速率。
a.活化能 b.△H c.平衡常数
(3)我国科学家研制新型催化剂,设计协同转化装置实现反应iii,工作原理如下所示。
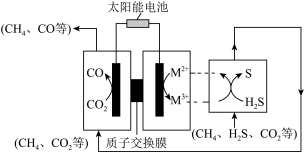
【方案1】若M3+/M2+=Fe3+/Fe2+。为了抑制离子水解,所含Fe3+、Fe2+的溶液调为较强的酸性。
①写出阳极区生成S的电极反应和离子方程式___________ 。
②结合电极反应和离子移动解释阴极区pH不变的原因(忽略溶液体积变化)___________
【方案2】若M3+/M2+=EDTA-Fe3+/EDTA-Fe2+ (配合物)。
已知:电解效率η的定义:
η(B)=n(生成B所用的电子)/ n(通过电极的电子)×100%
③测得η(EDTA-Fe3+)≈100%,η(CO) ≈80%。阴极放电的物质有___________
④为进一步确认CO2、H2S能协同转化,对CO的来源分析如下:
来源1.CO2通过电极反应产生CO
来源2.电解质(含碳元素)等物质发生降解,产生CO
设计实验探究,证实来源2不成立。实验方案是___________ 。
方案2明显优于方案1.该研究成果为天然气的净化、资源化转化提供了工业化解决思路。
(1)CO2转化为CO、H2S转化为S的反应如下:
i.2CO2(g)=2CO(g)+O2(g) △H1=+566kJ/mol
ii.2H2S(g)+O2(g)=2H2O(l)+2S(s) △H2=-530kJ/mol
iii.CO2、H2S转化生成CO、S等物质的热化学方程式是
(2)CO2性质稳定,是一种“惰性”分子。对于反应iii,通过设计合适的催化剂可以降低
a.活化能 b.△H c.平衡常数
(3)我国科学家研制新型催化剂,设计协同转化装置实现反应iii,工作原理如下所示。

【方案1】若M3+/M2+=Fe3+/Fe2+。为了抑制离子水解,所含Fe3+、Fe2+的溶液调为较强的酸性。
①写出阳极区生成S的电极反应和离子方程式
②结合电极反应和离子移动解释阴极区pH不变的原因(忽略溶液体积变化)
【方案2】若M3+/M2+=EDTA-Fe3+/EDTA-Fe2+ (配合物)。
已知:电解效率η的定义:
η(B)=n(生成B所用的电子)/ n(通过电极的电子)×100%
③测得η(EDTA-Fe3+)≈100%,η(CO) ≈80%。阴极放电的物质有
④为进一步确认CO2、H2S能协同转化,对CO的来源分析如下:
来源1.CO2通过电极反应产生CO
来源2.电解质(含碳元素)等物质发生降解,产生CO
设计实验探究,证实来源2不成立。实验方案是
方案2明显优于方案1.该研究成果为天然气的净化、资源化转化提供了工业化解决思路。
您最近一年使用:0次
解题方法
5 . 人类向大气中排放的NOx对环境会产生危害,脱除NOx是科学家研究的重要课题。
(1) NOx对环境的一种危害是____ 。
(2) NH3还原法可将NOx还原为N2进行脱除。
已知:
4NH3(g)+3O2(g)=2N2(g)+6H2O(g)△H1=-1530kJ/mol
N2(g)+O2(g)=2NO(g)△H2=+180kJ/mol
写出NH3还原NO反应的热化学方程式:____ 。
(3)碱性KMnO4氧化法也可将NOx进行脱除。
①用KMnO4(NaOH)溶液进行烟气中NO的脱除,将该离子方程式补充完整。____ NO+____ MnO4-+____ =NO2-+3NO3-+__ MnO42-+______
②下列叙述正确的是____ (填字母序号)。
A.将脱除后的混合溶液进行分离可获得氮肥
B.反应后混合溶液中:c( MnO4-)+2c(MnO42-)=c(K+)
C.在不同酸碱性条件下,KMnO4发生氧化还原反应的产物可能不同
③在实验室用KMnO4 ( NaOH)溶液对模拟烟气中的NO进行脱除。若将标准状况下224 L含NO体积分数为10%的模拟烟气进行处理,假设NO最终全部转化为NO3-,理论上需要KMnO4的质量为____ g(KMnO4摩尔质量为158 g·mol-l)。
(4)用Pl-g-C3N4光催化氧化法脱除NO的过程如下图所示。

①该脱除过程中,太阳能转化为___ 能。
②在酸性水溶液中,光催化脱除原理和电化学反应原理类似。g-C3N4端的反应:O2+2H++2e-=H2O2;Pl端的反应:___ ;NO2最终转化为HNO3的化学方程式:___________ 。
(1) NOx对环境的一种危害是
(2) NH3还原法可将NOx还原为N2进行脱除。
已知:
4NH3(g)+3O2(g)=2N2(g)+6H2O(g)△H1=-1530kJ/mol
N2(g)+O2(g)=2NO(g)△H2=+180kJ/mol
写出NH3还原NO反应的热化学方程式:
(3)碱性KMnO4氧化法也可将NOx进行脱除。
①用KMnO4(NaOH)溶液进行烟气中NO的脱除,将该离子方程式补充完整。
②下列叙述正确的是
A.将脱除后的混合溶液进行分离可获得氮肥
B.反应后混合溶液中:c( MnO4-)+2c(MnO42-)=c(K+)
C.在不同酸碱性条件下,KMnO4发生氧化还原反应的产物可能不同
③在实验室用KMnO4 ( NaOH)溶液对模拟烟气中的NO进行脱除。若将标准状况下224 L含NO体积分数为10%的模拟烟气进行处理,假设NO最终全部转化为NO3-,理论上需要KMnO4的质量为
(4)用Pl-g-C3N4光催化氧化法脱除NO的过程如下图所示。

①该脱除过程中,太阳能转化为
②在酸性水溶液中,光催化脱除原理和电化学反应原理类似。g-C3N4端的反应:O2+2H++2e-=H2O2;Pl端的反应:
您最近一年使用:0次
名校
6 . 硫及其化合物之间的转化具有重要意义。请按要求回答下列问题。
(1)土壤中的微生物可将大气中H2S经两步反应氧化成 ,两步反应的能量变化如图,写出1molH2S(g)全部氧化成
,两步反应的能量变化如图,写出1molH2S(g)全部氧化成 (aq)的热化学方程式为
(aq)的热化学方程式为___________ 。________ 。
(3)利用工业废碱渣(主要成分Na2CO3)吸收硫酸厂尾气中的SO2制备无水Na2SO3的成本低,优势明显,其流程如下。___________
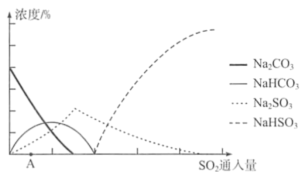
②下图为吸收塔中Na2CO3溶液与SO2反应过程中溶液组成变化。则初期反应(图中A点以前)的离子方程式是___________ ___________ 。
④为了降低由中和器所得溶液中Na2SO3的溶解度,从而提高结晶产率,中和器中加入的NaOH是过量的。
i.用化学反应原理解释NaOH过量的原因___________ 。
ii.结晶时应选择的最佳操作是___________ (选填字母)
a.95~100℃加热蒸发,直至蒸干
b.维持95~100℃蒸发浓缩至有大量晶体析出
c.95~100℃加热浓缩,冷却至室温结晶
⑤为检验Na2SO3成品中是否含少量Na2SO4,需选用的试剂是___________ 。
⑥KIO3滴定法可测定成品中Na2SO3的含量:室温下将0.1260g成品溶于水并加入淀粉做指示剂,再用酸性KIO3标准溶液(x mol/L)进行滴定至溶液恰好由无色变为蓝色,消耗KIO3标准溶液体积为y mL。
i.滴定终点前反应的离子方程式是:_______ ,___ +__
+__ =___+___(将方程式补充完整)
=___+___(将方程式补充完整)
ii.成品中Na2SO3 (M=126g/mol)的质量分数是___________ 。
(1)土壤中的微生物可将大气中H2S经两步反应氧化成
 ,两步反应的能量变化如图,写出1molH2S(g)全部氧化成
,两步反应的能量变化如图,写出1molH2S(g)全部氧化成 (aq)的热化学方程式为
(aq)的热化学方程式为
(3)利用工业废碱渣(主要成分Na2CO3)吸收硫酸厂尾气中的SO2制备无水Na2SO3的成本低,优势明显,其流程如下。

②下图为吸收塔中Na2CO3溶液与SO2反应过程中溶液组成变化。则初期反应(图中A点以前)的离子方程式是

④为了降低由中和器所得溶液中Na2SO3的溶解度,从而提高结晶产率,中和器中加入的NaOH是过量的。
i.用化学反应原理解释NaOH过量的原因
ii.结晶时应选择的最佳操作是
a.95~100℃加热蒸发,直至蒸干
b.维持95~100℃蒸发浓缩至有大量晶体析出
c.95~100℃加热浓缩,冷却至室温结晶
⑤为检验Na2SO3成品中是否含少量Na2SO4,需选用的试剂是
⑥KIO3滴定法可测定成品中Na2SO3的含量:室温下将0.1260g成品溶于水并加入淀粉做指示剂,再用酸性KIO3标准溶液(x mol/L)进行滴定至溶液恰好由无色变为蓝色,消耗KIO3标准溶液体积为y mL。
i.滴定终点前反应的离子方程式是:
 +__
+__ =___+___(将方程式补充完整)
=___+___(将方程式补充完整)ii.成品中Na2SO3 (M=126g/mol)的质量分数是
您最近一年使用:0次
名校
解题方法
7 . 硫及其化合物之间的转化具有重要意义。请按要求回答下列问题。
(1)土壤中的微生物可将大气中H2S 经两步反应氧化成SO ,两步反应的能量变化如图:
,两步反应的能量变化如图:

写出 1mol H2S g全部氧化成 SO (aq)的热化学方程式为
(aq)的热化学方程式为___________ 。
(2)将 SO2通入 0.1mol/L Ba(NO3)2溶液中会观察到有白色沉淀生成,该反应的离子方程式为___________ 。
(3)分别用煮沸和未煮沸过的蒸馏水配制 Ba(NO3)2和 BaCl2溶液,进行如下实验:

①实验 C 中,没有观察到白色沉淀,但 pH 传感器显示溶液呈酸性,用化学用语表示其原因___________ 。
②NaHSO3水溶液为酸性。下列关系正确的是___________
A.c(HSO ) > c(SO
) > c(SO ) > c(H2SO3)
) > c(H2SO3)
B.c(Na+)= c(HSO )+c(SO
)+c(SO ) + c(H2SO3)
) + c(H2SO3)
C.c(Na+)= c(HSO ) > c(H+) > c(OH-)
) > c(H+) > c(OH-)
D.c(Na+) + c(H+) = c(HSO ) + c(OH-) + c(SO
) + c(OH-) + c(SO )
)
③实验 B 中出现白色沉淀比实验 A 快很多。其原因可能是___________ 。
(1)土壤中的微生物可将大气中H2S 经两步反应氧化成SO
 ,两步反应的能量变化如图:
,两步反应的能量变化如图:
写出 1mol H2S g全部氧化成 SO
 (aq)的热化学方程式为
(aq)的热化学方程式为(2)将 SO2通入 0.1mol/L Ba(NO3)2溶液中会观察到有白色沉淀生成,该反应的离子方程式为
(3)分别用煮沸和未煮沸过的蒸馏水配制 Ba(NO3)2和 BaCl2溶液,进行如下实验:

①实验 C 中,没有观察到白色沉淀,但 pH 传感器显示溶液呈酸性,用化学用语表示其原因
②NaHSO3水溶液为酸性。下列关系正确的是
A.c(HSO
 ) > c(SO
) > c(SO ) > c(H2SO3)
) > c(H2SO3) B.c(Na+)= c(HSO
 )+c(SO
)+c(SO ) + c(H2SO3)
) + c(H2SO3) C.c(Na+)= c(HSO
 ) > c(H+) > c(OH-)
) > c(H+) > c(OH-)D.c(Na+) + c(H+) = c(HSO
 ) + c(OH-) + c(SO
) + c(OH-) + c(SO )
)③实验 B 中出现白色沉淀比实验 A 快很多。其原因可能是
您最近一年使用:0次



