名校
1 . 甲基叔戊基醚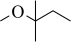 (TAME,简写为T)常用作汽油添加剂。在催化剂作用下,通过甲醇
(TAME,简写为T)常用作汽油添加剂。在催化剂作用下,通过甲醇 (简写为M)与2-甲基-2-丁烯(简写为A)的液相反应制得。通过控制条件,体系中主要发生如下反应(B为2-甲基-1-丁烯的简写,不考虑其他副反应):
(简写为M)与2-甲基-2-丁烯(简写为A)的液相反应制得。通过控制条件,体系中主要发生如下反应(B为2-甲基-1-丁烯的简写,不考虑其他副反应):


反应ⅱ:
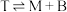

反应ⅲ:

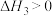
(1)磷钼酸(
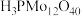 )可作为制备TAME反应催化剂的浸渍试剂。已知钼元素位于第五周期第ⅥB族,核外电子排布与Cr相似。基态钼原子的价层电子排布式为
)可作为制备TAME反应催化剂的浸渍试剂。已知钼元素位于第五周期第ⅥB族,核外电子排布与Cr相似。基态钼原子的价层电子排布式为(2)比较

 (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。(3)我国学者团队对制备TAME反应的催化剂进行了研究。研究表明:用不同浓度(1~3%)的磷钼酸浸渍催化剂,浓度越大催化剂催化活性越好。用浓度分别为1%、2%、3%的磷钼酸浸渍催化剂进行了三组实验,得到
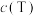 随时间的变化曲线如图所示。
随时间的变化曲线如图所示。
②下列说法正确的有
A.三组实验中,反应速率都随反应进程一直增大
B.平衡后加入惰性溶剂四氢呋喃稀释,
 减小
减小C.催化剂可加快化学反应速率,提高甲醇的平衡转化率
D.降低温度,反应ⅰ和ⅱ的正、逆反应速率都减小
E.达到平衡后,加入M,
 不变
不变(4)研究团队继续研究其他条件不变时,不同醇烯比
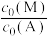 (甲醇M与烯烃A的起始物质的量浓度之比)对平衡的影响,当A起始浓度
(甲醇M与烯烃A的起始物质的量浓度之比)对平衡的影响,当A起始浓度 时,测得平衡时B和T的
时,测得平衡时B和T的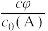 随
随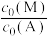 的变化曲线如图。
的变化曲线如图。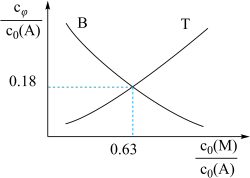
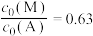 时,计算反应i的平衡常数
时,计算反应i的平衡常数
您最近半年使用:0次
名校
解题方法
2 . 科学研究表明: 存储能量的能力是
存储能量的能力是 的12000倍左右,在大气中的寿命可达740年,如表所示是几种化学键的键能(断裂或形成1mol化学键时吸收或释放的热量)
的12000倍左右,在大气中的寿命可达740年,如表所示是几种化学键的键能(断裂或形成1mol化学键时吸收或释放的热量)
回答下列问题:
(1)①过程
___________ (填“吸收”或“放出”)能量。
②反应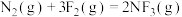
 =
=___________ 。
(2)已知:
①
 ;
;
②
 。
。
现有2mol由炭粉和氢气组成的悬浮气,在足量氧气中完全燃烧生成 (g)和
(g)和 (l),共放出679.0kJ的热量,则2mol悬浮气中C与
(l),共放出679.0kJ的热量,则2mol悬浮气中C与 的物质的量之比为
的物质的量之比为___________ 。
(3)电石( )可通过下列反应制备:
)可通过下列反应制备:
①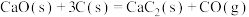
 ;
;
②
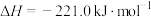 。
。
若不考虑热量损耗,物料转化率均为100%,最终炉中出来的气体只有CO。则为了维持热量平衡,每生产64g ,投料的量为56g CaO及
,投料的量为56g CaO及___________ mol C、___________ mol  。
。
 存储能量的能力是
存储能量的能力是 的12000倍左右,在大气中的寿命可达740年,如表所示是几种化学键的键能(断裂或形成1mol化学键时吸收或释放的热量)
的12000倍左右,在大气中的寿命可达740年,如表所示是几种化学键的键能(断裂或形成1mol化学键时吸收或释放的热量)| 化学键 | N≡N | F—F | N—F |
键能( ) ) | 946 | 154 | 283 |
(1)①过程

②反应
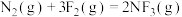
 =
=(2)已知:
①

 ;
;②

 。
。现有2mol由炭粉和氢气组成的悬浮气,在足量氧气中完全燃烧生成
 (g)和
(g)和 (l),共放出679.0kJ的热量,则2mol悬浮气中C与
(l),共放出679.0kJ的热量,则2mol悬浮气中C与 的物质的量之比为
的物质的量之比为(3)电石(
 )可通过下列反应制备:
)可通过下列反应制备:①
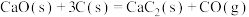
 ;
;②

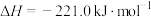 。
。若不考虑热量损耗,物料转化率均为100%,最终炉中出来的气体只有CO。则为了维持热量平衡,每生产64g
 ,投料的量为56g CaO及
,投料的量为56g CaO及 。
。
您最近半年使用:0次
3 . 化学反应过程中都伴随能量变化,吸热或放热是化学反应中能量变化的重要形式。回答下列问题:
(1)化学反应中伴随热量变化的本质原因是反应过程中形成化学键___________ ,断裂化学键___________ 。
(2)已知拆开1mol H—H键、1mol Cl—Cl键、1mol H—Cl键分别需要的能量是436kJ、243kJ、432kJ,则反应 的
的 =
=___________  。
。
(3)已知:
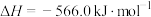 ;
;
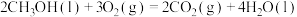
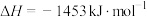 。
。
则 (l)不完全燃烧生成CO和
(l)不完全燃烧生成CO和 (l)的热化学方程式为
(l)的热化学方程式为___________ 。
(4)已知常温常压下,稀的强酸与稀的强碱溶液生成1mol (l)的反应热
(l)的反应热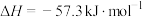 。
。
①表示稀硫酸与稀烧碱溶液生成1mol (l)的热化学方程式为
(l)的热化学方程式为___________ 。
②若用98%浓硫酸代替稀硫酸与稀烧碱溶液进行中和反应反应热测定,则所测得的
___________ (填“偏大”或“偏小”)。
(1)化学反应中伴随热量变化的本质原因是反应过程中形成化学键
(2)已知拆开1mol H—H键、1mol Cl—Cl键、1mol H—Cl键分别需要的能量是436kJ、243kJ、432kJ,则反应
 的
的 =
= 。
。(3)已知:

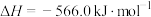 ;
;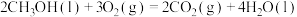
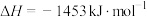 。
。则
 (l)不完全燃烧生成CO和
(l)不完全燃烧生成CO和 (l)的热化学方程式为
(l)的热化学方程式为(4)已知常温常压下,稀的强酸与稀的强碱溶液生成1mol
 (l)的反应热
(l)的反应热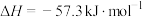 。
。①表示稀硫酸与稀烧碱溶液生成1mol
 (l)的热化学方程式为
(l)的热化学方程式为②若用98%浓硫酸代替稀硫酸与稀烧碱溶液进行中和反应反应热测定,则所测得的

您最近半年使用:0次
名校
解题方法
4 . 已知 (g)和
(g)和 (l)的燃烧热分别是1411.0
(l)的燃烧热分别是1411.0 和1366.8
和1366.8 ,则反应
,则反应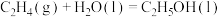 的
的 为
为
 (g)和
(g)和 (l)的燃烧热分别是1411.0
(l)的燃烧热分别是1411.0 和1366.8
和1366.8 ,则反应
,则反应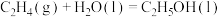 的
的 为
为A.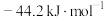 | B.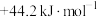 | C.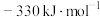 | D. |
您最近半年使用:0次
解题方法
5 . 利用 和
和 合成甲醇(
合成甲醇( ),在催化剂作用下涉及以下反应:
),在催化剂作用下涉及以下反应:
反应ⅰ
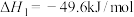
反应ⅱ
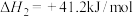
反应ⅲ

回答下列问题:
(1)反应ⅲ在______ (填“高温”、“低温”或“任意温度”)条件下能自发进行。
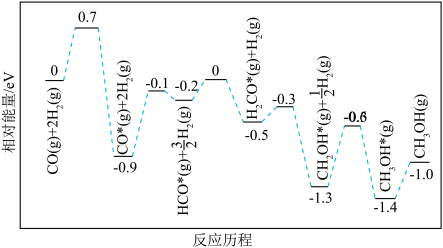
(2)反应ⅲ的反应历程如下图所示,图中数据表示微粒数目以及微粒的相对总能量,其中吸附在催化剂表面的物质用*标注,决定该过程的总反应速率的基元反应方程式为______ 。 和
和 合成
合成 涉及的三个反应,下列说法正确的是______(填标号)。
涉及的三个反应,下列说法正确的是______(填标号)。
(4)在恒压密闭容器中,按照 投料发生反应ⅰ和反应ⅱ。
投料发生反应ⅰ和反应ⅱ。
Ⅰ.反应达平衡时,测得 转化率和甲醇的选择性
转化率和甲醇的选择性 随温度的变化如图1所示。
随温度的变化如图1所示。______ K(填“473”、“513”或“553”)时,反应体系内甲醇的产量最高。
② 的平衡转化率随温度升高而增大的原因是
的平衡转化率随温度升高而增大的原因是______ 。
Ⅱ.用平衡分压代替平衡浓度可以得到平衡常数 ,
, 随温度的倒数(
随温度的倒数( )的变化关系如图2所示。(已知:分压=总压×该气体的物质的量分数;压强的单位为kPa)
)的变化关系如图2所示。(已知:分压=总压×该气体的物质的量分数;压强的单位为kPa)______ (填“m”或“n”)。
④通过调整温度可调控平衡时的分压比值 ,A点对应温度下,平衡时
,A点对应温度下,平衡时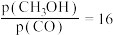 ,则
,则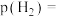
______ kPa。
⑤当体系总压为10kPa时,B点对应温度下体系达到平衡时 的转化率为80%,反应i的
的转化率为80%,反应i的
______  (用分数表示)。
(用分数表示)。
 和
和 合成甲醇(
合成甲醇( ),在催化剂作用下涉及以下反应:
),在催化剂作用下涉及以下反应:反应ⅰ

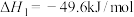
反应ⅱ

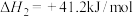
反应ⅲ


回答下列问题:
(1)反应ⅲ在
(2)反应ⅲ的反应历程如下图所示,图中数据表示微粒数目以及微粒的相对总能量,其中吸附在催化剂表面的物质用*标注,决定该过程的总反应速率的基元反应方程式为
 和
和 合成
合成 涉及的三个反应,下列说法正确的是______(填标号)。
涉及的三个反应,下列说法正确的是______(填标号)。A.减小 的浓度有利于提高 的浓度有利于提高 的转化率 的转化率 |
| B.当气体的平均相对分子质量保持不变时,说明反应体系已达平衡 |
| C.体系达平衡后,若压缩体积,则反应ⅰ平衡正向移动,反应ⅱ平衡不移动 |
D.选用合适的催化剂可以提高 在单位时间内的产量 在单位时间内的产量 |
(4)在恒压密闭容器中,按照
 投料发生反应ⅰ和反应ⅱ。
投料发生反应ⅰ和反应ⅱ。Ⅰ.反应达平衡时,测得
 转化率和甲醇的选择性
转化率和甲醇的选择性 随温度的变化如图1所示。
随温度的变化如图1所示。
②
 的平衡转化率随温度升高而增大的原因是
的平衡转化率随温度升高而增大的原因是Ⅱ.用平衡分压代替平衡浓度可以得到平衡常数
 ,
, 随温度的倒数(
随温度的倒数( )的变化关系如图2所示。(已知:分压=总压×该气体的物质的量分数;压强的单位为kPa)
)的变化关系如图2所示。(已知:分压=总压×该气体的物质的量分数;压强的单位为kPa)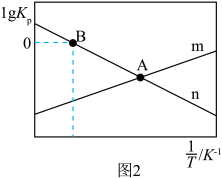
④通过调整温度可调控平衡时的分压比值
 ,A点对应温度下,平衡时
,A点对应温度下,平衡时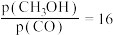 ,则
,则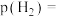
⑤当体系总压为10kPa时,B点对应温度下体系达到平衡时
 的转化率为80%,反应i的
的转化率为80%,反应i的
 (用分数表示)。
(用分数表示)。
您最近半年使用:0次
名校
6 . 化学反应中均伴随有能量变化。回答下列问题:
(1)下列反应中,反应物的总能量小于生成物的总能量的是___________ (填选项字母)。
A.Na2O2与H2O反应 B.乙醇的燃烧反应 C.CaCO3受热分解
(2)已知25℃时,下列物质的相对能量如表所示:
①表示 燃烧热的热化学方程式为
燃烧热的热化学方程式为___________ 。
②36g 分解生成
分解生成 和
和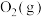
___________ (填“吸收”或“放出”)___________ kJ的热量。
(3)已知反应: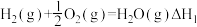

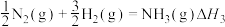
写出氨气和氧气反应生成NO2和水蒸气的热化学方程式___________ (用 、
、 、
、 、
、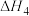 表示反应的
表示反应的 )
)
(4)硅光电池作为电源已广泛应用于人造卫星、灯塔和无人气象站等,工业制备纯硅的反应为
 ,若将生成的HCl通入100mL1mol/L的NaOH溶液中恰好完全反应,则此制备纯硅反应过程
,若将生成的HCl通入100mL1mol/L的NaOH溶液中恰好完全反应,则此制备纯硅反应过程___________ (填“吸收”或“放出”)的热量是___________ kJ。
(5)甲醇是一种新型的汽车动力燃料。
①以 和
和 为原料合成甲醇(CH3OH),反应的能量变化如下图所示,则图中A处应填写的内容为
为原料合成甲醇(CH3OH),反应的能量变化如下图所示,则图中A处应填写的内容为___________ 。
设CO以C≡O键构成,则工业制备甲醇的热化学方程式为___________ 。
(1)下列反应中,反应物的总能量小于生成物的总能量的是
A.Na2O2与H2O反应 B.乙醇的燃烧反应 C.CaCO3受热分解
(2)已知25℃时,下列物质的相对能量如表所示:
| 物质 |  | 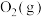 |  | 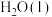 |
| 相对能量(kJ·mol-1) | 0 | 0 | -242 | -286 |
 燃烧热的热化学方程式为
燃烧热的热化学方程式为②36g
 分解生成
分解生成 和
和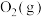
(3)已知反应:
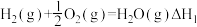

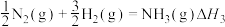
写出氨气和氧气反应生成NO2和水蒸气的热化学方程式
 、
、 、
、 、
、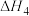 表示反应的
表示反应的 )
)(4)硅光电池作为电源已广泛应用于人造卫星、灯塔和无人气象站等,工业制备纯硅的反应为
 ,若将生成的HCl通入100mL1mol/L的NaOH溶液中恰好完全反应,则此制备纯硅反应过程
,若将生成的HCl通入100mL1mol/L的NaOH溶液中恰好完全反应,则此制备纯硅反应过程(5)甲醇是一种新型的汽车动力燃料。
①以
 和
和 为原料合成甲醇(CH3OH),反应的能量变化如下图所示,则图中A处应填写的内容为
为原料合成甲醇(CH3OH),反应的能量变化如下图所示,则图中A处应填写的内容为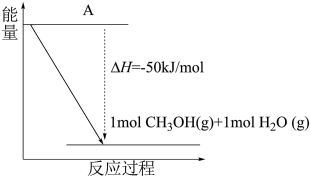
②工业上利用CO和H2来制备甲醇(CH3OH,结构式为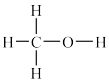 )气体。已知某些化学键的键能数据如下表:
)气体。已知某些化学键的键能数据如下表:
| 化学键 | C-C | C-H | H-H | C-O | C≡O | H-O |
| 键能/kJ·mol-1 | 348 | 413 | 436 | 358 | 1072 | 463 |
您最近半年使用:0次
解题方法
7 . 甲醇和乙醇都是清洁能源,也是重要的化工原料。回答下列问题:
(1)工业上利用合成气合成甲醇: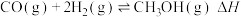
已知:① ;
;
②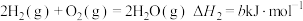 ;
;
③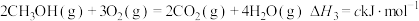
上述反应中的
___________  。
。
(2)一定温度下,在恒容密闭容器中充入1molCO和1molH2,在固体催化剂作用下合成甲醇: ,下列叙述错误的是___________(填字母)。
,下列叙述错误的是___________(填字母)。
(3)甲醇是一种潜在储氢材料。我国学者研究甲醇在钯基催化剂表面上分解制氢: ,其反应历程如图a所示(吸附在催化剂表面的物种用“*”表示)。
,其反应历程如图a所示(吸附在催化剂表面的物种用“*”表示)。___________ 下(高温、低温、任意温度)自发进行;图示历程包括___________ 个基元反应;其中决速反应是反应___________ (填序号),写出该步反应式:___________ 。
(4)工业上,可以采用CO2催化还原制备CH3OH、CH3CH2OH.发生反应如下:
① (主反应);
(主反应);
② (主反应);
(主反应);
③ (副反应)。
(副反应)。
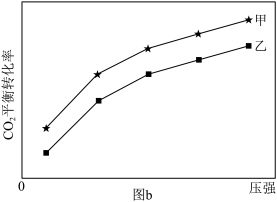
一定温度下,在甲、乙体积相同的反应容器中分别充入1molCO2和3molH2,发生上述反应,其中一个容器使用水分子膜分离技术,另一个容器不使用水分子膜分离技术。实验测得CO2平衡转化率与压强关系如图b所示。其他条件相同,增大压强,CO2平衡转化率增大,其原因是___________ ;采用水分子膜分离技术的容器是___________ (填“甲”或“乙”)。 为
为___________  。(写出数字表达式即可,分压=总压×物质的量分数)
。(写出数字表达式即可,分压=总压×物质的量分数)
(1)工业上利用合成气合成甲醇:
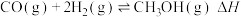
已知:①
 ;
;②
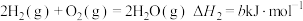 ;
;③
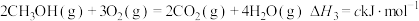
上述反应中的

 。
。(2)一定温度下,在恒容密闭容器中充入1molCO和1molH2,在固体催化剂作用下合成甲醇:
 ,下列叙述错误的是___________(填字母)。
,下列叙述错误的是___________(填字母)。| A.当CO体积分数不变时达到平衡状态 |
| B.平衡后充入少量氩气,平衡不移动 |
| C.平衡后再充入0.1molCO和0.1molH2,CO平衡转化率增大 |
| D.增大催化剂质量,正、逆反应速率同倍数增大 |
(3)甲醇是一种潜在储氢材料。我国学者研究甲醇在钯基催化剂表面上分解制氢:
 ,其反应历程如图a所示(吸附在催化剂表面的物种用“*”表示)。
,其反应历程如图a所示(吸附在催化剂表面的物种用“*”表示)。
(4)工业上,可以采用CO2催化还原制备CH3OH、CH3CH2OH.发生反应如下:
①
 (主反应);
(主反应);②
 (主反应);
(主反应);③
 (副反应)。
(副反应)。一定温度下,在甲、乙体积相同的反应容器中分别充入1molCO2和3molH2,发生上述反应,其中一个容器使用水分子膜分离技术,另一个容器不使用水分子膜分离技术。实验测得CO2平衡转化率与压强关系如图b所示。其他条件相同,增大压强,CO2平衡转化率增大,其原因是
 为
为 。(写出数字表达式即可,分压=总压×物质的量分数)
。(写出数字表达式即可,分压=总压×物质的量分数)
您最近半年使用:0次
名校
解题方法
8 . 我国科学家根据 在HZSM-5载体上的单层分散行为设计催化剂用于
在HZSM-5载体上的单层分散行为设计催化剂用于 选择性还原
选择性还原 。回答下列问题:
。回答下列问题:
已知:①
 kJ⋅mol
kJ⋅mol (
( )
)
②
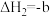 kJ⋅mol
kJ⋅mol (
( )
)
(1)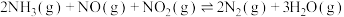

______ kJ⋅mol 。
。
(2)向恒容密闭容器中充入0.4 mol 和0.6 mol
和0.6 mol ,只发生反应①。下列叙述正确的是______(填标号)。
,只发生反应①。下列叙述正确的是______(填标号)。
(3)一定温度下,起始投料不变,单位时间内氮氧化物转化率、表面活泼氧量比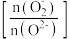 与催化剂组成类型的关系如下图所示。催化效能最佳的催化剂组成是
与催化剂组成类型的关系如下图所示。催化效能最佳的催化剂组成是______ (填具体催化剂名称)。 、2 mol
、2 mol  和4 mol
和4 mol  ,在不同组成的催化剂作用下,单位时间内氮氧化物的转化率与温度的关系如下图所示。
,在不同组成的催化剂作用下,单位时间内氮氧化物的转化率与温度的关系如下图所示。______ 。
②a→b段氮氧化物转化率变化的原因是____________ 。
③M点反应______ (填“达到”或“未达到”)平衡状态,判断依据是______ ,M→N段氮氧化物转化率变化的原因可能是____________ 。
(5)一定温度下,向体积为1 L的恒容密闭容器中充入1 mol 和2 mol
和2 mol ,在催化剂作用下发生反应:①
,在催化剂作用下发生反应:① :②
:②
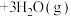 达到平衡时,NO转化率为70%,
达到平衡时,NO转化率为70%, 的选择性为50%[
的选择性为50%[ 的选择性
的选择性 ]该温度下,反应①的平衡常数
]该温度下,反应①的平衡常数
______ mol·L (列出计算式即可)。
(列出计算式即可)。
 在HZSM-5载体上的单层分散行为设计催化剂用于
在HZSM-5载体上的单层分散行为设计催化剂用于 选择性还原
选择性还原 。回答下列问题:
。回答下列问题:已知:①

 kJ⋅mol
kJ⋅mol (
( )
)②

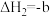 kJ⋅mol
kJ⋅mol (
( )
)(1)
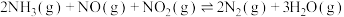

 。
。(2)向恒容密闭容器中充入0.4 mol
 和0.6 mol
和0.6 mol ,只发生反应①。下列叙述正确的是______(填标号)。
,只发生反应①。下列叙述正确的是______(填标号)。| A.恒温条件下,压强不随时间变化时反应达到平衡状态 |
B.平衡时温度不变,再充入1 mol  时平衡常数减小 时平衡常数减小 |
| C.反应达到平衡时放出的热量为0.1a kJ |
| D.加入高效催化剂,反应达到平衡时NO的转化率增大 |
(3)一定温度下,起始投料不变,单位时间内氮氧化物转化率、表面活泼氧量比
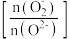 与催化剂组成类型的关系如下图所示。催化效能最佳的催化剂组成是
与催化剂组成类型的关系如下图所示。催化效能最佳的催化剂组成是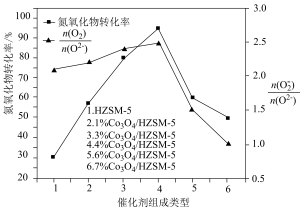
 、2 mol
、2 mol  和4 mol
和4 mol  ,在不同组成的催化剂作用下,单位时间内氮氧化物的转化率与温度的关系如下图所示。
,在不同组成的催化剂作用下,单位时间内氮氧化物的转化率与温度的关系如下图所示。
②a→b段氮氧化物转化率变化的原因是
③M点反应
(5)一定温度下,向体积为1 L的恒容密闭容器中充入1 mol
 和2 mol
和2 mol ,在催化剂作用下发生反应:①
,在催化剂作用下发生反应:① :②
:②
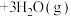 达到平衡时,NO转化率为70%,
达到平衡时,NO转化率为70%, 的选择性为50%[
的选择性为50%[ 的选择性
的选择性 ]该温度下,反应①的平衡常数
]该温度下,反应①的平衡常数
 (列出计算式即可)。
(列出计算式即可)。
您最近半年使用:0次
名校
解题方法
9 . I.化学反应在发生物质变化的同时伴随着能量变化,请回答下列问题:
(1)汽车发动机工作时会引发 和
和 反应,生成
反应,生成 等污染大气,其中生成
等污染大气,其中生成 的能量变化如图所示,则图中三种分子最稳定的是
的能量变化如图所示,则图中三种分子最稳定的是___________ ,图中对应反应的热化学方程式为___________ 。 可转化为
可转化为 ,
, 在空气中加热反应可制得铁系氧化物材料。
在空气中加热反应可制得铁系氧化物材料。
已知25℃,101 时:
时:
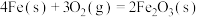
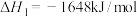


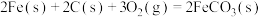
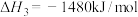
则

___________ 。
Ⅱ.某实验小组设计用0.55 的
的 溶液100
溶液100 与0.50
与0.50 的盐酸100
的盐酸100 置于如图所示的装置中进行测定中和反应反应热的实验。
置于如图所示的装置中进行测定中和反应反应热的实验。___________ ,装置中还存在的错误有___________ ;大烧杯杯口若不盖泡沫塑料板,测得中和反应的反应热 将
将___________ (填“偏大”、“偏小”或“无影响”)。
(4)实验中,所用 稍过量的原因是
稍过量的原因是___________ 。
(5)该实验小组做了三次实验,每次取盐酸和 溶液各100
溶液各100 ,并记录原始数据:
,并记录原始数据:
已知盐酸、 溶液密度均近似为1.00
溶液密度均近似为1.00 ,中和后混合液
,中和后混合液 ,则该中和反应的反应热
,则该中和反应的反应热
___________ 。(保留到小数点后1位)
(1)汽车发动机工作时会引发
 和
和 反应,生成
反应,生成 等污染大气,其中生成
等污染大气,其中生成 的能量变化如图所示,则图中三种分子最稳定的是
的能量变化如图所示,则图中三种分子最稳定的是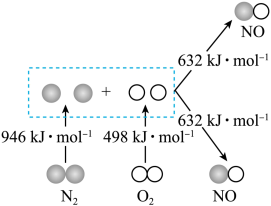
 可转化为
可转化为 ,
, 在空气中加热反应可制得铁系氧化物材料。
在空气中加热反应可制得铁系氧化物材料。已知25℃,101
 时:
时: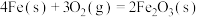
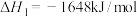


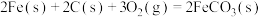
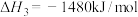
则


Ⅱ.某实验小组设计用0.55
 的
的 溶液100
溶液100 与0.50
与0.50 的盐酸100
的盐酸100 置于如图所示的装置中进行测定中和反应反应热的实验。
置于如图所示的装置中进行测定中和反应反应热的实验。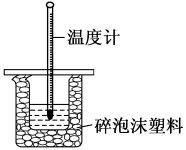
 将
将(4)实验中,所用
 稍过量的原因是
稍过量的原因是(5)该实验小组做了三次实验,每次取盐酸和
 溶液各100
溶液各100 ,并记录原始数据:
,并记录原始数据:| 实验序号 | 起始温度 /℃ /℃ | 终止温度 /℃ /℃ | 温差 /℃ /℃ | ||
| 盐酸 |  溶液 溶液 | 平均值 | |||
| 1 | 25.1 | 24.9 | 25.0 | 28.0 | 3.0 |
| 2 | 25.1 | 25.1 | 25.1 | 28.2 | 3.1 |
| 3 | 25.1 | 25.1 | 25.1 | 28.0 | 2.9 |
 溶液密度均近似为1.00
溶液密度均近似为1.00 ,中和后混合液
,中和后混合液 ,则该中和反应的反应热
,则该中和反应的反应热
您最近半年使用:0次
名校
解题方法
10 . 资源化利用CO2,不仅可以减少温室气体的排放,还可以获得燃料或重要的化工产品。
(1)CO2的捕集:
①CO2属于___________ 分子(填“极性”或“非极性”),其晶体(干冰)属于__________ 晶体。
②用饱和 溶液做吸收剂可“捕集”CO2。若所得溶液
溶液做吸收剂可“捕集”CO2。若所得溶液 ,溶液中c(HCO
,溶液中c(HCO ):c(CO
):c(CO )=
)=_______ ;(室温下, 的K1=4×10-7;K2=5×10-11)若吸收剂失效,可利用NaOH溶液使其再生,写出该反应的离子方程式
的K1=4×10-7;K2=5×10-11)若吸收剂失效,可利用NaOH溶液使其再生,写出该反应的离子方程式_____ 。
③聚合离子液体是目前广泛研究的CO2吸附剂。结合下图 分析聚合离子液体吸附CO2的有利条件是____________ 。
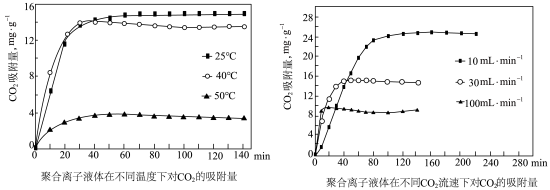
(2)生产尿素:工业上以CO2、 为原料生产尿素[CO(NH2)2],该反应分为二步进行:
为原料生产尿素[CO(NH2)2],该反应分为二步进行:
第一步: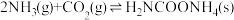
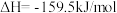
第二步:
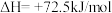
写出上述合成尿素的热化学方程式_______ 。
(3)合成乙酸:中国科学家首次以 、CO2和H2为原料高效合成乙酸,其反应路径如图所示:
、CO2和H2为原料高效合成乙酸,其反应路径如图所示:
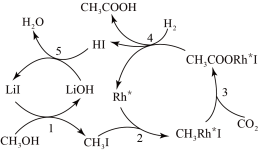
①原料中的 可通过电解法由
可通过电解法由 制取,用稀硫酸作电解质溶液,写出生成
制取,用稀硫酸作电解质溶液,写出生成 的电极反应式:
的电极反应式:____________ 。
②根据图示 ,写出总反应的化学方程式:_______ 。
(1)CO2的捕集:
①CO2属于
②用饱和
 溶液做吸收剂可“捕集”CO2。若所得溶液
溶液做吸收剂可“捕集”CO2。若所得溶液 ,溶液中c(HCO
,溶液中c(HCO ):c(CO
):c(CO )=
)= 的K1=4×10-7;K2=5×10-11)若吸收剂失效,可利用NaOH溶液使其再生,写出该反应的离子方程式
的K1=4×10-7;K2=5×10-11)若吸收剂失效,可利用NaOH溶液使其再生,写出该反应的离子方程式③聚合离子液体是目前广泛研究的CO2吸附剂。

(2)生产尿素:工业上以CO2、
 为原料生产尿素[CO(NH2)2],该反应分为二步进行:
为原料生产尿素[CO(NH2)2],该反应分为二步进行:第一步:
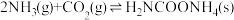
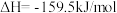
第二步:

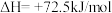
写出上述合成尿素的热化学方程式
(3)合成乙酸:中国科学家首次以
 、CO2和H2为原料高效合成乙酸,其反应路径如图所示:
、CO2和H2为原料高效合成乙酸,其反应路径如图所示:
①原料中的
 可通过电解法由
可通过电解法由 制取,用稀硫酸作电解质溶液,写出生成
制取,用稀硫酸作电解质溶液,写出生成 的电极反应式:
的电极反应式:②
您最近半年使用:0次
2024-04-04更新
|
281次组卷
|
3卷引用:辽宁省实验中学2024届高三高考适应性测试(二)化学试题



