名校
1 . 甲醇 是重要的化工原料。回答问题:
是重要的化工原料。回答问题:
(1)以甲醇为原料制备甲醛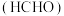 。
。
Ⅰ.脱氢法:CH3OH(g) HCHO(g)+H2(g) ΔH1=+86.1kJ·mol-1
HCHO(g)+H2(g) ΔH1=+86.1kJ·mol-1
Ⅱ.氧化法:CH3OH(g)+ O2(g)
O2(g) HCHO(g)+H2O(g) ΔH2
HCHO(g)+H2O(g) ΔH2
Ⅲ.深度氧化反应:HCHO(g)+ O2(g)
O2(g) CO(g)+H2O(g) ΔH3
CO(g)+H2O(g) ΔH3 O2(g)=H2O(g)ΔH4=-197.8kJ·mol-1,计算
O2(g)=H2O(g)ΔH4=-197.8kJ·mol-1,计算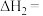
_______ 。
②图-1中两条曲线分别为反应Ⅰ和Ⅱ平衡常数 随温度变化关系的曲线,其中表示反应Ⅰ的为
随温度变化关系的曲线,其中表示反应Ⅰ的为_______ (填曲线标记字母)。
③图-2为甲醇氧化法在不同温度下甲醇转化率与甲醛产率的曲线图。600K以后,随温度升高,甲醛产率显著下降的主要原因是_______ 。
(2)一定条件下CO(g)+2H2(g) CH3OH(g) ΔH<0。在容积均恒为
CH3OH(g) ΔH<0。在容积均恒为 的Ⅰ、Ⅱ、Ⅲ三个恒温容器中分别充入1.0mol CO和2.0mol H2,分别在
的Ⅰ、Ⅱ、Ⅲ三个恒温容器中分别充入1.0mol CO和2.0mol H2,分别在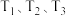 温度下反应,
温度下反应, 时
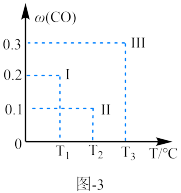
时 的体积分数如图-3所示,此时Ⅰ、Ⅱ、Ⅲ三个容器中一定达到化学平衡状态的是
的体积分数如图-3所示,此时Ⅰ、Ⅱ、Ⅲ三个容器中一定达到化学平衡状态的是_______ ;其化学平衡常数为_______ 。容器Ⅱ中, 内,
内, 的反应速率为
的反应速率为_______  。
。
 是重要的化工原料。回答问题:
是重要的化工原料。回答问题:(1)以甲醇为原料制备甲醛
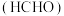 。
。Ⅰ.脱氢法:CH3OH(g)
 HCHO(g)+H2(g) ΔH1=+86.1kJ·mol-1
HCHO(g)+H2(g) ΔH1=+86.1kJ·mol-1Ⅱ.氧化法:CH3OH(g)+
 O2(g)
O2(g) HCHO(g)+H2O(g) ΔH2
HCHO(g)+H2O(g) ΔH2Ⅲ.深度氧化反应:HCHO(g)+
 O2(g)
O2(g) CO(g)+H2O(g) ΔH3
CO(g)+H2O(g) ΔH3
 O2(g)=H2O(g)ΔH4=-197.8kJ·mol-1,计算
O2(g)=H2O(g)ΔH4=-197.8kJ·mol-1,计算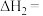
②图-1中两条曲线分别为反应Ⅰ和Ⅱ平衡常数
 随温度变化关系的曲线,其中表示反应Ⅰ的为
随温度变化关系的曲线,其中表示反应Ⅰ的为③图-2为甲醇氧化法在不同温度下甲醇转化率与甲醛产率的曲线图。600K以后,随温度升高,甲醛产率显著下降的主要原因是
(2)一定条件下CO(g)+2H2(g)
 CH3OH(g) ΔH<0。在容积均恒为
CH3OH(g) ΔH<0。在容积均恒为 的Ⅰ、Ⅱ、Ⅲ三个恒温容器中分别充入1.0mol CO和2.0mol H2,分别在
的Ⅰ、Ⅱ、Ⅲ三个恒温容器中分别充入1.0mol CO和2.0mol H2,分别在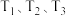 温度下反应,
温度下反应, 时
时 的体积分数如图-3所示,此时Ⅰ、Ⅱ、Ⅲ三个容器中一定达到化学平衡状态的是
的体积分数如图-3所示,此时Ⅰ、Ⅱ、Ⅲ三个容器中一定达到化学平衡状态的是 内,
内, 的反应速率为
的反应速率为 。
。
您最近半年使用:0次
名校
2 . 中国科学家首次实现了二氧化碳到淀粉的从头合成,CO2的捕集、利用与封存成为科学家研究的重要课题。
以CO2、C2H6为原料合成C2H4涉及的主要反应如下:
I.CO2(g)+C2H6(g) C2H4(g)+H2O(g)+CO(g) ΔH=+177kJ·mol-1 (主反应)
C2H4(g)+H2O(g)+CO(g) ΔH=+177kJ·mol-1 (主反应)
II.C2H6(g) CH4(g)+H2(g)+C(s) ΔH=+9kJ·mol-1 (副反应)
CH4(g)+H2(g)+C(s) ΔH=+9kJ·mol-1 (副反应)
(1)反应I的反应历程可分为如下两步:
i. C2H6(g) C2H4(g)+H2(g) ΔH1 (反应速率较快)
C2H4(g)+H2(g) ΔH1 (反应速率较快)
ii. H2(g)+CO2(g) H2O(g)+CO(g) ΔH2=+44kJ·mol-1 (反应速率较慢)
H2O(g)+CO(g) ΔH2=+44kJ·mol-1 (反应速率较慢)
①∆H1=_______
②相比于提高c(C2H6),提高c(CO2)对反应I速率影响更大,原因是_______ 。
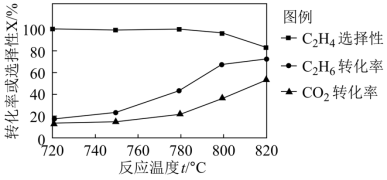
(2)向恒压密闭容器中充入CO2和C2H6合成C2H4,发生主反应,温度对催化剂K-Fe-Mn/Si-2性能的影响如图所示,工业生产综合各方面的因素,反应选择800℃的原因是_______ 。 C2H4(g)+2H2(g) ΔH>0,温度T时,向2L的恒容反应器中充入2molCH4,仅发生上述反应,反应过程中CH4的物质的量随时间变化如图所示:
C2H4(g)+2H2(g) ΔH>0,温度T时,向2L的恒容反应器中充入2molCH4,仅发生上述反应,反应过程中CH4的物质的量随时间变化如图所示:
____ (用含有x的代数式表示);当温度升高时,k正增大m倍,k逆增大n倍,则m_____ n(填“>”、“<”或“=”)。
以CO2、C2H6为原料合成C2H4涉及的主要反应如下:
I.CO2(g)+C2H6(g)
 C2H4(g)+H2O(g)+CO(g) ΔH=+177kJ·mol-1 (主反应)
C2H4(g)+H2O(g)+CO(g) ΔH=+177kJ·mol-1 (主反应)II.C2H6(g)
 CH4(g)+H2(g)+C(s) ΔH=+9kJ·mol-1 (副反应)
CH4(g)+H2(g)+C(s) ΔH=+9kJ·mol-1 (副反应)(1)反应I的反应历程可分为如下两步:
i. C2H6(g)
 C2H4(g)+H2(g) ΔH1 (反应速率较快)
C2H4(g)+H2(g) ΔH1 (反应速率较快)ii. H2(g)+CO2(g)
 H2O(g)+CO(g) ΔH2=+44kJ·mol-1 (反应速率较慢)
H2O(g)+CO(g) ΔH2=+44kJ·mol-1 (反应速率较慢)①∆H1=
②相比于提高c(C2H6),提高c(CO2)对反应I速率影响更大,原因是
(2)向恒压密闭容器中充入CO2和C2H6合成C2H4,发生主反应,温度对催化剂K-Fe-Mn/Si-2性能的影响如图所示,工业生产综合各方面的因素,反应选择800℃的原因是
 C2H4(g)+2H2(g) ΔH>0,温度T时,向2L的恒容反应器中充入2molCH4,仅发生上述反应,反应过程中CH4的物质的量随时间变化如图所示:
C2H4(g)+2H2(g) ΔH>0,温度T时,向2L的恒容反应器中充入2molCH4,仅发生上述反应,反应过程中CH4的物质的量随时间变化如图所示: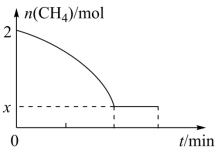

您最近半年使用:0次
3 . 热化学方程式是一种能够表明反应释放或吸收热量的热化学方程式。
(1)已知:①CH4(g)+2O2(g)=CO2(g)+2H2O(g) ΔH=-846.3kJ·mol-1
②CO(g)+H2O(g)=CO2(g)+H2(g) ΔH=+2.8kJ·mol-1
③2CO(g)+O2(g)=2CO2(g) ΔH=-566.0kJ·mol-1
反应CO2(g)+CH4(g)=2CO(g)+2H2(g)的ΔH=_____ 。
(2)已知下列反应的反应热:
①CH3COOH(1)+2O2(g)=2CO2(g)+2H2O(1) ΔH=-870.3kJ/mol
②C(s)+O2(g)=CO2(g) ΔH=-393.5kJ/mol
③2C(s)+2H2(g)+O2(g)=CH3COOH(1) ΔH=-488.3kJ/mol
请写出H2燃烧热的热化学方程式_____ 。
(3)在101kPa下,CH4(g)、H2(g)、C(s)的燃烧热分别为890.3kJ/mol、285.8kJ/mol和393.5kJ/mol,则CH4(g)分解为H2(g)、C(s)的热化学方程式_____ 。
(1)已知:①CH4(g)+2O2(g)=CO2(g)+2H2O(g) ΔH=-846.3kJ·mol-1
②CO(g)+H2O(g)=CO2(g)+H2(g) ΔH=+2.8kJ·mol-1
③2CO(g)+O2(g)=2CO2(g) ΔH=-566.0kJ·mol-1
反应CO2(g)+CH4(g)=2CO(g)+2H2(g)的ΔH=
(2)已知下列反应的反应热:
①CH3COOH(1)+2O2(g)=2CO2(g)+2H2O(1) ΔH=-870.3kJ/mol
②C(s)+O2(g)=CO2(g) ΔH=-393.5kJ/mol
③2C(s)+2H2(g)+O2(g)=CH3COOH(1) ΔH=-488.3kJ/mol
请写出H2燃烧热的热化学方程式
(3)在101kPa下,CH4(g)、H2(g)、C(s)的燃烧热分别为890.3kJ/mol、285.8kJ/mol和393.5kJ/mol,则CH4(g)分解为H2(g)、C(s)的热化学方程式
您最近半年使用:0次
4 .  的资源化不仅能减少
的资源化不仅能减少 排放,还能有效利用碳资源。
排放,还能有效利用碳资源。
(1) 制取低碳醇的反应如下:
制取低碳醇的反应如下:
反应Ⅰ:
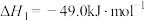
反应Ⅱ:

则 与
与 合成
合成 的热化学方程式为
的热化学方程式为___________ ;在密闭容器中,按 充入
充入 和
和 ,平衡时
,平衡时 、含碳物质的物质的量分数随温度变化的曲线如图所示,图中表示
、含碳物质的物质的量分数随温度变化的曲线如图所示,图中表示 组分的是曲线
组分的是曲线___________ (填序号)。

(2)250℃时,向 恒容密闭容器中通入
恒容密闭容器中通入 、
、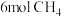 ,发生如下反应:
,发生如下反应: 。平衡时,各组分体积分数如下表所示。
。平衡时,各组分体积分数如下表所示。
该条件下, 的平衡转化率为
的平衡转化率为___________ ;向平衡体系中再通入 、
、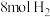 ,平衡
,平衡___________ (填“正向移动”、“逆向移动”或“不移动”)。
(3)用 溶液吸收
溶液吸收 可得
可得 溶液。室温下,
溶液。室温下,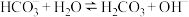 的平衡常数K=
的平衡常数K=___________ [已知: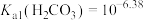 ]。在密闭容器中,向含有催化剂的
]。在密闭容器中,向含有催化剂的 溶液中通入
溶液中通入 制备
制备 ,测得
,测得 的转化率随温度的变化如图所示。在40℃至80℃过程中,转化率迅速上升的原因是
的转化率随温度的变化如图所示。在40℃至80℃过程中,转化率迅速上升的原因是___________ 。

 的资源化不仅能减少
的资源化不仅能减少 排放,还能有效利用碳资源。
排放,还能有效利用碳资源。(1)
 制取低碳醇的反应如下:
制取低碳醇的反应如下:反应Ⅰ:

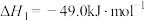
反应Ⅱ:


则
 与
与 合成
合成 的热化学方程式为
的热化学方程式为 充入
充入 和
和 ,平衡时
,平衡时 、含碳物质的物质的量分数随温度变化的曲线如图所示,图中表示
、含碳物质的物质的量分数随温度变化的曲线如图所示,图中表示 组分的是曲线
组分的是曲线
(2)250℃时,向
 恒容密闭容器中通入
恒容密闭容器中通入 、
、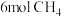 ,发生如下反应:
,发生如下反应: 。平衡时,各组分体积分数如下表所示。
。平衡时,各组分体积分数如下表所示。| 物质 |  |  | CO |  |
| 体积分数 | 0.1 | 0.1 | 0.4 | 0.4 |
 的平衡转化率为
的平衡转化率为 、
、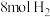 ,平衡
,平衡(3)用
 溶液吸收
溶液吸收 可得
可得 溶液。室温下,
溶液。室温下,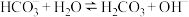 的平衡常数K=
的平衡常数K=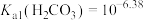 ]。在密闭容器中,向含有催化剂的
]。在密闭容器中,向含有催化剂的 溶液中通入
溶液中通入 制备
制备 ,测得
,测得 的转化率随温度的变化如图所示。在40℃至80℃过程中,转化率迅速上升的原因是
的转化率随温度的变化如图所示。在40℃至80℃过程中,转化率迅速上升的原因是
您最近半年使用:0次
5 . 磷元素有白磷、红磷等单质,白磷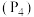 结构及晶胞如图所示,白磷和红磷转化的热化学方程式为
结构及晶胞如图所示,白磷和红磷转化的热化学方程式为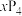 (白磷,s)
(白磷,s)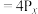 (红磷,s)
(红磷,s)  。下列说法正确的是
。下列说法正确的是

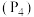 结构及晶胞如图所示,白磷和红磷转化的热化学方程式为
结构及晶胞如图所示,白磷和红磷转化的热化学方程式为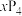 (白磷,s)
(白磷,s)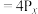 (红磷,s)
(红磷,s)  。下列说法正确的是
。下列说法正确的是
A. 属于共价晶体 属于共价晶体 |
B.白磷中的P—P—P夹角为 |
C.白磷晶胞中,P—P键的作用弱于 的分子间作用力 的分子间作用力 |
D.白磷(s)和红磷(s)在 中充分燃烧生成等量 中充分燃烧生成等量 ,白磷放出的热量更多 ,白磷放出的热量更多 |
您最近半年使用:0次
6 . 回答下列问题
(1)火箭升空需要高能的燃料,通常用肼(N2H4)作为燃料,N2O4做氧化剂。
已知:




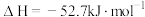
试写出气态肼在四氧化二氮气体中燃烧生成氮气和气态水的热化学方程式:
(2)t℃时,测得纯水中
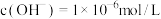 ,该温度下,0.5mol/LBa(OH)2溶液的pH=
,该温度下,0.5mol/LBa(OH)2溶液的pH=(3)CH3COONa和CH3COOH的混合溶液中
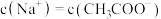 ,则该溶液呈
,则该溶液呈(4)一定温度下,向1L0.1mol·L-1CH3COOH溶液中加入0.1molCH3COONa固体,则醋酸的电离平衡向
(5)化工生产中常用FeS作沉淀剂除去工业废水中的Cu2+,其反应原理为
 。下列有关叙述正确的是
。下列有关叙述正确的是a.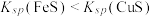
b.达到平衡时
c.该反应平衡常数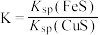
d.溶液中加入少量Na2S固体后,溶液中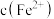 、
、 都减小
都减小
(6)科学家用氮化镓材料与铜组装成如图所示的人工光合系统实现CO2的再利用。

该电池的Cu电极上发生反应的电极方程式为
您最近半年使用:0次
7 . 请根据学过的知识回答下列问题:
(1)
 完全燃烧生成液态水时放出341.7kJ热量,则表示
完全燃烧生成液态水时放出341.7kJ热量,则表示 燃烧热的热化学方程
燃烧热的热化学方程___________ 。
(2)已知: 键的键能是
键的键能是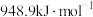 ,
, 键的键能是
键的键能是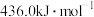 ,
, 键的键能是
键的键能是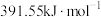 ,则
,则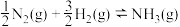

___________ 。
(3)已知:①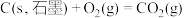

②

③

则298K时反应 的焓变:
的焓变:
___________ 。
(4)已知常温时红磷比白磷稳定,比较下列反应中 的大小:
的大小:
___________  。
。
①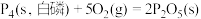

②

(5)现将一定量的稀氢氧化钠溶液、稀氢氧化钙溶液、稀氨水分别和
 的稀盐酸恰好完全反应,其反应热分别为
的稀盐酸恰好完全反应,其反应热分别为 、
、 、
、 ,则
,则 、
、 、
、 的大小关系为
的大小关系为___________ 。
(6)如图所示,某反应在不同条件下的反应历程分别为a、b。
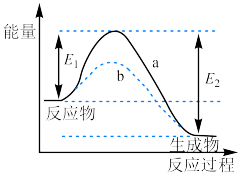
据图可判断出反应物的总键能___________ (填“>”“<”或“=”,下同)生成物的总键能,反应历程a、b的反应热___________ (填“相同”或“不相同”)。
(1)

 完全燃烧生成液态水时放出341.7kJ热量,则表示
完全燃烧生成液态水时放出341.7kJ热量,则表示 燃烧热的热化学方程
燃烧热的热化学方程(2)已知:
 键的键能是
键的键能是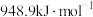 ,
, 键的键能是
键的键能是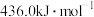 ,
, 键的键能是
键的键能是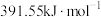 ,则
,则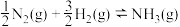

(3)已知:①
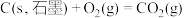

②


③


则298K时反应
 的焓变:
的焓变:
(4)已知常温时红磷比白磷稳定,比较下列反应中
 的大小:
的大小:
 。
。①
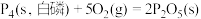

②


(5)现将一定量的稀氢氧化钠溶液、稀氢氧化钙溶液、稀氨水分别和

 的稀盐酸恰好完全反应,其反应热分别为
的稀盐酸恰好完全反应,其反应热分别为 、
、 、
、 ,则
,则 、
、 、
、 的大小关系为
的大小关系为(6)如图所示,某反应在不同条件下的反应历程分别为a、b。

据图可判断出反应物的总键能
您最近半年使用:0次
8 . 已知:已知热化学方程式:

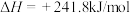
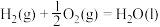
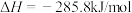
当1g液态水变为水蒸气时,其热量变化是

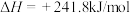
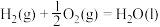
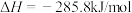
当1g液态水变为水蒸气时,其热量变化是
| A.吸热88kJ | B.吸热2.44kJ | C.放热44kJ | D.吸热44kJ |
您最近半年使用:0次
9 . 已知Fe2O2(s)+ C(s)=
C(s)=  CO2(g)+2Fe(s) △H=+234.1kJ·mol-1,C(s)+O2(g)=CO2(g) △H=-393.5kJ·mol-1,则2Fe(s)+
CO2(g)+2Fe(s) △H=+234.1kJ·mol-1,C(s)+O2(g)=CO2(g) △H=-393.5kJ·mol-1,则2Fe(s)+ O2(g)=Fe2O3(s)的△H是
O2(g)=Fe2O3(s)的△H是
 C(s)=
C(s)=  CO2(g)+2Fe(s) △H=+234.1kJ·mol-1,C(s)+O2(g)=CO2(g) △H=-393.5kJ·mol-1,则2Fe(s)+
CO2(g)+2Fe(s) △H=+234.1kJ·mol-1,C(s)+O2(g)=CO2(g) △H=-393.5kJ·mol-1,则2Fe(s)+ O2(g)=Fe2O3(s)的△H是
O2(g)=Fe2O3(s)的△H是| A.-824.4kJ·mol-1 | B.-627.6kJ·mol-1 |
| C.-744.7kJ·mol-1 | D.-169.4kJ·mol-1 |
您最近半年使用:0次
2024-03-18更新
|
289次组卷
|
2卷引用:海南省海桂中学2023-2024学年高二上学期12月教学检测(三)化学试题
名校
10 . 氢能是一种极具发展潜力的清洁能源,目前有以下制取氢气的方法:
(1)水煤气变换制氢:

已知: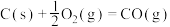
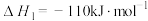

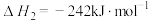


水煤气变换制氢体系中,一定时间内,CaO的添加情况与H2的体积分数关系如图。

①水煤气变换制氢反应的
_________ kJ·mol-1。
②添加CaO后H2的体积分数增大的原因是________ (用化学方程式表示)。
③纳米CaO和微米CaO相比,对应的H2体积分数更大的原因是:纳米CaO比微米CaO__________ 更大,从而与气体反应速率更快,相同时间内促进水煤气变换制氢反应正向进行的程度更大。
(2)甲醇水蒸气重整制氢: 。控制原料气
。控制原料气 ,体系中甲醇的平衡转化率与温度和压强的关系如图。
,体系中甲醇的平衡转化率与温度和压强的关系如图。
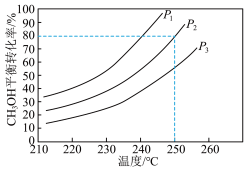
①甲醇水蒸气重整制氢反应在__________ 条件(填“高温”、“低温”或“任意温度”)下能自发进行。
②图中的压强由小到大的顺序是__________ ,理由是__________ 。
③温度为250℃、压强为 时,该反应的分压平衡常数
时,该反应的分压平衡常数
__________ (列出计算式,分压=总压×物质的量分数)。
(1)水煤气变换制氢:


已知:
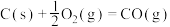
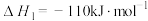

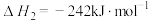


水煤气变换制氢体系中,一定时间内,CaO的添加情况与H2的体积分数关系如图。

①水煤气变换制氢反应的

②添加CaO后H2的体积分数增大的原因是
③纳米CaO和微米CaO相比,对应的H2体积分数更大的原因是:纳米CaO比微米CaO
(2)甲醇水蒸气重整制氢:
 。控制原料气
。控制原料气 ,体系中甲醇的平衡转化率与温度和压强的关系如图。
,体系中甲醇的平衡转化率与温度和压强的关系如图。
①甲醇水蒸气重整制氢反应在
②图中的压强由小到大的顺序是
③温度为250℃、压强为
 时,该反应的分压平衡常数
时,该反应的分压平衡常数
您最近半年使用:0次



