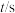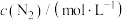解题方法
1 . 甲醇是重要的化工原料。回答下列问题:
(1)以Na2CO3固体为催化剂,甲醇脱氢可制得甲醛。反应机理如下:
(i)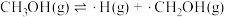 ;
;
(ii)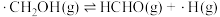 ;
;
(iii)
①(i)中反应物的总能量___________ (填“>”“=”或“<”)生成物的总能量。
②某温度时反应(i)、(ii)、(iii)的平衡常数依次为K1、K2、K3,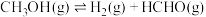 的平衡常数为K,则K=
的平衡常数为K,则K=___________ (用含K1、K2、K3的代数式表示)。
(2)向体积为1L恒容反应器中加入2mlCH3OH及适量催化剂,发生反应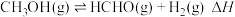 ,在T1、T2(T1<T2)时,CH3OH转化率与时间关系如图所示。
,在T1、T2(T1<T2)时,CH3OH转化率与时间关系如图所示。
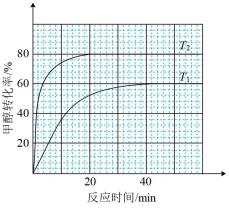
①T2温度下,20min时甲醇的体积分数为___________ %(保留三位有效数字),前20min平均反应速率v(HCHO)=___________  。
。
②T1温度下该反应的平衡常数Kp=___________ kPa(用平衡分压代替平衡浓度计算,分压=总压 物质的量分数,反应器内的初始压强为1
物质的量分数,反应器内的初始压强为1 103kPa)。
103kPa)。
(3)固体氧化物甲醇燃料电池是能效高、环境友好地转化成电能的全固态电源,工作原理如图所示。
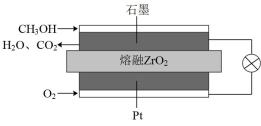
①石墨极上的反应式为___________ 。
②若通过用电器的电子的物质的量为1.2mol,则消耗标准状况下O2的体积为___________ L。
(1)以Na2CO3固体为催化剂,甲醇脱氢可制得甲醛。反应机理如下:
(i)
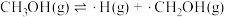 ;
;(ii)
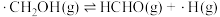 ;
;(iii)

①(i)中反应物的总能量
②某温度时反应(i)、(ii)、(iii)的平衡常数依次为K1、K2、K3,
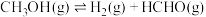 的平衡常数为K,则K=
的平衡常数为K,则K=(2)向体积为1L恒容反应器中加入2mlCH3OH及适量催化剂,发生反应
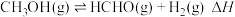 ,在T1、T2(T1<T2)时,CH3OH转化率与时间关系如图所示。
,在T1、T2(T1<T2)时,CH3OH转化率与时间关系如图所示。
①T2温度下,20min时甲醇的体积分数为
 。
。②T1温度下该反应的平衡常数Kp=
 物质的量分数,反应器内的初始压强为1
物质的量分数,反应器内的初始压强为1 103kPa)。
103kPa)。(3)固体氧化物甲醇燃料电池是能效高、环境友好地转化成电能的全固态电源,工作原理如图所示。

①石墨极上的反应式为
②若通过用电器的电子的物质的量为1.2mol,则消耗标准状况下O2的体积为
您最近一年使用:0次
2 . 研究氮氧化物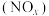 还原处理方法是环保领域的主要方向之一。上海复兴路的“生态马路”运用了“光触媒”技术,即在路面上涂了一层光催化剂涂料,可将汽车尾气中部分NO和
还原处理方法是环保领域的主要方向之一。上海复兴路的“生态马路”运用了“光触媒”技术,即在路面上涂了一层光催化剂涂料,可将汽车尾气中部分NO和 转化为
转化为 和
和 。
。
(1)在密闭容器中发生该反应,氮气浓度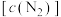 随温度
随温度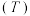 、时间
、时间 的变化关系如下表。
的变化关系如下表。
据此判断:
①
___________  (填“>”或“<”)。
(填“>”或“<”)。
② 时,
时, 内的
内的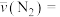
___________  。
。
(2)在绝热、恒容的密闭体系中充入一定量的 和
和 气体,反应达到平衡的标志是_______。
气体,反应达到平衡的标志是_______。
(3)计算机模拟 还原
还原 的反应经历以下3个步骤:
的反应经历以下3个步骤:
I: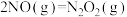
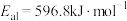
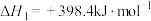
II:
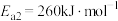
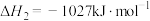
III :
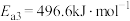
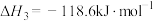
①反应过程的决速步骤是___________ (填“I”“II”或“III”)。
②总反应的热化学方程式为___________ 。
(4)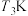 时,在刚性密闭容器中充入物质的量之比为
时,在刚性密闭容器中充入物质的量之比为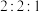 的
的 、
、 和
和 的混合气体,起始气体总压强为
的混合气体,起始气体总压强为 ,达到平衡时气体总压强为
,达到平衡时气体总压强为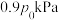 。实验测得:
。实验测得: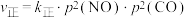 ,
,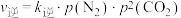 ,其中
,其中 、
、 分别为正、逆反应速率常数,只与温度有关;p为气体分压(分压=总压×物质的量分数)。
分别为正、逆反应速率常数,只与温度有关;p为气体分压(分压=总压×物质的量分数)。
①平衡后升高温度, 增大的倍数比
增大的倍数比 的
的___________ (填“大”或“小”)。
② 的平衡转化率为
的平衡转化率为___________ 。
③
___________ (用含 的代数式表示)。
的代数式表示)。
(5)该反应的某种催化剂的催化效率与NO的消耗速率随温度的变化关系如图所示。300~350℃之间,NO的消耗速率加快的原因是___________ 。

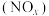 还原处理方法是环保领域的主要方向之一。上海复兴路的“生态马路”运用了“光触媒”技术,即在路面上涂了一层光催化剂涂料,可将汽车尾气中部分NO和
还原处理方法是环保领域的主要方向之一。上海复兴路的“生态马路”运用了“光触媒”技术,即在路面上涂了一层光催化剂涂料,可将汽车尾气中部分NO和 转化为
转化为 和
和 。
。(1)在密闭容器中发生该反应,氮气浓度
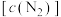 随温度
随温度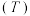 、时间
、时间 的变化关系如下表。
的变化关系如下表。
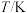 | 0 | 2 | 4 | 6 | 8 | 10 | 12 |
 | 0 | 0.10 | 0.18 | 0.25 | 0.25 | 0.25 | 0.25 |
 | 0 | 0.08 | 0.15 | 0.21 | 0.26 | 0.29 | 0.29 |
①

 (填“>”或“<”)。
(填“>”或“<”)。②
 时,
时, 内的
内的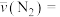
 。
。(2)在绝热、恒容的密闭体系中充入一定量的
 和
和 气体,反应达到平衡的标志是_______。
气体,反应达到平衡的标志是_______。| A.体系温度不变 | B. |
C. 的体积分数不变 的体积分数不变 | D. |
 还原
还原 的反应经历以下3个步骤:
的反应经历以下3个步骤:I:
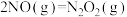
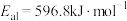
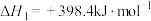
II:

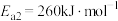
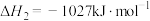
III :

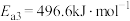
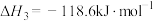
①反应过程的决速步骤是
②总反应的热化学方程式为
(4)
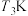 时,在刚性密闭容器中充入物质的量之比为
时,在刚性密闭容器中充入物质的量之比为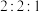 的
的 、
、 和
和 的混合气体,起始气体总压强为
的混合气体,起始气体总压强为 ,达到平衡时气体总压强为
,达到平衡时气体总压强为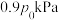 。实验测得:
。实验测得: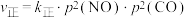 ,
,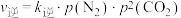 ,其中
,其中 、
、 分别为正、逆反应速率常数,只与温度有关;p为气体分压(分压=总压×物质的量分数)。
分别为正、逆反应速率常数,只与温度有关;p为气体分压(分压=总压×物质的量分数)。①平衡后升高温度,
 增大的倍数比
增大的倍数比 的
的②
 的平衡转化率为
的平衡转化率为③

 的代数式表示)。
的代数式表示)。(5)该反应的某种催化剂的催化效率与NO的消耗速率随温度的变化关系如图所示。300~350℃之间,NO的消耗速率加快的原因是

您最近一年使用:0次
3 . 已知:C(s)+H2O(g)=CO(g)+H2(g) ΔH=a kJ·mol-1
2C(s)+O2(g)=2CO(g) ΔH=-220 kJ·mol-1
H-H、O=O和O-H的键能分别为436 kJ·mol-1、496 kJ·mol-1和462 kJ·mol-1,则a为
2C(s)+O2(g)=2CO(g) ΔH=-220 kJ·mol-1
H-H、O=O和O-H的键能分别为436 kJ·mol-1、496 kJ·mol-1和462 kJ·mol-1,则a为
| A.-332 | B.-118 | C.+350 | D.+130 |
您最近一年使用:0次
2022-10-12更新
|
2118次组卷
|
132卷引用:福建省厦门双十中学2017-2018学年高二下学期期中考试化学试题
福建省厦门双十中学2017-2018学年高二下学期期中考试化学试题福建省福清西山学校高中部2020-2021学年高二上学期期中考试化学试题(已下线)2015届河南省实验中学高二上学期期中考试化学试卷(已下线)2014秋河北省唐山一中高二上学期期中化学试卷2015届福建省养正中学高三上学期第二次月考化学试卷2014-2015学年河北省正定中学高二下第三次月考化学试卷2015-2016学年河南洛阳高级中学高二上9月月考化学试卷2015-2016学年湖南常德市第一中学高二12月月考化学卷2015-2016学年广西钦州市钦南区高二上学期期中测试化学试卷2015-2016学年湖北荆州中学高二上期中测试化学试卷2015-2016学年浙江省湖州中学高二上学期期中化学试卷2015-2016学年湖北省宜昌金东方高级中学高二上学期期末化学试卷2016-2017学年河北冀州市中学高二上开学调研化学卷2016-2017学年河南郑州外国语学校高二上开学考试化学2016-2017学年陕西省西安中学高二上10月月考化学试卷2016-2017学年山东省枣庄二中高二第二次月考化学试卷2016-2017学年广东省湛江一中高二上第一次大考化学卷2016-2017学年河南省漯河中学高二上第一次月考化学卷2016-2017学年安徽师大附中高二上10月月考化学卷2016-2017学年安徽省宣城市郎溪中学等四校高二上期中化学卷2016-2017学年四川省达州市年高二上学期期末检测化学试卷河南省林州市第一中学2017-2018学年高二上学期开学考试化学试题河北省大名县第一中学2017-2018学年高二上学期第一次月考化学试题河北省邯郸市成安县第一中学2017-2018学年高二9月月考化学试题甘肃省兰州第一中学2017-2018学年高二上学期第一次月考(9月)化学试题安徽省铜陵市第一中学2017-2018学年高二10月月考化学试题黑龙江省饶河县高级中学2017-2018学年高二上学期第一次月考化学试题内蒙古巴彦淖尔市第一中学2017-2018学年高二9月月考化学试题A内蒙古巴彦淖尔市第一中学2017-2018学年高二9月月考化学试题B浙江省温州中学2017-2018学年高二上学期期中考试化学试题安徽省淮北市第一中学2017--2018学年度第一学期期中考试高二年级化学试题(已下线)黄金30题系列 高二化学(选修4) 小题好拿分【提升版】湖北省监利县实验高中2017-2018学年高二上学期期中考试化学试题山西省大同市第一中学2017-2018学年高二上学期期末考试化学试题【全国校级联考】内蒙古赤峰市重点高中(赤峰二中,平煤高级中学等)2017-2018学年高二下学期期末联考(A)化学试题甘肃省岷县二中2018-2019学年高二上学期第一次月考化学试题【全国百强校】湖北省武汉市华中师范大学第一附属中学2018-2019学年高二上学期期中检测化学试题河北省唐山市玉田县2018-2019学年高二上学期期中考试化学试题新疆维吾尔自治区昌吉市第九中学2018-2019学年高二上学期期末考试化学试题甘肃省天水市第一中学2017-2018学年高二暑假作业检测考试化学试题安徽省怀宁中学2019-2020学年高二上学期开学考试化学试题甘肃省兰州市第一中学2019-2020学年高二9月月考化学试题河北省唐山一中2019-2020学年高二上学期10月月考化学试题安徽省青阳县第一中学2019-2020学年高二10月月考化学试题宁夏吴忠中学2019-2020学年高二上学期期中考试化学试题湖南省益阳市第六中学2019-2020学年高二上学期期中考试化学试题四川省绵阳市南山中学实验学校2019-2020学年高二12月月考化学试题四川省蓬溪县蓬南中学2019-2020学年高二上学期第四次月考化学试题宁夏海原县第一中学2019-2020学年高二上学期期末考试化学试题江西省南昌市八一中学、洪都中学等六校2019-2020学年高二上学期期末联考化学试题广东省深圳实验学校2019-2020学年高二上学期期末考试化学试题云南省楚雄市实验中学2018—2019学年高二上学期11月月考化学试题广西壮族自治区贺州市桂梧高中2019-2020学年高二上学期第一次月考化学试题广东省湛江市第二十一中学2019-2020学年高二上学期期中考试化学试题(已下线)1.1.3 反应焓变的计算 练习——【高中新教材同步备课】鲁科版高中化学选择性必修1江苏省启东中学2020-2021学年高二上学期期初考试化学试题(已下线)1.3.2 反应热的计算(重点练)-2020-2021学年高二化学上学期十分钟同步课堂专练(人教版选修4)江苏省泰州中学2020-2021学年高二上学期期初检测化学试题(已下线)第01章 化学反应的热效应(B卷能力提高篇)-2020-2021学年高二化学选择性必修1同步单元AB卷(新教材人教版)(已下线)第一章 化学反应的热效应(基础过关)-2020-2021学年高二化学单元测试定心卷(人教版2019选择性必修一)(已下线)第01章 化学反应与能量转化(B卷能力提升篇)-2020-2021学年高二化学选择性必修1同步单元AB卷(新教材鲁科版)江苏省徐州市2020-2021学年高二上学期期初检测化学试题河北省邢台市第七中学2019-2020学年高二上学期10月月考化学试题安徽省安庆市宜秀区白泽湖中学2020-2021学年高二上学期第一次月考化学试题河南省安阳市第一中学2020-2021学年高二上学期第一次阶段考试化学试题辽宁省盘锦市第二高级中学2020-2021学年高二上学期第一次阶段性考试化学试题山东省济宁市曲阜市第一中学2020-2021学年高二上学期阶段性检测(9月月考)化学试题宁夏回族自治区海原县第一中学2020-2021学年高二上学期第一次月考化学试题内蒙古自治区通辽市科左后旗甘旗卡第二高级中学2020-2021学年高二上学期期中考试化学试题山东省德州市第一中学2020-2021学年高二上学期期中检测化学试题宁夏银川一中2020-2021学年高二上学期期末考试化学试题黑龙江省龙东南六校2020-2021学年高二上学期期末联考化学试题黑龙江省七台河市勃利县高级中学2020-2021学年高二3月月考化学试题(已下线)【镇江新东方】高二上第二次月考新疆乌鲁木齐市第八中学2018-2019学年高二上学期期中考试化学试题甘肃省民勤县第一中学2021-2022学年高二上学期第一次月考化学试题安徽省合肥市第六中学2021-2022学年高二上学期月考化学试题青海省西宁市北外附属新华联国际学校2021-2022学年高二上学期第一次月考化学(理)试题甘肃省庆阳市第六中学2021-2022学年高二上学期第一次月考化学(理)试题山西省乡宁县第一中学2021-2022高二上学期第一次月考化学试题新疆昌吉州2021-2022学年高二上学期期末考试化学试题江西省新余市2021-2022学年高二上学期期末检测化学试题安徽省亳州市第一中学2021-2022学年高二上学期第二次月考化学试题广西桂林市第十八中学2021-2022学年高二下学期开学考试化学试题新疆石河子第二中学2021-2022学年高二上学期第二次月考化学试题山东省济南市莱芜第四中学2021-2022学年高二上学期第一次质量检测化学试题 黑龙江省密山市牡丹江管理局高级中学2021-2022学年高二上学期期末考试化学试题北京市顺义区第一中学2022-2023学年高二上学期10月月考化学试题湖北省黄州中学2022--2023学年高二上学期10月月考化学试题湖北省武汉市东湖中学2022-2023学年高二上学期期中考试化学试题浙江省浙江大学附属中学(玉泉校区)2022-2023学年高二上学期期中考试 高二化学试卷(已下线)【2022】【高二化学】【期中考】-180(已下线)【知识图鉴】单元讲练测选择性必修1第1单元03巩固练第二节 反应热的计算河北省新乐市第一中学2022-2023学年高二上学期11月期中考试化学试题江西省永修县第一中学2023-2024学年高二上学期10月月考化学试题陕西省渭南市瑞泉中学2023-2024学年高二上学期第一次质量检测化学试题江苏省无锡市市北高级中学2023-2024学年高二下学期6月月考化学试题2014年全国普通高等学校招生统一考试理科综合能力测试化学(重庆卷)2015届河北省衡水冀州中学高三12月月考化学试卷2014-2015辽宁省沈阳二中高一下学期4月月考化学试卷2016届西藏日喀则地区一中高三10月月考理综化学试卷重庆市第十八中学2016-2017学年高一下学期期中考试化学试题天津市南开区2017届高三基础训练化学试题2018版化学(苏教版)高考总复习专题六课时跟踪训练--化学反应的热效应河北省衡水市安平中学2018届高三上学期期中考试化学试题宁夏长庆高级中学2018届高三第四次月考理综化学试卷辽宁省实验中学2017-2018学年高一下学期期中考试理科化学试题【全国百强校】黑龙江省牡丹江市第一高级中学2019届高三上学期10月月考化学试题【市级联考】内蒙古鄂尔多斯市2019届高三上学期期中考试化学试题河北省衡水市安平县安平中学2019届高三上学期期中考试化学试题(已下线)2019高考备考二轮复习精品资料-专题8 化学反应中与能量变化(教学案)浙江省东阳中学2018-2019学年高一下学期期中考试化学试题甘肃省酒泉市敦煌中学2020届高三上学期第二次调研考试化学试题【懂做原理题】2020届高三化学选修4二轮专题练——盖斯定律的应用【选择提升24题】2020届高三化学选修4二轮专题练——盖斯定律的应用【选择精编25题】河南省平顶山市鲁山县第一高级中学2019-2020高一下学期5月考试化学试题黑龙江省大庆市第四中学2020届高三下学期4月月考理综化学试题广东省广州大学附属中学2019-2020学年高一下学期期末考试化学试题吉林省长春实验中学2019-2020学年高一6月月考化学试题广东省广州大学附属中学等三校2019~2020学年高一下学期期末联考化学试题黑龙江省双鸭山市第一中学2021届高三上学期第一次月考化学试题黑龙江省哈尔滨市南岗区哈尔滨师范大学附属中学2021届高三上学期期中考试化学试题黑龙江省大庆市铁人中学2020-2021学年高一下学期期末考试化学试题黑龙江省哈尔滨师范大学附属中学2020-2021学年高一下学期期末考试化学(理)试题(已下线)课时29 盖斯定律及反应热计算-2022年高考化学一轮复习小题多维练(全国通用)黑龙江省海林市朝鲜族中学2020届高三上学期第二次月考化学试题浙江省绍兴市诸暨中学2021-2022学年高一上学期期中考试(实验班)化学试题浙江省宁波市九校2021-2022学年高一下学期6月联考化学试题湖北省黄冈市麻城第二中学2021-2022学年高一下学期4月月考化学试题安徽省安庆二中2022-2023学年高一下学期5月月考化学试题山东省鄄城县第一中学2022-2023学年高一下学期3月月考化学试题
4 .  是一种重要的化工原料,被广泛应用在工农业生产中。已知反应:
是一种重要的化工原料,被广泛应用在工农业生产中。已知反应:
I.
Ⅱ.
Ⅲ.
(1)请写出甲烷裂解制取炭黑和氢气的热化学方程式_______ 。
(2)根据反应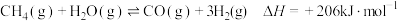 ,回答下列问题:
,回答下列问题:
①800 时,平衡常数
时,平衡常数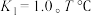 测得密闭容器中各物质达到平衡时物质的量浓度分别为:
测得密闭容器中各物质达到平衡时物质的量浓度分别为: ,则T℃
,则T℃_______ 800℃(填“>”、“<”或“ ”)。
”)。
②一定条件下,将 与
与 按物质的量之比
按物质的量之比 ∶
∶ 置于恒容密闭容器中反应,下列能说明该反应达到平衡状态的是
置于恒容密闭容器中反应,下列能说明该反应达到平衡状态的是_______ 。
A.体系中混合气体密度不变
B. 与
与 的转化率相等
的转化率相等
C.反应体系压强不再改变
D. 与
与 物质的量之比不再改变
物质的量之比不再改变
E.混合气体的平均相对分子质量不变
(3)以甲烷为燃料的新型电池得到广泛应用。如图是甲烷燃料电池工作原理的示意图。
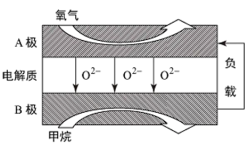
①B极上的电极反应式为_______ 。
②以该燃料电池作电源,用石墨作电极电解CuSO4溶液,当阳极收集到112L(标准状况)气体时,消耗甲烷的体积为_______ L(标准状况)。
 是一种重要的化工原料,被广泛应用在工农业生产中。已知反应:
是一种重要的化工原料,被广泛应用在工农业生产中。已知反应:I.

Ⅱ.

Ⅲ.

(1)请写出甲烷裂解制取炭黑和氢气的热化学方程式
(2)根据反应
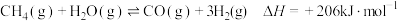 ,回答下列问题:
,回答下列问题:①800
 时,平衡常数
时,平衡常数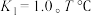 测得密闭容器中各物质达到平衡时物质的量浓度分别为:
测得密闭容器中各物质达到平衡时物质的量浓度分别为: ,则T℃
,则T℃ ”)。
”)。②一定条件下,将
 与
与 按物质的量之比
按物质的量之比 ∶
∶ 置于恒容密闭容器中反应,下列能说明该反应达到平衡状态的是
置于恒容密闭容器中反应,下列能说明该反应达到平衡状态的是A.体系中混合气体密度不变
B.
 与
与 的转化率相等
的转化率相等C.反应体系压强不再改变
D.
 与
与 物质的量之比不再改变
物质的量之比不再改变E.混合气体的平均相对分子质量不变
(3)以甲烷为燃料的新型电池得到广泛应用。如图是甲烷燃料电池工作原理的示意图。

①B极上的电极反应式为
②以该燃料电池作电源,用石墨作电极电解CuSO4溶液,当阳极收集到112L(标准状况)气体时,消耗甲烷的体积为
您最近一年使用:0次
名校
5 . 氮及其化合物在科研及生产中均有者重要的应用。根据学知识回答下列问题:
(1)氨气与氧气在一定压强和800℃条件下发生催化氧化反应时,可发生不同反应,
反应i:4NH3(g)+5O2(g) 4NO(g)+6H2O(g) △H=-905kJ·mol-1 产率98%
4NO(g)+6H2O(g) △H=-905kJ·mol-1 产率98%
反应ii:4NH3(g)+3O2(g) 2N2(g)+6H2O(g) △H=-1268kJ·mol-1产率2%
2N2(g)+6H2O(g) △H=-1268kJ·mol-1产率2%
①该条件下氮气被氧气氧化为NO的热化学方程式为_______ 。
②在一定压强和800℃条件下发生催化氧化反应时,反应i的产率大于反应ii产率的原因可能是催化剂对反应i的_______ 比反应ii大。
③反应i与反应ii有关物质产率与温度的关系如图。下列说法正确的是_______ (填序号)。
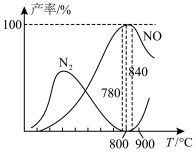
A.氨催化氧化生成NO时,温度应控制在780~840℃之间
B.提高物料比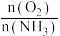 的值,主要目的的是提高反应速率
的值,主要目的的是提高反应速率
C.对反应加压可提高反应物转化率
D.高于900℃时NO的产率降低的原因可能与高温下催化剂的活性降低有关
(2)某科研小组向一密闭容器中通入4molN2、2molO2(g),控制适当条件使其发生如下反应:2N2(g)+O2(g) 2N2O(g) △H>0,测出O2的某种平衡物理量X(体积百分数或转化率)随着温度、压强变化而变化的情况如图所示。
2N2O(g) △H>0,测出O2的某种平衡物理量X(体积百分数或转化率)随着温度、压强变化而变化的情况如图所示。
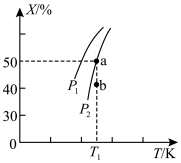
X_______ (填“能”或“不能”)表示平衡体系中O2的体积百分数;b点浓度商Qc与对应温度下的K比较:Qc_______ K(填“>”“=”或“<”)。
(3)为了研究反应的热效应,我国的科研人员计算了在一定范围内下列反应的平衡常数Kp。
i.N2H4(1) N2(g)+2H2(g) △H0 Kp0
N2(g)+2H2(g) △H0 Kp0
ii.N2H4(1)
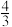 NH3(g)+
NH3(g)+ N2(g) △H1 Kp1
N2(g) △H1 Kp1
iii.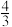 NH3(g)
NH3(g) 
 N2(g)+2H2(g) △H2Kp2
N2(g)+2H2(g) △H2Kp2
①t℃时,在恒容容器中,加入足量N2H4(1)发生反应i和ii。平衡时,测得容器内压强为22kPa,p(H2)=p(NH3),反应i的平衡常数Kp0=_______ kPa3。
②若①中反应平衡后,保持温度不变,将反应容器容积扩大2倍,反应再次平衡后,c(N2)相比原平衡时_______ (填“增大”“减小”或“不变”)。
③1gKp1-T和lgKp2-T的线性关系图如下图所示,据此分析:
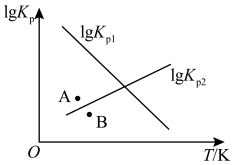
△H0_______ (填“大于”或“小于”)0;对于反应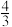 NH3(g)
NH3(g) 
 N2(g)+2H2(g),图中v正(A)
N2(g)+2H2(g),图中v正(A)_______ v正(B)(填“大于”“小于”或“等于”)。
(1)氨气与氧气在一定压强和800℃条件下发生催化氧化反应时,可发生不同反应,
反应i:4NH3(g)+5O2(g)
 4NO(g)+6H2O(g) △H=-905kJ·mol-1 产率98%
4NO(g)+6H2O(g) △H=-905kJ·mol-1 产率98%反应ii:4NH3(g)+3O2(g)
 2N2(g)+6H2O(g) △H=-1268kJ·mol-1产率2%
2N2(g)+6H2O(g) △H=-1268kJ·mol-1产率2%①该条件下氮气被氧气氧化为NO的热化学方程式为
②在一定压强和800℃条件下发生催化氧化反应时,反应i的产率大于反应ii产率的原因可能是催化剂对反应i的
③反应i与反应ii有关物质产率与温度的关系如图。下列说法正确的是

A.氨催化氧化生成NO时,温度应控制在780~840℃之间
B.提高物料比
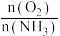 的值,主要目的的是提高反应速率
的值,主要目的的是提高反应速率C.对反应加压可提高反应物转化率
D.高于900℃时NO的产率降低的原因可能与高温下催化剂的活性降低有关
(2)某科研小组向一密闭容器中通入4molN2、2molO2(g),控制适当条件使其发生如下反应:2N2(g)+O2(g)
 2N2O(g) △H>0,测出O2的某种平衡物理量X(体积百分数或转化率)随着温度、压强变化而变化的情况如图所示。
2N2O(g) △H>0,测出O2的某种平衡物理量X(体积百分数或转化率)随着温度、压强变化而变化的情况如图所示。
X
(3)为了研究反应的热效应,我国的科研人员计算了在一定范围内下列反应的平衡常数Kp。
i.N2H4(1)
 N2(g)+2H2(g) △H0 Kp0
N2(g)+2H2(g) △H0 Kp0ii.N2H4(1)

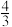 NH3(g)+
NH3(g)+ N2(g) △H1 Kp1
N2(g) △H1 Kp1iii.
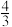 NH3(g)
NH3(g) 
 N2(g)+2H2(g) △H2Kp2
N2(g)+2H2(g) △H2Kp2①t℃时,在恒容容器中,加入足量N2H4(1)发生反应i和ii。平衡时,测得容器内压强为22kPa,p(H2)=p(NH3),反应i的平衡常数Kp0=
②若①中反应平衡后,保持温度不变,将反应容器容积扩大2倍,反应再次平衡后,c(N2)相比原平衡时
③1gKp1-T和lgKp2-T的线性关系图如下图所示,据此分析:

△H0
 NH3(g)
NH3(g) 
 N2(g)+2H2(g),图中v正(A)
N2(g)+2H2(g),图中v正(A)
您最近一年使用:0次
2022-06-02更新
|
642次组卷
|
2卷引用:福建省质优生“筑梦”联考2022-2023学年高二下学期化学试题
名校
解题方法
6 . 低碳烷烃脱氢制低碳烯烃对有效利用化石能源有重要意义。
(1)乙烷脱氢制乙烯
主反应:C2H6(g) C2H4(g)+H2(g) △H1
C2H4(g)+H2(g) △H1
副反应:2C2H6(g) C2H4(g)+2CH4(g) △H2
C2H4(g)+2CH4(g) △H2
C2H6(g) 2C(s)+3H2(g) △H3
2C(s)+3H2(g) △H3
①标准摩尔生成焓是指在25℃和101kPa,由最稳定的单质生成1mol化合物的焓变。利用表中数据计算△H1___ 。
②一定条件下,有利于提高C2H6平衡转化率的措施是___ (填标号)。
A.高温 B.高压 C.原料气中掺入H2 D.保持恒压,加稀有气体
③在800℃、恒容条件下,2L密闭容器中,1molC2H6进行脱氢反应,测得平衡体系气体有0.3molC2H6、0.6molC2H4、0.1molCH4和xmolH2,则x=___ ,主反应K=___ mol•L-1。
(2)使用PtSn—Mg(2—Zn)Al进行乙烷脱氢催化性能研究。不同温度下,乙烷转化率及乙烯选择性随反应时间的变化曲线分别如图a、图b。

催化剂的最佳工作温度为___ 。
(1)乙烷脱氢制乙烯
主反应:C2H6(g)
 C2H4(g)+H2(g) △H1
C2H4(g)+H2(g) △H1副反应:2C2H6(g)
 C2H4(g)+2CH4(g) △H2
C2H4(g)+2CH4(g) △H2C2H6(g)
 2C(s)+3H2(g) △H3
2C(s)+3H2(g) △H3①标准摩尔生成焓是指在25℃和101kPa,由最稳定的单质生成1mol化合物的焓变。利用表中数据计算△H1
| 物质 | C2H6(g) | C2H4(g) | CH4(g) | H2(g) |
| 标准摩尔生成焓/kJ•mol-1 | -84.7 | +52.3 | -74.8 | 0 |
A.高温 B.高压 C.原料气中掺入H2 D.保持恒压,加稀有气体
③在800℃、恒容条件下,2L密闭容器中,1molC2H6进行脱氢反应,测得平衡体系气体有0.3molC2H6、0.6molC2H4、0.1molCH4和xmolH2,则x=
(2)使用PtSn—Mg(2—Zn)Al进行乙烷脱氢催化性能研究。不同温度下,乙烷转化率及乙烯选择性随反应时间的变化曲线分别如图a、图b。

催化剂的最佳工作温度为
您最近一年使用:0次
7 . 化学链燃烧(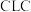 )是利用载氧体将空气中的氧传输至燃料的新技术,与传统燃烧方式相比,避免了空气和燃料的直接接触,有利于高效捕集
)是利用载氧体将空气中的氧传输至燃料的新技术,与传统燃烧方式相比,避免了空气和燃料的直接接触,有利于高效捕集 。基于
。基于 载氧体的甲烷化学链燃烧技术示意图如下。
载氧体的甲烷化学链燃烧技术示意图如下。
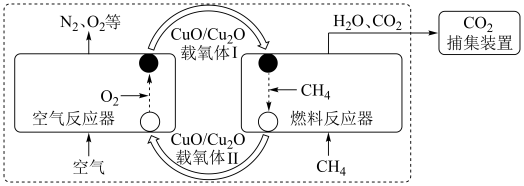
空气反应器与燃料反应器中发生的反应分别为:
①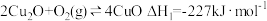
②
(1)反应

_______  。
。
(2)反应②的平衡常数表达式
_______ 。
(3)氧的质量分数:载氧体Ⅰ_______ (填“>”“=”或“<”)载氧体Ⅱ。
(4)往盛有 载氧体的刚性密闭容器中充入空气【氧气的物质的量分数
载氧体的刚性密闭容器中充入空气【氧气的物质的量分数 为21%】,发生反应①。平衡时
为21%】,发生反应①。平衡时 随反应温度T变化的曲线如图所示。
随反应温度T变化的曲线如图所示。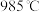 时
时 的平衡转化率
的平衡转化率
_______ (保留2位有效数字)。
(5)根据下图, 随温度升高而增大的原因是
随温度升高而增大的原因是_______ 。反应温度必须控制在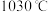 以下,原因是
以下,原因是_______ 。

(6)载氧体掺杂改性,可加快化学链燃烧速率。使用不同掺杂的 载氧体,反应②活化能如下表所示。
载氧体,反应②活化能如下表所示。
由表中数据判断:使用_______ (填“氧化铝”或“膨润土”)掺杂的载氧体反应较快;使用氧化铝或者膨润土掺杂的载氧体,单位时间内燃料反应器释放的热量分别为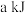 、
、 ,则a
,则a_______ b(填“>”“=”或“<”)。
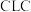 )是利用载氧体将空气中的氧传输至燃料的新技术,与传统燃烧方式相比,避免了空气和燃料的直接接触,有利于高效捕集
)是利用载氧体将空气中的氧传输至燃料的新技术,与传统燃烧方式相比,避免了空气和燃料的直接接触,有利于高效捕集 。基于
。基于 载氧体的甲烷化学链燃烧技术示意图如下。
载氧体的甲烷化学链燃烧技术示意图如下。
空气反应器与燃料反应器中发生的反应分别为:
①
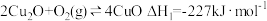
②

(1)反应


 。
。(2)反应②的平衡常数表达式

(3)氧的质量分数:载氧体Ⅰ
(4)往盛有
 载氧体的刚性密闭容器中充入空气【氧气的物质的量分数
载氧体的刚性密闭容器中充入空气【氧气的物质的量分数 为21%】,发生反应①。平衡时
为21%】,发生反应①。平衡时 随反应温度T变化的曲线如图所示。
随反应温度T变化的曲线如图所示。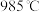 时
时 的平衡转化率
的平衡转化率
(5)根据下图,
 随温度升高而增大的原因是
随温度升高而增大的原因是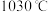 以下,原因是
以下,原因是
(6)载氧体掺杂改性,可加快化学链燃烧速率。使用不同掺杂的
 载氧体,反应②活化能如下表所示。
载氧体,反应②活化能如下表所示。| 载氧体掺杂物质 | 氧化铝 | 膨润土 |
活化能/ |  | 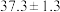 |
 、
、 ,则a
,则a
您最近一年使用:0次
2021-11-09更新
|
5667次组卷
|
7卷引用:福建省龙岩第一中学2021-2022学年高二下学期开学考试(实验班)化学试题
福建省龙岩第一中学2021-2022学年高二下学期开学考试(实验班)化学试题福建省福州市福建师范大学附属中学2022-2023学年高二下学期期末化学试题2021年新高考福建化学高考真题北京市铁路第二中学2022-2023学年高二上学期期中检测化学试题(已下线)专题15 化学反应原理综合题-三年(2020-2022)高考真题分项汇编(已下线)专题17 原理综合题(已下线)专题17 原理综合题
10-11高二·江西上饶·阶段练习
8 . 在温度、容积相同的3个密闭容器中,按不同方式投入反应物,保持恒温、恒容,测得反应达到平衡时的有关数据如下(已知N2(g)+3H2(g) 2NH3(g) ∆H=-92.4kJ/mol)
2NH3(g) ∆H=-92.4kJ/mol)
下列说法正确的是
 2NH3(g) ∆H=-92.4kJ/mol)
2NH3(g) ∆H=-92.4kJ/mol)| 容器 | 甲 | 乙 | 丙 |
| 反应物投入量 | 1 mol N2、3 mol H2 | 2 mol NH3 | 4 mol NH3 |
| NH3浓度(mol/L) | c1 | c2 | c3 |
| 反应的能量变化 | 放出a kJ | 吸收b kJ | 吸收c kJ |
| 体系压强 | p1 | p2 | p3 |
| 反应物转化率 | a1 | a2 | a3 |
| A.2c1>c3 | B.a+b=92.4 | C.2p1<p3 | D.a2+a3>1 |
您最近一年使用:0次
2021-10-20更新
|
2016次组卷
|
25卷引用:福建师范大学附属中学2021-2022学年高二上学期期中考试化学试题
福建师范大学附属中学2021-2022学年高二上学期期中考试化学试题(已下线)2011-2012学年江西省上饶县中学高二第一次月考化学试卷2015-2016学年四川省新津中学高二10月月考化学试卷2016-2017学年黑龙江省铁人中学高二上开学测化学卷湖北省沙市中学2017-2018学年高二上学期期中考试化学试题安徽省淮南市第二中学2017-2018学年高二上学期第二次月考化学试题内蒙古北京八中乌兰察布分校2017-2018学年高二下学期第二次调研考试化学试题【全国百强校】宁夏回族自治区银川市第一中学2018-2019学年高二上学期期末考试化学试题新疆乌鲁木齐市二十三中学2018-2019学年高二10月月考化学试题步步为赢 高二化学寒假作业:作业六 化学平衡中的模型构建与等效平衡云南省楚雄市楚雄实验中学2018—2019学年高二上学期9月月考化学试题鲁科版(2019)选择性必修1 第2章 化学反应的方向、限度与速率 第4节 化学反应条件的优化—工业合成氨山东省临沂市沂水一中2020-2021学年高二9月月考化学试题江西省赣州市会昌县会昌中学2020-2021学年高二上学期第一次月考化学试题河南省安阳市第一中学2020-2021学年高二上学期第一次阶段考试化学试题山西省运城市景胜中学2020-2021学年高二10月月考化学试题黑吉两省十校2020-2021学年高二上学期期中联考(吉雅2校用)化学试题天津市咸水沽第二中学2021-2022学年高二上学期第一次月考化学试题江西省吉安市峡江中学2021-2022学年高二上学期开学考试化学(理科)试题百所名校联考-选修四模块综合检测夯基提能2020届高三化学选择题对题专练——选修四化学反应原理—— 转化率与产率的相关计算2020届高三化学选修4二轮专题练——等效平衡专练【精编23题】(已下线)第23讲 化学平衡状态 化学平衡的移动 (精讲)——2021年高考化学一轮复习讲练测(已下线)第七单元 化学反应速率与化学平衡(B卷 真题滚动练)-2022年高考化学一轮复习单元滚动双测卷(新高考地区专用)浙江省宁波市镇海中学2022-2023学年高三上学期(10月)选考模拟一化学试题
9 . 当今,世界多国相继规划了碳达峰、碳中和的时间节点。因此,研发二氧化碳利用技术,降低空气中二氧化碳含量成为研究热点。
(1)大气中的二氧化碳主要来自于煤、石油及其他含碳化合物的燃烧。已知25℃时,相关物质的燃烧热数据如表:
(1)则25℃时H2(g)和C(石墨,s)生成C6H6(l)的热化学方程式为________ 。
(2)雨水中含有来自大气的CO2,溶于水中的CO2进一步和水反应,发生电离:
①CO2(g)=CO2(aq)
②CO2(aq)+H2O(l)=H+(aq)+HCO (aq)
(aq)
25℃时,反应②的平衡常数为K2。
溶液中CO2的浓度与其在空气中的分压成正比(分压=总压×物质的量分数),比例系数为ymol•L-1•kPa-1,当大气压强为pkPa,大气中CO2(g)的物质的量分数为x时,溶液中H+浓度为________ mol•L-1(写出表达式,考虑水的电离,忽略HCO 的电离)
的电离)
(3)105℃时,将足量的某碳酸氢盐(MHCO3)固体置于真空恒容容器中,存在如下平衡:2MHCO3(s)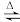 M2CO3(s)+H2O(g)+CO2(g)。上述反应达平衡时体系的总压为46kPa。
M2CO3(s)+H2O(g)+CO2(g)。上述反应达平衡时体系的总压为46kPa。
保持温度不变,开始时在体系中先通入一定量的CO2(g),再加入足量MHCO3(s),欲使平衡时体系中水蒸气的分压小于5kPa,CO2(g)的初始压强应大于________ kPa。
(4)我国科学家研究Li—CO2电池,取得了重大科研成果,回答下列问题:
①Li—CO2电池中,Li为单质锂片,则该电池中的CO2在___ (填“正”或“负”)极发生电化学反应。研究表明,该电池反应产物为碳酸锂和单质碳,且CO2电还原后与锂离子结合形成碳酸锂按以下4个步骤进行,写出步骤Ⅲ的离子方程式。
Ⅰ.2CO2+2e-=C2O Ⅱ.C2O
Ⅱ.C2O =CO2+CO
=CO2+CO
Ⅲ.__________ Ⅳ.CO +2Li+=Li2CO3
+2Li+=Li2CO3
②研究表明,在电解质水溶液中,CO2气体可被电化学还原。
Ⅰ.CO2在碱性介质中电还原为正丙醇(CH3CH2CH2OH)的电极反应方程式为_________ 。
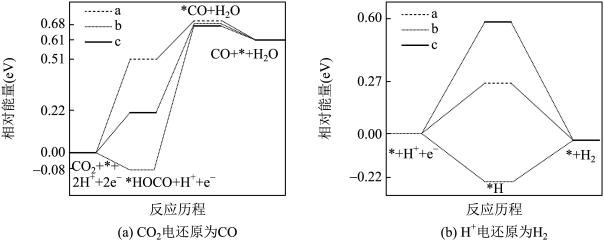
Ⅱ.在电解质水溶液中,三种不同催化剂(a、b、c)上CO2电还原为CO的反应进程中(H+被还原为H2的反应可同时发生),相对能量变化如图.由此判断,CO2电还原为CO从易到难的顺序为_______ (用a、b、c字母排序)。
(1)大气中的二氧化碳主要来自于煤、石油及其他含碳化合物的燃烧。已知25℃时,相关物质的燃烧热数据如表:
| 物质 | H2(g) | C(石墨,s) | C6H6(l) |
| 燃烧热△H(kJ•mol-1) | -285.8 | -393.5 | -3267.5 |
(2)雨水中含有来自大气的CO2,溶于水中的CO2进一步和水反应,发生电离:
①CO2(g)=CO2(aq)
②CO2(aq)+H2O(l)=H+(aq)+HCO
 (aq)
(aq)25℃时,反应②的平衡常数为K2。
溶液中CO2的浓度与其在空气中的分压成正比(分压=总压×物质的量分数),比例系数为ymol•L-1•kPa-1,当大气压强为pkPa,大气中CO2(g)的物质的量分数为x时,溶液中H+浓度为
 的电离)
的电离)(3)105℃时,将足量的某碳酸氢盐(MHCO3)固体置于真空恒容容器中,存在如下平衡:2MHCO3(s)
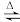 M2CO3(s)+H2O(g)+CO2(g)。上述反应达平衡时体系的总压为46kPa。
M2CO3(s)+H2O(g)+CO2(g)。上述反应达平衡时体系的总压为46kPa。保持温度不变,开始时在体系中先通入一定量的CO2(g),再加入足量MHCO3(s),欲使平衡时体系中水蒸气的分压小于5kPa,CO2(g)的初始压强应大于
(4)我国科学家研究Li—CO2电池,取得了重大科研成果,回答下列问题:
①Li—CO2电池中,Li为单质锂片,则该电池中的CO2在
Ⅰ.2CO2+2e-=C2O
 Ⅱ.C2O
Ⅱ.C2O =CO2+CO
=CO2+CO
Ⅲ.
 +2Li+=Li2CO3
+2Li+=Li2CO3②研究表明,在电解质水溶液中,CO2气体可被电化学还原。
Ⅰ.CO2在碱性介质中电还原为正丙醇(CH3CH2CH2OH)的电极反应方程式为
Ⅱ.在电解质水溶液中,三种不同催化剂(a、b、c)上CO2电还原为CO的反应进程中(H+被还原为H2的反应可同时发生),相对能量变化如图.由此判断,CO2电还原为CO从易到难的顺序为

您最近一年使用:0次
2021-06-09更新
|
10549次组卷
|
12卷引用:福建省龙岩第一中学2021-2022学年高二上学期第二次月考化学试题(实验班)
福建省龙岩第一中学2021-2022学年高二上学期第二次月考化学试题(实验班)2021年新高考河北化学高考真题(已下线)考点18 化学平衡状态 化学平衡移动-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)考点18 化学平衡状态 化学平衡移动-备战2022年高考化学一轮复习考点帮(浙江专用)2021年河北省高考化学试卷变式题10-18题(已下线)专题12 化学反应原理综合题—2022年高考化学二轮复习讲练测(全国版)-练习(已下线)回归教材重难点09 化学反应原理综合-【查漏补缺】2022年高考化学三轮冲刺过关(新高考专用)(已下线)押新高考卷17题 化学反应原理综合题-备战2022年高考化学临考题号押题(新高考通版)(已下线)专题15 化学反应原理综合题-三年(2020-2022)高考真题分项汇编(已下线)考点22 化学平衡状态与化学平衡移动-备战2023年高考化学一轮复习考点帮(全国通用)(已下线)专题17 原理综合题(已下线)专题17 原理综合题
10 . 含氮化合物和含碳化合物对环境、生产和人类生命活动有很大影响。请回答下列有关问题:
(1)用CH4将氮氧化合物还原为无毒气体,可改善汽车尾气对环境的影响。相关反应历程如图所示。
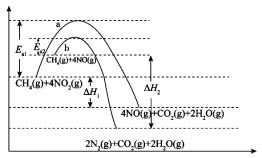
①反应a加入催化剂,可使Ea1_______ (填“增大”“减小”或“不变”);相同条件下,反应速率b比a_______ (填“快”或“慢”),原因是_______ ;反应 CH4(g) +2NO2(g) ═ N2(g) +2H2O(g)+CO2(g) ∆H ═_____ kJ·mol -1(用含∆H1、∆H2的代数式表示)。
②T℃时,向恒容密闭容器加入一定量的CH4和NO2,下列能表明反应CH4(g) +2NO2(g) N2(g) +2H2O(g) +CO2(g) 已达到平衡状态的是
N2(g) +2H2O(g) +CO2(g) 已达到平衡状态的是_______ 。
A.容器内气体颜色保持不变 B.v正(N2) = 2v逆(NO2)
C.容器内压强保持不变 D.容器内混合气体的密度保持不变
(2)反应CO(g) +2H2(g) CH3OH(g) ∆H<0是一种碳资源化处理的途径,在不同温度下,向容积为2 L的密闭容器内加入4mol的CO和8mol H2,CH3OH的物质的量随时间的变化情况如图:
CH3OH(g) ∆H<0是一种碳资源化处理的途径,在不同温度下,向容积为2 L的密闭容器内加入4mol的CO和8mol H2,CH3OH的物质的量随时间的变化情况如图:
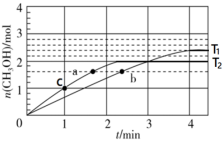
①T1_______ T2,(填“>”或“<”)。
②T1时,前3min内用H2表示的反应速率v(H2)为_______ ( 保留两位有效数字),T2时,反应的化学平衡常数K ═_______ 。
③若容器容积不变,可增加氢气平衡转化率的措施有_______ (任填一项)。
④已知:v正═k正x (CO) x2(H2) ,v逆 ═k逆x (CH3OH),k正和k逆分别为正、逆反应速率常数,x为物质的量分数,c点时v正:v逆═_______ 。
(1)用CH4将氮氧化合物还原为无毒气体,可改善汽车尾气对环境的影响。相关反应历程如图所示。

①反应a加入催化剂,可使Ea1
②T℃时,向恒容密闭容器加入一定量的CH4和NO2,下列能表明反应CH4(g) +2NO2(g)
 N2(g) +2H2O(g) +CO2(g) 已达到平衡状态的是
N2(g) +2H2O(g) +CO2(g) 已达到平衡状态的是A.容器内气体颜色保持不变 B.v正(N2) = 2v逆(NO2)
C.容器内压强保持不变 D.容器内混合气体的密度保持不变
(2)反应CO(g) +2H2(g)
 CH3OH(g) ∆H<0是一种碳资源化处理的途径,在不同温度下,向容积为2 L的密闭容器内加入4mol的CO和8mol H2,CH3OH的物质的量随时间的变化情况如图:
CH3OH(g) ∆H<0是一种碳资源化处理的途径,在不同温度下,向容积为2 L的密闭容器内加入4mol的CO和8mol H2,CH3OH的物质的量随时间的变化情况如图:
①T1
②T1时,前3min内用H2表示的反应速率v(H2)为
③若容器容积不变,可增加氢气平衡转化率的措施有
④已知:v正═k正x (CO) x2(H2) ,v逆 ═k逆x (CH3OH),k正和k逆分别为正、逆反应速率常数,x为物质的量分数,c点时v正:v逆═
您最近一年使用:0次