解题方法
1 . 工业合成尿素以NH3和CO2作为原料,在合成塔中存在如下转化:
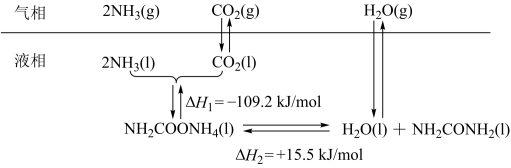
回答下列问题:
(1)液相中,合成尿素总反应的热化学方程式为: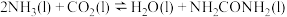 ∆H=
∆H=_______ 
(2)在不同温度下,反应中CO2的转化率与时间的关系如图1。
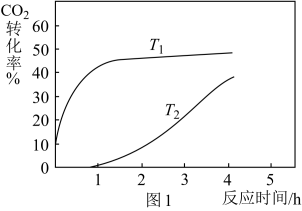
①温度T1_______ T2(填“>”、“<”或“=”),原因是_______ 。
②保持容器体积不变,在反应初期,可以提高单位时间内CO2转化率措施有_______ 。
a.增大氨气的浓度b.通入惰性气体
c.升高温度d.增大水的分压(分压=总压×物质的量分数)
(3)在液相中,CO2的平衡转化率与温度、初始氨碳比 、初始水碳比
、初始水碳比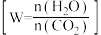 关系如图2。
关系如图2。
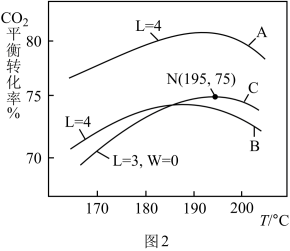
①曲线A、B,W较大的曲线是_______ (填“A”或“B”)。
②其它条件不变时,随着温度的升高,平衡转化率下降的原因是_______ 。
③对于液相反应常用某组分M达到平衡时的物质的量分数x(M)表示平衡常数(记作Kx),195℃时,则该反应中N点的平衡常数Kx=_______ 。

回答下列问题:
(1)液相中,合成尿素总反应的热化学方程式为:
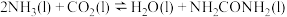 ∆H=
∆H=
(2)在不同温度下,反应中CO2的转化率与时间的关系如图1。

①温度T1
②保持容器体积不变,在反应初期,可以提高单位时间内CO2转化率措施有
a.增大氨气的浓度b.通入惰性气体
c.升高温度d.增大水的分压(分压=总压×物质的量分数)
(3)在液相中,CO2的平衡转化率与温度、初始氨碳比
 、初始水碳比
、初始水碳比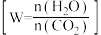 关系如图2。
关系如图2。
①曲线A、B,W较大的曲线是
②其它条件不变时,随着温度的升高,平衡转化率下降的原因是
③对于液相反应常用某组分M达到平衡时的物质的量分数x(M)表示平衡常数(记作Kx),195℃时,则该反应中N点的平衡常数Kx=
您最近一年使用:0次
2 . 合成气用途非常广泛,可以煤、天然气等为原料生产。回答下列问题:
(1)用H2O(g)和O2重整CH4制合成气的热化学方程式如下:
(水蒸气重整)CH4(g)+ H2O(g)=CO(g)+3H2(g) ∆H=+ 206 kJ·mol-1
(氧气重整)CH4(g)+0.5O2(g)=CO(g)+2H2(g) ∆H=-36 kJ·mol-1
①2H2(g)+O2(g)=2H2O(g)的∆H=_______ kJ·mol-1。
②为了保持热平衡,同时用两种方式重整,不考虑热量损失,理论上得到的合成气中n(CO): n(H2)=1 :____ (保留两位小数)。
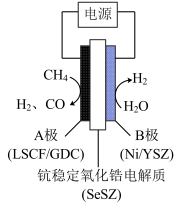
③用水蒸气电催化重整甲烷的装置如图。装置工作时,O2-向_____ (填“A”或“B’)极迁移;阳极发生的电极反应为___________ 。_____ (填“大于”“等于”或“小于”)0。
②气体的总压强:a点_____ (填“大于”“等于”或“小于”)b点,理由是_________ 。
③c点时,反应C(s) +CO2(g) 2CO(g)的Kp=
2CO(g)的Kp=_____ (填数值)。
④在恒容密闭容器中充入0. 5 mol CO、2 mol H2O(g)只发生反应(II),图中d点处达到平衡时,CO的转化率为_______ ;达到平衡时,向容器中再充入0.5 mol CO、2 mol H2O(g),重新达到平衡时,CO的平衡转化率_______ (填“增大”“减小”或“不变”)。
(1)用H2O(g)和O2重整CH4制合成气的热化学方程式如下:
(水蒸气重整)CH4(g)+ H2O(g)=CO(g)+3H2(g) ∆H=+ 206 kJ·mol-1
(氧气重整)CH4(g)+0.5O2(g)=CO(g)+2H2(g) ∆H=-36 kJ·mol-1
①2H2(g)+O2(g)=2H2O(g)的∆H=
②为了保持热平衡,同时用两种方式重整,不考虑热量损失,理论上得到的合成气中n(CO): n(H2)=1 :
③用水蒸气电催化重整甲烷的装置如图。装置工作时,O2-向

②气体的总压强:a点
③c点时,反应C(s) +CO2(g)
 2CO(g)的Kp=
2CO(g)的Kp=④在恒容密闭容器中充入0. 5 mol CO、2 mol H2O(g)只发生反应(II),图中d点处达到平衡时,CO的转化率为
您最近一年使用:0次
2020-03-27更新
|
100次组卷
|
2卷引用:福建省永安市第一中学2020届高三下学期3月模拟考试 理科综合化学
3 . 氮、磷及其化合物在生产、生活中有重要的用途。回答下列问题:
Ⅰ.(1)氮的固定是几百年来科学家一直研究的课题。
下表列举了不同温度下大气固氮和工业固氮的部分K值。
①分析数据可知:大气固氮反应属于_____ (填“吸热”或“放热”)反应。
②分析数据可知;人类不适合大规模模拟大气固氮的原因_____ 。
(2)NaNO2是一种食品添加剂(有毒性,市场上常误与食盐混淆)。可用酸性KMnO4溶液检验,完成其反应的离子方程式。MnO +NO
+NO +
+_____ =Mn2++NO +H2O。
+H2O。
(3)工业生产以NH3和CO2为原料合成尿素[CO(NH2)2],反应的化学方程式为: 2NH3(g)+CO2(g) CO(NH2)2(l)+H2O(l) △H<0。T1℃时,在2 L的密闭容器中充入NH3和CO2模拟工业生产,若原料气中的NH3和CO2的物质的量之比(氨碳比)
CO(NH2)2(l)+H2O(l) △H<0。T1℃时,在2 L的密闭容器中充入NH3和CO2模拟工业生产,若原料气中的NH3和CO2的物质的量之比(氨碳比) = x,如图是CO2平衡转化率(α)与氨碳比(x)的关系。
= x,如图是CO2平衡转化率(α)与氨碳比(x)的关系。
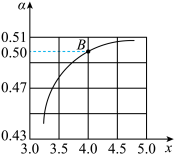
其它条件不变时,α随着x增大而增大的原因是____ ;图中的B点处NH3的平衡转化率为____ 。
II.(4)红磷P(s)和Cl2(g)发生反应生成PCl3(g)和 PCl5(g),反应过程如下。
2P(s) + 3Cl2(g)=2PCl3(g) △H1=-612 kJ· mol-1
2P(s) + 5Cl2(g)=2PCl5(g) △H2=-798 kJ· mol-1
气态PCl5生成气态PCl3和Cl2的热化学方程式为________ 。
(5)直链聚磷酸是由n个磷酸分子通过分子间脱水形成的,常用于制取阻燃剂聚磷酸铵。直链低聚磷酸铵的化学式可表示为(NH4)(n+2)PnOx,x=___ (用n表示)。
(6)一定温度下,向浓度均为0.20 mol·L-1的MgCl2和CaCl2混合溶液中逐滴加入Na3PO4,先生成__ 沉淀(填化学式);当测得溶液中钙离子沉淀完全(浓度小于10-5 mol·L-1)时,溶液中的另一种金属阳离子的物质的量浓度c = ______ mol·L-1。(已知:Ksp[Mg3(PO4)2] =6.0×10-29,Ksp[Ca3(PO4)2]=6.0×10-26。)
Ⅰ.(1)氮的固定是几百年来科学家一直研究的课题。
下表列举了不同温度下大气固氮和工业固氮的部分K值。
| 反应 | 大气固氮 N2(g)+O2(g)  2NO(g) 2NO(g) | 工业固氮 N2(g)+3H2(g)  2NH3(g) 2NH3(g) | |||
| 温度/℃ | 27 | 2000 | 25 | 400 | 450 |
| K | 3.8×10-31 | 0.1 | 5×108 | 0.507 | 0.152 |
②分析数据可知;人类不适合大规模模拟大气固氮的原因
(2)NaNO2是一种食品添加剂(有毒性,市场上常误与食盐混淆)。可用酸性KMnO4溶液检验,完成其反应的离子方程式。MnO
 +NO
+NO +
+ +H2O。
+H2O。(3)工业生产以NH3和CO2为原料合成尿素[CO(NH2)2],反应的化学方程式为: 2NH3(g)+CO2(g)
 CO(NH2)2(l)+H2O(l) △H<0。T1℃时,在2 L的密闭容器中充入NH3和CO2模拟工业生产,若原料气中的NH3和CO2的物质的量之比(氨碳比)
CO(NH2)2(l)+H2O(l) △H<0。T1℃时,在2 L的密闭容器中充入NH3和CO2模拟工业生产,若原料气中的NH3和CO2的物质的量之比(氨碳比) = x,如图是CO2平衡转化率(α)与氨碳比(x)的关系。
= x,如图是CO2平衡转化率(α)与氨碳比(x)的关系。
其它条件不变时,α随着x增大而增大的原因是
II.(4)红磷P(s)和Cl2(g)发生反应生成PCl3(g)和 PCl5(g),反应过程如下。
2P(s) + 3Cl2(g)=2PCl3(g) △H1=-612 kJ· mol-1
2P(s) + 5Cl2(g)=2PCl5(g) △H2=-798 kJ· mol-1
气态PCl5生成气态PCl3和Cl2的热化学方程式为
(5)直链聚磷酸是由n个磷酸分子通过分子间脱水形成的,常用于制取阻燃剂聚磷酸铵。直链低聚磷酸铵的化学式可表示为(NH4)(n+2)PnOx,x=
(6)一定温度下,向浓度均为0.20 mol·L-1的MgCl2和CaCl2混合溶液中逐滴加入Na3PO4,先生成
您最近一年使用:0次
解题方法
4 . “一碳化学”是指以含一个碳原子的化合物(如CO2、CO、CH4、CH3OH等)为初始反应物,合成一系列重要的化工原料和燃料的化学。
(1)以CO2和NH3为原料合成尿素是利用CO2的成功范例。在尿素合成塔中的主要反应可表示如下:
反应I:2NH3(g)+CO2(g) NH2COONH4(s) ∆H1
NH2COONH4(s) ∆H1
反应II:NH2COONH4(s) CO(NH2)2(s)+H2O(g) ∆H2=+72.49kJ/mol
CO(NH2)2(s)+H2O(g) ∆H2=+72.49kJ/mol
总反应:2NH3(g)+CO2(g) CO(NH2)2(s)+H2O(g) ∆H3=-86.98kJ/mol
CO(NH2)2(s)+H2O(g) ∆H3=-86.98kJ/mol
请回答下列问题:
①反应I的∆H1=__ kJ/mol。
②反应II一般在__ (填“高温或“低温")条件下有利于该反应的进行。
③一定温度下,在体积固定的密闭容器中按计量比投料进行反应I,下列能说明反应达到了平衡状态的是__ (填字母序号)。
A.混合气体的平均相对分子质量不再变化
B.容器内气体总压强不再变化
C.2v正(NH3)=v逆(CO2)
D.容器内混合气体的密度不再变化
(2)将CO2和H2按物质的量之比为1:3充入一定体积的密闭容器中,发生反应:CO2(g)+3H2(g)=CH3OH(g)+H2O(g) ∆H。测得CH3OH的物质的量在不同温度下随时间的变化关系如图所示。

①根据图示判断∆H__ 0(填“>”或“<”)。
②一定温度下,在容积均为2L的两个密闭容器中,按如下方式加入反应物,10min后达到平衡。
若甲容器平衡后气体的压强为开始时的0.8倍,则反应10min内甲容器中以CH3OH(g)表示的化学反应速率为__ ,此温度下的化学平衡常数为__ (保留两位小数);要使平衡后乙容器与甲容器中相同组分的体积分数相等,且起始时维持化学反应向逆反应方向进行,则乙容器中c的取值范围为__ 。
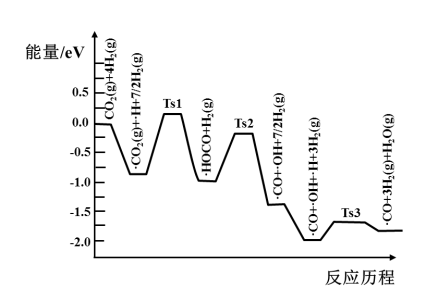
(3)氢气可将CO2还原为甲烷,反应为CO2(g)+4H2(g) CH4(g)+2H2O(g)。ShyamKattel等结合实验与计算机模拟结果,研究了在Pt/SiO2催化剂表面上CO2与H2的反应历程,前三步历程如图所示其中吸附在Pt/SiO2催化剂表面用“·”标注,Ts表示过渡态。物质吸附在催化剂表面,形成过渡态的过程会
CH4(g)+2H2O(g)。ShyamKattel等结合实验与计算机模拟结果,研究了在Pt/SiO2催化剂表面上CO2与H2的反应历程,前三步历程如图所示其中吸附在Pt/SiO2催化剂表面用“·”标注,Ts表示过渡态。物质吸附在催化剂表面,形成过渡态的过程会__ (填“放出热量”或“吸收热量”);反应历程中最小能垒(活化能)步骤的化学方程式为__ 。
(1)以CO2和NH3为原料合成尿素是利用CO2的成功范例。在尿素合成塔中的主要反应可表示如下:
反应I:2NH3(g)+CO2(g)
 NH2COONH4(s) ∆H1
NH2COONH4(s) ∆H1反应II:NH2COONH4(s)
 CO(NH2)2(s)+H2O(g) ∆H2=+72.49kJ/mol
CO(NH2)2(s)+H2O(g) ∆H2=+72.49kJ/mol总反应:2NH3(g)+CO2(g)
 CO(NH2)2(s)+H2O(g) ∆H3=-86.98kJ/mol
CO(NH2)2(s)+H2O(g) ∆H3=-86.98kJ/mol请回答下列问题:
①反应I的∆H1=
②反应II一般在
③一定温度下,在体积固定的密闭容器中按计量比投料进行反应I,下列能说明反应达到了平衡状态的是
A.混合气体的平均相对分子质量不再变化
B.容器内气体总压强不再变化
C.2v正(NH3)=v逆(CO2)
D.容器内混合气体的密度不再变化
(2)将CO2和H2按物质的量之比为1:3充入一定体积的密闭容器中,发生反应:CO2(g)+3H2(g)=CH3OH(g)+H2O(g) ∆H。测得CH3OH的物质的量在不同温度下随时间的变化关系如图所示。

①根据图示判断∆H
②一定温度下,在容积均为2L的两个密闭容器中,按如下方式加入反应物,10min后达到平衡。
| 容器 | 甲 | 乙 |
| 反应物投入量 | 1molCO2、3molH2 | amolCO2、bmolH2 cmolCH3OH(g)、cmolH2O(g)(a、b、c均不为零) |
若甲容器平衡后气体的压强为开始时的0.8倍,则反应10min内甲容器中以CH3OH(g)表示的化学反应速率为
(3)氢气可将CO2还原为甲烷,反应为CO2(g)+4H2(g)
 CH4(g)+2H2O(g)。ShyamKattel等结合实验与计算机模拟结果,研究了在Pt/SiO2催化剂表面上CO2与H2的反应历程,前三步历程如图所示其中吸附在Pt/SiO2催化剂表面用“·”标注,Ts表示过渡态。物质吸附在催化剂表面,形成过渡态的过程会
CH4(g)+2H2O(g)。ShyamKattel等结合实验与计算机模拟结果,研究了在Pt/SiO2催化剂表面上CO2与H2的反应历程,前三步历程如图所示其中吸附在Pt/SiO2催化剂表面用“·”标注,Ts表示过渡态。物质吸附在催化剂表面,形成过渡态的过程会
您最近一年使用:0次
名校
解题方法
5 . 低碳经济是指在可持续发展理念指导下,尽可能地减少煤炭、石油等高碳能源消耗,减少温室气体排放,达到经济社会发展与生态环境保护双赢的一种经济发展形态。下列是有关碳元素的相关转化,回答下列问题:
(1)已知甲醇是一种清洁燃料,制备甲醇是煤液化的重要方向。若已知H2(g)、CO(g)、CH3OH(l)的燃烧热分别为∆H=-285.8kJ/mol、△H=-283.0kJ/mol、△H=-726.5kJ/mol,CO(g)+2H2(g) CH3OH(l)△H=
CH3OH(l)△H=________ kJ/mol。
(2)一定温度下,一定可以提高甲醇合成速率的措施有( )
a.增大起始通入 值
值
b.恒温恒容,再通入氦气
c.使用新型的高效正催化剂
d.将产生的甲醇及时移走
e.压缩体积,增大压强
(3)在恒温恒容条件下,下列说法可以判定反应CO(g)+2H2(g) CH3OH(g)已经达到平衡状态的是
CH3OH(g)已经达到平衡状态的是( )
a.体系中碳氢单键数目不再改变
b.体系中n(CO):n(H2)不再改变
c.体系中压强或者平均摩尔质量不再改变
d.单位时间内消耗氢气和CH3OH的物质的量相等
(4)在恒压的容器中,曲线X、Y、Z分别表示在T1°C、T2°C和T3°C三种温度下合成甲醇气体的过程。控制不同的原料投料比,CO的平衡转化率如图所示:
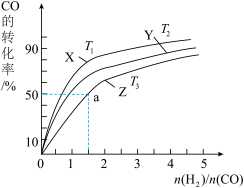
①温度T1°C、T2°C和T3°C由高到低的顺序为:_________________ ;
②若温度为T3°C时,体系压强保持50aMPa,起始反应物投料比n(H2)/n(CO)=1.5,则平衡时CO和CH3OH的分压之比为__________ ,该反应的压强平衡常数Kp的计算式为__________ 。(Kp生成物分压幂的乘积与反应物分压幂的乘积的比值,某物质的分压等于总压强×该物质的物质的量分数)。
(1)已知甲醇是一种清洁燃料,制备甲醇是煤液化的重要方向。若已知H2(g)、CO(g)、CH3OH(l)的燃烧热分别为∆H=-285.8kJ/mol、△H=-283.0kJ/mol、△H=-726.5kJ/mol,CO(g)+2H2(g)
 CH3OH(l)△H=
CH3OH(l)△H=(2)一定温度下,一定可以提高甲醇合成速率的措施有
a.增大起始通入
 值
值b.恒温恒容,再通入氦气
c.使用新型的高效正催化剂
d.将产生的甲醇及时移走
e.压缩体积,增大压强
(3)在恒温恒容条件下,下列说法可以判定反应CO(g)+2H2(g)
 CH3OH(g)已经达到平衡状态的是
CH3OH(g)已经达到平衡状态的是a.体系中碳氢单键数目不再改变
b.体系中n(CO):n(H2)不再改变
c.体系中压强或者平均摩尔质量不再改变
d.单位时间内消耗氢气和CH3OH的物质的量相等
(4)在恒压的容器中,曲线X、Y、Z分别表示在T1°C、T2°C和T3°C三种温度下合成甲醇气体的过程。控制不同的原料投料比,CO的平衡转化率如图所示:

①温度T1°C、T2°C和T3°C由高到低的顺序为:
②若温度为T3°C时,体系压强保持50aMPa,起始反应物投料比n(H2)/n(CO)=1.5,则平衡时CO和CH3OH的分压之比为
您最近一年使用:0次
解题方法
6 .  是燃烧和代谢的最终产物,也是造成温室效应的废气,但
是燃烧和代谢的最终产物,也是造成温室效应的废气,但 作为一种资源,开发和利用的前景十分诱人.
作为一种资源,开发和利用的前景十分诱人.
I、利用太阳能,以 为原料制取炭黑的流程如图所示.过程2的化学方程式为
为原料制取炭黑的流程如图所示.过程2的化学方程式为______ .
Ⅱ、近年科学家提出“绿色自由”构想.把含有大量 的空气吹入
的空气吹入 溶液中,再把
溶液中,再把 从溶液中提取出来,并使之与
从溶液中提取出来,并使之与 反应生成.其工艺流程如图所示:
反应生成.其工艺流程如图所示:
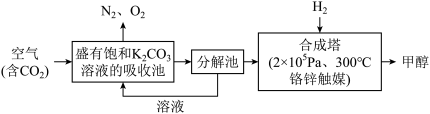
 由吸收池导入分解池中的主要物质的化学式是
由吸收池导入分解池中的主要物质的化学式是______ .
 上述流程中
上述流程中______  填化学式
填化学式 可循环使用,体现了该流程的“绿色”.
可循环使用,体现了该流程的“绿色”.
 不同温度下,在1L恒容密闭容器中充入2mol
不同温度下,在1L恒容密闭容器中充入2mol  和5mol
和5mol  ,相同时间内测得
,相同时间内测得 的转化率随温度变化如图所示:
的转化率随温度变化如图所示:
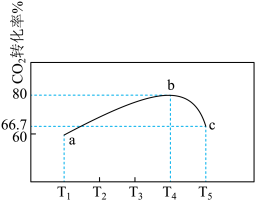
 合成塔中发生的化学反应方程式为
合成塔中发生的化学反应方程式为______ .
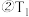 时a点ʋ(正)
时a点ʋ(正)______ ʋ(逆)(填“ ”,“
”,“ ”,“
”,“ ”);
”);
 计算温度为
计算温度为 时b的平衡常数为
时b的平衡常数为______ .
 为检验吸收池中饱和
为检验吸收池中饱和 溶液是否充足,量取100mL吸收液用
溶液是否充足,量取100mL吸收液用 盐酸滴定,生成的
盐酸滴定,生成的 标准状况下
标准状况下 随
随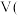 盐酸
盐酸 变化关系如图所示:
变化关系如图所示:
则该100mL吸收液还可吸收标准状况下______ 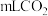 .
.
Ⅲ 以稀硫酸为电解质溶液,惰性材料为电极,利用太阳能将
以稀硫酸为电解质溶液,惰性材料为电极,利用太阳能将 转化为低碳烯烃,工作原理如图所示.
转化为低碳烯烃,工作原理如图所示.
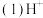 的移动方向是
的移动方向是______  填从左至右或从右至左
填从左至右或从右至左
 产生乙烯的电极反应式为
产生乙烯的电极反应式为______ .
 是燃烧和代谢的最终产物,也是造成温室效应的废气,但
是燃烧和代谢的最终产物,也是造成温室效应的废气,但 作为一种资源,开发和利用的前景十分诱人.
作为一种资源,开发和利用的前景十分诱人.I、利用太阳能,以
 为原料制取炭黑的流程如图所示.过程2的化学方程式为
为原料制取炭黑的流程如图所示.过程2的化学方程式为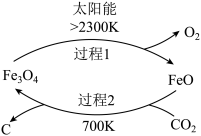
Ⅱ、近年科学家提出“绿色自由”构想.把含有大量
 的空气吹入
的空气吹入 溶液中,再把
溶液中,再把 从溶液中提取出来,并使之与
从溶液中提取出来,并使之与 反应生成.其工艺流程如图所示:
反应生成.其工艺流程如图所示:
 由吸收池导入分解池中的主要物质的化学式是
由吸收池导入分解池中的主要物质的化学式是 上述流程中
上述流程中 填化学式
填化学式 可循环使用,体现了该流程的“绿色”.
可循环使用,体现了该流程的“绿色”. 不同温度下,在1L恒容密闭容器中充入2mol
不同温度下,在1L恒容密闭容器中充入2mol  和5mol
和5mol  ,相同时间内测得
,相同时间内测得 的转化率随温度变化如图所示:
的转化率随温度变化如图所示:
 合成塔中发生的化学反应方程式为
合成塔中发生的化学反应方程式为 时a点ʋ(正)
时a点ʋ(正) ”,“
”,“ ”,“
”,“ ”);
”); 计算温度为
计算温度为 时b的平衡常数为
时b的平衡常数为 为检验吸收池中饱和
为检验吸收池中饱和 溶液是否充足,量取100mL吸收液用
溶液是否充足,量取100mL吸收液用 盐酸滴定,生成的
盐酸滴定,生成的 标准状况下
标准状况下 随
随 盐酸
盐酸 变化关系如图所示:
变化关系如图所示: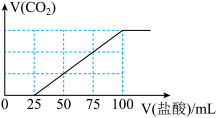
则该100mL吸收液还可吸收标准状况下
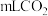 .
.Ⅲ
 以稀硫酸为电解质溶液,惰性材料为电极,利用太阳能将
以稀硫酸为电解质溶液,惰性材料为电极,利用太阳能将 转化为低碳烯烃,工作原理如图所示.
转化为低碳烯烃,工作原理如图所示.
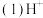 的移动方向是
的移动方向是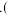 填从左至右或从右至左
填从左至右或从右至左
 产生乙烯的电极反应式为
产生乙烯的电极反应式为
您最近一年使用:0次
2020-01-07更新
|
112次组卷
|
3卷引用:福建省莆田第十五中学2019届高三上学期期中考试化学试题
名校
解题方法
7 . 甲醇是一种优质燃料,在工业上常用CO和H2合成甲醇,反应方程式为CO(g)+2H2(g)  CH3OH(g)。
CH3OH(g)。
已知:
①CO(g)+1/2O2(g)=CO2(g) △H1=-283.0kJ/mol
②H2(g)+1/2O2(g)=H2O(g) △H2=-241.8kJ/mol
③CH3OH(g)+3/2O2(g)=CO2(g)+2H2O(g) △H3=-192.2kJ/mol
回答下列问题:
(1)计算CO(g)+2H2(g) CH3OH(g)的反应热△H4=
CH3OH(g)的反应热△H4=________________ 。
(2)若在绝热、恒容的密闭容器中充入1 mol CO、2 mol H2,发生CO(g)+2H2(g) CH3OH(g)反应,下列示意图正确且能说明反应在进行到t1时刻为平衡状态的是
CH3OH(g)反应,下列示意图正确且能说明反应在进行到t1时刻为平衡状态的是________ (填选项字母)。
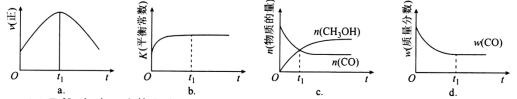
(3)T1℃时,在一个体积为5 L的恒容容器中充入1 mol CO、2 mol H2,经过5 min达到平衡,CO的转化率为0.8,则5 min内用H2表示的反应速率为v(H2)=_______________________ 。T1℃时,在另一体积不变的密闭容器中也充入1 mol CO、2 mol H2,达到平衡时CO的转化率为0.7,则该容器的体积______ 5 L(填“>”“<”或“=”);T1℃时,CO(g)+2H2(g)  CH3OH(g)的平衡常数K=
CH3OH(g)的平衡常数K=____________________________ 。
(4)为了提高燃料的利用率可以将甲醇设计为燃料电池,写出KOH作电解质溶液时,甲醇燃料电池的负极反应式:_________________________ 。该电池负极与水库的铁闸相连时,可以保护铁闸不被腐蚀,这种电化学保护方法叫做___________ 。
(5)含有甲醇的废水随意排放会造成水污染,可用ClO2将其氧化为CO2,然后再加碱中和即可。写出处理甲醇酸性废水过程中,ClO2与甲醇反应的离子方程式:_________ 。
 CH3OH(g)。
CH3OH(g)。已知:
①CO(g)+1/2O2(g)=CO2(g) △H1=-283.0kJ/mol
②H2(g)+1/2O2(g)=H2O(g) △H2=-241.8kJ/mol
③CH3OH(g)+3/2O2(g)=CO2(g)+2H2O(g) △H3=-192.2kJ/mol
回答下列问题:
(1)计算CO(g)+2H2(g)
 CH3OH(g)的反应热△H4=
CH3OH(g)的反应热△H4=(2)若在绝热、恒容的密闭容器中充入1 mol CO、2 mol H2,发生CO(g)+2H2(g)
 CH3OH(g)反应,下列示意图正确且能说明反应在进行到t1时刻为平衡状态的是
CH3OH(g)反应,下列示意图正确且能说明反应在进行到t1时刻为平衡状态的是
(3)T1℃时,在一个体积为5 L的恒容容器中充入1 mol CO、2 mol H2,经过5 min达到平衡,CO的转化率为0.8,则5 min内用H2表示的反应速率为v(H2)=
 CH3OH(g)的平衡常数K=
CH3OH(g)的平衡常数K=(4)为了提高燃料的利用率可以将甲醇设计为燃料电池,写出KOH作电解质溶液时,甲醇燃料电池的负极反应式:
(5)含有甲醇的废水随意排放会造成水污染,可用ClO2将其氧化为CO2,然后再加碱中和即可。写出处理甲醇酸性废水过程中,ClO2与甲醇反应的离子方程式:
您最近一年使用:0次
2018-12-11更新
|
157次组卷
|
2卷引用:福建省惠安惠南中学2019届高三上学期期中考试化学试题
名校
解题方法
8 . 随着科技的进步,合理利用资源、保护环境成为当今社会关注的焦点。甲胺铅碘(CH3NH3PbI3)用作全固态钙钛矿敏化太阳能电池的敏化剂,可由CH3NH2、PbI2及HI为原料合成,制取甲胺的反应为CH3OH(g)+NH3(g) CH3NH2(g)+H2O(g) ΔH。回答下列问题:
CH3NH2(g)+H2O(g) ΔH。回答下列问题:
(1)上述反应中所需的甲醇工业上利用水煤气合成,已知
①CO(g)+ O2(g)═CO2(g) △H1=-284kJ/mol
O2(g)═CO2(g) △H1=-284kJ/mol
②H2(g)+ O2(g)═H2O(g) △H2=-248kJ/mol
O2(g)═H2O(g) △H2=-248kJ/mol
③CH3OH(g)+ O2(g)═CO2(g)+2H2O(g) △H3=-651kJ/mol
O2(g)═CO2(g)+2H2O(g) △H3=-651kJ/mol
CO(g)+2H2(g) CH3OH(g)ΔH=
CH3OH(g)ΔH=___ 。
(2)在一定条件下,将1molCO和2molH2通入密闭容器中进行反应,当改变某一外界条件(温度或压强)时,CH3OH的体积分数φ(CH3OH)变化趋势如图所示:

①平衡时,M点CH3OH的体积分数为10%,则CO的转化率为____ 。
②X轴上b点的数值比a点___ (填“大”或“小”)。某同学认为图中Y轴表示温度,你认为他判断的理由是___ 。
(3)实验室可由四氧化三铅和氢碘酸反应制备难溶的PbI2,常温下,PbI2饱和溶液(呈黄色)中c(Pb2+)=1.0×10-3mol·L-1,则Ksp(PbI2)=___ ;已知Ksp(PbCl2)=1.6×10-5,则转化反应PbI2(s)+2Cl-(aq) PbCl2(s)+2I-(aq)的平衡常数K=
PbCl2(s)+2I-(aq)的平衡常数K=___ 。
(4)分解HI曲线和液相法制备HI反应曲线分别如图1和图2所示:

①反应H2(g)+I2(g) 2HI(g)的ΔH
2HI(g)的ΔH__ (填大于或小于)0。
②将二氧化硫通入碘水中会发生反应:SO2+I2+2H2O 3H++HSO4-+2I-,I2+I-
3H++HSO4-+2I-,I2+I- I3-,图2中曲线a、b分别代表的微粒是
I3-,图2中曲线a、b分别代表的微粒是___ 、___ (填微粒符号);由图2知要提高碘的还原率,除控制温度外,还可以采取的措施是___ 。
 CH3NH2(g)+H2O(g) ΔH。回答下列问题:
CH3NH2(g)+H2O(g) ΔH。回答下列问题:(1)上述反应中所需的甲醇工业上利用水煤气合成,已知
①CO(g)+
 O2(g)═CO2(g) △H1=-284kJ/mol
O2(g)═CO2(g) △H1=-284kJ/mol②H2(g)+
 O2(g)═H2O(g) △H2=-248kJ/mol
O2(g)═H2O(g) △H2=-248kJ/mol③CH3OH(g)+
 O2(g)═CO2(g)+2H2O(g) △H3=-651kJ/mol
O2(g)═CO2(g)+2H2O(g) △H3=-651kJ/molCO(g)+2H2(g)
 CH3OH(g)ΔH=
CH3OH(g)ΔH=(2)在一定条件下,将1molCO和2molH2通入密闭容器中进行反应,当改变某一外界条件(温度或压强)时,CH3OH的体积分数φ(CH3OH)变化趋势如图所示:

①平衡时,M点CH3OH的体积分数为10%,则CO的转化率为
②X轴上b点的数值比a点
(3)实验室可由四氧化三铅和氢碘酸反应制备难溶的PbI2,常温下,PbI2饱和溶液(呈黄色)中c(Pb2+)=1.0×10-3mol·L-1,则Ksp(PbI2)=
 PbCl2(s)+2I-(aq)的平衡常数K=
PbCl2(s)+2I-(aq)的平衡常数K=(4)分解HI曲线和液相法制备HI反应曲线分别如图1和图2所示:

①反应H2(g)+I2(g)
 2HI(g)的ΔH
2HI(g)的ΔH②将二氧化硫通入碘水中会发生反应:SO2+I2+2H2O
 3H++HSO4-+2I-,I2+I-
3H++HSO4-+2I-,I2+I- I3-,图2中曲线a、b分别代表的微粒是
I3-,图2中曲线a、b分别代表的微粒是
您最近一年使用:0次
2019-11-19更新
|
352次组卷
|
3卷引用:福建省仙游第一中学、福州八中2020届高三上学期第三次质检(期中)考试化学试题
名校
解题方法
9 . CCUS是一种二氧化碳的捕获、利用与封存的技术,这种技术可将CO2资源化,产生经济效益。请回答下列问题:
(1)利用废气中的CO2为原料可制取甲醇。一定条件下,在恒容密闭容器中发生反应CO2(g)+3H2(g) CH3OH(g)+H2O(g)。
CH3OH(g)+H2O(g)。
①已知:H2(g)、CH3OH(1)的燃烧热(△H)分别为-285.8kJ·mol-1和-726.5kJ·mol-1;
CH3OH (1)===CH3OH (g) △H=+35.2kJ·mol-1;
H2O(1)===H2O(g) △H=+44kJ·mol-1。
则CO2(g)+3H2(g) CH3OH(g)+H2O(g) △H=
CH3OH(g)+H2O(g) △H=___________ kJ·mol-1。有利于提高H2平衡转化率的条件是___________ (填选项字母)。
A.高温低压 B.低温高压 C.高温高压 D.低温低压
②某温度下,向体积为2L的容器中充入6molH2、4 mol CO2,发生反应CO2(g)+3H2(g) CH3OH(g)+H2O(g),达到平衡时H2的转化率为50%,其平衡常数为
CH3OH(g)+H2O(g),达到平衡时H2的转化率为50%,其平衡常数为___________ (保留两位有效数字)。
③起始条件(T1℃、2L密闭容器)如表所示:
达到平衡时,该反应的平衡常数:K(I)___________ K(Ⅱ)(填“>”“<”或“=”,下同);平衡时CH3OH的浓度:c(I)___________ c(Ⅱ)。
(2)CO2可用来合成低碳烯烃:2CO2(g)+6H2(g) CH2=CH2(g)+4H2O(g) △H=-127.8 kJ·mol-1。0.1MPa下,按n(CO2)︰n(H2)=1︰3的投料比充入体积固定的密闭容器中,发生上述反应,不同温度(T)下平衡时的四种气态物质的质量分数(
CH2=CH2(g)+4H2O(g) △H=-127.8 kJ·mol-1。0.1MPa下,按n(CO2)︰n(H2)=1︰3的投料比充入体积固定的密闭容器中,发生上述反应,不同温度(T)下平衡时的四种气态物质的质量分数(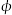 )如图所示:
)如图所示:
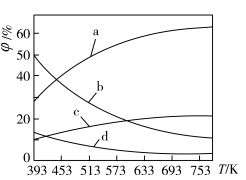
①曲线b、c表示的物质分别为___________ 、___________ (填化学式)。
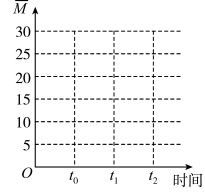
②保持温度不变,在体积为VL的恒容容器中以n(CO2)︰n(H2)=2︰3的投料比加入反应物,t0时达到化学平衡。t1时将容器体积瞬间扩大至2VL并保持不变,t2时重新达到平衡。请在图中画出容器内混合气体的平均相对分子质量M随时间的变化图象_________ 。
(1)利用废气中的CO2为原料可制取甲醇。一定条件下,在恒容密闭容器中发生反应CO2(g)+3H2(g)
 CH3OH(g)+H2O(g)。
CH3OH(g)+H2O(g)。①已知:H2(g)、CH3OH(1)的燃烧热(△H)分别为-285.8kJ·mol-1和-726.5kJ·mol-1;
CH3OH (1)===CH3OH (g) △H=+35.2kJ·mol-1;
H2O(1)===H2O(g) △H=+44kJ·mol-1。
则CO2(g)+3H2(g)
 CH3OH(g)+H2O(g) △H=
CH3OH(g)+H2O(g) △H=A.高温低压 B.低温高压 C.高温高压 D.低温低压
②某温度下,向体积为2L的容器中充入6molH2、4 mol CO2,发生反应CO2(g)+3H2(g)
 CH3OH(g)+H2O(g),达到平衡时H2的转化率为50%,其平衡常数为
CH3OH(g)+H2O(g),达到平衡时H2的转化率为50%,其平衡常数为③起始条件(T1℃、2L密闭容器)如表所示:
| CO2/mol | H2/mol | CH3OH/mol | H2O/mol | |
| I(恒温恒容) | 2 | 6 | 0 | 0 |
| II(绝热恒容) | 0 | 0 | 2 | 2 |
达到平衡时,该反应的平衡常数:K(I)
(2)CO2可用来合成低碳烯烃:2CO2(g)+6H2(g)
 CH2=CH2(g)+4H2O(g) △H=-127.8 kJ·mol-1。0.1MPa下,按n(CO2)︰n(H2)=1︰3的投料比充入体积固定的密闭容器中,发生上述反应,不同温度(T)下平衡时的四种气态物质的质量分数(
CH2=CH2(g)+4H2O(g) △H=-127.8 kJ·mol-1。0.1MPa下,按n(CO2)︰n(H2)=1︰3的投料比充入体积固定的密闭容器中,发生上述反应,不同温度(T)下平衡时的四种气态物质的质量分数(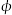 )如图所示:
)如图所示:
①曲线b、c表示的物质分别为
②保持温度不变,在体积为VL的恒容容器中以n(CO2)︰n(H2)=2︰3的投料比加入反应物,t0时达到化学平衡。t1时将容器体积瞬间扩大至2VL并保持不变,t2时重新达到平衡。请在图中画出容器内混合气体的平均相对分子质量M随时间的变化图象

您最近一年使用:0次
2019-02-17更新
|
708次组卷
|
2卷引用:福建2020届高三化学总复习专题训练——选修四化学反应原理测试
名校
解题方法
10 . 羰基硫(COS)是全球硫循环的重要中间体,也是有机合成中的重要原料,是化学工作者重要的研究对象。已知:
Ⅰ.COS(g)+H2(g)⇌H2S(g)+CO(g) △Hl=-17kJ/mol;
Ⅱ.COS(g)+H2O(g)⇌H2S(g)+CO2(g) △H2=-35kJ/mol。
回答下列问题:
(1)反应CO(g)+H2O(g)⇌H2(g)+CO2(g)的△H=________ 。
(2)在充有催化剂的恒压密闭容器中进行反应I。设起始充入的n(H2):n(COS)=m,相同时间内测得COS转化率与m和温度(T)的关系如图所示。
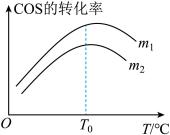 ①m1
①m1________ m2(填>、<或=)。
②温度高于T0时,COS转化率减小的可能原因为_________ 。
A.有副反应发生。
B.反应的△H增大。
C.催化剂活性降低。
D.逆反应速率增大的倍数小于正反应速率增大的倍数
(3)在恒温、恒容密闭容器中.进行反应I。下列说法中能说明反应I已达到平衡状态的是___________ 。
A.c(H2S)=c(CO) B.v正(H2)=v逆(H2S)
C.容器中气体密度保持不变 D.容器中混合气体平均摩尔质量保持不变
E.c(COS)保持不变
(4)某温度下,向体积为2 L的恒容密闭容器中通入5 mol COS(g)和5 molH2O(g),发生反应Ⅱ,5 min后反应达到平衡,测得COS(g)的转化率为80%。
①反应从起始至5 min内,用H2S浓度变化表示的平均反应速度v(H2S)=________ 。
②该温度下,上述反应的平衡常数K=________ 。
③其他条件相同时,既能使上述反应中COS的平衡转化率降低,又能使反应速率加快的做法是________ 。
A.缩小容器容积 B.升高温度
C.分离出硫化氢 D.加入一定量H2O(g)
Ⅰ.COS(g)+H2(g)⇌H2S(g)+CO(g) △Hl=-17kJ/mol;
Ⅱ.COS(g)+H2O(g)⇌H2S(g)+CO2(g) △H2=-35kJ/mol。
回答下列问题:
(1)反应CO(g)+H2O(g)⇌H2(g)+CO2(g)的△H=
(2)在充有催化剂的恒压密闭容器中进行反应I。设起始充入的n(H2):n(COS)=m,相同时间内测得COS转化率与m和温度(T)的关系如图所示。
 ①m1
①m1②温度高于T0时,COS转化率减小的可能原因为
A.有副反应发生。
B.反应的△H增大。
C.催化剂活性降低。
D.逆反应速率增大的倍数小于正反应速率增大的倍数
(3)在恒温、恒容密闭容器中.进行反应I。下列说法中能说明反应I已达到平衡状态的是
A.c(H2S)=c(CO) B.v正(H2)=v逆(H2S)
C.容器中气体密度保持不变 D.容器中混合气体平均摩尔质量保持不变
E.c(COS)保持不变
(4)某温度下,向体积为2 L的恒容密闭容器中通入5 mol COS(g)和5 molH2O(g),发生反应Ⅱ,5 min后反应达到平衡,测得COS(g)的转化率为80%。
①反应从起始至5 min内,用H2S浓度变化表示的平均反应速度v(H2S)=
②该温度下,上述反应的平衡常数K=
③其他条件相同时,既能使上述反应中COS的平衡转化率降低,又能使反应速率加快的做法是
A.缩小容器容积 B.升高温度
C.分离出硫化氢 D.加入一定量H2O(g)
您最近一年使用:0次
2018-11-19更新
|
1331次组卷
|
2卷引用:福建省莆田第二十五中学2020届高三上学期期末考试化学试题



