1 . Ⅰ.在氮及其化合物的化工生产中,对有关反应的反应原理进行研究有着重要意义。
(1)一定温度下,将2 mol N2和6 mol H2置于1 L的恒容密闭容器中发生如下反应: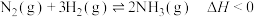 ,测得不同温度、不同时间段内合成氨反应中N2的转化率,数据如下:
,测得不同温度、不同时间段内合成氨反应中N2的转化率,数据如下:
①上表中T1_______ T2(用含“>”“<”“=”的关系式表示),其中a、b、80%三者的大小关系是_______ (用含“>”“<”“=”的关系式表示)。
②研究表明,合成氨的速率与相关物质的浓度关系为 ,k为速率常数。以下说法正确的是
,k为速率常数。以下说法正确的是_______ (填字母序号)。
A.升高温度,k值增大
B.T2℃时若容器内混合气体平均相对分子质量为12且保持不变,则反应达到平衡状态
C.一定温度下将原容器中的NH3及时分离出来可使v减小
D.合成氨达到平衡后,增大c(N2)可使正反应速率在达到新平衡的过程中始终增大
③已知某温度下该反应达平衡时各物质均为1 mol,容器容积为1 L,保持温度和压强不变,又充入3 mol N2后,平衡_______ (填“向左移动”“向右移动”或“不移动”)。
Ⅱ.甲醚(CH3OCH)是重要的化工原料,可用CO和H2制得,总反应的热化学方程式如为 。该过程可分为以下两步反应完成:
。该过程可分为以下两步反应完成:
甲醇合成反应:_______。
甲醇脱水反应: 。
。
(2)起始时向容器中投入2 mol CO和4 mol H2,测得某时刻上述总反应中放出的热量为51.5 kJ,此时CO的转化率为_______ 。
(3)请写出甲醇合成反应的热化学方程式:_______ 。
(4)在一定条件下,将CO和H2按体积比1:2充入恒容密闭容器中,反应生成CH3OCH3(g)和H2O(g)。下列能说明该反应达到平衡状态的是_______ (填字母)。
a.混合气体的总物质的量保持不变
b.混合气体的密度保持不变
c.CH3OCH3(g)和H2O(g)的物质的量之比保持不变
d.每生成1 mol CH3OCH3(g),同时生成2 mol CO
(1)一定温度下,将2 mol N2和6 mol H2置于1 L的恒容密闭容器中发生如下反应:
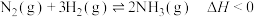 ,测得不同温度、不同时间段内合成氨反应中N2的转化率,数据如下:
,测得不同温度、不同时间段内合成氨反应中N2的转化率,数据如下:| 1小时 | 2小时 | 3小时 | 4小时 | |
| T1 | 30% | 50% | 80% | 80% |
| T2 | 35% | 60% | a | b |
①上表中T1
②研究表明,合成氨的速率与相关物质的浓度关系为
 ,k为速率常数。以下说法正确的是
,k为速率常数。以下说法正确的是A.升高温度,k值增大
B.T2℃时若容器内混合气体平均相对分子质量为12且保持不变,则反应达到平衡状态
C.一定温度下将原容器中的NH3及时分离出来可使v减小
D.合成氨达到平衡后,增大c(N2)可使正反应速率在达到新平衡的过程中始终增大
③已知某温度下该反应达平衡时各物质均为1 mol,容器容积为1 L,保持温度和压强不变,又充入3 mol N2后,平衡
Ⅱ.甲醚(CH3OCH)是重要的化工原料,可用CO和H2制得,总反应的热化学方程式如为
 。该过程可分为以下两步反应完成:
。该过程可分为以下两步反应完成:甲醇合成反应:_______。
甲醇脱水反应:
 。
。(2)起始时向容器中投入2 mol CO和4 mol H2,测得某时刻上述总反应中放出的热量为51.5 kJ,此时CO的转化率为
(3)请写出甲醇合成反应的热化学方程式:
(4)在一定条件下,将CO和H2按体积比1:2充入恒容密闭容器中,反应生成CH3OCH3(g)和H2O(g)。下列能说明该反应达到平衡状态的是
a.混合气体的总物质的量保持不变
b.混合气体的密度保持不变
c.CH3OCH3(g)和H2O(g)的物质的量之比保持不变
d.每生成1 mol CH3OCH3(g),同时生成2 mol CO
您最近一年使用:0次
解题方法
2 . 利用反应A可将释放的CO2转化为具有工业利用价值的产品。
反应A:
已知:
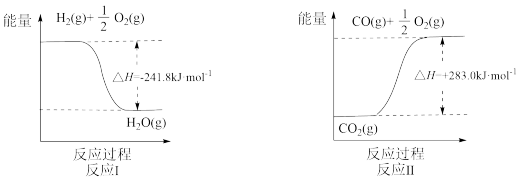
(1)反应Ⅱ是___________ 反应(填“吸热”或“放热”),其原因是___________ 。
(2)反应A的热化学方程式是___________ 。
反应A:

已知:

(1)反应Ⅱ是
(2)反应A的热化学方程式是
您最近一年使用:0次
2022-01-28更新
|
98次组卷
|
2卷引用:山西省晋中市平遥县第二中学2021-2022学年高二上学期12月考试化学试题
3 . 李克强总理在十三届全国人民代表大会第四次会议上作政府工作报告时指出:优化产业结构和能源结构,扎实做好碳达峰、碳中和各项工作。碳中和是指一个组织在一年内的二氧化碳排放通过二氧化碳去除技术达到平衡。
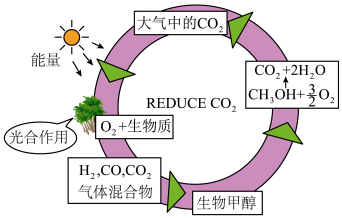
(1)科研人员借助太阳能用二氧化碳制备甲醇等燃料的催化转化是迄今为止最接近光合作用的方法,并且实现了二氧化碳的循环(如图所示),下列说法错误的是___________ (填字母)。
A.图中能量转化形式有两种
B.使用催化剂可以提高单位时间内反应物的转化率
C.利用太阳能开发甲醇等液态燃料有利于环境保护
D.该工艺中的H2目前只能由电解水获得
(2)CO2加氢还可制备甲酸(HCOOH)。
①工业上利用甲酸的能量关系转换图如图所示:
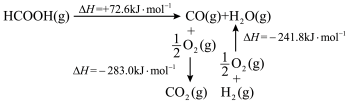
反应CO2(g)+H2(g) HCOOH(g)的焓变△H=
HCOOH(g)的焓变△H=___________ kJ·mol-1。
②温度为T1℃时,将等物质的量的CO2和H2充入体积为1L的密闭容器中发生反应:CO2(g)+H2(g) HCOOH(g) K=2。
HCOOH(g) K=2。
实验测得:v正=k正c(CO2)·c(H2),v逆=k逆c(HCOOH),k正、k逆为速率常数。T1℃时,k逆=___________ k正。
③温度为T2℃时,k正=1.9k逆,则T2℃时平衡压强___________ (填“>”“<”或“=”)T1℃时平衡压强,理由是___________ 。
(3)工业上常用氨水吸收含碳燃料燃烧时产生的温室气体CO2,其产物之一是NH4HCO3。已知常温下碳酸的电离常数Ka1=4.4×10-7、Ka2=4.7×10-11,NH3·H2O的电离常数Kb=1.8×10-5,写出NH4HCO3水解反应的化学方程式:___________ ,选用上述数据计算该反应的平衡常数Kh=___________ (保留三位有效数字)。
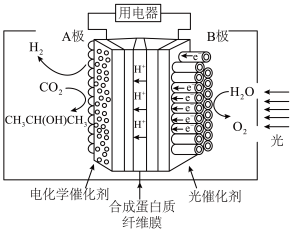
(4)某光电催化反应器如图所示,A极是Pt/CNT电极,B极是TiO2电极。写出A极由CO2制异丙醇的电极反应式:___________ 。
(1)科研人员借助太阳能用二氧化碳制备甲醇等燃料的催化转化是迄今为止最接近光合作用的方法,并且实现了二氧化碳的循环(如图所示),下列说法错误的是

A.图中能量转化形式有两种
B.使用催化剂可以提高单位时间内反应物的转化率
C.利用太阳能开发甲醇等液态燃料有利于环境保护
D.该工艺中的H2目前只能由电解水获得
(2)CO2加氢还可制备甲酸(HCOOH)。
①工业上利用甲酸的能量关系转换图如图所示:

反应CO2(g)+H2(g)
 HCOOH(g)的焓变△H=
HCOOH(g)的焓变△H=②温度为T1℃时,将等物质的量的CO2和H2充入体积为1L的密闭容器中发生反应:CO2(g)+H2(g)
 HCOOH(g) K=2。
HCOOH(g) K=2。实验测得:v正=k正c(CO2)·c(H2),v逆=k逆c(HCOOH),k正、k逆为速率常数。T1℃时,k逆=
③温度为T2℃时,k正=1.9k逆,则T2℃时平衡压强
(3)工业上常用氨水吸收含碳燃料燃烧时产生的温室气体CO2,其产物之一是NH4HCO3。已知常温下碳酸的电离常数Ka1=4.4×10-7、Ka2=4.7×10-11,NH3·H2O的电离常数Kb=1.8×10-5,写出NH4HCO3水解反应的化学方程式:
(4)某光电催化反应器如图所示,A极是Pt/CNT电极,B极是TiO2电极。写出A极由CO2制异丙醇的电极反应式:

您最近一年使用:0次
解题方法
4 . CO2的回收与利用是科学家研究的热点课题。
已知:反应ICO2(g)+3H2(g) CH3OH(g)+H2O(g)△H1=-58kJ·mol-1
CH3OH(g)+H2O(g)△H1=-58kJ·mol-1
反应ICO2(g)+H2(g) CO(g)+H2O(g)△H2=+41kJ·mol-1
CO(g)+H2O(g)△H2=+41kJ·mol-1
(1)CO(g)和H2(g)反应生成CH3OH(g)的热化学方程式为______________ 。
(2)某实验过程中,控制压强一定,将CO2和H2按一定的初始投料比、一定流速通过催化剂,经过相同时间测得如下实验数据(反应未达到平衡状态):
表中实验数据表明,升高温度,CO2实际转化率提高而甲醇的选择性降低。其原因是____________________________ 。
(3)在一定条件下,选择合适的催化剂只进行反应CO2(g)+H2(g) CO(g)+H2O(g)。调整CO2和H2初始投料比,测得在一定投料比和一定温度下,该反应CO2的平衡转化率如图(各点对应的反应温度可能相同,也可能不同)。
CO(g)+H2O(g)。调整CO2和H2初始投料比,测得在一定投料比和一定温度下,该反应CO2的平衡转化率如图(各点对应的反应温度可能相同,也可能不同)。
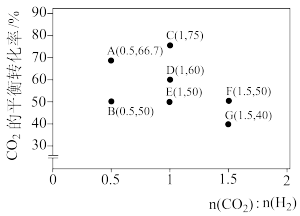
已知:Kx是以物质的量分数表示的化学平衡常数。
①经分析,A、E和G三点对应的反应温度相同,结合数据说明判断理由_______________ 。
②已知反应速率v=v正-v逆=k正x(CO2)x(H2)-k逆x(CO)x(H2O),k正、k逆分别为正、逆向反应速率常数,x为物质的量分数。C、D、E三点中k正-k逆最大的是___________ ,A、B、F三点中v逆最大的是___________ 。计算E点所示的投料比在从起始到平衡的过程中,当CO2转化率达到50%时, =
=___________ 。
(4)关于合成甲醇过程中用到的催化剂,下列说法错误的是___________ (填字母)。
A.参与了反应,改变了反应历程和△HB.使k正和k逆增大,但二者增大倍数不同
C.降低了反应的活化能D.提高了CO2的平衡转化率
已知:反应ICO2(g)+3H2(g)
 CH3OH(g)+H2O(g)△H1=-58kJ·mol-1
CH3OH(g)+H2O(g)△H1=-58kJ·mol-1反应ICO2(g)+H2(g)
 CO(g)+H2O(g)△H2=+41kJ·mol-1
CO(g)+H2O(g)△H2=+41kJ·mol-1(1)CO(g)和H2(g)反应生成CH3OH(g)的热化学方程式为
(2)某实验过程中,控制压强一定,将CO2和H2按一定的初始投料比、一定流速通过催化剂,经过相同时间测得如下实验数据(反应未达到平衡状态):
T/K | CO2实际转化率/% | 甲醇的选择性/% |
543 | 12.3 | 42.3 |
553 | 15.3 | 39.1 |
(3)在一定条件下,选择合适的催化剂只进行反应CO2(g)+H2(g)
 CO(g)+H2O(g)。调整CO2和H2初始投料比,测得在一定投料比和一定温度下,该反应CO2的平衡转化率如图(各点对应的反应温度可能相同,也可能不同)。
CO(g)+H2O(g)。调整CO2和H2初始投料比,测得在一定投料比和一定温度下,该反应CO2的平衡转化率如图(各点对应的反应温度可能相同,也可能不同)。
已知:Kx是以物质的量分数表示的化学平衡常数。
①经分析,A、E和G三点对应的反应温度相同,结合数据说明判断理由
②已知反应速率v=v正-v逆=k正x(CO2)x(H2)-k逆x(CO)x(H2O),k正、k逆分别为正、逆向反应速率常数,x为物质的量分数。C、D、E三点中k正-k逆最大的是
 =
=(4)关于合成甲醇过程中用到的催化剂,下列说法错误的是
A.参与了反应,改变了反应历程和△HB.使k正和k逆增大,但二者增大倍数不同
C.降低了反应的活化能D.提高了CO2的平衡转化率
您最近一年使用:0次
5 . 工业接触法制硫酸的关键工序是 的催化氧化:
的催化氧化: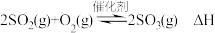 。回答下列问题:
。回答下列问题:
(1)当加入催化剂时,该反应机理为:
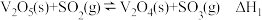
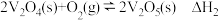
有关反应过程中的能量变化如图所示,下列说法错误的是_______ (填标号)
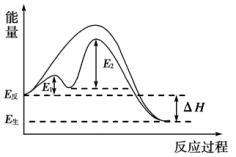
A. B.
B.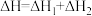
C. 是该反应的催化剂 D.加入催化剂后反应的活化能为
是该反应的催化剂 D.加入催化剂后反应的活化能为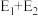
(2)一定条件下,将 和
和 混合置于
混合置于 密闭容器中发生反应:
密闭容器中发生反应: ,当反应从开始进行到
,当反应从开始进行到 时达到平衡状态,测得此时的压强是反应开始时的0.8倍。
时达到平衡状态,测得此时的压强是反应开始时的0.8倍。
① 内用
内用 表示的平均反应速率为
表示的平均反应速率为_______ 。
②达到平衡时 的转化率为
的转化率为_______ 。
③能说明该反应已达到平衡状态的是_______ (填标号)。
A.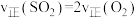 B.
B. 的生成速率等于
的生成速率等于 的生成速率
的生成速率
C.容器内压强保持不变 D.混合气体的平均相对分子质量不变
E.容器内密度保持不变 F.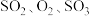 物质的量比为
物质的量比为
④该条件下的平衡常数K=_______ ;上述反应中,正反应速率为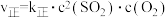 ,逆反应速率为
,逆反应速率为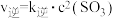 ,其中
,其中 为速率常数,则
为速率常数,则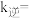
_______  。
。
 的催化氧化:
的催化氧化: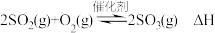 。回答下列问题:
。回答下列问题:(1)当加入催化剂时,该反应机理为:
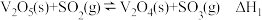
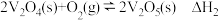
有关反应过程中的能量变化如图所示,下列说法错误的是

A.
 B.
B.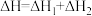
C.
 是该反应的催化剂 D.加入催化剂后反应的活化能为
是该反应的催化剂 D.加入催化剂后反应的活化能为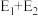
(2)一定条件下,将
 和
和 混合置于
混合置于 密闭容器中发生反应:
密闭容器中发生反应: ,当反应从开始进行到
,当反应从开始进行到 时达到平衡状态,测得此时的压强是反应开始时的0.8倍。
时达到平衡状态,测得此时的压强是反应开始时的0.8倍。①
 内用
内用 表示的平均反应速率为
表示的平均反应速率为②达到平衡时
 的转化率为
的转化率为③能说明该反应已达到平衡状态的是
A.
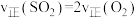 B.
B. 的生成速率等于
的生成速率等于 的生成速率
的生成速率C.容器内压强保持不变 D.混合气体的平均相对分子质量不变
E.容器内密度保持不变 F.
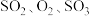 物质的量比为
物质的量比为
④该条件下的平衡常数K=
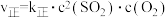 ,逆反应速率为
,逆反应速率为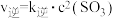 ,其中
,其中 为速率常数,则
为速率常数,则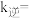
 。
。
您最近一年使用:0次
2021-03-18更新
|
146次组卷
|
2卷引用:山西省(晋中市)2020-2021学年高二上学期期末调研化学试题
名校
解题方法
6 .  是一种廉价的碳资源,其综合利用具有重要意义,用
是一种廉价的碳资源,其综合利用具有重要意义,用 与
与 为原料合成尿素
为原料合成尿素 是固定和利用
是固定和利用 的成功范例。
的成功范例。
已知:①
②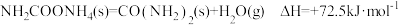
③
则:反应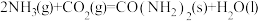 的
的 为
为
 是一种廉价的碳资源,其综合利用具有重要意义,用
是一种廉价的碳资源,其综合利用具有重要意义,用 与
与 为原料合成尿素
为原料合成尿素 是固定和利用
是固定和利用 的成功范例。
的成功范例。已知:①

②
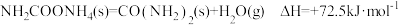
③

则:反应
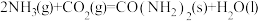 的
的 为
为A. | B.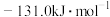 |
C.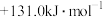 | D. |
您最近一年使用:0次
2021-03-18更新
|
1380次组卷
|
7卷引用:山西省(晋中市)2020-2021学年高二上学期期末调研化学试题



