名校
1 . 下列反应中生成物总能量高于反应物总能量的是
| A.氧化钙溶于水 | B.铁粉与硫粉共热 |
| C.强酸强碱中和 | D.氢氧化钡晶体与氯化铵晶体的反应 |
您最近一年使用:0次
2023-11-27更新
|
165次组卷
|
3卷引用:上海市复兴高级中学2022-2023学年高二上学期期中考试化学(等级考)试题
名校
2 . 正丁烷(CH3CH2CH2CH3)催化裂解为乙烷和乙烯的反应历程如下(*代表催化剂):
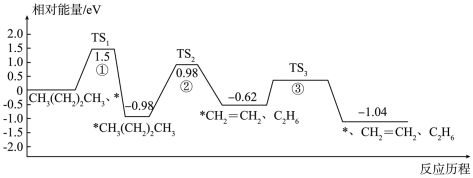
下列说法正确的是

下列说法正确的是
| A.使用催化剂能降低该反应的△H |
B.过渡态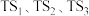 中稳定性最强的是TS1 中稳定性最强的是TS1 |
| C.正丁烷裂解生成乙烷和乙烯的反应为放热反应 |
| D.正丁烷裂解生成乙烷和乙烯的决速步骤是反应① |
您最近一年使用:0次
2023-11-20更新
|
208次组卷
|
4卷引用:上海市吴淞中学2023-2024学年高二上学期第二次学科质量检测 化学试卷
3 . 如图是 的能量示意图。下列说法正确的是
的能量示意图。下列说法正确的是
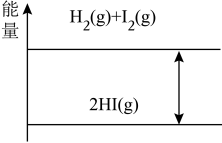
 的能量示意图。下列说法正确的是
的能量示意图。下列说法正确的是
| A.该反应是吸热反应 | B.该反应物总能量高于生成物总能量 |
| C.放热反应的发生都不需要加热 | D.该反应中H2为氧化剂 |
您最近一年使用:0次
名校
4 . 实验室研究CH3OH合成反应化学平衡的影响因素,有利于提高CH3OH的产率。以CO2、H2为原料合成CH3OH涉及的主要反应如下:
Ⅰ.CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g) ΔH1=-49.5kJ·mol-1
Ⅱ.CO(g)+2H2(g)⇌CH3OH(g) ΔH2=-90.4kJ·mol-1
Ⅲ.CO2(g)+H2(g)⇌CO(g)+H2O(g) ΔH3>0
不同压强下,按照n(CO2)∶n(H2)=1∶3投料,实验测定CH3OH的平衡产率(图1)和CO2的平衡转化率(图2)随温度的变化关系如图所示。回答问题
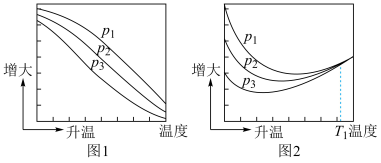
(1)图1中,一定压强下,CH3OH的平衡产率随温度升高而下降的原因是______ 。
(2)图1中,压强p1、p2、p3由大到小的顺序为______ 。
(3)图2中T1温度时,三条曲线几乎交于一点的原因是______ 。
(4)为同时提高CO2的平衡转化率和CH3OH的平衡产率,应选择的反应条件为______。
Ⅰ.CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g) ΔH1=-49.5kJ·mol-1
Ⅱ.CO(g)+2H2(g)⇌CH3OH(g) ΔH2=-90.4kJ·mol-1
Ⅲ.CO2(g)+H2(g)⇌CO(g)+H2O(g) ΔH3>0
不同压强下,按照n(CO2)∶n(H2)=1∶3投料,实验测定CH3OH的平衡产率(图1)和CO2的平衡转化率(图2)随温度的变化关系如图所示。回答问题

(1)图1中,一定压强下,CH3OH的平衡产率随温度升高而下降的原因是
(2)图1中,压强p1、p2、p3由大到小的顺序为
(3)图2中T1温度时,三条曲线几乎交于一点的原因是
(4)为同时提高CO2的平衡转化率和CH3OH的平衡产率,应选择的反应条件为______。
| A.低温、高压 | B.高温、低压 | C.低温、低压 | D.高温、高压 |
您最近一年使用:0次
5 . 二氧化碳催化加氢制甲醇,有利于减少温室气体二氧化碳。回答下列问题:二氧化碳加氢制甲醇的总反应可表示为:CO2(g)+3H2(g)=CH3OH(g)+H2O(g)。该反应一般认为通过如下步骤来实现:
①CO2(g)+H2(g)=CO(g)+H2O(g) △H1=+41kJ•mol-1
②CO(g)+2H2(g)=CH3OH(g) △H2=-90kJ•mol-1
(1)总反应的△H=________ kJ•mol-1。
(2)下列示意图中能体现上述反应能量变化的是________ 。判断的理由是________ 。
A.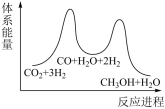 B.
B.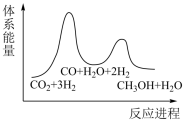 C.
C.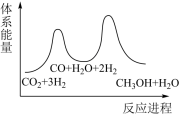
①CO2(g)+H2(g)=CO(g)+H2O(g) △H1=+41kJ•mol-1
②CO(g)+2H2(g)=CH3OH(g) △H2=-90kJ•mol-1
(1)总反应的△H=
(2)下列示意图中能体现上述反应能量变化的是
A.
 B.
B. C.
C.
您最近一年使用:0次
名校
解题方法
6 . 如图所示H2和Cl2反应生成HCl的能量变化示意图,由图可知
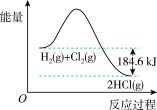

| A..反应物总能量低于生成物总能量 |
| B.H2+Cl2=2HCl+184.6kJ |
| C.H2(g)+Cl2(g)=2HCl(l) △H<-184.6kJ/mol |
| D.1molCl2(g)的能量高于2molHCl(g)的能量 |
您最近一年使用:0次
名校
解题方法
7 . 电喷雾电离等方法得到的M+(Fe+、Co+或Ni+等)匀O3反应可得MO+在一定条件下,MO++CH4=M++CH3OH,直接参与化学键变化的元素被替换为更重的同位素时,反应速率会变慢。MO+与CH4或CT4体系的能量随反应进程的变化如图所示,下列说法错误的是
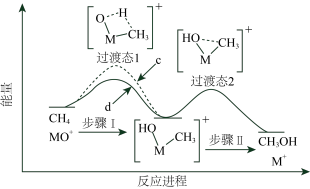

| A.该反应是放热反应 |
| B.步骤Ⅰ和步骤Ⅱ中氢原子的成键方式均发生了变化 |
| C.MO+与CT4反应的能量变化为曲线c |
| D.相同情况下,MO+与CHT3反应,氚代甲醇CT3OH的产量大于CHT2OT |
您最近一年使用:0次
2023-10-28更新
|
461次组卷
|
3卷引用:上海市青浦高中2023-2024学年高二上学期期末考试化学模拟试卷
上海市青浦高中2023-2024学年高二上学期期末考试化学模拟试卷重庆市第八中学校2023-2024学年高三上学期10月期中考试化学试题(已下线)题型06 反应热的判断及计算-2024年高考化学答题技巧与模板构建
名校
8 . 下列变化过程,属于放热反应的是___________ (填写序号)。
①浓 稀释 ②酸碱中和反应 ③
稀释 ②酸碱中和反应 ③ 在
在 中燃烧 ④固体
中燃烧 ④固体 溶于水 ⑤液态水变成水蒸气 ⑥碳在高温条件下还原
溶于水 ⑤液态水变成水蒸气 ⑥碳在高温条件下还原
①浓
 稀释 ②酸碱中和反应 ③
稀释 ②酸碱中和反应 ③ 在
在 中燃烧 ④固体
中燃烧 ④固体 溶于水 ⑤液态水变成水蒸气 ⑥碳在高温条件下还原
溶于水 ⑤液态水变成水蒸气 ⑥碳在高温条件下还原
您最近一年使用:0次
名校
解题方法
9 . 已知N-H键、O=O键、H-O键键能分别为391kJ·mol-1、497kJ·mol-1、463kJ·mol-1,N2H4(g)与O2(g)反应的能量变化如图所示:
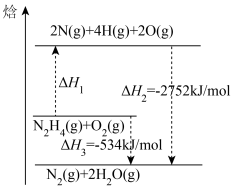
(1)N2H4(g)与O2(g)的反应是___________ (放热/吸热)反应。
(2)N2H4(g)中N-N键的键能为___________ 。
(3)N2(g)中N N键的键能为
N键的键能为___________ 。
(4)美国加利福尼亚大学圣地亚哥的 G·N·SChrauzer等人用氮气和水蒸气在触媒上,光照射下合成高能气态联氨初获成功,该反应的热化学方程式为:___________ 。
(5)在实验室中可以用次氯酸钠和氨气常温制备联氨,反应的离子方程式为:___________ 。
(6)联氨(N2H4)在水中电离方式与NH3相似,若将NH3视为一元弱碱,则N2H4是一种二元弱碱。根据以上信息,推断下列关于N2H4的说法不正确的是_________

(1)N2H4(g)与O2(g)的反应是
(2)N2H4(g)中N-N键的键能为
(3)N2(g)中N
 N键的键能为
N键的键能为(4)美国加利福尼亚大学圣地亚哥的 G·N·SChrauzer等人用氮气和水蒸气在触媒上,光照射下合成高能气态联氨初获成功,该反应的热化学方程式为:
(5)在实验室中可以用次氯酸钠和氨气常温制备联氨,反应的离子方程式为:
(6)联氨(N2H4)在水中电离方式与NH3相似,若将NH3视为一元弱碱,则N2H4是一种二元弱碱。根据以上信息,推断下列关于N2H4的说法不正确的是_________
| A.它与硫酸形成的酸式盐可以表示为N2H5HSO4 |
| B.它溶于水所得的溶液中共有4种离子 |
C.它溶于水发生电离的第一步可表示为:N2H4+H2O N2H N2H +OH- +OH- |
| D.若已知联氨和四氧化二氮可以做火箭推进剂,两者反应产物可以是氮气和水 |
您最近一年使用:0次
名校
10 . 已知: 与足量
与足量 充分燃烧生成液态水时放出
充分燃烧生成液态水时放出 热量。
热量。
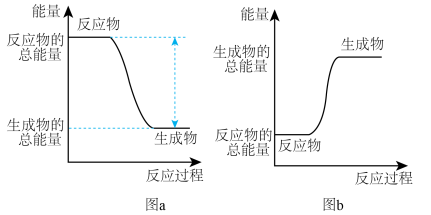
(1)该反应的能量变化可用图中的___________ (填字母)表示。
(2)写出 燃烧生成液态水的热化学反应方程式
燃烧生成液态水的热化学反应方程式___________ 。
(3)关于热化学方程式: 的说法正确的是___________。
的说法正确的是___________。
 与足量
与足量 充分燃烧生成液态水时放出
充分燃烧生成液态水时放出 热量。
热量。
(1)该反应的能量变化可用图中的
(2)写出
 燃烧生成液态水的热化学反应方程式
燃烧生成液态水的热化学反应方程式(3)关于热化学方程式:
 的说法正确的是___________。
的说法正确的是___________。| A.热化学方程式中化学计量数表示分子数 | B.该反应 大于零 大于零 |
C.该反应的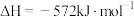 | D.该反应可表示 水分解时的热效应 水分解时的热效应 |
您最近一年使用:0次



