解题方法
1 . Ⅰ.现有部分元素的性质与原子(或分子)结构如表所示:
回答下列问题:
(1)T是_______ (填元素符号)。元素X在周期表的位置_______ 。
(2)Y与Z相比,金属性较强的是_____ (填元素符号),下列表述中能证明这一事实的是_______ (填标号)。
A.Y单质的熔点比Z单质的低
B.Y的化合价比Z的低
C.Y单质与水反应比Z单质与水反应剧烈得多
(3)Z的最高价氧化物属于_______ 氧化物(“酸性”、“碱性”或“两性”),写出Y、Z最高价氧化物对应水化物反应的离子方程式____ 。
Ⅱ.2SO2(g)+O2(g) 2SO3(g)反应过程的能量变化如图所示。
2SO3(g)反应过程的能量变化如图所示。
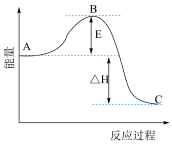
已知1mol SO2(g)氧化为1mol SO3的ΔH=-99kJ·mol-1.请回答下列问题:
(4)图中A、C分别表示_______ 、_______ 。
(5)图中△H=_______ kJ·mol-1。
(6)已知单质硫的燃烧热为296KJ·mol-1,计算由S(s)生成3 molSO3(g)的△H_______ 。
元素 | 元素性质与原子(或分子)结构 |
| T | 最外层电子数是次外层电子数的3倍 |
| X | 常温下单质分子为双原子分子,是空气的主要成分,分子比较稳定 |
| Y | M层比K层少一个电子 |
| Z | 有三个电子层,M层上有3个电子 |
(1)T是
(2)Y与Z相比,金属性较强的是
A.Y单质的熔点比Z单质的低
B.Y的化合价比Z的低
C.Y单质与水反应比Z单质与水反应剧烈得多
(3)Z的最高价氧化物属于
Ⅱ.2SO2(g)+O2(g)
 2SO3(g)反应过程的能量变化如图所示。
2SO3(g)反应过程的能量变化如图所示。
已知1mol SO2(g)氧化为1mol SO3的ΔH=-99kJ·mol-1.请回答下列问题:
(4)图中A、C分别表示
(5)图中△H=
(6)已知单质硫的燃烧热为296KJ·mol-1,计算由S(s)生成3 molSO3(g)的△H
您最近一年使用:0次
名校
2 . 某同学用下列装置进行元素化合物性质的实验,下列实验装置不能达到实验目的的是


| A.验证Na和水反应是否为放热反应 | B.检验Na2O2与H2O反应有O2生成 |
| C.观察纯碱的焰色 | D.观察气球的变化,证明Cl2可与NaOH反应 |
您最近一年使用:0次
解题方法
3 . 为了探究化学能与热能的转化,某实验小组设计了如图所示的三套实验装置:
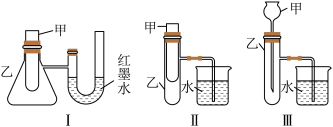
(1)上述3个装置中,不能证明“铜与浓硝酸反应是吸热反应还是放热反应”的是(不能用手触摸和使用温度计)_____ 。
(2)某同学选用装置I进行实验(实验前U形管里液面左右相平),在甲试管里加入适量氢氧化钠溶液与稀盐酸,U形管中可观察到的现象是_____ ,说明该反应属于____ (填“吸热反应”或“放热反应”)。
(3)为定量测定(2)中反应的反应热,使50mL0.50mol•L-1盐酸与50mL0.55mol•L-1NaOH溶液在简易量热计中进行中和反应。回答下列问题:
①该实验中NaOH的浓度大于盐酸的浓度的作用是_____ 。
②实验中若改用60mL0.50mol•L-1盐酸与50mL0.55mol•L-1NaOH溶液进行反应,与上述实验相比,所求中和热_____ (填“相等”或“不相等”)。
(4)已知一些化学键的键能数据如表所示:
请根据键能数据估算CH4(g)和F2(g)反应生成CF4(g)和HF(g)的热化学方程式:_____ 。
(5)已知反应:N2(g)+O2(g)=2NO(g) △H1
2H2(g)+O2(g)=2H2O(g) △H2
N2(g)+3H2(g)=2NH3(g) △H3
利用上述三个反应,计算4NH3(g)+5O2(g)=4NO(g)+6H2O(g)△H4的反应焓变为____ (用含△H1、△H2、△H3的式子表示)。

(1)上述3个装置中,不能证明“铜与浓硝酸反应是吸热反应还是放热反应”的是(不能用手触摸和使用温度计)
(2)某同学选用装置I进行实验(实验前U形管里液面左右相平),在甲试管里加入适量氢氧化钠溶液与稀盐酸,U形管中可观察到的现象是
(3)为定量测定(2)中反应的反应热,使50mL0.50mol•L-1盐酸与50mL0.55mol•L-1NaOH溶液在简易量热计中进行中和反应。回答下列问题:
①该实验中NaOH的浓度大于盐酸的浓度的作用是
②实验中若改用60mL0.50mol•L-1盐酸与50mL0.55mol•L-1NaOH溶液进行反应,与上述实验相比,所求中和热
(4)已知一些化学键的键能数据如表所示:
| 化学键 | C-H | C-F | H-F | F-F |
| 键能/kJ•mol-1 | 414 | 489 | 565 | 155 |
(5)已知反应:N2(g)+O2(g)=2NO(g) △H1
2H2(g)+O2(g)=2H2O(g) △H2
N2(g)+3H2(g)=2NH3(g) △H3
利用上述三个反应,计算4NH3(g)+5O2(g)=4NO(g)+6H2O(g)△H4的反应焓变为
您最近一年使用:0次
名校
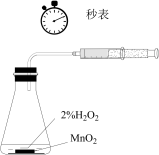
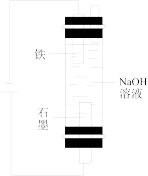
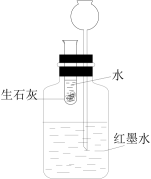
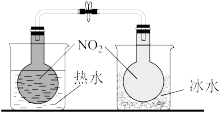
4 . 利用下列实验装置无法实现实验目的的是
 |  |  |  |
| ① | ② | ③ | ④ |
| A.用装置①测量2%双氧水分解生成O2的化学反应速率 |
B.用装置②制备 并能较长时间观察其颜色 并能较长时间观察其颜色 |
| C.用装置③证明生石灰与水反应是放热反应 |
| D.用装置④探究温度对化学平衡的影响 |
您最近一年使用:0次
2021-11-18更新
|
226次组卷
|
3卷引用:山东省青岛市4区市2021-2022学年高二上学期期中考试化学试题
5 . 溶液中的反应大多都是离子反应,请按要求回答下列问题:
(1)要求设计实验证明盐类水解是吸热过程,有四位学生分别做了以下实验,其中根据实验现象得出的结论正确的是___ (填字母标号)。
(2)泡沫灭火器的反应原理是盐类水解,请写出其离子方程式:___ 。
(3)将一定浓度的CH3COOH溶液和NaOH溶液等体积混合,测得所得溶液的pH=7,则该溶液中离子浓度的大小关系是___ 。
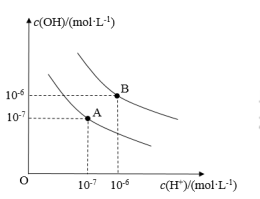
(4)已知水在25℃和95℃时的电离平衡曲线如图所示:95℃时,将pH=9的NaOH溶液与pH=4的H2SO4,溶液混合,若所得混合溶液的pH=7,则NaOH溶液与H2SO4,溶液的体积比为___ 。
(5)在一定温度下,有以下三种酸:a.醋酸 b.硫酸 c.盐酸。
①当三种酸物质的量浓度相同时,三种溶液中水的电离程度由大到小的顺序是___ (用a、b、c表示,下同)。
②当三种酸的pH相同、体积相同时,分别加入足量的锌,产生H2的体积(相同状况)大小关系为___ 。
(1)要求设计实验证明盐类水解是吸热过程,有四位学生分别做了以下实验,其中根据实验现象得出的结论正确的是
| A.甲学生:在醋酸钠溶液中滴入酚酞试液,加热后溶液红色加深,说明盐类水解是吸热的 |
| B.乙学生:将硝酸铵晶体溶于水,水温下降,说明硝酸铵水解是吸热的 |
| C.丙学生:在盐酸中加入同温度的氨水,混合液温度下降,说明盐类水解是吸热的 |
| D.丁学生:在醋酸钠溶液中加入醋酸钠晶体,溶液温度下降,说明盐类水解是吸热的 |
(3)将一定浓度的CH3COOH溶液和NaOH溶液等体积混合,测得所得溶液的pH=7,则该溶液中离子浓度的大小关系是
(4)已知水在25℃和95℃时的电离平衡曲线如图所示:95℃时,将pH=9的NaOH溶液与pH=4的H2SO4,溶液混合,若所得混合溶液的pH=7,则NaOH溶液与H2SO4,溶液的体积比为

(5)在一定温度下,有以下三种酸:a.醋酸 b.硫酸 c.盐酸。
①当三种酸物质的量浓度相同时,三种溶液中水的电离程度由大到小的顺序是
②当三种酸的pH相同、体积相同时,分别加入足量的锌,产生H2的体积(相同状况)大小关系为
您最近一年使用:0次
6 . 实验操作对应的现象与结论均正确的是
| 选项 | 实验操作 | 现象 | 结论 |
| A | 常温下将Ba(OH)2·8H2O晶体与NH4Cl晶体在小烧杯中混合 | 烧杯壁变凉 | 该反应正向是熵减的反应 |
| B | 分别测定常温下0.1mol/LNa2SO3溶液和Na2CO3溶液的pH | pH:Na2CO3>Na2SO3 | 非金属性:S>C |
| C | 将0.1mol/L的弱酸HA稀释成0.01mol/L,测量稀释前后溶液pH | pH增大 | 稀释后HA电离程度减小 |
| D | 向含有酚酞的Na2CO3溶液中加入少量BaCl2固体, | 溶液红色变浅 | 证明Na2CO3溶液中存在水解平衡 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
7 . 为了探究化学能与热能的转化,某实验小组设计了如图所示的三套实验装置:
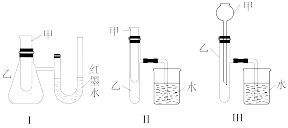
(1)上述 个装置中,不能证明“铜与浓硝酸反应是吸热反应还是放热反应”的是
个装置中,不能证明“铜与浓硝酸反应是吸热反应还是放热反应”的是 不能用手触摸和使用温度计
不能用手触摸和使用温度计
_______ 。
(2)某同学选用装置Ⅰ进行实验 实验前
实验前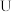 形管里液面左右相平
形管里液面左右相平 ,在甲试管里加入适量氢氧化钠溶液与稀盐酸,
,在甲试管里加入适量氢氧化钠溶液与稀盐酸,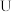 形管中可观察到的现象是
形管中可观察到的现象是_______ ,说明该反应属于_______  填“吸热”或“放热”
填“吸热”或“放热” 反应。
反应。
(3)为定量测定(2)中反应的反应热,使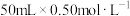 盐酸与
盐酸与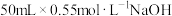 溶液在简易量热计中进行中和反应。该实验中
溶液在简易量热计中进行中和反应。该实验中 的浓度大于
的浓度大于 的浓度的作用是
的浓度的作用是_______ 。
(4)已知一些化学键的键能数据如表所示:
请根据键能数据估算 和
和 反应生成
反应生成 和
和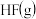 的热化学方程式:
的热化学方程式:_______ 。

(1)上述
 个装置中,不能证明“铜与浓硝酸反应是吸热反应还是放热反应”的是
个装置中,不能证明“铜与浓硝酸反应是吸热反应还是放热反应”的是 不能用手触摸和使用温度计
不能用手触摸和使用温度计
(2)某同学选用装置Ⅰ进行实验
 实验前
实验前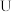 形管里液面左右相平
形管里液面左右相平 ,在甲试管里加入适量氢氧化钠溶液与稀盐酸,
,在甲试管里加入适量氢氧化钠溶液与稀盐酸,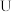 形管中可观察到的现象是
形管中可观察到的现象是 填“吸热”或“放热”
填“吸热”或“放热” 反应。
反应。(3)为定量测定(2)中反应的反应热,使
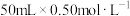 盐酸与
盐酸与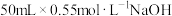 溶液在简易量热计中进行中和反应。该实验中
溶液在简易量热计中进行中和反应。该实验中 的浓度大于
的浓度大于 的浓度的作用是
的浓度的作用是(4)已知一些化学键的键能数据如表所示:
| 化学键 |  |  |  |  |
键能 | 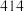 | 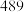 |  | 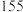 |
 和
和 反应生成
反应生成 和
和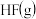 的热化学方程式:
的热化学方程式:
您最近一年使用:0次
解题方法
8 . 某化学兴趣小组进行了下列实验。
实验1:
(1)实验1-2中,燃烧的蜡烛熄灭的原因是___________ 。
(2)实验1-3中,反应生成氧气的化学方程式为___________ 。
实验2:
【提出问题】实验1-3中燃烧的蜡烛为什么会熄灭?
【猜想】I.蜡烛燃烧生成的二氧化碳导致其熄灭。
II.过氧化氢分解时吸收热量,蜡烛周围的温度降低到着火点以下,导致其熄灭。
III.过氧化氢分解产生的水雾导致蜡烛熄灭。
【进行实验】
【解释与结论】
(3)甲同学认为猜想I不成立,他的依据是___________ 。
(4)通过实验验证,可以得出猜想___________ (填序号)成立。
【反思与评价】
(5)依据上述实验,若保持实验1-3中蜡烛不熄灭,可采用的方法有___________ 。
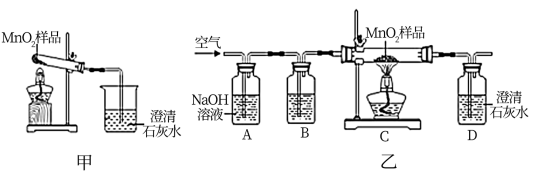
实验3:取实验1、2中使用的二氧化锰样品进行图甲实验,加热时发现导管口有气泡产生,澄清石灰水变浑浊。于是小组同学对气体来源进行探究。
【猜想】二氧化锰样品中可能混有炭粉,炭粉发生反应生成了该气体。
(6)【进行实验】利用图乙所示的装置进行实验,其中B装置的作用是检验A中的反应是否完全,则B中的试剂是___________ ,实验中观察到D处澄清石灰水变浑浊。他们又用氮气代替空气(氮气不参与该实验中的任何反应),重复上述实验,发现D处澄清的石灰水也变浑浊。
(7)【结论】通过实验证明,二氧化锰中混有炭粉,炭粉与___________ 反应产生了二氧化碳。
实验1:
| 序号 | 1-1 | 1-2 | 1-3 |
| 操作 | 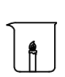 | 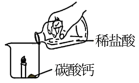 | 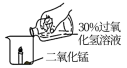 |
| 现象 | 燃烧的蜡烛保持原状 | 燃烧的蜡烛熄灭 | 剧烈反应,有大量气泡和水雾生成,燃烧的蜡烛熄灭了 |
(2)实验1-3中,反应生成氧气的化学方程式为
实验2:
【提出问题】实验1-3中燃烧的蜡烛为什么会熄灭?
【猜想】I.蜡烛燃烧生成的二氧化碳导致其熄灭。
II.过氧化氢分解时吸收热量,蜡烛周围的温度降低到着火点以下,导致其熄灭。
III.过氧化氢分解产生的水雾导致蜡烛熄灭。
【进行实验】
| 序号 | 2-1 | 2-2 | 2-3 |
| 操作 | 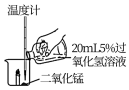 | 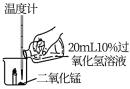 |  |
| 现象 | 有气泡产生,蜡烛火焰无明显变化,温度升高不明显 | 有较多气泡和少量水雾产生,蜡烛燃烧更旺,火焰明亮,温度升高较明显 | 剧烈反应,有大量气泡和水雾生成,燃烧的蜡烛熄灭,温度升高明显。 |
(3)甲同学认为猜想I不成立,他的依据是
(4)通过实验验证,可以得出猜想
【反思与评价】
(5)依据上述实验,若保持实验1-3中蜡烛不熄灭,可采用的方法有
实验3:取实验1、2中使用的二氧化锰样品进行图甲实验,加热时发现导管口有气泡产生,澄清石灰水变浑浊。于是小组同学对气体来源进行探究。

【猜想】二氧化锰样品中可能混有炭粉,炭粉发生反应生成了该气体。
(6)【进行实验】利用图乙所示的装置进行实验,其中B装置的作用是检验A中的反应是否完全,则B中的试剂是
(7)【结论】通过实验证明,二氧化锰中混有炭粉,炭粉与
您最近一年使用:0次
解题方法
9 . 为了探究化学能与热能的转化,某实验小组设计了如图所示三套实验装置:

(1)上述3个装置中,不能用于探究“镁与稀盐酸反应是吸热反应还是放热反应”的是___________ (选填“I”、“II”或“III”)。:
(2)某同学选用装置I进行实验(实验前U形管里液面左右相平),在甲试管里加入适量氢氧化钡溶液与稀硫酸,U形管中可观察到的现象是___________ ,说明该反应属于___________ (选填“吸热”或“放热”)反应。
(3)为探究固体M溶于水的热效应,选择装置II进行实验(在甲试管中进行)。
①若M为钠,则实验过程中烧杯中可观察到的现象是___________ 。
②若观察到烧杯里产生气泡,则说明M溶于水___________ (选填“一定是放热反应”、“一定是吸热反应”或“可能是放热反应”);
③若实验过程中观察到烧杯里的导管内形成一段水柱,则M可能是___________ 。
(4)至少有两种实验方法能证明超氧化钾与水的反应(4KO2+2H2O=4KOH+3O2↑)是放热反应还是吸热反应。
方法①:选择上述装置___________ 进行实验;
方法②:取适量超氧化钾粉末用脱脂棉包裹并放在石棉网上,向脱脂棉上滴加几滴蒸馏水,片刻后,若观察到棉花燃烧,则说明该反应是___________ (选填“吸热”或“放热”)反应。

(1)上述3个装置中,不能用于探究“镁与稀盐酸反应是吸热反应还是放热反应”的是
(2)某同学选用装置I进行实验(实验前U形管里液面左右相平),在甲试管里加入适量氢氧化钡溶液与稀硫酸,U形管中可观察到的现象是
(3)为探究固体M溶于水的热效应,选择装置II进行实验(在甲试管中进行)。
①若M为钠,则实验过程中烧杯中可观察到的现象是
②若观察到烧杯里产生气泡,则说明M溶于水
③若实验过程中观察到烧杯里的导管内形成一段水柱,则M可能是
(4)至少有两种实验方法能证明超氧化钾与水的反应(4KO2+2H2O=4KOH+3O2↑)是放热反应还是吸热反应。
方法①:选择上述装置
方法②:取适量超氧化钾粉末用脱脂棉包裹并放在石棉网上,向脱脂棉上滴加几滴蒸馏水,片刻后,若观察到棉花燃烧,则说明该反应是
您最近一年使用:0次
2021-11-14更新
|
374次组卷
|
3卷引用:山西省吕梁市柳林县2021-2022学年高二上学期期中考试化学试题
10 . I.如图是某锌-铜原电池装置的示意图:Zn:65
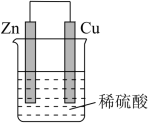
(1)负极的反应式为_______ ,外电路中每转移NA个电子,负极电极质量减小_______ 克。
(2)某电化学装置如图所示(电极a、b均为碳棒)。
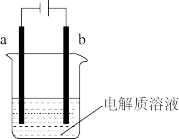
烧杯中盛有100mL 0.2mol/L CuSO4溶液。通电反应一段时间,在两极收集到的气体体积相等 ,则此段时间e-转移的物质的量为_______ mol。
Ⅱ.为了探究化学能与热能的转化,某实验小组设计了如下三套实验装置:
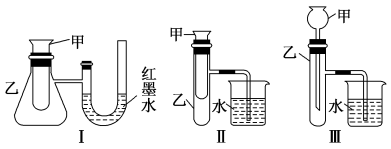
(3)上述装置中,能用来证明“锌和稀硫酸反应是吸热反应还是放热反应”的是_______ (填序号)。
(4)某同学选用装置I进行实验(实验前U形管里液面左右相平),在甲试管里加入食盐水和稀盐酸,再加入一生铁块。一段时间后U形管中可观察到的现象是_______ 。

(1)负极的反应式为
(2)某电化学装置如图所示(电极a、b均为碳棒)。

烧杯中盛有100mL 0.2mol/L CuSO4溶液。通电反应一段时间,在
Ⅱ.为了探究化学能与热能的转化,某实验小组设计了如下三套实验装置:

(3)上述装置中,能用来证明“锌和稀硫酸反应是吸热反应还是放热反应”的是
(4)某同学选用装置I进行实验(实验前U形管里液面左右相平),在甲试管里加入食盐水和稀盐酸,再加入一生铁块。一段时间后U形管中可观察到的现象是
您最近一年使用:0次



