解题方法
1 . I.研究化学反应中的能量变化可以为提高工业生产效率提供指导性的理论依据。请结合所学化学反应原理相关知识回答下列问题:
(1)计算化学反应中的能量变化有多种途径。通过化学键的键能计算。已知:
计算可得:

_______  。
。
(2)通过盖斯定律计算。已知下列反应的反应热为:
①CH3COOH(l)+2O2(g)=2CO2(g)+2H2O(l) ΔH=−870.3kJ∙mol−1
②C(s)+O2(g)=CO2(g) ΔH=−393.5kJ∙mol−1
③H2(g)+ O2(g)=H2O(l) ΔH=−285.8kJ∙mol−1。
O2(g)=H2O(l) ΔH=−285.8kJ∙mol−1。
试计算下列反应的反应热:2C(s)+2H2(g)+O2(g)=CH3COOH(l) ΔH=_______  。
。
Ⅱ.某温度时,在一个容积为 的密闭容器中,
的密闭容器中,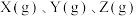 三种物质的物质的量随时间的变化曲线如图所示。根据图中数据,填写下列空白。
三种物质的物质的量随时间的变化曲线如图所示。根据图中数据,填写下列空白。

(3)该反应的化学方程式为_______ 。
(4)反应开始至 ,气体
,气体 的平均反应速率
的平均反应速率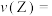
_______ mol∙L-1.min-1。
(5)反应开始至 ,气体X的转化率
,气体X的转化率_______ 。
Ⅲ.现有反应aA(g)+bB(g)⇌pC(g),达到平衡后,当升高温度时,B的浓度减小;当减小压强时,混合体系中C的质量分数也减小,则:
(6)该反应是_______ 热反应,且a+b_______ p(填“>”“<”或“=”)。
(7)减压时,A的质量分数_______ (填“增大”“减小”或“不变”,下同),正反应速率_______ 。
(8)若降低温度,则平衡时,B、C的浓度之比c(B)/c(C)将_______ 。
(9)若B是有色物质,A、C均为无色物质,则加入C(体积不变)时混合物的颜色_______ (填“变浅”“变深”或“不变”)。
(1)计算化学反应中的能量变化有多种途径。通过化学键的键能计算。已知:
| 化学键 |  |  |  |
键能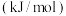 | 436 | 247 | 434 |


 。
。(2)通过盖斯定律计算。已知下列反应的反应热为:
①CH3COOH(l)+2O2(g)=2CO2(g)+2H2O(l) ΔH=−870.3kJ∙mol−1
②C(s)+O2(g)=CO2(g) ΔH=−393.5kJ∙mol−1
③H2(g)+
 O2(g)=H2O(l) ΔH=−285.8kJ∙mol−1。
O2(g)=H2O(l) ΔH=−285.8kJ∙mol−1。试计算下列反应的反应热:2C(s)+2H2(g)+O2(g)=CH3COOH(l) ΔH=
 。
。Ⅱ.某温度时,在一个容积为
 的密闭容器中,
的密闭容器中,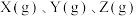 三种物质的物质的量随时间的变化曲线如图所示。根据图中数据,填写下列空白。
三种物质的物质的量随时间的变化曲线如图所示。根据图中数据,填写下列空白。
(3)该反应的化学方程式为
(4)反应开始至
 ,气体
,气体 的平均反应速率
的平均反应速率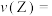
(5)反应开始至
 ,气体X的转化率
,气体X的转化率Ⅲ.现有反应aA(g)+bB(g)⇌pC(g),达到平衡后,当升高温度时,B的浓度减小;当减小压强时,混合体系中C的质量分数也减小,则:
(6)该反应是
(7)减压时,A的质量分数
(8)若降低温度,则平衡时,B、C的浓度之比c(B)/c(C)将
(9)若B是有色物质,A、C均为无色物质,则加入C(体积不变)时混合物的颜色
您最近一年使用:0次
2 . 我国政府庄严承诺,到2020年,单位GDP二氧化碳排放比2005年下降40%~50%。CO2可转化成有机物实现碳循环有效降低碳排放。
(1)在体积为2 L的恒容密闭容器中,充入2 mol CO2和6 mol H2,一定条件下反应:CO2(g)+3H2(g) CH3OH(g)+H2O(g) △H=-49.0 kJ·mol-1,测得CO2和CH3OH(g)浓度随时间变化如图所示。
CH3OH(g)+H2O(g) △H=-49.0 kJ·mol-1,测得CO2和CH3OH(g)浓度随时间变化如图所示。
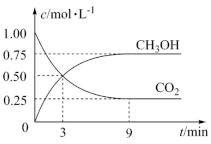
①计算:从0 min到3 min,H2的平均反应速率v(H2)=_______ mol·L-1·min-1。
②能说明上述反应达到平衡状态的是_______ (填序号)
A.c(CO2)∶c(H2)=1∶3
B.混合气体的密度不再发生变化
C.单位时间内消耗3molH2,同时生成l mol H2O
D.CO2的体积分数在混合气体中保持不变
③反应达到平衡后,保持其他条件不变,能加快反应速率且使体系中气体的物质的量减少,可采取的措施有_______ (填编号)
A.升高温度 B.缩小容器体积 C.再充入CO2气体 D.使用合适的催化剂
(2)在容积相同的密闭容器里,分别充入等量的氮气和氢气,在不同温度下发生反应:N2(g)+3H2(g) 2NH3(g),并分别在相同的时间内测定其中NH3的质量分数(y轴所表示的),绘成图象如图所示,请回答:
2NH3(g),并分别在相同的时间内测定其中NH3的质量分数(y轴所表示的),绘成图象如图所示,请回答:
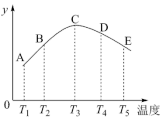
①A、B、C、D、E五点中,肯定未达到平衡点的是_______ 。
②此可逆反应的正反应是_______ 热反应(填“吸”或“放”)。
(1)在体积为2 L的恒容密闭容器中,充入2 mol CO2和6 mol H2,一定条件下反应:CO2(g)+3H2(g)
 CH3OH(g)+H2O(g) △H=-49.0 kJ·mol-1,测得CO2和CH3OH(g)浓度随时间变化如图所示。
CH3OH(g)+H2O(g) △H=-49.0 kJ·mol-1,测得CO2和CH3OH(g)浓度随时间变化如图所示。
①计算:从0 min到3 min,H2的平均反应速率v(H2)=
②能说明上述反应达到平衡状态的是
A.c(CO2)∶c(H2)=1∶3
B.混合气体的密度不再发生变化
C.单位时间内消耗3molH2,同时生成l mol H2O
D.CO2的体积分数在混合气体中保持不变
③反应达到平衡后,保持其他条件不变,能加快反应速率且使体系中气体的物质的量减少,可采取的措施有
A.升高温度 B.缩小容器体积 C.再充入CO2气体 D.使用合适的催化剂
(2)在容积相同的密闭容器里,分别充入等量的氮气和氢气,在不同温度下发生反应:N2(g)+3H2(g)
 2NH3(g),并分别在相同的时间内测定其中NH3的质量分数(y轴所表示的),绘成图象如图所示,请回答:
2NH3(g),并分别在相同的时间内测定其中NH3的质量分数(y轴所表示的),绘成图象如图所示,请回答:
①A、B、C、D、E五点中,肯定未达到平衡点的是
②此可逆反应的正反应是
您最近一年使用:0次
名校
解题方法
3 . 我国力争2030年前实现碳达峰,2060年前实现碳中和。 的捕集利用已成为科学家们研究的重要课题。
的捕集利用已成为科学家们研究的重要课题。 加氢可转化为二甲醚
加氢可转化为二甲醚 ,反应原理为:
,反应原理为: 。该反应的能量变化如图所示。
。该反应的能量变化如图所示。
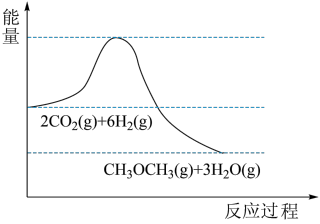
回答问题:
(1)该反应为_____ (填“放热”或“吸热”)反应。
(2)在固定体积的密闭容器中发生该反应,能说明该反应达到平衡状态的是_____ (填字母)。
a. 的含量保持不变
的含量保持不变
b.混合气体的密度不变
c.混合气体的平均相对分子质量不变
d.
(3)在体积为 密闭容器中充入
密闭容器中充入 和
和 ,测得
,测得 、
、 的物质的量随时间变化如图所示。
的物质的量随时间变化如图所示。
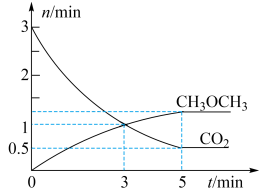

回答下列问题:
① 内,
内,
_____ 。
②反应达到平衡状态时, 的体积分数为
的体积分数为_____ %(保留1位小数)。
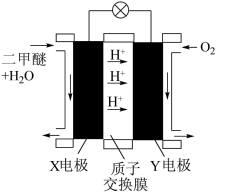
③“二甲醚 酸性燃料池”的工作原理示意图如图所示。X电极反应式
酸性燃料池”的工作原理示意图如图所示。X电极反应式_____ ;若此燃料电池电路中转移 电子,则消耗的
电子,则消耗的 在标准状况下的体积为
在标准状况下的体积为_____ L。
(4)实验室用 溶液与
溶液与 溶液反应探究条件的改变对化学反应速率的影响,设计的实验方案如下表(已知
溶液反应探究条件的改变对化学反应速率的影响,设计的实验方案如下表(已知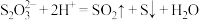 ):
):
①对比实验1和2可探究_____ 因素对化学反应速率的影响。
②对比实验1和3来探究浓度对化学反应速率的影响,则
_____ 。
 的捕集利用已成为科学家们研究的重要课题。
的捕集利用已成为科学家们研究的重要课题。 加氢可转化为二甲醚
加氢可转化为二甲醚 ,反应原理为:
,反应原理为: 。该反应的能量变化如图所示。
。该反应的能量变化如图所示。
回答问题:
(1)该反应为
(2)在固定体积的密闭容器中发生该反应,能说明该反应达到平衡状态的是
a.
 的含量保持不变
的含量保持不变b.混合气体的密度不变
c.混合气体的平均相对分子质量不变
d.

(3)在体积为
 密闭容器中充入
密闭容器中充入 和
和 ,测得
,测得 、
、 的物质的量随时间变化如图所示。
的物质的量随时间变化如图所示。

回答下列问题:
①
 内,
内,
②反应达到平衡状态时,
 的体积分数为
的体积分数为③“二甲醚
 酸性燃料池”的工作原理示意图如图所示。X电极反应式
酸性燃料池”的工作原理示意图如图所示。X电极反应式 电子,则消耗的
电子,则消耗的 在标准状况下的体积为
在标准状况下的体积为
(4)实验室用
 溶液与
溶液与 溶液反应探究条件的改变对化学反应速率的影响,设计的实验方案如下表(已知
溶液反应探究条件的改变对化学反应速率的影响,设计的实验方案如下表(已知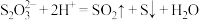 ):
):| 实验序号 | 体积/mL | 温度/℃ | 溶液出现浑浊的时间/s | ||
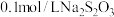 溶液 溶液 | 水 | 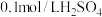 溶液 溶液 | |||
| 1 | 2.0 | 0.0 | 2.0 | 25 | 8 |
| 2 | 2.0 | 0.0 | 2.0 | 50 | 5 |
| 3 | 1.0 | V | 2.0 | 25 | 10 |
②对比实验1和3来探究浓度对化学反应速率的影响,则

您最近一年使用:0次
2023-08-15更新
|
266次组卷
|
2卷引用:新疆生产建设兵团第三师图木舒克市第一中学2023-2024学年高二下学期开学考试化学试卷
名校
解题方法
4 . SO2、NOx的含量是衡量大气污染的一个重要指标。工业上常采用催化还原法或吸收法处理SO2,催化还原SO2不仅可以消除SO2污染,而且可以得到有价值的中单质硫,采取氨水吸收NOx的方法去除NOx的污染,生成硝酸铵。
(1)已知CH4和S的燃烧热分别为a kJ/mol和bkJ/mol。在复合组分催化剂作用下,甲烷可使SO2转化为S,同时生成CO2和液态水,该反应的热化方程式为___________ 。
(2)用H2还原SO2生成S的反应分两步完成,如图甲所示,该过程中相关物质的物质的量浓度随时间的变化关系如图乙所示:
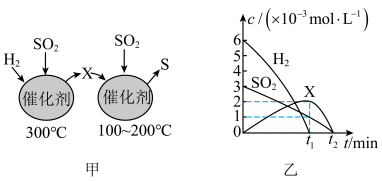
分析可知X为___________ (写化学式);0-t1时间段的反应温度为___________ ,0-t1时间段用SO2表示的化学反应速率为___________ 。
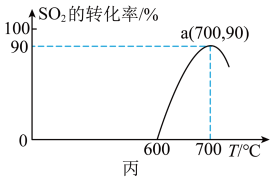
(3)焦炭催化还原SO2生成S2的化学方程式为 2C(s)+2SO2 (g)=S2(g)+2CO2(g)。在恒容容器中,浓度为1mol/L的SO2与足量焦炭反应,SO2的转化率随温度的变化如图丙所示。700℃时该反应的平衡常数为___________ 。
(4)25℃时,用1mol/L的Na2SO3溶液吸收SO2,当溶液的pH=7时,溶液中各离子浓度的大小关系为___________ 。(已知:H2SO3的电离常数Ka1=1.3×10-2,Ka2=6.2×10-8)
(5)利用双离子交换膜电解法可以从含硝酸铵的工业废水里生产硝酸和氨。阳极室得到的物质是___________ ,写出阳极反应方程式___________ ;阴极室得到的物质是___________ ,写出阴极反应及获得相应物质的方程式___________ 、___________ 。
(1)已知CH4和S的燃烧热分别为a kJ/mol和bkJ/mol。在复合组分催化剂作用下,甲烷可使SO2转化为S,同时生成CO2和液态水,该反应的热化方程式为
(2)用H2还原SO2生成S的反应分两步完成,如图甲所示,该过程中相关物质的物质的量浓度随时间的变化关系如图乙所示:

分析可知X为
(3)焦炭催化还原SO2生成S2的化学方程式为 2C(s)+2SO2 (g)=S2(g)+2CO2(g)。在恒容容器中,浓度为1mol/L的SO2与足量焦炭反应,SO2的转化率随温度的变化如图丙所示。700℃时该反应的平衡常数为

(4)25℃时,用1mol/L的Na2SO3溶液吸收SO2,当溶液的pH=7时,溶液中各离子浓度的大小关系为
(5)利用双离子交换膜电解法可以从含硝酸铵的工业废水里生产硝酸和氨。阳极室得到的物质是
您最近一年使用:0次
5 . 由于温室效应和资源短缺等问题,如何降低大气中的CO2含量并加以开发利用引起了各界的普遍重视。目前工业上有一种方法是用CO2生产燃料甲醇。一定条件下发生反应:CO2(g)+3H2(g)  CH3OH(g)+H2O(g),该反应的能量变化如图所示:
CH3OH(g)+H2O(g),该反应的能量变化如图所示:

(1)上述反应平衡常数K的表达式为_______ ,温度降低,平衡常K_______ (填“增大”、“不变”或“减小”)。
(2)在体积为2L的密闭容器中,充入1molCO2和3molH2,测得5min末CO2的物质的量变化了0.5mol。从反应开始到5min末,用氢气浓度变化表示的平均反应速率v(H2)=_______ 。
(3)在相同温度容积不变的条件下,能说明该反应已达平衡状态的是_______(填写序号字母)。
 CH3OH(g)+H2O(g),该反应的能量变化如图所示:
CH3OH(g)+H2O(g),该反应的能量变化如图所示:
(1)上述反应平衡常数K的表达式为
(2)在体积为2L的密闭容器中,充入1molCO2和3molH2,测得5min末CO2的物质的量变化了0.5mol。从反应开始到5min末,用氢气浓度变化表示的平均反应速率v(H2)=
(3)在相同温度容积不变的条件下,能说明该反应已达平衡状态的是_______(填写序号字母)。
| A.n(CO2)∶n(H2)∶n(CH3OH)∶n(H2O)=1∶3∶1∶1 | B.容器内压强保持不变 |
| C.H2的消耗速率与CH3OH的消耗速率之比为3∶1 | D.容器内的密度保持不变 |
您最近一年使用:0次
6 . 氮是动植物生长不可缺少的元素,合成氨反应中的能量变化如图所示。

(1)反应过程中断裂的化学键有___________ 。
(2)该反应是___________ 反应(填“吸热”或“放热”),生成1mol (g)的能量变化为
(g)的能量变化为___________ kJ(用含 、
、 的代数式表示)。
的代数式表示)。
(3)下列措施能提高合成氨反应速率的有___________(填字母序号)。
(4)在体积为2L的密闭容器中,加入1mol 、3mol
、3mol ,反应过程中物质的浓度随时间变化的关系如图所示。
,反应过程中物质的浓度随时间变化的关系如图所示。

①0~ 时间段内,用
时间段内,用 表示的反应速率
表示的反应速率
___________  (用含
(用含 的代数式表示)。
的代数式表示)。
②反应进行到 时,下列各项能表明反应达到化学平衡状态的是
时,下列各项能表明反应达到化学平衡状态的是___________ (填字母序号)。
A.容器中气体的密度不变
B.容器中气体的压强不变
C.氨气的百分含量不变
D.消耗3mol 的同时生成
的同时生成

(1)反应过程中断裂的化学键有
(2)该反应是
 (g)的能量变化为
(g)的能量变化为 、
、 的代数式表示)。
的代数式表示)。(3)下列措施能提高合成氨反应速率的有___________(填字母序号)。
| A.使用高效催化剂 | B.恒温恒容再充入氢气 |
| C.降低反应温度 | D.扩大容器容积 |
 、3mol
、3mol ,反应过程中物质的浓度随时间变化的关系如图所示。
,反应过程中物质的浓度随时间变化的关系如图所示。
①0~
 时间段内,用
时间段内,用 表示的反应速率
表示的反应速率
 (用含
(用含 的代数式表示)。
的代数式表示)。②反应进行到
 时,下列各项能表明反应达到化学平衡状态的是
时,下列各项能表明反应达到化学平衡状态的是A.容器中气体的密度不变
B.容器中气体的压强不变
C.氨气的百分含量不变
D.消耗3mol
 的同时生成
的同时生成
您最近一年使用:0次
2022-07-02更新
|
152次组卷
|
2卷引用:新疆阿勒泰地区2022-2023学年高一下学期期末考试化学试题
名校
解题方法
7 . Ⅰ.回答下列问题:
(1)反应 常用于精盐中碘含量测定。某同学利用该反应探究浓度对反应速率的影响。实验时均加入1mL淀粉溶液作指示剂,若不经计算,直接通过褪色时间的长短判断浓度与反应速率的关系,下列试剂中应选择
常用于精盐中碘含量测定。某同学利用该反应探究浓度对反应速率的影响。实验时均加入1mL淀粉溶液作指示剂,若不经计算,直接通过褪色时间的长短判断浓度与反应速率的关系,下列试剂中应选择_________ (填序号)。
①1mL0.006mol·L-1的碘水 ②1mL0.06mol·L-1的碘水
③4mL0.06mol·L-1的 Na2S2O3溶液 ④4mL0.006mol·L-1的Na2S2O3溶液
(2)若某同学选取②③进行实验,测得褪色时间为4s,计算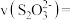
_________ 。
Ⅱ.将一定量纯净的氨基甲酸铵(NH2COONH4)置于特制的密闭真空容器中(假设容器体积不变,固体试样体积忽略不计),在恒定温度下使其达到分解平衡:NH2COONH4(s) 2NH3(g)+CO2(g)。
2NH3(g)+CO2(g)。
(3)下列不能判断该分解反应已经达到化学平衡状态的是_________ (填选项);
A.密闭容器中氨气的物质的量不变 B.2v生(NH3)=v耗(CO2)
C.形成6个N-H键的同时有2个C=O键断裂 D.密闭容器中总压强保持不变
E.容器中CO2与NH3的物质的量之比保持不变
III.在2L密闭容器内,800℃时反应: 2NO(g)+O2(g) 2NO2(g)体系中,n(NO)随时间的变化如表:
2NO2(g)体系中,n(NO)随时间的变化如表:
(4)下图中表示NO2的变化的曲线_____ (填字母);
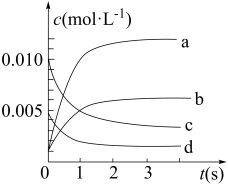
(5)800℃,0~2s内,NO的转化率是___________ ;
(6)用NO表示该反应从起始到平衡时间内的平均速率v=___________ 。
(1)反应
 常用于精盐中碘含量测定。某同学利用该反应探究浓度对反应速率的影响。实验时均加入1mL淀粉溶液作指示剂,若不经计算,直接通过褪色时间的长短判断浓度与反应速率的关系,下列试剂中应选择
常用于精盐中碘含量测定。某同学利用该反应探究浓度对反应速率的影响。实验时均加入1mL淀粉溶液作指示剂,若不经计算,直接通过褪色时间的长短判断浓度与反应速率的关系,下列试剂中应选择①1mL0.006mol·L-1的碘水 ②1mL0.06mol·L-1的碘水
③4mL0.06mol·L-1的 Na2S2O3溶液 ④4mL0.006mol·L-1的Na2S2O3溶液
(2)若某同学选取②③进行实验,测得褪色时间为4s,计算
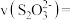
Ⅱ.将一定量纯净的氨基甲酸铵(NH2COONH4)置于特制的密闭真空容器中(假设容器体积不变,固体试样体积忽略不计),在恒定温度下使其达到分解平衡:NH2COONH4(s)
 2NH3(g)+CO2(g)。
2NH3(g)+CO2(g)。(3)下列不能判断该分解反应已经达到化学平衡状态的是
A.密闭容器中氨气的物质的量不变 B.2v生(NH3)=v耗(CO2)
C.形成6个N-H键的同时有2个C=O键断裂 D.密闭容器中总压强保持不变
E.容器中CO2与NH3的物质的量之比保持不变
III.在2L密闭容器内,800℃时反应: 2NO(g)+O2(g)
 2NO2(g)体系中,n(NO)随时间的变化如表:
2NO2(g)体系中,n(NO)随时间的变化如表:| 时间(s) | 0 | 1 | 2 | 3 | 4 | 5 |
| n(NO)(mol) | 0.020 | 0.010 | 0.006 | 0.0048 | 0.004 | 0.004 |

(5)800℃,0~2s内,NO的转化率是
(6)用NO表示该反应从起始到平衡时间内的平均速率v=
您最近一年使用:0次
8 . T℃时,在2L刚性密闭容器中使X(g)与Y(g)发生反应生成Z(g)。反应过程中X、Y、Z的浓度变化如图1所示;若保持其他条件不变,温度分别为T1和T2时,Y的体积百分含量与时间的关系如图2所示。则下列结论错误 的是


A.容器中发生的反应可表示为3X(g)+Y(g) 2Z(g) 2Z(g) |
| B.保持其他条件不变,升高温度,X的转化率增大 |
| C.反应进行的前3min内,用X表示的反应速率v(X)=0.2mol·L-1·min-1 |
| D.若改变反应条件,使反应进程如图3所示,则改变的条件是使用催化剂 |
您最近一年使用:0次
2022-07-28更新
|
327次组卷
|
2卷引用:新疆乌鲁木齐市第八中学2022-2023学年高二上学期期中考试化学试题
9 . I.在恒温恒容的密闭容器中,当下列物理量不再发生变化时:①混合气体的压强 ②混合气体的密度③混合气体的总物质的量 ④混合气体的平均相对分子质量 ⑤混合气体的颜色。
(1)一定能证明2SO2(g)+O2(g) 2SO3(g)达到平衡状态的是
2SO3(g)达到平衡状态的是______ (填序号,下同)。
(2)一定能证明 A(s)+2B(g) C(g)+D(g)达到平衡状态的是
C(g)+D(g)达到平衡状态的是_______ 。(注:B、C、D均为无色物质)
II.某温度时,在一个1L的恒容容器中,X、Y、Z均为气体,三种物质的物质的量随时间的变化曲线如图所示。根据图中数据填空:
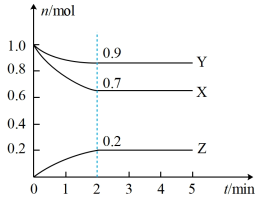
(1)反应开始至2min,以气体Y表示的平均反应速率为________ ;
(2)该反应的化学方程式为___________ ;
(3)X的转化率___________ ,生成的Z的百分含量___________
(4)amolX与bmolY的混合气体发生上述反应,反应到某时刻各物质的量恰好满足:n(X)=n(Y)=2n(Z),则原混合气体中a:b=___________ 。
(1)一定能证明2SO2(g)+O2(g)
 2SO3(g)达到平衡状态的是
2SO3(g)达到平衡状态的是(2)一定能证明 A(s)+2B(g)
 C(g)+D(g)达到平衡状态的是
C(g)+D(g)达到平衡状态的是II.某温度时,在一个1L的恒容容器中,X、Y、Z均为气体,三种物质的物质的量随时间的变化曲线如图所示。根据图中数据填空:

(1)反应开始至2min,以气体Y表示的平均反应速率为
(2)该反应的化学方程式为
(3)X的转化率
(4)amolX与bmolY的混合气体发生上述反应,反应到某时刻各物质的量恰好满足:n(X)=n(Y)=2n(Z),则原混合气体中a:b=
您最近一年使用:0次
名校
解题方法
10 . 氮是地球上含量丰富的一种元素,氮及其化合物在工农业生产、生活中有着重要作用,合成氨工业在国民生产中有重要意义。以下是关于合成氨的有关问题,请回答:
(1)若在一容积为2L的密闭容器中加入0.2mol的N2和0.6mol的H2在一定条件下发生反应:N2(g)+3H2(g) 2NH3(g)ΔH<0,若在5分钟时反应达到平衡,此时测得NH3的物质的量为0.2mol。则前5分钟的平均反应速率v(N2)=
2NH3(g)ΔH<0,若在5分钟时反应达到平衡,此时测得NH3的物质的量为0.2mol。则前5分钟的平均反应速率v(N2)=__________ 。平衡时H2的转化率为__________ %。
(2)平衡后,若提高H2的转化率,可以采取的措施有__________ 。
A.加了催化剂
B.增大容器体积
C.降低反应体系的温度
D.加入一定量N2
(3)若在0.5L的密闭容器中,一定量的氮气和氢气进行如下反应:N2(g)+3H2(g) 2NH3(g)ΔH<0,其化学平衡常数K与温度T的关系如表所示:
2NH3(g)ΔH<0,其化学平衡常数K与温度T的关系如表所示:
请完成下列问题:
①试比较K1、K2的大小,K1__________ K2(填“<”“>”或“=”);
②400℃时,反应2NH3(g) N2(g)+3H2(g)的化学平衡常数为
N2(g)+3H2(g)的化学平衡常数为__________ 。当测得NH3、N2和H2物质的量分别为3mol、2mol和1mol时,则该反应的v(N2)正__________ v(N2)逆(填“<”“>”或“=”)。
(4)根据化学反应速率和化学平衡理论,联系合成氨的生产实际,你认为下列说法不正确的是__________ 。
A.化学反应速率理论可指导怎样在一定时间内快出产品
B.勒夏特列原理可指导怎样使用有限原料多出产品
C.催化剂的使用是提高产品产率的有效方法
D.正确利用化学反应速率和化学反应限度理论都可以提高化工生产的综合经济效益
(1)若在一容积为2L的密闭容器中加入0.2mol的N2和0.6mol的H2在一定条件下发生反应:N2(g)+3H2(g)
 2NH3(g)ΔH<0,若在5分钟时反应达到平衡,此时测得NH3的物质的量为0.2mol。则前5分钟的平均反应速率v(N2)=
2NH3(g)ΔH<0,若在5分钟时反应达到平衡,此时测得NH3的物质的量为0.2mol。则前5分钟的平均反应速率v(N2)=(2)平衡后,若提高H2的转化率,可以采取的措施有
A.加了催化剂
B.增大容器体积
C.降低反应体系的温度
D.加入一定量N2
(3)若在0.5L的密闭容器中,一定量的氮气和氢气进行如下反应:N2(g)+3H2(g)
 2NH3(g)ΔH<0,其化学平衡常数K与温度T的关系如表所示:
2NH3(g)ΔH<0,其化学平衡常数K与温度T的关系如表所示:| T/℃ | 200 | 300 | 400 |
| K | K1 | K2 | 0.5 |
①试比较K1、K2的大小,K1
②400℃时,反应2NH3(g)
 N2(g)+3H2(g)的化学平衡常数为
N2(g)+3H2(g)的化学平衡常数为(4)根据化学反应速率和化学平衡理论,联系合成氨的生产实际,你认为下列说法不正确的是
A.化学反应速率理论可指导怎样在一定时间内快出产品
B.勒夏特列原理可指导怎样使用有限原料多出产品
C.催化剂的使用是提高产品产率的有效方法
D.正确利用化学反应速率和化学反应限度理论都可以提高化工生产的综合经济效益
您最近一年使用:0次
2020-06-13更新
|
1377次组卷
|
4卷引用:新疆生产建设兵团第三师图木舒克市第一中学2023-2024学年高二上学期第二次月考试化学试卷



