名校
解题方法
1 . CH3OH、CO、CH4等都是重要的能源,也是重要的化工原料。
(1)为倡导“节能减排”和“低碳经济”,降低大气中CO2的含量,有效地开发利用CO2,工业上可以用CO2来生产甲醇燃料。在体积为2 L的密闭容器中,充入1 mol CO2和3 mol H2,一定条件下发生反应:CO2(g)+3H2(g) CH3OH(g)+H2O(g)。经测得CH3OH和CO2的物质的量随时间变化如图所示。
CH3OH(g)+H2O(g)。经测得CH3OH和CO2的物质的量随时间变化如图所示。
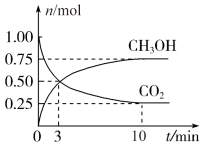
①从反应开始到平衡,CO2的平均反应速率v(CO2)=____ 。
②达到平衡时,H2的浓度为____ mol/L。
(2)工业上也可以用CO和H2为原料制备CH3OH,反应方程式为:CO(g)+2H2(g) CH3OH(g),在一体积固定的密闭容器中投入一定量的CO和H2进行上述反应。下列叙述中能说明上述反应达到平衡状态的是
CH3OH(g),在一体积固定的密闭容器中投入一定量的CO和H2进行上述反应。下列叙述中能说明上述反应达到平衡状态的是____ 。
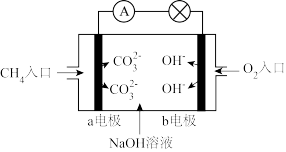
(3)某种甲烷燃料电池的工作原理如图所示氧气通入的一极为电源的____ 极,a电极反应式:____ ,b电极反应式:____ 。
(4)当电路中累计有2 mol电子通过时,消耗的甲烷体积为(在标准状况下)____ L。
(1)为倡导“节能减排”和“低碳经济”,降低大气中CO2的含量,有效地开发利用CO2,工业上可以用CO2来生产甲醇燃料。在体积为2 L的密闭容器中,充入1 mol CO2和3 mol H2,一定条件下发生反应:CO2(g)+3H2(g)
 CH3OH(g)+H2O(g)。经测得CH3OH和CO2的物质的量随时间变化如图所示。
CH3OH(g)+H2O(g)。经测得CH3OH和CO2的物质的量随时间变化如图所示。
①从反应开始到平衡,CO2的平均反应速率v(CO2)=
②达到平衡时,H2的浓度为
(2)工业上也可以用CO和H2为原料制备CH3OH,反应方程式为:CO(g)+2H2(g)
 CH3OH(g),在一体积固定的密闭容器中投入一定量的CO和H2进行上述反应。下列叙述中能说明上述反应达到平衡状态的是
CH3OH(g),在一体积固定的密闭容器中投入一定量的CO和H2进行上述反应。下列叙述中能说明上述反应达到平衡状态的是| A.反应中CO与CH3OH的物质的量之比为1:1 |
| B.混合气体的压强不随时间的变化而变化 |
| C.单位时间内每消耗1 mol CO,同时生成1 mol CH3OH |
| D.CH3OH的质量分数在混合气体中保持不变 |
(4)当电路中累计有2 mol电子通过时,消耗的甲烷体积为(在标准状况下)

您最近一年使用:0次
2022-05-12更新
|
440次组卷
|
3卷引用:河南省南阳市2021-2022学年高一下学期期中质量评估化学试题
名校
解题方法
2 . t℃时,将1mol气体A和1mol气体B充入容积为2L的恒容密闭容器中,发生反应: ,测得4min时体系中有0.4molB和
,测得4min时体系中有0.4molB和 C。请回答下列问题:
C。请回答下列问题:
(1)
______ ,0~4min内用A(g)表示的平均反应速率为______  。
。
(2)下列表述能说明上述反应已经达到平衡状态的是______ (填字母)。
a.相同时间内,消耗A(g)和生成C(g)的物质的量之比为1:2
b.物质B(g)的质量分数不再发生变化
c.混合气体的平均相对分子质量不再发生变化
d.混合气体的密度不再发生变化
(3)某化学兴趣小组的同学为了研究上述反应的反应速率,将A(g)、B(g)在一定条件下反应,测得C(g)的反应速率随时间的变化如图所示。______ (填“放热”或“吸热”)反应,后测得速率为0的原因是______ 。
(4)已知:1molA(g)、B(g)、C(g)中的化学键全部断裂形成气态原子所需要的能量如下表所示。
上述反应在6min时达到平衡,此时测得A的物质的量浓度为 。
。
①A的平衡转化率为______ ( )。
)。
②根据表中数据计算出该反应达到平衡过程中的能量变化为______ kJ(用含x、y、z的代数式表示)。
 ,测得4min时体系中有0.4molB和
,测得4min时体系中有0.4molB和 C。请回答下列问题:
C。请回答下列问题:(1)

 。
。(2)下列表述能说明上述反应已经达到平衡状态的是
a.相同时间内,消耗A(g)和生成C(g)的物质的量之比为1:2
b.物质B(g)的质量分数不再发生变化
c.混合气体的平均相对分子质量不再发生变化
d.混合气体的密度不再发生变化
(3)某化学兴趣小组的同学为了研究上述反应的反应速率,将A(g)、B(g)在一定条件下反应,测得C(g)的反应速率随时间的变化如图所示。

(4)已知:1molA(g)、B(g)、C(g)中的化学键全部断裂形成气态原子所需要的能量如下表所示。
物质 | A | B | C |
能量/( | x | y | z |
 。
。①A的平衡转化率为
 )。
)。②根据表中数据计算出该反应达到平衡过程中的能量变化为
您最近一年使用:0次
3 . 甲醇(CH3OH)是一种重要的化工原料。已知
CH3OH(1) + O2(g) = CO(g) + 2H2O(g) ; △H = -443.64 kJ·mol-1
2CO (g) + O2(g) = 2CO2(g) ; △H = -566.00 kJ·mol-1
H2O(1) = H2O (g) ; △H = +44.00 kJ·mol-1
(1)试写出能表示CH3OH(l)燃烧热的热化学方程式:_______ 。
(2)800℃时A、B、C三种气体在恒容密闭容器中反应时的浓度变化如图所示,分析图像,回答下列问题:
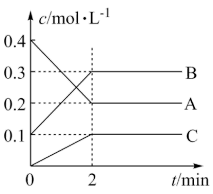
①该反应的方程式为_______ 。
②2min内,用B表示的反应速率为_______ 。
③下列能说明该反应达到平衡状态的是_______ 。
A.体系压强保持不变 B.容器中气体密度保持不变 C.混合气体平均摩尔质量保持不变 D.每消耗2mol A的同时生成1mol C E.A、B、C浓度之比为2:2:1 F.混合气体中A的质量分数保持不变
④为加快该反应的反应速率,可采取的措施是_______ 。
A.恒容通入He B.分离出B C.选择高效的催化剂 D.适当升高体系温度
CH3OH(1) + O2(g) = CO(g) + 2H2O(g) ; △H = -443.64 kJ·mol-1
2CO (g) + O2(g) = 2CO2(g) ; △H = -566.00 kJ·mol-1
H2O(1) = H2O (g) ; △H = +44.00 kJ·mol-1
(1)试写出能表示CH3OH(l)燃烧热的热化学方程式:
(2)800℃时A、B、C三种气体在恒容密闭容器中反应时的浓度变化如图所示,分析图像,回答下列问题:

①该反应的方程式为
②2min内,用B表示的反应速率为
③下列能说明该反应达到平衡状态的是
A.体系压强保持不变 B.容器中气体密度保持不变 C.混合气体平均摩尔质量保持不变 D.每消耗2mol A的同时生成1mol C E.A、B、C浓度之比为2:2:1 F.混合气体中A的质量分数保持不变
④为加快该反应的反应速率,可采取的措施是
A.恒容通入He B.分离出B C.选择高效的催化剂 D.适当升高体系温度
您最近一年使用:0次
4 . 习近平总书记在党的二十大报告中指出“实现碳达峰碳中和是一场广泛而深刻的经济社会系统性变革”。其中研发 的利用技术,将
的利用技术,将 转化为能源是缓解温室效应和解决能源问题的方案之一。请回答下列问题:
转化为能源是缓解温室效应和解决能源问题的方案之一。请回答下列问题:
(1)某科研小组用电化学方法将 转化为
转化为 实现再利用,转化的基本原理如图甲所示。
实现再利用,转化的基本原理如图甲所示。

①M极发生的电极反应式为_______ ;该电池电流流向为_______ (填“M→N”或“N→M”)。
②工作一段时间后,N电极室中的溶液
_______ (填“增大”“减小”或“不变”)。
(2)由 和
和 制备合成气(
制备合成气( 、
、 ),再由合成气制备
),再由合成气制备 的反应转化关系如图乙所示,制备合成气的反应中,若生成
的反应转化关系如图乙所示,制备合成气的反应中,若生成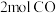 ,反应Ⅰ和Ⅱ中共转移电子的物质的量为
,反应Ⅰ和Ⅱ中共转移电子的物质的量为_______ 。

(3)科学家提出以TO2为催化剂, 光热化学循环分解法,达到减少大气中CO2含量的目的,反应机理和相关数据入图丙所示,全过程的热化学方程式为_______ 。

(4)已知以 、
、 为原料合成
为原料合成 涉及的反应如下:
涉及的反应如下:
反应ⅰ: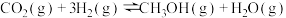
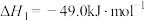
反应ⅱ: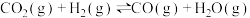
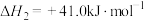
反应ⅲ:

一定温度和催化剂条件下,一定量的 、
、 和
和 (已知
(已知 不参与反应)在总压强为
不参与反应)在总压强为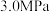 的密闭容器中进行上述反应,平衡时
的密闭容器中进行上述反应,平衡时 的转化率、
的转化率、 和
和 的选择性随温度的变化曲线如图丁所示。
的选择性随温度的变化曲线如图丁所示。

①图丁中曲线b表示物质_______ 的变化(填“ ”“
”“ ”或“
”或“ ”)。
”)。
②某温度下, 反应到达平衡,测得容器中
反应到达平衡,测得容器中 的体积分数为12.5%。此时用
的体积分数为12.5%。此时用 的分压表示
的分压表示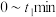 内的反应速率
内的反应速率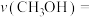
_______  。
。
 的利用技术,将
的利用技术,将 转化为能源是缓解温室效应和解决能源问题的方案之一。请回答下列问题:
转化为能源是缓解温室效应和解决能源问题的方案之一。请回答下列问题:(1)某科研小组用电化学方法将
 转化为
转化为 实现再利用,转化的基本原理如图甲所示。
实现再利用,转化的基本原理如图甲所示。
①M极发生的电极反应式为
②工作一段时间后,N电极室中的溶液

(2)由
 和
和 制备合成气(
制备合成气( 、
、 ),再由合成气制备
),再由合成气制备 的反应转化关系如图乙所示,制备合成气的反应中,若生成
的反应转化关系如图乙所示,制备合成气的反应中,若生成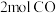 ,反应Ⅰ和Ⅱ中共转移电子的物质的量为
,反应Ⅰ和Ⅱ中共转移电子的物质的量为
(3)科学家提出以TO2为催化剂, 光热化学循环分解法,达到减少大气中CO2含量的目的,反应机理和相关数据入图丙所示,全过程的热化学方程式为

| 物质的量 | 物质 | 完全断键所需吸收的总能量 |
| 1mol |  | 1598kJ |
| 1mol |  | 1072kJ |
| 1mol |  | 496kJ |
 、
、 为原料合成
为原料合成 涉及的反应如下:
涉及的反应如下:反应ⅰ:
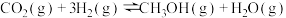
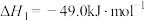
反应ⅱ:
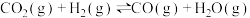
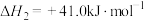
反应ⅲ:


一定温度和催化剂条件下,一定量的
 、
、 和
和 (已知
(已知 不参与反应)在总压强为
不参与反应)在总压强为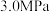 的密闭容器中进行上述反应,平衡时
的密闭容器中进行上述反应,平衡时 的转化率、
的转化率、 和
和 的选择性随温度的变化曲线如图丁所示。
的选择性随温度的变化曲线如图丁所示。
①图丁中曲线b表示物质
 ”“
”“ ”或“
”或“ ”)。
”)。②某温度下,
 反应到达平衡,测得容器中
反应到达平衡,测得容器中 的体积分数为12.5%。此时用
的体积分数为12.5%。此时用 的分压表示
的分压表示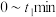 内的反应速率
内的反应速率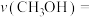
 。
。
您最近一年使用:0次
2023-10-24更新
|
147次组卷
|
2卷引用:湘豫名校联考2023-2024学年高三上学期一轮诊断化学试题
5 . 氮及其化合物在生产生活中有广泛的应用,按要求回答下列问题:
(1)工业合成氨的反应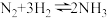 是一个可逆反应,反应条件是高温、高压,并且需要合适的催化剂。已知断裂
是一个可逆反应,反应条件是高温、高压,并且需要合适的催化剂。已知断裂 相应化学键需要的能量如下。若反应生成
相应化学键需要的能量如下。若反应生成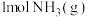 ,可
,可_____ (填“吸收”或“放出”)热量_____  。
。
(2)恒温下,将1molN2和3molH2置于体积为2L的密闭容器中进行反应。若5min时测得氢气浓度为0.9mol/L,则用氨气表示5min内的化学反应速率为_____ mol/(L·min),5min时反应过程体系总压强与初始时的总压强之比为_____
(3)消除NO污染物,可在一定条件下,用CO与NO反应生成CO2和N2,在恒容密闭容中充入4molCO和4molNO发生2CO(g)+2NO(g)⇌N2(g)+2CO2(g)反应。为提高此反应的速率,下列措施可行的是_____(填字母)。
(4)汽车尾气中含有的 是造成城市空气污染的主要因素之一,通过
是造成城市空气污染的主要因素之一,通过 传感器可监测汽车尾气中
传感器可监测汽车尾气中 含量,其工作原理如图所示:
含量,其工作原理如图所示:
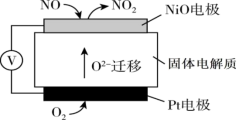
 电极为
电极为_____ (填“正极”或“负极”), 电极上发生的电极反应式为
电极上发生的电极反应式为_____ 。
(1)工业合成氨的反应
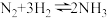 是一个可逆反应,反应条件是高温、高压,并且需要合适的催化剂。已知断裂
是一个可逆反应,反应条件是高温、高压,并且需要合适的催化剂。已知断裂 相应化学键需要的能量如下。若反应生成
相应化学键需要的能量如下。若反应生成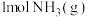 ,可
,可 。
。| 化学键 |  |  |  |
| 能量 |  | 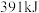 |  |
(2)恒温下,将1molN2和3molH2置于体积为2L的密闭容器中进行反应。若5min时测得氢气浓度为0.9mol/L,则用氨气表示5min内的化学反应速率为
(3)消除NO污染物,可在一定条件下,用CO与NO反应生成CO2和N2,在恒容密闭容中充入4molCO和4molNO发生2CO(g)+2NO(g)⇌N2(g)+2CO2(g)反应。为提高此反应的速率,下列措施可行的是_____(填字母)。
| A.充入氦气 | B.降低温度 | C.使用适合催化剂 | D.移出CO2 |
(4)汽车尾气中含有的
 是造成城市空气污染的主要因素之一,通过
是造成城市空气污染的主要因素之一,通过 传感器可监测汽车尾气中
传感器可监测汽车尾气中 含量,其工作原理如图所示:
含量,其工作原理如图所示:
 电极为
电极为 电极上发生的电极反应式为
电极上发生的电极反应式为
您最近一年使用:0次
名校
6 . 已知有以下有机反应(图1)与反应装置(图2):
下列说法不正确的是

 |  | 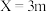 | 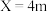 | 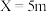 | 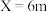 | 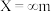 | |
| 物质A | 40% | 30% | 10% | 5% | 4% | 2% | 0% |
| 物质B | 40% | 30% | 10% | 5% | 4% | 2% | 0% |
| 物质C | 15% | 30% | 65% | 60% | 40% | 20% | 1% |
| 物质D | 5% | 10% | 15% | 30% | 52% | 76% | 99% |
| A.物质D相比于物质C在该反应中更稳定 |
| B.反应1的活化能小于反应2的活化能 |
C.增大B气流的流速,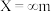 处 处 的比值不变 的比值不变 |
| D.若需提高物质C的产率,可将管道的出口设计相对更远 |
您最近一年使用:0次
2024-02-03更新
|
377次组卷
|
3卷引用:河南省南阳市邓州市第六高级中学校2023-2024学年高二下学期开学测试化学试题
河南省南阳市邓州市第六高级中学校2023-2024学年高二下学期开学测试化学试题 浙江省义乌中学2024届高三上学期首考适应性考试化学试题(已下线)专题06 化学反应速率与化学平衡-【好题汇编】2024年高考化学一模试题分类汇编(全国通用)
7 . 煤的气化和液化是工业上获得清洁能源的重要手段。
I.煤的气化的重要反应为
 。
。
(1)下列叙述能说明上述反应达到平衡状态的是___________(填序号)。
II.煤的液化主要产品是甲醇等,甲醇是一种重要的基础化工原料,工业上可通过多种途径合成甲醇。
(2)二氧化碳和氢气在一定条件下也可合成甲醇:
 。将
。将 和
和 充入1L恒容密闭容器中,在一定条件下合成甲醇,测得
充入1L恒容密闭容器中,在一定条件下合成甲醇,测得 的平衡转化率与温度的关系如图所示:
的平衡转化率与温度的关系如图所示:

①
___________ 0(填“>”或“<”)。
②1150K下,若2min时反应达到平衡,则0~2min内,
___________  。
。
③已知c点时容器内的压强为p,则在1150K下该反应的压强平衡常数
___________ ( 是用气体的分压替代浓度计算的平衡常数,气体分压=总压
是用气体的分压替代浓度计算的平衡常数,气体分压=总压 物质的量分数)。
物质的量分数)。
I.煤的气化的重要反应为

 。
。(1)下列叙述能说明上述反应达到平衡状态的是___________(填序号)。
A.单位时间内生成 的同时生成 的同时生成 |
B.混合气体中组分的质量百分含量: |
C.反应速率 |
| D.在恒温恒容密闭容器中,混合气体的密度不变 |
II.煤的液化主要产品是甲醇等,甲醇是一种重要的基础化工原料,工业上可通过多种途径合成甲醇。
(2)二氧化碳和氢气在一定条件下也可合成甲醇:

 。将
。将 和
和 充入1L恒容密闭容器中,在一定条件下合成甲醇,测得
充入1L恒容密闭容器中,在一定条件下合成甲醇,测得 的平衡转化率与温度的关系如图所示:
的平衡转化率与温度的关系如图所示:
①

②1150K下,若2min时反应达到平衡,则0~2min内,

 。
。③已知c点时容器内的压强为p,则在1150K下该反应的压强平衡常数

 是用气体的分压替代浓度计算的平衡常数,气体分压=总压
是用气体的分压替代浓度计算的平衡常数,气体分压=总压 物质的量分数)。
物质的量分数)。
您最近一年使用:0次
名校
解题方法
8 . 合成氨反应N2(g)+3H2(g) 2NH3(g)是目前最有效的工业固氮方法,解决数亿人口生存问题。
2NH3(g)是目前最有效的工业固氮方法,解决数亿人口生存问题。
(1)反应历程中各步势能变化如图所示,其中吸附在催化剂表面的物种用*标注。
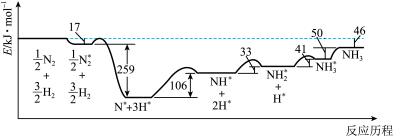
该历程中反应速率最慢的步骤的方程式为________ 。
(2)在T℃、压强为0.9MPa条件下,向一恒压密闭容器中通入 =3的混合气体,体系中各气体的含量与时间变化关系如图所示:
=3的混合气体,体系中各气体的含量与时间变化关系如图所示:

①以下叙述不能 说明该条件下反应达到平衡状态的是_________ (填字母)。
a.氨气的体积分数保持不变
b.容器中 保持不变
保持不变
c.气体平均相对分子质量保持不变
d.气体密度保持不变
e.3v(H2)=v(N2)
②反应20min时达到平衡,则0~20min内v(H2)=________ MPa•min-1,该反应的Kp=_______ MPa-2(保留小数点后两位)。(Kp为以分压表示的平衡常数)
③若起始条件相同,在恒容容器中发生反应,则达到平衡时H2的含量符合图中_________ 点(填“d”“e”“f”或“g”)。
(3)氨化脱硝过程发生反应4NO(g)+4NH3(g)+O2(g)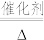 4N2(g)+6H2O(g) △H<0,分析420℃的脱硝效率低于390℃的脱硝效率可能的原因
4N2(g)+6H2O(g) △H<0,分析420℃的脱硝效率低于390℃的脱硝效率可能的原因_________ 。
(4)25℃用甲酸吸收氨气可得到HCOONH4溶液。已知:25℃时甲酸的Ka=1.75×10-5,NH3•H2O的Kb=2×10-5。则反应NH3•H2O+HCOOH HCOO-+NH
HCOO-+NH +H2O的平衡常数K=
+H2O的平衡常数K=________ 。
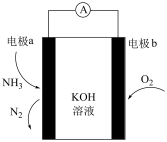
(5)化学气敏传感器可用于监测环境中NH3的含量,其工作原理示意图NH3如图。电极a上的电极反应式为:________ 。
 2NH3(g)是目前最有效的工业固氮方法,解决数亿人口生存问题。
2NH3(g)是目前最有效的工业固氮方法,解决数亿人口生存问题。(1)反应历程中各步势能变化如图所示,其中吸附在催化剂表面的物种用*标注。

该历程中反应速率最慢的步骤的方程式为
(2)在T℃、压强为0.9MPa条件下,向一恒压密闭容器中通入
 =3的混合气体,体系中各气体的含量与时间变化关系如图所示:
=3的混合气体,体系中各气体的含量与时间变化关系如图所示:
①以下叙述
a.氨气的体积分数保持不变
b.容器中
 保持不变
保持不变c.气体平均相对分子质量保持不变
d.气体密度保持不变
e.3v(H2)=v(N2)
②反应20min时达到平衡,则0~20min内v(H2)=
③若起始条件相同,在恒容容器中发生反应,则达到平衡时H2的含量符合图中
(3)氨化脱硝过程发生反应4NO(g)+4NH3(g)+O2(g)
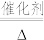 4N2(g)+6H2O(g) △H<0,分析420℃的脱硝效率低于390℃的脱硝效率可能的原因
4N2(g)+6H2O(g) △H<0,分析420℃的脱硝效率低于390℃的脱硝效率可能的原因
(4)25℃用甲酸吸收氨气可得到HCOONH4溶液。已知:25℃时甲酸的Ka=1.75×10-5,NH3•H2O的Kb=2×10-5。则反应NH3•H2O+HCOOH
 HCOO-+NH
HCOO-+NH +H2O的平衡常数K=
+H2O的平衡常数K=(5)化学气敏传感器可用于监测环境中NH3的含量,其工作原理示意图NH3如图。电极a上的电极反应式为:

您最近一年使用:0次
2023-10-17更新
|
209次组卷
|
3卷引用:河南省南阳市第一中学校2023-2024学年高三上学期第三次月考化学试题
9 . 2021年全国两会上“碳达峰”和“碳中和”被首次写入政府工作报告, 的回收和利用越来越受到国际社会的重视。
的回收和利用越来越受到国际社会的重视。
I.利用 合成甲醇。
合成甲醇。
(1)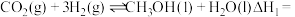
___________ 。
(2) 加氢制甲醇,甲醇与CO是主要产物,发生的平行反应:
加氢制甲醇,甲醇与CO是主要产物,发生的平行反应:
Ⅰ.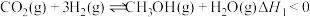
Ⅱ.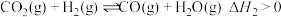
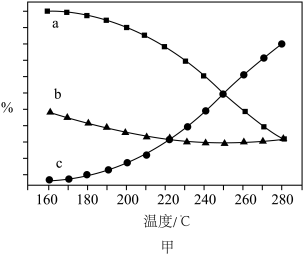
①对于反应 ,
,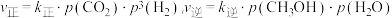 ,其中
,其中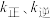 分别为正逆反应速率常数,
分别为正逆反应速率常数, 为气体分压。则升高温度,
为气体分压。则升高温度,
___________ (填“变大”“变小”或“不变”);
②温度对该反应平衡体系中CO、 的百分含量影响如图甲所示,曲线a、b、c对应物质的化学式分别为
的百分含量影响如图甲所示,曲线a、b、c对应物质的化学式分别为___________ 、___________ 、___________ ;
③某温度下,向压强为p的恒容密闭容器中按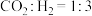 进行投料,若平衡时
进行投料,若平衡时 的产率为0.6,
的产率为0.6, 的物质的量为1.0mol,则平衡时容器内压强为
的物质的量为1.0mol,则平衡时容器内压强为___________ 。
Ⅱ.利用 合成二甲醚
合成二甲醚
(3)合成二甲醚反应: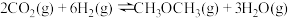 ,将2mol
,将2mol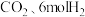 通入容积为2L的恒容密闭容器中合成二甲醚,200℃时容器内
通入容积为2L的恒容密闭容器中合成二甲醚,200℃时容器内 的物质的量随时间的变化如图乙所示:
的物质的量随时间的变化如图乙所示:
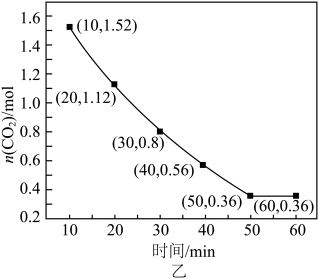
①30~40min内,消耗 的平均反应速率为
的平均反应速率为___________  ;
;
②能说明反应已达平衡状态的是___________ (填标号)。
a.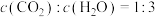
b.断裂2个H-H键,同时断裂2个H-O键
c.密闭容器内压强不变
d.混合气体的密度不变
(4)向一恒容密闭容器中充入3mol 和6mol
和6mol  ,开始测得气体的总压为4.5MPa,在一定温度下合成二甲醚,10min后达到平衡,测得
,开始测得气体的总压为4.5MPa,在一定温度下合成二甲醚,10min后达到平衡,测得 的转化率为50%,该反应的平衡常数
的转化率为50%,该反应的平衡常数
___________ 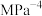 (保留2位有效数字,用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)
(保留2位有效数字,用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)
 的回收和利用越来越受到国际社会的重视。
的回收和利用越来越受到国际社会的重视。I.利用
 合成甲醇。
合成甲醇。| 物质 |  |  |  |
| 燃烧热 |  |  |  |
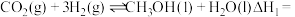
(2)
 加氢制甲醇,甲醇与CO是主要产物,发生的平行反应:
加氢制甲醇,甲醇与CO是主要产物,发生的平行反应:Ⅰ.
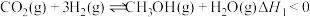
Ⅱ.
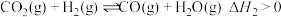
①对于反应
 ,
,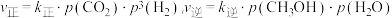 ,其中
,其中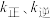 分别为正逆反应速率常数,
分别为正逆反应速率常数, 为气体分压。则升高温度,
为气体分压。则升高温度,
②温度对该反应平衡体系中CO、
 的百分含量影响如图甲所示,曲线a、b、c对应物质的化学式分别为
的百分含量影响如图甲所示,曲线a、b、c对应物质的化学式分别为
③某温度下,向压强为p的恒容密闭容器中按
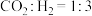 进行投料,若平衡时
进行投料,若平衡时 的产率为0.6,
的产率为0.6, 的物质的量为1.0mol,则平衡时容器内压强为
的物质的量为1.0mol,则平衡时容器内压强为Ⅱ.利用
 合成二甲醚
合成二甲醚(3)合成二甲醚反应:
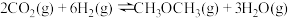 ,将2mol
,将2mol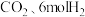 通入容积为2L的恒容密闭容器中合成二甲醚,200℃时容器内
通入容积为2L的恒容密闭容器中合成二甲醚,200℃时容器内 的物质的量随时间的变化如图乙所示:
的物质的量随时间的变化如图乙所示:
①30~40min内,消耗
 的平均反应速率为
的平均反应速率为 ;
;②能说明反应已达平衡状态的是
a.
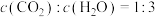
b.断裂2个H-H键,同时断裂2个H-O键
c.密闭容器内压强不变
d.混合气体的密度不变
(4)向一恒容密闭容器中充入3mol
 和6mol
和6mol  ,开始测得气体的总压为4.5MPa,在一定温度下合成二甲醚,10min后达到平衡,测得
,开始测得气体的总压为4.5MPa,在一定温度下合成二甲醚,10min后达到平衡,测得 的转化率为50%,该反应的平衡常数
的转化率为50%,该反应的平衡常数
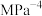 (保留2位有效数字,用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)
(保留2位有效数字,用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)
您最近一年使用:0次
名校
解题方法
10 . 甲烷、甲醇( )、甲醛(HCHO)等含有一个碳原子的物质称为“一碳”化合物,广泛应用于化工、医药、能源等方面,研究“一碳”化合物的化学称为“一碳”化学。
)、甲醛(HCHO)等含有一个碳原子的物质称为“一碳”化合物,广泛应用于化工、医药、能源等方面,研究“一碳”化合物的化学称为“一碳”化学。
(1)已知:①

②
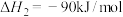
根据盖斯定律,反应 的
的
___________  ,反应能在
,反应能在___________ (填“高温”或“低温”)自发进行。
(2)工业上合成甲醇的反应: ,在一个密闭容器中,充入1molCO和
,在一个密闭容器中,充入1molCO和 发生反应,测得平衡时
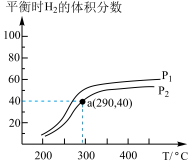
发生反应,测得平衡时 的体积分数与温度、压强的关系如图所示。压强
的体积分数与温度、压强的关系如图所示。压强
___________  (填“大于”或“小于”),该反应达到平衡的标志是
(填“大于”或“小于”),该反应达到平衡的标志是___________ (填标号)。
A.反应速率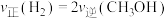
B.容器内CO和 物质的量之比为
物质的量之比为
C.混合气体的质量不再变化
D.混合气体的平均摩尔质量不再变化
(3)我国科学家制备了一种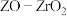 催化剂,实现
催化剂,实现 高选择性合成
高选择性合成 。气相催化合成过程中,
。气相催化合成过程中, 转化率(x)及
转化率(x)及 选择性(s)随温度的变化曲线如图。据此回答:
选择性(s)随温度的变化曲线如图。据此回答:

①生成 的最佳温度约为
的最佳温度约为___________ 。
②温度升高, 转化率升高,但产物
转化率升高,但产物 含量降低的原因:
含量降低的原因:___________ 。
(4)对于气体参与的反应如反应④[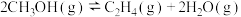 ,
, ],可以用某组分的压强(Pa)变化来表示化学反应速率,在温度和体积不变的密闭容器中充入一定量的
],可以用某组分的压强(Pa)变化来表示化学反应速率,在温度和体积不变的密闭容器中充入一定量的 发生反应④,在10分钟内,容器的压强由xkPa升高到ykPa,则这段时间该反应的化学反应速率
发生反应④,在10分钟内,容器的压强由xkPa升高到ykPa,则这段时间该反应的化学反应速率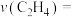
___________  。该反应的速率方程式为
。该反应的速率方程式为 ,
, ,
, 、
、 表示速率常数,与温度、活化能有关。升高温度,
表示速率常数,与温度、活化能有关。升高温度, 的变化程度
的变化程度___________ (填“大于”、或“等于”) 的变化程度。
的变化程度。
 )、甲醛(HCHO)等含有一个碳原子的物质称为“一碳”化合物,广泛应用于化工、医药、能源等方面,研究“一碳”化合物的化学称为“一碳”化学。
)、甲醛(HCHO)等含有一个碳原子的物质称为“一碳”化合物,广泛应用于化工、医药、能源等方面,研究“一碳”化合物的化学称为“一碳”化学。(1)已知:①


②

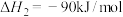
根据盖斯定律,反应
 的
的
 ,反应能在
,反应能在(2)工业上合成甲醇的反应:
 ,在一个密闭容器中,充入1molCO和
,在一个密闭容器中,充入1molCO和 发生反应,测得平衡时
发生反应,测得平衡时 的体积分数与温度、压强的关系如图所示。压强
的体积分数与温度、压强的关系如图所示。压强
 (填“大于”或“小于”),该反应达到平衡的标志是
(填“大于”或“小于”),该反应达到平衡的标志是
A.反应速率
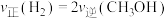
B.容器内CO和
 物质的量之比为
物质的量之比为
C.混合气体的质量不再变化
D.混合气体的平均摩尔质量不再变化
(3)我国科学家制备了一种
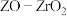 催化剂,实现
催化剂,实现 高选择性合成
高选择性合成 。气相催化合成过程中,
。气相催化合成过程中, 转化率(x)及
转化率(x)及 选择性(s)随温度的变化曲线如图。据此回答:
选择性(s)随温度的变化曲线如图。据此回答:
①生成
 的最佳温度约为
的最佳温度约为②温度升高,
 转化率升高,但产物
转化率升高,但产物 含量降低的原因:
含量降低的原因:(4)对于气体参与的反应如反应④[
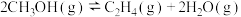 ,
, ],可以用某组分的压强(Pa)变化来表示化学反应速率,在温度和体积不变的密闭容器中充入一定量的
],可以用某组分的压强(Pa)变化来表示化学反应速率,在温度和体积不变的密闭容器中充入一定量的 发生反应④,在10分钟内,容器的压强由xkPa升高到ykPa,则这段时间该反应的化学反应速率
发生反应④,在10分钟内,容器的压强由xkPa升高到ykPa,则这段时间该反应的化学反应速率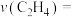
 。该反应的速率方程式为
。该反应的速率方程式为 ,
, ,
, 、
、 表示速率常数,与温度、活化能有关。升高温度,
表示速率常数,与温度、活化能有关。升高温度, 的变化程度
的变化程度 的变化程度。
的变化程度。
您最近一年使用:0次
2023-08-06更新
|
470次组卷
|
3卷引用:河南省兰考县第一高级中学2023-2024学年高二上学期期中考试化学试题



