名校
解题方法
1 . 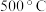 ,将
,将 和
和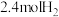 充入体积为
充入体积为 的已装有催化剂的恒容密闭容器中发生合成氨反应
的已装有催化剂的恒容密闭容器中发生合成氨反应 ,“此反应放热,下列说法正确的是
,“此反应放热,下列说法正确的是
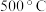 ,将
,将 和
和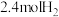 充入体积为
充入体积为 的已装有催化剂的恒容密闭容器中发生合成氨反应
的已装有催化剂的恒容密闭容器中发生合成氨反应 ,“此反应放热,下列说法正确的是
,“此反应放热,下列说法正确的是A.平衡时, 的浓度可能为 的浓度可能为 |
| B.容器内气体的密度不再随时间改变说明该反应已达到平衡状态 |
C.若已知生成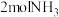 放出 放出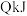 的热量,则该反应达平衡时放出的热量小于 的热量,则该反应达平衡时放出的热量小于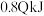 |
D.反应平衡后,向容器中充入一定体积的氨气,使容器中气体总压强增大,则 、 、 均增大 均增大 |
您最近半年使用:0次
名校
解题方法
2 . 湖北省十堰地区发现大量铌、钽等稀土矿产。萃取剂P204用于萃取稀土金属铌的反应为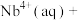
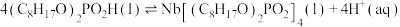 。某温度下,萃取铌离子的溶液中
。某温度下,萃取铌离子的溶液中 与时间变化关系如图所示。
与时间变化关系如图所示。
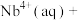
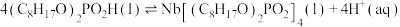 。某温度下,萃取铌离子的溶液中
。某温度下,萃取铌离子的溶液中 与时间变化关系如图所示。
与时间变化关系如图所示。
A.其他条件不变, 时萃取反应已停止 时萃取反应已停止 |
B. 增大,萃取平衡向左移动,平衡常数减小 增大,萃取平衡向左移动,平衡常数减小 |
C.萃取反应的正反应速率: |
D. 段 段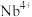 平均反应速率 平均反应速率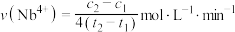 |
您最近半年使用:0次
7日内更新
|
117次组卷
|
3卷引用:2024届河南省名校高三下学期压轴卷(2)理综试卷-高中化学
3 . 合成氨对于合成化肥工业具有重要意义。回答下列问题:
(1)一定温度下,向容积恒定的密闭容器中,通入一定量的 和
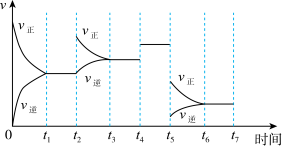
和 ,反应达到平衡后,仅改变某一外界条件,反应速率与时间的变化关系如图所示,其中
,反应达到平衡后,仅改变某一外界条件,反应速率与时间的变化关系如图所示,其中 、
、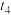 、
、 时刻所改变的条件可能是:
时刻所改变的条件可能是:
__________ (填标号,下同),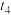
__________ ,
__________ 。
(2)温度为T℃时,将 和
和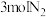 通入2L恒容密闭容器中,15min末,容器内的压强不再改变,测得
通入2L恒容密闭容器中,15min末,容器内的压强不再改变,测得 的转化率为20%。
的转化率为20%。
①下列情况能表明该反应已达到平衡状态的有__________ (填标号)。
A.混合气体的密度不再改变
B. 的物质的量分数不再改变
的物质的量分数不再改变
C.消耗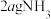 的同时消耗了
的同时消耗了
D.断裂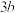 个
个 键的同时断裂
键的同时断裂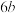 个
个 键
键
②0~15min内, 的平均反应速率
的平均反应速率
__________  ;达到平衡时,容器内
;达到平衡时,容器内 的质量为
的质量为__________ g。
(3)法国化学家勒夏特列根据大量的事实总结出一条经验规律:如果改变影响平衡的一个因素(如温度、压强或参加反应的物质的浓度),平衡就向着能够减弱这种改变的方向移动仅从产率角度考虑,合成氨应在__________ (填“高”或“低”)温条件下进行。工业上通常选择在400~500℃下进行,原因可能是__________ 。
(1)一定温度下,向容积恒定的密闭容器中,通入一定量的
 和
和 ,反应达到平衡后,仅改变某一外界条件,反应速率与时间的变化关系如图所示,其中
,反应达到平衡后,仅改变某一外界条件,反应速率与时间的变化关系如图所示,其中 、
、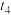 、
、 时刻所改变的条件可能是:
时刻所改变的条件可能是:

(2)温度为T℃时,将
 和
和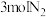 通入2L恒容密闭容器中,15min末,容器内的压强不再改变,测得
通入2L恒容密闭容器中,15min末,容器内的压强不再改变,测得 的转化率为20%。
的转化率为20%。①下列情况能表明该反应已达到平衡状态的有
A.混合气体的密度不再改变
B.
 的物质的量分数不再改变
的物质的量分数不再改变C.消耗
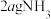 的同时消耗了
的同时消耗了
D.断裂
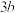 个
个 键的同时断裂
键的同时断裂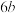 个
个 键
键②0~15min内,
 的平均反应速率
的平均反应速率
 ;达到平衡时,容器内
;达到平衡时,容器内 的质量为
的质量为(3)法国化学家勒夏特列根据大量的事实总结出一条经验规律:如果改变影响平衡的一个因素(如温度、压强或参加反应的物质的浓度),平衡就向着能够减弱这种改变的方向移动仅从产率角度考虑,合成氨应在
您最近半年使用:0次
4 . 往1L的恒容绝热容器中充入1.5mol气体N,容器内各成分的物质的量随时间变化的曲线如图。已知反应物和生成物均为气体。下列说法正确的是
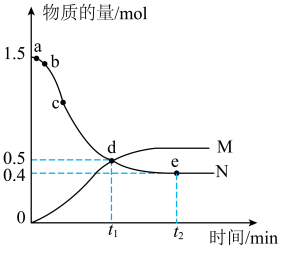
| A.ab段平均反应速率大于bc段平均反应速率 |
| B.d点时,反应达到平衡状态 |
C.总反应方程式为 |
| D.反应达到平衡时,M的体积分数约为58% |
您最近半年使用:0次
5 . 学习化学反应速率和限度能够指导促进工业生产。
Ⅰ.汽车发动机工作时会引发 和
和 反应,生成
反应,生成 等污染大气,其中生成NO的能量变化如图所示,
等污染大气,其中生成NO的能量变化如图所示,_______ ;若反应生成2molNO气体应_______ (填“释放”或“吸收”)_______ kJ能量。
Ⅱ.某研究小组用CO和H2模拟工业合成甲醇,发生反应: 在1L的恒容密闭容器内充入1molCO和2mol
在1L的恒容密闭容器内充入1molCO和2mol ,加入合适催化剂后保持某温度不变发生上述反应,并用压力计监测容器内压强的变化如下:
,加入合适催化剂后保持某温度不变发生上述反应,并用压力计监测容器内压强的变化如下:
(2)①下列说法正确的是_______ (填标号)。
a.容器内气体的密度不变,则反应达到平衡
b.容器内气体的平均相对分子质量不变,则反应达到平衡
c.若向平衡体系中充入Ar后,甲醇的生成速率降低
d.容器内CO和 物质的量之比不变,则反应达到平衡
物质的量之比不变,则反应达到平衡
e.CO的转化率不再变化,则反应达到平衡
②从反应开始到20min时, 的平均反应速率为
的平均反应速率为_______ 。
③该条件下,反应 达到平衡时CO的转化率为
达到平衡时CO的转化率为_______ 。
(3)从断键和成键角度分析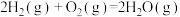 反应中能量的变化。部分化学键的键能如下表:
反应中能量的变化。部分化学键的键能如下表:
则生成 放出热量
放出热量_______ kJ。
(4)NaClO溶液在不同温度下可对烟气中的硫、硝脱除,一定时间内,其脱除率如图所示: 脱除率高于NO,可能的原因是
脱除率高于NO,可能的原因是_______ 。
②烟气中 和NO体积比为4:1,烟气与50℃时的吸收液转化生成的
和NO体积比为4:1,烟气与50℃时的吸收液转化生成的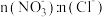 =
=_______ 。
Ⅰ.汽车发动机工作时会引发
 和
和 反应,生成
反应,生成 等污染大气,其中生成NO的能量变化如图所示,
等污染大气,其中生成NO的能量变化如图所示,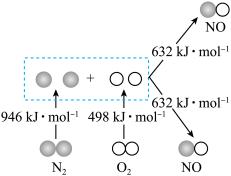
Ⅱ.某研究小组用CO和H2模拟工业合成甲醇,发生反应:
 在1L的恒容密闭容器内充入1molCO和2mol
在1L的恒容密闭容器内充入1molCO和2mol ,加入合适催化剂后保持某温度不变发生上述反应,并用压力计监测容器内压强的变化如下:
,加入合适催化剂后保持某温度不变发生上述反应,并用压力计监测容器内压强的变化如下:| 反应时间/min0 | 0 | 5 | 10 | 15 | 20 | 30 |
| 压强/MPa | 25.2 | 21.6 | 18.9 | 17.4 | 16.8 | 16.8 |
(2)①下列说法正确的是
a.容器内气体的密度不变,则反应达到平衡
b.容器内气体的平均相对分子质量不变,则反应达到平衡
c.若向平衡体系中充入Ar后,甲醇的生成速率降低
d.容器内CO和
 物质的量之比不变,则反应达到平衡
物质的量之比不变,则反应达到平衡e.CO的转化率不再变化,则反应达到平衡
②从反应开始到20min时,
 的平均反应速率为
的平均反应速率为③该条件下,反应
 达到平衡时CO的转化率为
达到平衡时CO的转化率为(3)从断键和成键角度分析
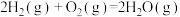 反应中能量的变化。部分化学键的键能如下表:
反应中能量的变化。部分化学键的键能如下表:| 化学键 |  |  |  |
| 键能(kJ/mol) | 436 | 496 | 463 |
 放出热量
放出热量(4)NaClO溶液在不同温度下可对烟气中的硫、硝脱除,一定时间内,其脱除率如图所示:
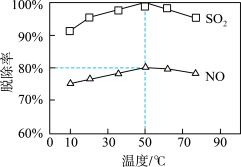
 脱除率高于NO,可能的原因是
脱除率高于NO,可能的原因是②烟气中
 和NO体积比为4:1,烟气与50℃时的吸收液转化生成的
和NO体积比为4:1,烟气与50℃时的吸收液转化生成的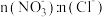 =
=
您最近半年使用:0次
名校
6 . 某温度下,在 恒容密闭容器中
恒容密闭容器中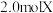 发生反应
发生反应 ,有关数据如下:
,有关数据如下:
下列说法错误的是
 恒容密闭容器中
恒容密闭容器中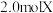 发生反应
发生反应 ,有关数据如下:
,有关数据如下:时间段 | 产物 的平均生成速率 的平均生成速率 |
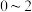 | 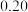 |
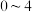 | 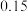 |
 |  |
A. 时, 时, 的浓度大于 的浓度大于 |
B. 时,反应未达到平衡状态 时,反应未达到平衡状态 |
C. 时, 时, 的体积分数约为 的体积分数约为 |
D. 时, 时, 的物质的量为 的物质的量为 |
您最近半年使用:0次
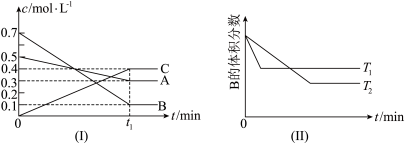
7 . I.T℃时,A气体与B气体反应生成C气体,反应过程中A、B、C浓度变化如图(Ⅰ)所示,若保持其他条件不变,温度分别为T1和T2时,B的体积分数与时间的关系如(Ⅱ)所示:
(1)反应的化学方程式为___________ 。
(2)当反应达到平衡后升高平衡体系的温度(保持体积不变),混合气体的平均相对分子质量___________ (填“变大”、“变小”或“不变”)。
Ⅱ.在一定体积的密闭容器中,进行如下化学反应:CO2(g)+H2(g) CO(g)+H2O(g)
CO(g)+H2O(g)
其化学平衡常数K和温度t的关系如下表:
回答下列问题:
(3)一般说化学平衡常数数值K___________ ,通常认为该反应进行较完全。
(4)该反应为___________ 反应(填“吸热”或“放热”)。
(5)能判断该反应是否达到化学平衡状态的依据是___________。
(6)某温度下,在2L的密闭容器中,加入1molCO2和1molH2充分反应达平衡时,CO平衡浓度为0.25mol/L,试判断此时的温度为___________ 。
(1)反应的化学方程式为
(2)当反应达到平衡后升高平衡体系的温度(保持体积不变),混合气体的平均相对分子质量
Ⅱ.在一定体积的密闭容器中,进行如下化学反应:CO2(g)+H2(g)
 CO(g)+H2O(g)
CO(g)+H2O(g)其化学平衡常数K和温度t的关系如下表:
| t/℃ | 700 | 800 | 830 | 1000 | 1200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
(3)一般说化学平衡常数数值K
(4)该反应为
(5)能判断该反应是否达到化学平衡状态的依据是___________。
| A.v正(H2) = v逆(H2O) | B.反应停止,正、逆反应速率都等于零 |
| C.容器中压强不再发生变化 | D.混合气体中c(CO2)不变 |
(6)某温度下,在2L的密闭容器中,加入1molCO2和1molH2充分反应达平衡时,CO平衡浓度为0.25mol/L,试判断此时的温度为
您最近半年使用:0次
名校
解题方法
8 . 将 气体和
气体和 气体在
气体在 的密闭容器中混合并在一定条件下发生如下反应:
的密闭容器中混合并在一定条件下发生如下反应: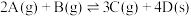 ,若经
,若经 后测得
后测得 的浓度为
的浓度为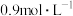 ,则下列几种说法中正确的是
,则下列几种说法中正确的是
① 末物质
末物质 的物质的量为
的物质的量为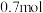
②用物质 表示的平均反应速率为
表示的平均反应速率为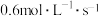
③ 时,物质
时,物质 的转化率为
的转化率为
④用 来表示反应速率,其速率之比为2:1:3
来表示反应速率,其速率之比为2:1:3
 气体和
气体和 气体在
气体在 的密闭容器中混合并在一定条件下发生如下反应:
的密闭容器中混合并在一定条件下发生如下反应: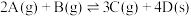 ,若经
,若经 后测得
后测得 的浓度为
的浓度为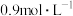 ,则下列几种说法中正确的是
,则下列几种说法中正确的是①
 末物质
末物质 的物质的量为
的物质的量为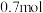
②用物质
 表示的平均反应速率为
表示的平均反应速率为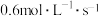
③
 时,物质
时,物质 的转化率为
的转化率为
④用
 来表示反应速率,其速率之比为2:1:3
来表示反应速率,其速率之比为2:1:3| A.①③④ | B.①②③④ |
| C.②④ | D.③④ |
您最近半年使用:0次
名校
解题方法
9 . 工业上,常用水蒸气通过炽热的焦炭制得水煤气(主要成分为CO和 ),其反应的化学方程式为
),其反应的化学方程式为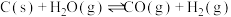 ,请回答下列问题:
,请回答下列问题:
(1)上述反应的能量变化图像如图所示。下列反应的能量变化与上述反应相同的是_______。
(2)一定条件下,焦炭和水蒸气在体积一定的密闭容器中进行反应,下列有关说法正确的是_______。
(3)在体积均为2L的甲、乙两个恒容密闭容器中,分别加入相同质量的一定量炭粉和2.8mol水蒸气,在不同温度下反应的过程如图所示:
_______ 。
②甲容器中,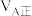
_______ 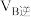 (填“<”“>”或“=”下同)。
(填“<”“>”或“=”下同)。
③反应过程中,两个容器温度:甲_______ 乙。
(4)乙容器中C点时,CO的物质的量百分数为_______ 。
 ),其反应的化学方程式为
),其反应的化学方程式为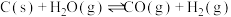 ,请回答下列问题:
,请回答下列问题:(1)上述反应的能量变化图像如图所示。下列反应的能量变化与上述反应相同的是_______。

| A.铝粉与氧化铁的反应 | B.氯化铵与 的反应 的反应 |
| C.锌片与稀硫酸的反应 | D.钠与冷水的反应 |
(2)一定条件下,焦炭和水蒸气在体积一定的密闭容器中进行反应,下列有关说法正确的是_______。
| A.充入He使容器压强增大,提高反应速率 |
B.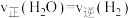 ,说明反应达到平衡状态 ,说明反应达到平衡状态 |
| C.容器中焦炭的质量不再变化,说明反应达到平衡状态 |
D.容器中水蒸气与氢气的体积比为 时,说明反应达到平衡状态 时,说明反应达到平衡状态 |
(3)在体积均为2L的甲、乙两个恒容密闭容器中,分别加入相同质量的一定量炭粉和2.8mol水蒸气,在不同温度下反应的过程如图所示:
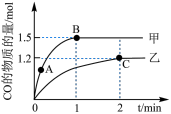

②甲容器中,
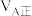
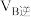 (填“<”“>”或“=”下同)。
(填“<”“>”或“=”下同)。③反应过程中,两个容器温度:甲
(4)乙容器中C点时,CO的物质的量百分数为
您最近半年使用:0次
2024-05-03更新
|
234次组卷
|
2卷引用:河南省焦作市博爱县第一中学2023-2024学年高一下学期4月期中考试化学试题
名校
解题方法
10 . CI4分)某化学小组欲测定酸性条件下 溶液与
溶液与 溶液反应的化学反应速率,所用试剂为
溶液反应的化学反应速率,所用试剂为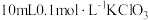 溶液和
溶液和 溶液,所得溶液中
溶液,所得溶液中 的浓度
的浓度 随时间变化的曲线如图1和
随时间变化的曲线如图1和 的速率
的速率 随时间的变化关系如图2:
随时间的变化关系如图2:_____ 。
 (已配平)
(已配平)
(2)根据实验数据可知,该反应在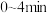 的平均反应速率
的平均反应速率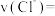
_____ 。
(3)下列说法正确的是_____
A.若纵坐标为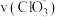 的
的 曲线与图2中的曲线不能重合
曲线与图2中的曲线不能重合
B.图中阴影部分的面积表示 时间内
时间内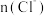 的增大
的增大
C.后期反应速率下降的主要原因是反应物浓度减少
(4)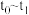 段该反应速率增大,为探究可能的原因,设计如下方案探究影响化学反应速率的因素:
段该反应速率增大,为探究可能的原因,设计如下方案探究影响化学反应速率的因素:
已知: 对该反应无影响;
对该反应无影响;
可供选择的试剂有:A. 固体 B.
固体 B. 固体C.
固体C. D.
D.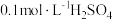 E.
E.
①方案I中所选试剂_____ ,方案Ⅱ中所选试剂_____ 。
②方案Ⅱ烧杯①中加入 水的作用是
水的作用是_____ 。
③除方案I和方案Ⅱ外,请再提出一种可能加快化学反应速率的假设_____ 。
 溶液与
溶液与 溶液反应的化学反应速率,所用试剂为
溶液反应的化学反应速率,所用试剂为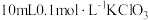 溶液和
溶液和 溶液,所得溶液中
溶液,所得溶液中 的浓度
的浓度 随时间变化的曲线如图1和
随时间变化的曲线如图1和 的速率
的速率 随时间的变化关系如图2:
随时间的变化关系如图2: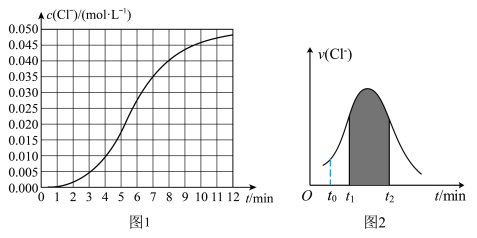
 (已配平)
(已配平)(2)根据实验数据可知,该反应在
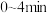 的平均反应速率
的平均反应速率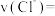
(3)下列说法正确的是
A.若纵坐标为
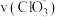 的
的 曲线与图2中的曲线不能重合
曲线与图2中的曲线不能重合B.图中阴影部分的面积表示
 时间内
时间内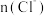 的增大
的增大C.后期反应速率下降的主要原因是反应物浓度减少
(4)
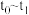 段该反应速率增大,为探究可能的原因,设计如下方案探究影响化学反应速率的因素:
段该反应速率增大,为探究可能的原因,设计如下方案探究影响化学反应速率的因素:已知:
 对该反应无影响;
对该反应无影响;可供选择的试剂有:A.
 固体 B.
固体 B. 固体C.
固体C. D.
D.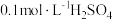 E.
E.
| 方案 | 假设 | 数据处理 | 具体实验操作 |
| I | 反应产物 对反应有催化作用,加快了化学反应速率 对反应有催化作用,加快了化学反应速率 | 取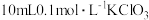 溶液于烧杯中,先加入_____(填字母),再加入 溶液于烧杯中,先加入_____(填字母),再加入 溶液。 溶液。 | 绘制溶液中 浓度 浓度 随时间变化的曲线与图1对比 随时间变化的曲线与图1对比 |
| Ⅱ | 反应中溶液酸性增强,加快了化学反应速率 | 分别向两个烧杯中加入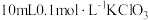 溶液。 溶液。烧杯①:加入  水: 水:烧杯②:加入  _____(填字母)。 _____(填字母)。再分别向两个烧杯中加入  溶液。 溶液。 |
②方案Ⅱ烧杯①中加入
 水的作用是
水的作用是③除方案I和方案Ⅱ外,请再提出一种可能加快化学反应速率的假设
您最近半年使用:0次



