1 . 甲硫醇(CH3SH)是重要的有机化工中间体,可用于合成维生素。通过CH3OH和H2S合成CH3SH的主要反应为:
Ⅰ.
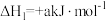
Ⅱ.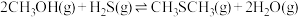
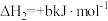
回答下列问题:
(1)计算反应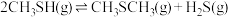 的△H=
的△H=________ kJ/mol。
(2)T1℃时,向恒容密闭容器中充入一定量CH3OH(g)和H2S(g)发生反应,下列事实能说明反应达到平衡状态的是________ (填选项字母);若按相同比例再充入一定量CH3OH(g)和H2S(g),CH3OH(g)的平衡转化率将________ (填“变大”“变小”或“不变”)。
A.容器内气体密度不再发生变化 B.混合气体的平均相对分子质量不再发生变化
C.H2S(g)的体积分数不再发生变化 D.CH3SCH3(g)和H2O(g)的物质的量之比不再变化
(3)T2℃时,向压强为P0的恒压密闭容器中按物质的量之比为1:2充入CH3OH(g)和H2S(g)发生反应,达到平衡时,CH3OH(g)的转化率为80%,CH3SCH3(g)的体积分数为5%。
①计算H2S(g)的选择性为________ (CH3SH的选择性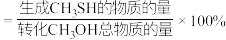 )。
)。
②反应Ⅰ的平衡常数Kp=________ (Kp是用分压表示的平衡常数,结果保留两位小数)。
(4)在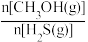 =1:2、反应压力为0.7Mpa条件下,气体按90 mL/min的速率通过催化剂表面发生反应,每分钟反应体系中CH3OH(g)转化率、CH3SH(g)选择性随温度的变化如图甲所示,催化机理如图乙所示。
=1:2、反应压力为0.7Mpa条件下,气体按90 mL/min的速率通过催化剂表面发生反应,每分钟反应体系中CH3OH(g)转化率、CH3SH(g)选择性随温度的变化如图甲所示,催化机理如图乙所示。________ Mpa/min(结果保留两位有效数字)。
②当温度高于370℃时,CH3OH(g)转化率随温度升高而降低的原因可能为________ 。
③从电负性的角度描述ⅲ→ⅰ中脱水的过程:________ 。
Ⅰ.

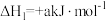
Ⅱ.
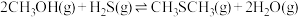
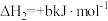
回答下列问题:
(1)计算反应
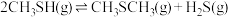 的△H=
的△H=(2)T1℃时,向恒容密闭容器中充入一定量CH3OH(g)和H2S(g)发生反应,下列事实能说明反应达到平衡状态的是
A.容器内气体密度不再发生变化 B.混合气体的平均相对分子质量不再发生变化
C.H2S(g)的体积分数不再发生变化 D.CH3SCH3(g)和H2O(g)的物质的量之比不再变化
(3)T2℃时,向压强为P0的恒压密闭容器中按物质的量之比为1:2充入CH3OH(g)和H2S(g)发生反应,达到平衡时,CH3OH(g)的转化率为80%,CH3SCH3(g)的体积分数为5%。
①计算H2S(g)的选择性为
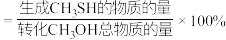 )。
)。②反应Ⅰ的平衡常数Kp=
(4)在
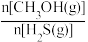 =1:2、反应压力为0.7Mpa条件下,气体按90 mL/min的速率通过催化剂表面发生反应,每分钟反应体系中CH3OH(g)转化率、CH3SH(g)选择性随温度的变化如图甲所示,催化机理如图乙所示。
=1:2、反应压力为0.7Mpa条件下,气体按90 mL/min的速率通过催化剂表面发生反应,每分钟反应体系中CH3OH(g)转化率、CH3SH(g)选择性随温度的变化如图甲所示,催化机理如图乙所示。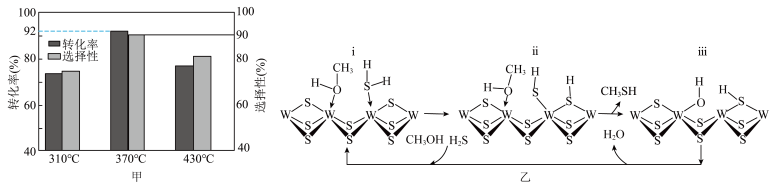
②当温度高于370℃时,CH3OH(g)转化率随温度升高而降低的原因可能为
③从电负性的角度描述ⅲ→ⅰ中脱水的过程:
您最近半年使用:0次
名校
2 . 化学反应过程既有物质变化也有能量变化。
Ⅰ.关于工业合成氨的反应,已知H-H键、N-H键、N≡N键的键能分别为436 、391
、391 、946
、946 。请根据键能的数据判断下列问题。
。请根据键能的数据判断下列问题。
(1)由 和
和 合成氨时,需要
合成氨时,需要_____________ (填“吸收”或“放出”)能量,写出该反应的热化学方程式_________________ 。
Ⅱ.原电池是化学能转化为电能的装置。
(2)肼(液态)—过氧化氢碱性燃料电池由于其较高的能量密度而备受关注,其工作原理如图。_______ (填“氧化反应”或“还原反应”),电池工作过程中, 向极移动
向极移动_________ (填“A”或“B”);
②该燃料电池的总反应方程式可表示为__________ 。在标准状况下,若A极区产生11.2L  ,则外电路中理论上通过的电子的物质的量是
,则外电路中理论上通过的电子的物质的量是__________ mol。
Ⅲ.某温度时,在一个2L的密闭容器中,X、Y、Z三种气体物质的物质的量随时间的变化曲线如图所示。根据图中数据填空:_____________ 。
(4)反应开始至2min,以气体X表示的平均反应速率为___________ 。
(5)下列措施能增大反应速率的是_________ 。
A.升高温度 B.加入高效催化剂
C.持容器压强不变,充入一定量氦气 D.保持容器容积不变,充入气体X
E.保持容器容积不变,充入一定量氦气
(6)能说明上述反应达到平衡状态的是 。(填字母)
Ⅰ.关于工业合成氨的反应,已知H-H键、N-H键、N≡N键的键能分别为436
 、391
、391 、946
、946 。请根据键能的数据判断下列问题。
。请根据键能的数据判断下列问题。(1)由
 和
和 合成氨时,需要
合成氨时,需要Ⅱ.原电池是化学能转化为电能的装置。
(2)肼(液态)—过氧化氢碱性燃料电池由于其较高的能量密度而备受关注,其工作原理如图。
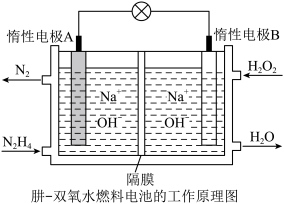
 向极移动
向极移动②该燃料电池的总反应方程式可表示为
 ,则外电路中理论上通过的电子的物质的量是
,则外电路中理论上通过的电子的物质的量是Ⅲ.某温度时,在一个2L的密闭容器中,X、Y、Z三种气体物质的物质的量随时间的变化曲线如图所示。根据图中数据填空:
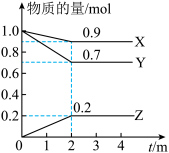
(4)反应开始至2min,以气体X表示的平均反应速率为
(5)下列措施能增大反应速率的是
A.升高温度 B.加入高效催化剂
C.持容器压强不变,充入一定量氦气 D.保持容器容积不变,充入气体X
E.保持容器容积不变,充入一定量氦气
(6)能说明上述反应达到平衡状态的是 。(填字母)
| A.混合气体的压强不随时间的变化而变化 | B. |
| C.X体积分数保持不变 | D.混合气体的密度不随时间的变化而变化 |
您最近半年使用:0次
名校
3 . 一定条件下,对于反应 ,若X、Y、Z的起始浓度分别为
,若X、Y、Z的起始浓度分别为 、
、 、
、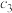 (均不为零)。达到平衡时,X、Y、Z的浓度分别为0.1
(均不为零)。达到平衡时,X、Y、Z的浓度分别为0.1 、0.3
、0.3 和0.08
和0.08 ,则下列判断合理的是
,则下列判断合理的是
①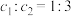
②平衡时,Y和Z的生成速率之比为2∶3
③X和Y转化量之比为1∶1
④ 的取值范围为
的取值范围为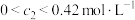
 ,若X、Y、Z的起始浓度分别为
,若X、Y、Z的起始浓度分别为 、
、 、
、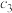 (均不为零)。达到平衡时,X、Y、Z的浓度分别为0.1
(均不为零)。达到平衡时,X、Y、Z的浓度分别为0.1 、0.3
、0.3 和0.08
和0.08 ,则下列判断合理的是
,则下列判断合理的是①
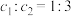
②平衡时,Y和Z的生成速率之比为2∶3
③X和Y转化量之比为1∶1
④
 的取值范围为
的取值范围为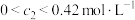
| A.①② | B.①④ | C.②③ | D.③④ |
您最近半年使用:0次
4 . Ⅰ。在下列事实中,什么因素影响了化学反应速率?
(1)集气瓶中有 和
和 的混合气体,在瓶外点燃镁条时发生爆炸
的混合气体,在瓶外点燃镁条时发生爆炸___________ ;
黄铁矿煅烧时要粉碎成细小的矿粒。___________ ;
熔化的 放出气泡很慢,加入少量
放出气泡很慢,加入少量 后很快产生气体。
后很快产生气体。___________ ;
夏天食品容易变质,冬天就不易发生该现象。___________ ;
同样大小的石灰石分别在 的盐酸和
的盐酸和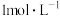 的盐酸中反应,反应速率不同。
的盐酸中反应,反应速率不同。___________ 。
Ⅱ。某温度时,在 密闭容器中
密闭容器中 三种气态物质的物质的量
三种气态物质的物质的量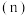 随时间
随时间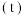 变化的曲线如图所示,由图中数据分析:
变化的曲线如图所示,由图中数据分析:___________ 。
(3)反应开始至 ,用
,用 表示的平均反应速率为
表示的平均反应速率为___________ 。此时, 的转化率为
的转化率为___________ 。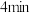 时,加入1体积
时,加入1体积 ,反应速率
,反应速率___________ (填“变大”、“变小”、“不变”)
(4)下列叙述不能说明上述反应达到化学平衡状态的是___________ (填序号)。
A. 的物质的量不随时间变化而变化
的物质的量不随时间变化而变化
B. 的质量分数不随时间变化而变化
的质量分数不随时间变化而变化
C.混合气体的总物质的量不随时间变化而变化
D.
E.
F.单位时间内每消耗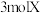 ,同时生成
,同时生成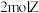
(1)集气瓶中有
 和
和 的混合气体,在瓶外点燃镁条时发生爆炸
的混合气体,在瓶外点燃镁条时发生爆炸黄铁矿煅烧时要粉碎成细小的矿粒。
熔化的
 放出气泡很慢,加入少量
放出气泡很慢,加入少量 后很快产生气体。
后很快产生气体。夏天食品容易变质,冬天就不易发生该现象。
同样大小的石灰石分别在
 的盐酸和
的盐酸和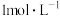 的盐酸中反应,反应速率不同。
的盐酸中反应,反应速率不同。Ⅱ。某温度时,在
 密闭容器中
密闭容器中 三种气态物质的物质的量
三种气态物质的物质的量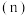 随时间
随时间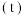 变化的曲线如图所示,由图中数据分析:
变化的曲线如图所示,由图中数据分析: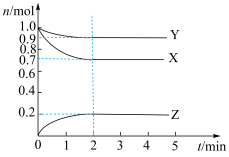
(3)反应开始至
 ,用
,用 表示的平均反应速率为
表示的平均反应速率为 的转化率为
的转化率为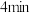 时,加入1体积
时,加入1体积 ,反应速率
,反应速率(4)下列叙述不能说明上述反应达到化学平衡状态的是
A.
 的物质的量不随时间变化而变化
的物质的量不随时间变化而变化 B.
 的质量分数不随时间变化而变化
的质量分数不随时间变化而变化C.混合气体的总物质的量不随时间变化而变化
D.

E.

F.单位时间内每消耗
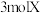 ,同时生成
,同时生成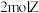
您最近半年使用:0次
名校
解题方法
5 . 按要求回答下列问题:
(1)某汽车安全气囊的气体发生剂主要含有叠氮化钠( )、
)、 、
、 等物质。
等物质。
①汽车受到猛烈碰撞时,点火器点火引发 迅速分解,生成氢气和金属钠,同时释放大量的热,关于该反应过程中的能量变化示意图正确的是
迅速分解,生成氢气和金属钠,同时释放大量的热,关于该反应过程中的能量变化示意图正确的是_______ (填字母)。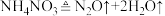 ,推测安全气囊中
,推测安全气囊中 的作用有
的作用有_______ 。
(2)以 为催化剂的光热化学循环分解
为催化剂的光热化学循环分解 反应,为温室气体减排提供了一个新途径,该反应的机理及各分子化学键完全断裂时的能量变化如图所示。
反应,为温室气体减排提供了一个新途径,该反应的机理及各分子化学键完全断裂时的能量变化如图所示。_______ 转化为化学能。
②根据数据计算,分解1 mol 需
需_______ (填“吸收”或“释放”)_______ kJ的能量。
(3)汽车尾气净化装置中,三元催化剂能将一氧化碳、碳氢化合物和氮氧化物转化为无毒气体,某研究小组模拟实验,计算反应速率。一定条件下,在2 L密闭容器内,反应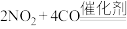
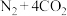 ,
,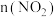 时间变化如表:
时间变化如表:
0~2s内用CO表示该反应的平均速率为_______ 。
(4)氮气可作为脱硝剂,在恒温恒容密闭容器中充入一定量的NO和 ,在一定条件下发生反应:
,在一定条件下发生反应: 。
。
①能说明该反应已达到平衡状态的标志是_______ (填标号)
A.反应速率
B.容器内压强不再随时间而发生变化
C.容器内 的物质的量分数不再随时间而发生变化
的物质的量分数不再随时间而发生变化
D.容器内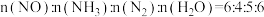
②某次实验中测得容器内NO及 的物质的量随时间变化如图。
的物质的量随时间变化如图。
_______  (填>“<”或“=”),d点对应的速率关系是
(填>“<”或“=”),d点对应的速率关系是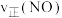
_______ 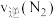 (填“>”“<”或“=”)。
(填“>”“<”或“=”)。
(1)某汽车安全气囊的气体发生剂主要含有叠氮化钠(
 )、
)、 、
、 等物质。
等物质。①汽车受到猛烈碰撞时,点火器点火引发
 迅速分解,生成氢气和金属钠,同时释放大量的热,关于该反应过程中的能量变化示意图正确的是
迅速分解,生成氢气和金属钠,同时释放大量的热,关于该反应过程中的能量变化示意图正确的是A.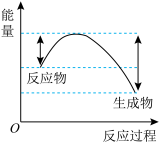 B.
B.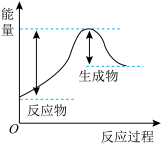 C.
C.
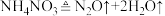 ,推测安全气囊中
,推测安全气囊中 的作用有
的作用有(2)以
 为催化剂的光热化学循环分解
为催化剂的光热化学循环分解 反应,为温室气体减排提供了一个新途径,该反应的机理及各分子化学键完全断裂时的能量变化如图所示。
反应,为温室气体减排提供了一个新途径,该反应的机理及各分子化学键完全断裂时的能量变化如图所示。
②根据数据计算,分解1 mol
 需
需(3)汽车尾气净化装置中,三元催化剂能将一氧化碳、碳氢化合物和氮氧化物转化为无毒气体,某研究小组模拟实验,计算反应速率。一定条件下,在2 L密闭容器内,反应
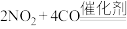
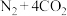 ,
,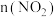 时间变化如表:
时间变化如表:| 时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
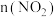 /mol /mol | a | b | c | d | e | f |
(4)氮气可作为脱硝剂,在恒温恒容密闭容器中充入一定量的NO和
 ,在一定条件下发生反应:
,在一定条件下发生反应: 。
。①能说明该反应已达到平衡状态的标志是
A.反应速率

B.容器内压强不再随时间而发生变化
C.容器内
 的物质的量分数不再随时间而发生变化
的物质的量分数不再随时间而发生变化D.容器内
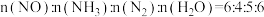
②某次实验中测得容器内NO及
 的物质的量随时间变化如图。
的物质的量随时间变化如图。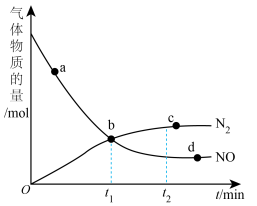

 (填>“<”或“=”),d点对应的速率关系是
(填>“<”或“=”),d点对应的速率关系是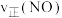
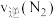 (填“>”“<”或“=”)。
(填“>”“<”或“=”)。
您最近半年使用:0次
名校
6 .  是一种无色有刺激性气味的液体,在生产生活中有重要用途,也是一种重要的化工原料。
是一种无色有刺激性气味的液体,在生产生活中有重要用途,也是一种重要的化工原料。
(1)已知利用合成气(主要成分 和
和 )在催化剂的作用下合成甲醇,发生反应为:
)在催化剂的作用下合成甲醇,发生反应为: 。反应过程中的能量变化如图所示,该反应为
。反应过程中的能量变化如图所示,该反应为_____________________ (填“放热”或“吸热”)反应。 (
( ,石墨)与适量
,石墨)与适量 反应生成
反应生成 和
和 ,吸收
,吸收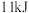 热量,请写出热化学方程式:
热量,请写出热化学方程式:_____________________________________________________ 。
(3)现在实验室中用 和
和 反应模拟甲醇合成反应,在
反应模拟甲醇合成反应,在 恒容密闭容器内,
恒容密闭容器内,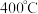 时发生反应:
时发生反应: ,体系中
,体系中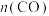 随时间的变化如表:
随时间的变化如表:
①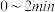 内,以
内,以 表示的该反应速率
表示的该反应速率
_____________________ 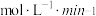 ;
;
②下列措施不能提高反应速率的有_____________________ (请用相应字母填空);
 升高温度
升高温度  恒
恒 、恒
、恒 下充入
下充入
 及时分离出
及时分离出
 恒
恒 、恒
、恒 下充入
下充入
 加入高效催化剂
加入高效催化剂
③下列叙述能说明反应达到平衡状态的是_____________________ (请用相应字母填空);
 和
和 的浓度保持不变
的浓度保持不变 
 每生成
每生成 的同时有
的同时有 键形成
键形成
 容器内气体密度保持不变
容器内气体密度保持不变
 容器内质量保持不变
容器内质量保持不变
 是一种无色有刺激性气味的液体,在生产生活中有重要用途,也是一种重要的化工原料。
是一种无色有刺激性气味的液体,在生产生活中有重要用途,也是一种重要的化工原料。(1)已知利用合成气(主要成分
 和
和 )在催化剂的作用下合成甲醇,发生反应为:
)在催化剂的作用下合成甲醇,发生反应为: 。反应过程中的能量变化如图所示,该反应为
。反应过程中的能量变化如图所示,该反应为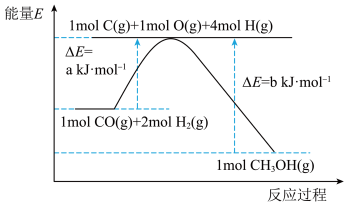
 (
( ,石墨)与适量
,石墨)与适量 反应生成
反应生成 和
和 ,吸收
,吸收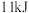 热量,请写出热化学方程式:
热量,请写出热化学方程式:(3)现在实验室中用
 和
和 反应模拟甲醇合成反应,在
反应模拟甲醇合成反应,在 恒容密闭容器内,
恒容密闭容器内,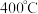 时发生反应:
时发生反应: ,体系中
,体系中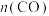 随时间的变化如表:
随时间的变化如表:时间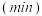 | 0 | 1 | 2 | 3 | 5 |
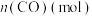 | 0.020 | 0.011 | 0.008 | 0.007 | 0.007 |
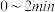 内,以
内,以 表示的该反应速率
表示的该反应速率
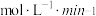 ;
;②下列措施不能提高反应速率的有
 升高温度
升高温度  恒
恒 、恒
、恒 下充入
下充入
 及时分离出
及时分离出
 恒
恒 、恒
、恒 下充入
下充入
 加入高效催化剂
加入高效催化剂③下列叙述能说明反应达到平衡状态的是
 和
和 的浓度保持不变
的浓度保持不变 
 每生成
每生成 的同时有
的同时有 键形成
键形成 容器内气体密度保持不变
容器内气体密度保持不变 容器内质量保持不变
容器内质量保持不变
您最近半年使用:0次
解题方法
7 . 研究氮氧化物 (NOₓ)的还原处理方法是环保领域的主要方向之一、回答下列问题:
 .用H2还原NO的反应为
.用H2还原NO的反应为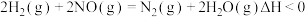

(1)该反应的正反应速率方程可表示为 ,某温度下,测得正反应速率v正与c(NO)或c(H
,某温度下,测得正反应速率v正与c(NO)或c(H )的变化关系如图1所示。
)的变化关系如图1所示。
___________ ,
___________ 。
(2)研究表明上述反应历程分两步基元反应:
i. ;
;
ii.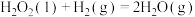 。
。
根据 (1)所给信息判断,H 还原 NO 总反应的速率由反应
还原 NO 总反应的速率由反应___________ (填“ i”或“ii” ) 决定。
(3)将一定量的H 和NO置于以下条件下发生反应(起始容器的体积、温度、压强均相同),到达平衡时,H
和NO置于以下条件下发生反应(起始容器的体积、温度、压强均相同),到达平衡时,H 的平衡转化率最大的是
的平衡转化率最大的是___________ 。
a. 恒温恒容 b.恒温恒压 c. 恒容绝热
 .脱除汽车尾气中 NO 和CO包括以下两个反应:
.脱除汽车尾气中 NO 和CO包括以下两个反应:
反应i. ;
;
反应ii. 。
。
反应过程中各物质相对能量如图 2 (TS表示过渡态): 的热化学方程式为
的热化学方程式为___________ 。
将恒定组成的NO和CO混合气体通入不同温度的反应器,相同时间内检测物质浓度,结果如图3。___________ (填“高温”或者“低温”)。
(6)实验过程中,高于340℃后N O浓度逐渐减小,试分析发生该变化的原因是
O浓度逐渐减小,试分析发生该变化的原因是___________ 。
(7)450℃时, 该时间段内NO的脱除率=___________ (保留2位有效数字, NO的脱除率
 .用H2还原NO的反应为
.用H2还原NO的反应为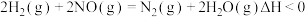

(1)该反应的正反应速率方程可表示为
 ,某温度下,测得正反应速率v正与c(NO)或c(H
,某温度下,测得正反应速率v正与c(NO)或c(H )的变化关系如图1所示。
)的变化关系如图1所示。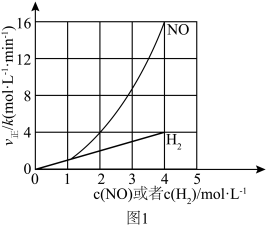


(2)研究表明上述反应历程分两步基元反应:
i.
 ;
;ii.
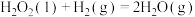 。
。根据 (1)所给信息判断,H
 还原 NO 总反应的速率由反应
还原 NO 总反应的速率由反应(3)将一定量的H
 和NO置于以下条件下发生反应(起始容器的体积、温度、压强均相同),到达平衡时,H
和NO置于以下条件下发生反应(起始容器的体积、温度、压强均相同),到达平衡时,H 的平衡转化率最大的是
的平衡转化率最大的是a. 恒温恒容 b.恒温恒压 c. 恒容绝热
 .脱除汽车尾气中 NO 和CO包括以下两个反应:
.脱除汽车尾气中 NO 和CO包括以下两个反应:反应i.
 ;
;反应ii.
 。
。反应过程中各物质相对能量如图 2 (TS表示过渡态):
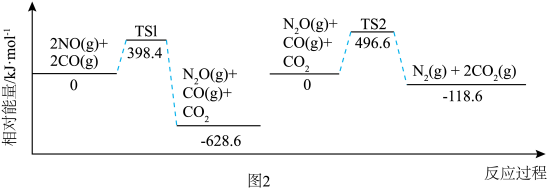
 的热化学方程式为
的热化学方程式为将恒定组成的NO和CO混合气体通入不同温度的反应器,相同时间内检测物质浓度,结果如图3。
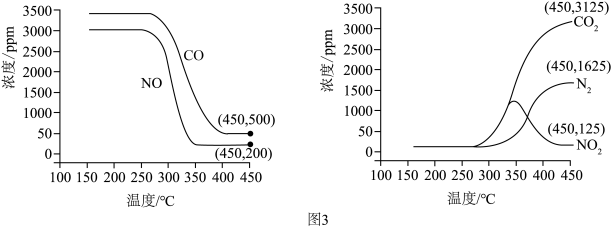
(6)实验过程中,高于340℃后N
 O浓度逐渐减小,试分析发生该变化的原因是
O浓度逐渐减小,试分析发生该变化的原因是(7)450℃时, 该时间段内NO的脱除率=

您最近半年使用:0次
解题方法
8 . 在体积为1 L的密闭容器中充入1 mol CO2和3 mol H2,一定条件下发生反应: ,测得CO2和CH3OH的浓度随时间的变化如图所示。
,测得CO2和CH3OH的浓度随时间的变化如图所示。
______  。
。
(2)平衡时CO2的转化率为______ 。
(3)下列能说明上述反应达到平衡状态的是______(填字母)。
(4)平衡时混合气体中CH3OH(g)的体积分数是______ 。
(5)该反应的平衡常数
______ 。
 ,测得CO2和CH3OH的浓度随时间的变化如图所示。
,测得CO2和CH3OH的浓度随时间的变化如图所示。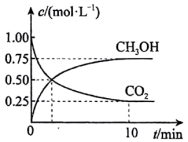

 。
。(2)平衡时CO2的转化率为
(3)下列能说明上述反应达到平衡状态的是______(填字母)。
| A.反应中CO2与CH3OH的物质的量浓度之比为1∶1 |
| B.混合气体的密度不随时间的变化而变化 |
| C.单位时间内消耗3 mol H2,同时生成1 mol H2O |
| D.CO2的体积分数在混合气体中保持不变 |
(5)该反应的平衡常数

您最近半年使用:0次
名校
解题方法
9 . 空气中的氮氧化物主要来源:化石燃料燃烧、工业制硝酸尾气、汽车尾气。
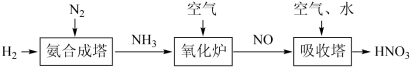
I.请根据以下工业制硝酸的原理示意图回答含氮化合物相关的问题:___________ 。
(2)用NaClO溶液吸收硝酸尾气,可提高尾气中NO的去除率。在酸性NaClO溶液中,HClO氧化NO生成 和
和 ,其离子方程式为
,其离子方程式为___________ 。
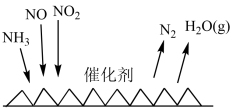
(3)“吸收塔”尾部会有含NO、NO2等氮氧化物的尾气排出,为消除它们对环境的破坏作用,目前应用最广泛的烟气氮氧化物脱除技术是NH3催化还原氮氧化物(SCR)技术。反应原理如图所示:___________ 。
II.甲烷在一定条件下可以消除氮氧化物污染。
(4)已知25℃、101kPa时,1g甲烷不完全燃烧生成CO和液态水时放出37.96kJ热量,则1mol甲烷不完全燃烧的热化学方程式为___________ 。
(5)甲烷与NO2发生的反应为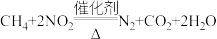 ,在体积固定的密闭容器中,每次实验均加入
,在体积固定的密闭容器中,每次实验均加入 和
和 ,使
,使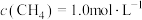 、
、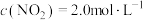 ,在不同条件下进行反应,测得
,在不同条件下进行反应,测得 随时间的变化情况如下表:
随时间的变化情况如下表:
①实验1中,在10~20min内,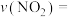
___________ ,40min时v(正)___________ v(逆)(填:“大于”、“小于”、“等于”)。
②0~20min内,实验2比实验1反应速率快的原因可能是___________ 。
I.请根据以下工业制硝酸的原理示意图回答含氮化合物相关的问题:
(2)用NaClO溶液吸收硝酸尾气,可提高尾气中NO的去除率。在酸性NaClO溶液中,HClO氧化NO生成
 和
和 ,其离子方程式为
,其离子方程式为(3)“吸收塔”尾部会有含NO、NO2等氮氧化物的尾气排出,为消除它们对环境的破坏作用,目前应用最广泛的烟气氮氧化物脱除技术是NH3催化还原氮氧化物(SCR)技术。反应原理如图所示:
II.甲烷在一定条件下可以消除氮氧化物污染。
(4)已知25℃、101kPa时,1g甲烷不完全燃烧生成CO和液态水时放出37.96kJ热量,则1mol甲烷不完全燃烧的热化学方程式为
(5)甲烷与NO2发生的反应为
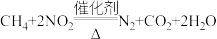 ,在体积固定的密闭容器中,每次实验均加入
,在体积固定的密闭容器中,每次实验均加入 和
和 ,使
,使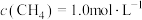 、
、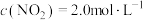 ,在不同条件下进行反应,测得
,在不同条件下进行反应,测得 随时间的变化情况如下表:
随时间的变化情况如下表:| 实验序号 | 时间/min 浓度  温度/℃ | 10 | 20 | 30 | 40 | 50 |
| 1 | 800 | 0.80 | 0.67 | 0.57 | 0.50 | 0.50 |
| 2 | 800 | 0.60 | 0.50 | 0.50 | 0.50 | 0.50 |
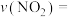
②0~20min内,实验2比实验1反应速率快的原因可能是
您最近半年使用:0次
名校
解题方法
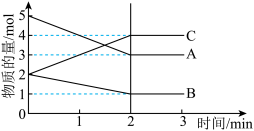
10 . Ⅰ.某可逆反应在体积为5L的密闭容器中进行,0~3min内各物质的物质的量的变化情况如图所示(A、B、C均为气体)。___________ 。
(2)反应开始至2min时,B的平均反应速率为___________ 。
(3)能说明该反应已达到平衡状态的是___________ (填字母)。
a.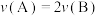 b.容器内压强保持不变
b.容器内压强保持不变
c. d.容器内混合气体的密度保持不变
d.容器内混合气体的密度保持不变
e.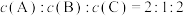 f.混合气体的平均相对分子质量保持不变
f.混合气体的平均相对分子质量保持不变
(4)将a mol A与b mol B的混合气体通入5L的密闭容器中并发生上述反应,反应到某时刻各物质的量恰好满足: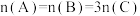 ,则原混合气体中
,则原混合气体中
___________ 。
Ⅱ.生产生活中的化学反应都伴随着能量的变化,请根据有关知识回答下列问题:
(5)冷敷袋在日常生活中有降温、保鲜和镇痛等用途。制作冷敷袋可以利用___________ (填“放热”或“吸热”)的化学变化或物理变化。
(6) “即热饭盒”给人们生活带来方便,它可利用下面___________ (填字母)反应释放的热量加热食物。
A,生石灰和水 B.浓硫酸和水
(7)如图是CO和 反应生成
反应生成 的能量变化图,写出该反应的热化学方程式:
的能量变化图,写出该反应的热化学方程式:___________ 。
(2)反应开始至2min时,B的平均反应速率为
(3)能说明该反应已达到平衡状态的是
a.
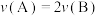 b.容器内压强保持不变
b.容器内压强保持不变c.
 d.容器内混合气体的密度保持不变
d.容器内混合气体的密度保持不变e.
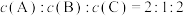 f.混合气体的平均相对分子质量保持不变
f.混合气体的平均相对分子质量保持不变(4)将a mol A与b mol B的混合气体通入5L的密闭容器中并发生上述反应,反应到某时刻各物质的量恰好满足:
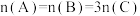 ,则原混合气体中
,则原混合气体中
Ⅱ.生产生活中的化学反应都伴随着能量的变化,请根据有关知识回答下列问题:
(5)冷敷袋在日常生活中有降温、保鲜和镇痛等用途。制作冷敷袋可以利用
(6) “即热饭盒”给人们生活带来方便,它可利用下面
A,生石灰和水 B.浓硫酸和水
(7)如图是CO和
 反应生成
反应生成 的能量变化图,写出该反应的热化学方程式:
的能量变化图,写出该反应的热化学方程式: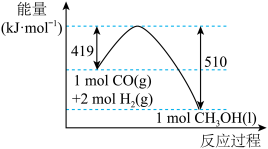
您最近半年使用:0次



